
- •1. Уравнение Лагранжа примеры его составления. Функция Лагранжа, ее свойства.
- •Свойства функции Лагранжа
- •2. Законы сохранения, соответствующие фундаментальным симметриям: энергия, импульс, момент импульса.
- •В общем случае теорема об изменении обобщенной энергии имеет вид
- •3. Канонические уравнения Гамильтона. Первые интегралы уравнений Гамильтона. Эквивалентность лагранжевого и гамильтонового формализма.
- •4. Движение в центральных полях. Кеплерова задача. Параметрическое уравнение. Траектории движения.
- •5. Уравнения Максвелла.
- •6. Проводники и диэлектрики.
- •7. Граничные условия для векторов электрического поля.
- •7.3. Условия для касательных составляющих векторов и
- •8. Граничные условия для векторов магнитного поля
- •9. Скалярный и векторный потенциалы заряда, движущегося с постоянной скоростью; формула Лоренца.
- •10. Преобразования Лоренца для проекций векторов и . Инварианты электромагнитного поля.
- •11. Полное описание квантовой системы. Принцип суперпозиции. Ортогональность и нормировка собственных функций эрмитовых операторов. Базис пространства состояний. Чистые и смешанные состояния.
- •13. Общие свойства решений одномерного уравнения Шрёдингера. Частица в прямоугольной потенциальной яме бесконечной и конечной "глубины". Спектр энергии и собственные функции.
- •14. Квантовое движение в центральном поле. Состояния электрона в поле ядра. Атом водорода и водородоподобные ионы. Квантовые числа.
- •15. Гармонический осциллятор в энергетическом представлении. Операторы рождения и уничтожения. Спектр энергии и собственные функции.
- •Общие условия равновесия и устойчивости
- •Равновесие гомогенной системы
- •18. Фазовые переходы. Фазовые переходы 1-го рода. Уравнение Клапейрона-Клаузиуса. Фазовые переходы 2-го рода. Уравнение Эренфеста. Критические и закритические явления.
18. Фазовые переходы. Фазовые переходы 1-го рода. Уравнение Клапейрона-Клаузиуса. Фазовые переходы 2-го рода. Уравнение Эренфеста. Критические и закритические явления.
При равновесии, а следовательно, и при фазовых превращениях химические потенциалы вещества в фазах, а также давление (при плоской поверхности) и температура фаз всегда одинаковы. Что же касается других термических и калорических величин (или соответствующих им производных разных порядков от энергии Гиббса), то они при фазовых превращениях теряют непрерывность. Фазовые превращения, при которых скачком изменяется удельный объем v и поглощается (или выделяется) теплота называются фазовыми переходами первого рода. Объем и энтропия выражаются через первые производные энергии Гиббса:
![]()
Исходя из этого, Эренфест предложил
классификацию
фазовых переходов, по которой
порядок фазового перехода определяется
порядком тех производных термодинамического
потенциала, которые при переходе
испытывают скачки: при фазовых переходах
первого рода испытывают скачки (все
или только некоторые) первые производные
энергии Гиббса, при фазовых переходах
второго рода первые производные энергии
Гиббса непрерывны,
но испытывают скачки его вторые
ппоизводные—теплоемкость(СР=![]() ),
сжимаемость (
),
сжимаемость (![]() ),
коэффициент теплового расширения (
),
коэффициент теплового расширения (
![]() ).
).
В настоящее время известны фазовые переходы первого рода: плавление, кипение, переход проводника из нормального состояния в сверхпроводящее в магнитном поле, переходы из одной кристаллической модификации в другую и т. д., фазовый переход второго рода — превращение проводника из нормального состояния в сверхпроводящее при отсутствии магнитного поля, а также большое число фазовых переходов, при которых вторые производные термодинамического потенциала обращаются в бесконечность (критические переходы): критический переход жидкость —газ, переход ферромагнетика в парамагнетик, сегнетоэлектрический переход и др. Критические переходы не укладываются в классификацию фазовых переходов Эренфеста, указывая на ее ограниченность.
Основным уравнением,
характеризующим фазовые переходы
первого рода,
является дифференциальное уравнение
Клапейрона — Клаузиуса. Это уравнение
получается из условия равенства
химических потенциалов при равновесии
двух фаз
![]() и связывает между собой теплоту перехода,
скачок удельного объема и наклон кривой
равновесия в точке перехода.
и связывает между собой теплоту перехода,
скачок удельного объема и наклон кривой
равновесия в точке перехода.
Из формулы следует
уравнение кривой равновесия р=р(Т).
Однако дифференциальное уравнение
кривой равновесия имеет нораздо более
простой вид и связывает медлу собой
указанные выше лекщгко измеряемые
величины:
![]() .
(12.3)
.
(12.3)
Уравнение является
дифференциальным уравнением кривой
равновесия и называется уравнением
Клапейрона — Клаузиуса. Чаще
его записывают в виде:
![]() (12.4)
(12.4)
где
![]() — теплота перехода на моль или грамм
вещества; v"
— v'
—
изменение
объема соответствующей массы вещества.
Главное применение уравнения состоит
в вычислении удельных
теплот испарения, возгонки, плавления
и изменения модификации.
— теплота перехода на моль или грамм
вещества; v"
— v'
—
изменение
объема соответствующей массы вещества.
Главное применение уравнения состоит
в вычислении удельных
теплот испарения, возгонки, плавления
и изменения модификации.
Если на систему действует не давление
р, а какая-либо другая обобщенная
сила А, то
мы получаем общее
дифференциальное уравнение
кривой равновесия двух фаз однокомпонентной
системы:
![]() .(s
– изменение энтропии , а – скачок
внешнего параметра).
.(s
– изменение энтропии , а – скачок
внешнего параметра).
Уравнением Клапейрона
— Клаузиуса:![]() определяет изменение температуры
фазового перехода (например, точки
замерзания или кипения) с изменением
давления.
определяет изменение температуры
фазового перехода (например, точки
замерзания или кипения) с изменением
давления.
ФАЗОВЫЕ ПЕРЕХОДЫ ВТОРОГО РОДА. УРАВНЕНИЕ ЭРЕНФЕСТА
В отличие от фазовых переходов первого рода при фазовых переходах второго рода никакого скачка в изменении состояния не происходит. Состояние системы изменяется непрерывно, и в точках фазового перехода состояния фаз совпадают. Тепловой эффект перехода равен нулю, и удельный объем остается прежним (s’’=s’, v’’=v’), но теплоемкость Ср, коэффициент теплового расширения и сжимаемость испытывают скачки. Связь между этими скачками и наклоном кривой равновесия в точке перехода определяется уравнениями Эренфеста, который впервые (1933) ввел представление о фазовых переходах второго рода при рассмотрении перехода Неl в Неll.
До недавнего времени к фазовым переходам второго рода помимо сверхпроводящего перехода при отсутствии магнитного поля относили также превращение железа в точке Кюри в парамагнитное состояние, переход Неl в Неll, многие превращения в кристаллах. По современным представлениям, только сверхпроводящий переход при Н = 0 является переходом второго рода по Эренфесту, остальные же из названных переходов имеют другую природу.
Найдем уравнения Эренфеста. Правая часть уравнения Клапейрона — Клаузиуса (12.3) в точке фазового перехода второго рода принимает вид неопределенности О/О. Для ее раскрытия воспользуемся правилом Лопиталя. Дифференцируя числитель и знаменатель правой части (12.3) или по Т, или по р, получаем уравнения Эренфеста:
![]()
![]()
В общем случае, если на систему действует обобщенная сила А, которой соответствует внешний параметр а, уравнения Эренфеста будут иметь вид (то же, с заменой р на А, v на а).
Уравнения Эренфеста связывают скачки вторых производных термодинамического потенциала не только при фазовых переходах второго рода, но и в случае целого ряда фазовых переходов первого рода. Примером такого перехода первого рода является переход из упорядоченного состояния в неупорядоченное в сплавах AuCu3, AuCu и др. Характерной особенностью этих фазовых переходов является постоянство скачков объема и энтропии на всей линии превращения:
![]() ,
(12.12)
,
(12.12)
так что на диаграмме Т, р наклон
линии фазового равновесия dp/dT=![]() S/
V
оказывается
постоянным и, следовательно, сама эта
линия есть прямая (линейные фазовые
переходы первого рода). Дифференцируя
уравнение (12.12)
по температуре
вдоль линии равновесия,
получаем выражения откуда
непосредственно следуют уравнения
Эренфеста.
S/
V
оказывается
постоянным и, следовательно, сама эта
линия есть прямая (линейные фазовые
переходы первого рода). Дифференцируя
уравнение (12.12)
по температуре
вдоль линии равновесия,
получаем выражения откуда
непосредственно следуют уравнения
Эренфеста.
Таким образом, уравнения Эренфеста определяют широкий класс фазовых превращений — линейные фазовые переходы первого рода и фазовые переходы второго рода.
КРИТИЧЕСКИЕ И ЗАКРИТИЧЕСКИЕ ЯВЛЕНИЯ
В 1860 г. Д. И. Менделеев, исследуя зависимость поверхностного натяжения жидкостей от температуры, установил, что при некоторой температуре, названной им температурой абсолютного кипения, поверхностное натяжение исчезает. При этом обе сосуществующие фазы (жидкость и пар) становятся тождественными. Такое состояние характеризуется определенными значениями температуры Ткр, давления ркр и объема Vкр и называется критическим состоянием. Кривая равновесия жидкости и пара на диаграмме Т, р кончается в критической точке.
На основании этих экспериментальных исследований Дж. В. Гиббс (1876) и независимо от него А. Г. Столетов (1879) сформулировали основные положения классической термодинамической теории критических явлений. По Гиббсу — Столетову, критическая фаза представляет собой предельный случай двухфазного равновесия, когда обе равновесно сосуществующие фазы становятся тождественными. Иначе говоря, это устойчивое состояние однородной системы, лежащее на границе устойчивости по отношению к виртуальным изменениям каждой ее координаты при постоянстве других термодинамических сил.
Математически граница устойчивости однородной системы по отношению к таким виртуальным изменениям ее координат определяется обращением в равенства термодинамических неравенств, характеризующих эту устойчивость однородной системы: (dp/dV)T=0, (dT/dV)p=0, (dT/dS)p=0, (dp/dS)T=0.
Условия устойчивости критического состояния: T S- p V>0.
Критическое состояние определяется четырьмя уравнениями для функции двух переменных, не может в данном случае привести к противоречию, так как, согласно термодинамическому тождеству
![]() только
два из приведенных уравнений являются
независимыми.
только
два из приведенных уравнений являются
независимыми.

Критическое состояние системы жидкость — пар — это однокомпонентная, однофазная система, поэтому по правилу фаз n<k число степеней свободы критического состояния fкр=k-n=0.
Это означает, что критическое состояние простой однокомпонентной системы возможно лишь при определенных температуре, давлении и объеме, т. е. в одной критической точке Ткр, ркр, Vкр, Параметры критической точки зависят только от свойств данного вещества.
С изменением термодинамических сил, действующих на систему, изменяются различные характеристики фазового перехода первого рода (ФП I рода). Так, при повышении температуры и давления в системе жидкость — пар уменьшаются удельная теплота перехода и области метастабильных и неустойчивых состояний (см. рис. 46). Предельным случаем ФП I рода является критический переход.
Как показывается в статистической физике, коэффициенты устойчивости обратно пропорциональны флуктуациям различных физических величин. С приближением к критической точке флуктуации растут. За критической точкой существуют только устойчивые состояния, поэтому в этой области невозможно сосуществование фаз, имеющих границу раздела. Анализ термодинамической устойчивости закритической фазы привел В. К. Семенченко к построению термодинамики непрерывных фазовых переходов.
Как уже упоминалось, рассмотрение изотерм вблизи критической точки показывает, что точки перегиба на этих изотермах имеются и в закритической области. Но точка перегиба на кривой соответствует экстремумам на кривых для ее первых производных, В точках квазиспинодали флуктуации достигают при данных условиях наибольшего значения и система превращается в смесь флуктуационных зародышей обеих граничных (далеких от этого состояния) фаз — квазифазу или мезофазное состояние*, не теряя своей макроскопической однородности. Поскольку минимум устойчивости является поворотной точкой в отношении изменения свойств фаз, он до некоторой степени аналогичен точке фазового перехода второго рода и условно его можно считать за точку закритического перехода. При этом, конечно, не нужно забывать, что закритический переход происходит на конечном интервале Т, р и других термодинамических сил. Поэтому в условной точке закритического перехода не происходит скачков энтропии, объема и других я,-, а только их быстрое изменение. Работа и удельная теплота перехода также равны по этой причине нулю. Сами коэффициенты устойчивости изменяются также непрерывно, а не скачком; в этом состоит отличие закритических переходов от ФП II рода по Эренфесту.
До сих пор мы для определенности пользовались диаграммами, относящимися к флюидным системам, т. е. системам газ — жидкость. Однако все изложенное применимо и к анизотропным системам, а также к системам, фазы которых отличаются по своим магнитным или электрическим свойствам (ферро-и антиферромагнетики, сверхпроводники и сегнетоэлектрики разных типов).
Очень интересный случай критического перехода в анизотропной среде представляет а-^-переход в кварце. Он сопровождается резко выраженной критической опалесценцией и экстремумами нескольких КУ. Но самым интересным является возможность непосредственного наблюдения смешанного состояния обеих граничных фаз.
19. Микроканоническое и каноническое распределения Гиббса. Статистический интеграл системы. Энтропия. Большое каноническое распределение (классический и квантовый случай). Термодинамическая эквивалентность канонических распределений.
Рассмотрим многочастичную термодинамически равновесную систему. Основная идея статфизики состоит в замене среднего по времени (b(q, р)); функции b(q, p)
данной системы средним значением b(q,
p) этой функции по ансамблю
определенным образом распределенных
систем
![]() где фазовая плотность распределения
p(q, p)
для равновесных систем, очевидно, не
зависит от времени и удовлетворяет
условию нормировки
где фазовая плотность распределения
p(q, p)
для равновесных систем, очевидно, не
зависит от времени и удовлетворяет
условию нормировки
![]() Задача состоит в том, чтобы найти p(q,
p), удовлетворяющую
равенству
Задача состоит в том, чтобы найти p(q,
p), удовлетворяющую
равенству
![]() Для этого обратимся прежде всего к
основному уравнению статистической
физики классических систем — уравнению
Лнувилля. Из него получаем
Для этого обратимся прежде всего к
основному уравнению статистической
физики классических систем — уравнению
Лнувилля. Из него получаем
![]() откуда следует, что равновесная функция
распределения p(q,
p) является интегралом
движения уравнений Гамильтона или
функцией интегралов движения:
откуда следует, что равновесная функция
распределения p(q,
p) является интегралом
движения уравнений Гамильтона или
функцией интегралов движения:
![]() В соответствии с введенным Гиббсом
(отвечающим термодинамике) статистическим
определением энтропии (см. ниже) функция
p(q, p)
зависит лишь от однозначных аддитивных
интегралов движения. Известны три
таких интеграла движения: энергия Н,
импульс Р и момент импульса М. Поэтому
В соответствии с введенным Гиббсом
(отвечающим термодинамике) статистическим
определением энтропии (см. ниже) функция
p(q, p)
зависит лишь от однозначных аддитивных
интегралов движения. Известны три
таких интеграла движения: энергия Н,
импульс Р и момент импульса М. Поэтому
![]() Для равновесной системы частиц в
неподвижном сосуде импульс Р и момент
импульса М равны нулю. Поэтому в этом
случае для систем с заданным числом
частиц фазовая плотность распределения
зависит лишь от функции Гамильтона Для
определения явного вида функции
распределения в статистической
физике принимается в качестве основного
положения постулат равной априорной
вероятности любого микросостояния
равновесной изолированной системы, т.
е. принимается, что для изолированной
системы, имеющей энергию Е с точностью
(определяемой заданием макроскопических
условий) и число частиц N в объеме V,
функция распределения p(q,
p) постоянна в слое и равна
нулю вне этого слоя:
Для равновесной системы частиц в
неподвижном сосуде импульс Р и момент
импульса М равны нулю. Поэтому в этом
случае для систем с заданным числом
частиц фазовая плотность распределения
зависит лишь от функции Гамильтона Для
определения явного вида функции
распределения в статистической
физике принимается в качестве основного
положения постулат равной априорной
вероятности любого микросостояния
равновесной изолированной системы, т.
е. принимается, что для изолированной
системы, имеющей энергию Е с точностью
(определяемой заданием макроскопических
условий) и число частиц N в объеме V,
функция распределения p(q,
p) постоянна в слое и равна
нулю вне этого слоя:
 Равновероятностное
распределение микросостояний
изолированной системы называется
микроканоническим распределением, а
соответствующий ансамбль — микроканоническим
ансамблем. С помощью б-функции
микроканоническое распределение (12.9)
можно записать в виде
Равновероятностное
распределение микросостояний
изолированной системы называется
микроканоническим распределением, а
соответствующий ансамбль — микроканоническим
ансамблем. С помощью б-функции
микроканоническое распределение (12.9)
можно записать в виде
![]()
П остоянная
g(E, N,
V) определяется из
условия нормировки
остоянная
g(E, N,
V) определяется из
условия нормировки
![]() и имеет смысл плотности распределения
фазового объема по энергии.
Действительно, интеграл от g(E')
по допустимым значениям энергии, меньшим
Е (Еmin<E'<Е),
равен фазовому объему (приведенному),
заключенному внутри гиперповерхности
Н(q, р) =Е. Увеличение
фазового объема Г(Е) при
возрастании энергии на величину Е
называется статистическим весом
макроскопического состояния системы
с энергией E и равно
и имеет смысл плотности распределения
фазового объема по энергии.
Действительно, интеграл от g(E')
по допустимым значениям энергии, меньшим
Е (Еmin<E'<Е),
равен фазовому объему (приведенному),
заключенному внутри гиперповерхности
Н(q, р) =Е. Увеличение
фазового объема Г(Е) при
возрастании энергии на величину Е
называется статистическим весом
макроскопического состояния системы
с энергией E и равно
![]() где g(E) —
энергетическая плотность фазового
объема, или, поскольку точки фазового
объема изображают состояния, плотность
состояний системы с данной энергией Е.
Можно показать, что микроканоническое
распределение обеспечивает равенство
среднего по макроканоническому ансамблю
среднему по времени функции координат
к импульсов систем. Такие системы
называются эргодическими. Обоснование
(исходя из механики) эргодичности
многочастичных систем и возможности
замены средних по времени средними по
микроканоническому ансамблю носит
название эргодической проблемы. Эта
проблема несмотря на ряд полученных
важных результатов еще ждет своего
решения. Для построения термодинамики
многочастичной системы достаточно,
как известно, определить один из ее
термодинамических потенциалов. Остальные
величины находятся уже методами самой
термодинамики. При независимых
макроскопических параметрах E,
V, N, которыми
определяется термодинамическое состояние
рассматриваемой системы, термодинамическим
потенциалом является энтропия. Гиббс
определяет ее как величину, пропорциональную
логарифму фазового объема
где g(E) —
энергетическая плотность фазового
объема, или, поскольку точки фазового
объема изображают состояния, плотность
состояний системы с данной энергией Е.
Можно показать, что микроканоническое
распределение обеспечивает равенство
среднего по макроканоническому ансамблю
среднему по времени функции координат
к импульсов систем. Такие системы
называются эргодическими. Обоснование
(исходя из механики) эргодичности
многочастичных систем и возможности
замены средних по времени средними по
микроканоническому ансамблю носит
название эргодической проблемы. Эта
проблема несмотря на ряд полученных
важных результатов еще ждет своего
решения. Для построения термодинамики
многочастичной системы достаточно,
как известно, определить один из ее
термодинамических потенциалов. Остальные
величины находятся уже методами самой
термодинамики. При независимых
макроскопических параметрах E,
V, N, которыми
определяется термодинамическое состояние
рассматриваемой системы, термодинамическим
потенциалом является энтропия. Гиббс
определяет ее как величину, пропорциональную
логарифму фазового объема
![]() где k — универсальная
постоянная, равная постоянной Больцмана.
Можно показать, что определенная таким
образом энтропия обладает известными
термодинамическими свойствами.
где k — универсальная
постоянная, равная постоянной Больцмана.
Можно показать, что определенная таким
образом энтропия обладает известными
термодинамическими свойствами.
Заметим, что поскольку при определении
энтропии в статистическом пределе
(N=>,
V=>,
V/N = v
= const) следует учитывать
только основную асимптотику по числу
частиц —N, то определение
статистической энтропии не является
единственным. Так, например, можно
использовать вместо эквивалентные
выражения в виде логарифмов или плотности
состояний
![]() i статистического веса
i статистического веса
![]() Логарифмический вид выражений для
энтропии обусловлен требованием ее
аддитивности, в частности, для
невзаимодействующих подсистем.
Вычисление фазового объема или
статистического веса даже для
относительно простых статистических
систем .представляют трудную задачу.
Поэтому микроканоническое распределение
используется в основном не для вычисления
термодинамических функций конкретных
систем, а для общетеоретического
рассмотрения. Каноническое распределение
Найдем распределение по состояниям
(функцию распределения в фазовом
пространстве) неизолированной (но
замкнутой) системы, находящейся в
тепловом контакте с другой системой
значительно больших размеров (по
числу степеней свободы) — термостатом.
Т — температура термостата и системы,
находим каноническое распределение
Гиббса
Логарифмический вид выражений для
энтропии обусловлен требованием ее
аддитивности, в частности, для
невзаимодействующих подсистем.
Вычисление фазового объема или
статистического веса даже для
относительно простых статистических
систем .представляют трудную задачу.
Поэтому микроканоническое распределение
используется в основном не для вычисления
термодинамических функций конкретных
систем, а для общетеоретического
рассмотрения. Каноническое распределение
Найдем распределение по состояниям
(функцию распределения в фазовом
пространстве) неизолированной (но
замкнутой) системы, находящейся в
тепловом контакте с другой системой
значительно больших размеров (по
числу степеней свободы) — термостатом.
Т — температура термостата и системы,
находим каноническое распределение
Гиббса


 где
— kT
называется модулем канонического
распределения, а константа A
содержит все не зависящие от q
и р величины и определяется из условия
нормировки Входящий интеграл
где
— kT
называется модулем канонического
распределения, а константа A
содержит все не зависящие от q
и р величины и определяется из условия
нормировки Входящий интеграл
 называется статистич. интегралом
системы, а определяемая
называется статистич. интегралом
системы, а определяемая
![]() есть ее энергия Гельмгольца F(T,V,N).
Действительно, вычислим внутренние
уравнению Гиббса—Гельмгольца
есть ее энергия Гельмгольца F(T,V,N).
Действительно, вычислим внутренние
уравнению Гиббса—Гельмгольца
![]() т. е. что внутренняя энергия статистической
системы равна среднему значению ее
функции Гамильтона по каноническому
распределению Гиббса как и должно
быть в соответствии с физическим
смыслом Е. Поскольку функция Гамильтона
системы равна сумме кинетической и
потенциальной энергий ее частиц, а
кинетическая энергия есть квадратичная
функция импульсов, то интегрирование
по ним в может быть произведено и мы
получим
т. е. что внутренняя энергия статистической
системы равна среднему значению ее
функции Гамильтона по каноническому
распределению Гиббса как и должно
быть в соответствии с физическим
смыслом Е. Поскольку функция Гамильтона
системы равна сумме кинетической и
потенциальной энергий ее частиц, а
кинетическая энергия есть квадратичная
функция импульсов, то интегрирование
по ним в может быть произведено и мы
получим

![]() называется конфигурационным интегралом.
Интегрирование по импульсам канонического
распределения Гиббса легко выполняется
и дает конфигурационное распределение
Гиббса
называется конфигурационным интегралом.
Интегрирование по импульсам канонического
распределения Гиббса легко выполняется
и дает конфигурационное распределение
Гиббса
 Энергия Гельмгольца
Энергия Гельмгольца
![]()
![]() — тепловая длина волны де Бройля. Таким
образом вычисление энергии Гельмгольца,
а следовательно, и всех термодинамических
функций многочастичной системы
сводится к вычислению ее конфигурационного
интеграла (12.24). С помощью известных
термодинамических соотношений (5.17)
— тепловая длина волны де Бройля. Таким
образом вычисление энергии Гельмгольца,
а следовательно, и всех термодинамических
функций многочастичной системы
сводится к вычислению ее конфигурационного
интеграла (12.24). С помощью известных
термодинамических соотношений (5.17)
![]()
 С помощью канонического распределения
находим, что энтропия
С помощью канонического распределения
находим, что энтропия
с истемы
пропорциональна среднему значению
логарифма плотности вероятности, а
не является
истемы
пропорциональна среднему значению
логарифма плотности вероятности, а
не является
средним значением какой-либо механической
величины. Большое каноническое
распределение Определим теперь
распределение по состояниям открытой
системы в термостате, называемое
большим каноническим распределением
Гиббса. С такими системами мы встречаемся
в целом ряде приложений. Кроме того,
использование большого канонического
распределения во многих случаях
оказывается более эффективным, чем
микроканонического и канонического
распределений. Рассмотрим малую
систему, которая находится в тепловом
и материальном контакте с термостатом,
обмениваясь с ним не только энергией,
но и частицами. Границы, отделяющие
систему от термостата в некотором смысле
условны: они фиксируют лишь ее объем V
и другие внешние параметры а, но не
энергию Е и число частиц N.
В соответствии с этим термодинамическое
состояние системы определяется
переменными Т, V, N.
Большое каноническое распределение
получим аналогично выводу канонического,
исходя из микроканонического распределения
для изолированной объединенной (термостат
и изучаемая малая система) системы с
энергией ЕО и числом частиц NO.
Отличие в рассматриваемом случае
системы состоит в том, что теперь
следует в явном виде указывать число
частиц в ней. Таким образом, подобно
функция распределения системы с
переменным числом частиц в термостате
имеет вид:
 где индексы о к т относятся соответственно
к объединенной системе и к термостату.
Поскольку мы будем предполагать, что
для энергии E и числа
частиц N подсистемы
справедливы неравенства
где индексы о к т относятся соответственно
к объединенной системе и к термостату.
Поскольку мы будем предполагать, что
для энергии E и числа
частиц N подсистемы
справедливы неравенства
 то в первом приближении
то в первом приближении
![]() где учтено, что
где учтено, что
![]() Подставляя (12.45) в (12.44), находим
распределение Гиббса большое каноническое
Подставляя (12.45) в (12.44), находим
распределение Гиббса большое каноническое

 большой статистический интеграл (сумма),
большой статистический интеграл (сумма),
![]() большой термодинамический потенциал.
Действительно, термодинамические
параметры —число частиц и внутренняя
энергия —определяемые соответствующими
частными производными большого
термодинамического потенциала,
совпадают со средними значениями числа
частиц и функции Гамильтона по большому
каноническому распределению Г
большой термодинамический потенциал.
Действительно, термодинамические
параметры —число частиц и внутренняя
энергия —определяемые соответствующими
частными производными большого
термодинамического потенциала,
совпадают со средними значениями числа
частиц и функции Гамильтона по большому
каноническому распределению Г иббса
(12.46).
иббса
(12.46).
Термодинамическая эквивалентность канонических распределений Мы рассмотрели три гиббсовских распределения: микроканоническое — для изолированных систем, каноническое — для неизолированных закрытых систем в термостате и большое каноническое—для неизолированных открытых систем в термостате.За исключением немногих случаев, использование этих распределений для каждой из названных систем приводит в статистическом пределе (N=>, V=>, V/N = u = const) к термодинамически эквивалентным результатам. Это означает, что каноническим и большим каноническим распределениями можно пользоваться также для описания изолированных систем, что практически является очень важным. Во всех практически важных случаях относительная' флуктуация энергии очень мала и в статистическом пределе стремится к нулю. Малость величины относительной флуктуации означает, что значения энергии системы в термостате сколько-нибудь отличные от средней энергии, рактически невероятны.
Энергии, заметно отличающиеся от Н,
чрезвычайно маловероятны, и система
ведет себя практически как изолированная.
Это и приводит к термодинамической
эквивалентности результатов, полученных
с помощью канонического и микроканонического
распределений. Аналогично с помощью
большого канонического распределения
находим: относительная флуктуация
числа частиц в системах большого
канонического ансамбля
![]()
стремится к нулю в статистическом пределе. Отсюда следует эквивалентность большого канонического и канонического распределений. Заметим, что, несмотря на термодинамическую эквивалентность статистических ансамблей, расчеты величины флуктуации, проведенные с их помощью, приводят к различным результатам. Как видно из формулы, относительная флуктуация энергии системы в термостате не будет малой тогда, когда бесконечно большая теплоемкость, и аналогично относительная флуктуация не будет малой при нулевая величина коэффициента устойчивости. Это имеет место, как известно из термодинамики, в критическом состоянии и в двухфазных системах. В этих случаях канонические ансамбли не эквивалентны. основы КВАНТОВОЙ СТАТИСТИКИ Квантовые микроканоническое и каноническое распределения. Определение микроканонического и канонического распределений квантовых систем в целом аналогично рассмотренному классическому случаю. Роль функции распределения играет теперь статистический оператор р или набор коэффициентов wk. определяющих вероятностное распределение по чистым состояниям.
Как следует из уравнения Неймана, равновесный статистический оператор коммутирует с гамильтонианом И для покоящейся системы является его функцией. Поэтому необходимо задать зависимость коэффициентов wk от энергии Ek.
Если число квантовых состояний
изолированной системы, имеющей энергию
Е с определенным отклонением Е<Е,
равно Г(E),
то в соответствии с постулатом равной
априорной вероятности состояний
таких систем имеем квантовое
микроканоническое распределение

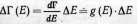 из условия нормировки (13.1):
из условия нормировки (13.1):
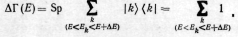 а полное число состояний равно
а полное число состояний равно
 Энтропия квантовой статистической
системы определяется формулами,
Энтропия квантовой статистической
системы определяется формулами,
 Отсюда получаем квантовое каноническое
распределение по состояниям
Отсюда получаем квантовое каноническое
распределение по состояниям
![]()
 или после нормировки
или после нормировки

![]() называется статистической суммой, а
называется статистической суммой, а
![]() есть энергия Гельмгольца квантовой
системы, в чем легко убедиться.
Заметим, что каноническое распределение
определяет также распределение по
энергиям для системы с невырожденными
уровнями энергии. При наличии вырождения,
когда одному и тому же энергетическому
уровню Е соответствует gt
различных состояний, вероятность такого
вырожденного значения энергии равна
есть энергия Гельмгольца квантовой
системы, в чем легко убедиться.
Заметим, что каноническое распределение
определяет также распределение по
энергиям для системы с невырожденными
уровнями энергии. При наличии вырождения,
когда одному и тому же энергетическому
уровню Е соответствует gt
различных состояний, вероятность такого
вырожденного значения энергии равна
 Зная энергию Гельмгольца, как функцию
своих естественных переменных, все
другие термодинамические параметры
можно найти методами термодинамики.
Энтропия системы равна
Зная энергию Гельмгольца, как функцию
своих естественных переменных, все
другие термодинамические параметры
можно найти методами термодинамики.
Энтропия системы равна
 Таким образом, исследование квантовой
статистической системы с помощью
канонического распределения сводится
к следующей процедуре:
Таким образом, исследование квантовой
статистической системы с помощью
канонического распределения сводится
к следующей процедуре:
а) вначале решается динамическая задача по определению энергетического спектра Е; и соответствующего набора квантовых чисел i путем решения уравнения Шредингера;
б) потом рассчитывается статистическая сумма (13.11) системы и ее энергия Гельмгольца F(Q, V, N) (13.12);в) и далее вычисляются термодинамические характеристики системы. Квантовое большое каноническое распределение. Рассмотрим свойства открытых квантовых систем в термостате. Макроскопически такие системы описываются переменными Т, V, N. Границы, отделяющие систему от термостата, проницаемы для частиц. Соответствующее этим условиям распределение по состояниям — большое каноническое распределение — может быть получено подобно каноническому, исходя из микроканонического распределения для объединенной изолированной системы с энергией E0 и числом частиц N0. При этом в дополнение к неравенству для энергии системы необходимо добавить неравенство для числа ее частиц Отсюда, используя микроканоннческое распределение для объединенной системы, находим большое каноническое распределение по состояниям i квантовой открытой системы а термостате:
![]()

![]() большой термодинамический потенциал.
Действительно, вычисленные с помощью
(13.19) по формулам термодинамики энергия
и число частиц системы равны соответствующим
средним по большому каноническому
распределению:
большой термодинамический потенциал.
Действительно, вычисленные с помощью
(13.19) по формулам термодинамики энергия
и число частиц системы равны соответствующим
средним по большому каноническому
распределению:
![]()
 Энтропия системы, как и в случае
канонического распределения определяется
средним значением логарифма функции
распределения:
Энтропия системы, как и в случае
канонического распределения определяется
средним значением логарифма функции
распределения:
 Таким образом, при использовании большого
канонического распределения для
исследования квантовых статистических
систем необходимо прежде всего определить
энергетический спектр системы из решения
уравнения Шредингера
Таким образом, при использовании большого
канонического распределения для
исследования квантовых статистических
систем необходимо прежде всего определить
энергетический спектр системы из решения
уравнения Шредингера
![]() Причем в отличие от канонического
распределения требуется найти
зависимость спектра для произвольного
числа частиц N, в том
числе и для малых N~
1. Затем следует расчет большой
статистической суммы и большого
термодинамического потенциала .
Далее методами термодинамики вычисляются
все необходимые термодинамические
характеристики системы.
Причем в отличие от канонического
распределения требуется найти
зависимость спектра для произвольного
числа частиц N, в том
числе и для малых N~
1. Затем следует расчет большой
статистической суммы и большого
термодинамического потенциала .
Далее методами термодинамики вычисляются
все необходимые термодинамические
характеристики системы.
20. Статистическая термодинамика квантовых идеальных одноатомных газов. Распределение Бозе-Эйнштейна и Ферми-Дирака. Сопоставление распределений М.-Б., Б.-Э. и Ф.-Д. Вырождение квантовых газов. Теплоёмкость твёрдых тел.
При температурах Т<Т0 (
![]() )
система частиц становится квантовой.
Квантовые частицы помимо волновых
свойств обладают собственным (спиновым)
механическим моментом. Его величина
равна
)
система частиц становится квантовой.
Квантовые частицы помимо волновых
свойств обладают собственным (спиновым)
механическим моментом. Его величина
равна
![]() h
,где спин s – целое (включая
нуль) или полуцелое положительное число,
определяемое природой частиц. Таким
образом, состояние квантовой частицы
данного типа определяется волновой
функцией
Ψ(x,y,z)
и спиновым числом ms
(характеризующим одно из возможных
значений проекций спинового момента
на фиксированную ось). Возможны 2s+1
состояний с заданной волновой функцией,
отличающейся ориентацией спина.
h
,где спин s – целое (включая
нуль) или полуцелое положительное число,
определяемое природой частиц. Таким
образом, состояние квантовой частицы
данного типа определяется волновой
функцией
Ψ(x,y,z)
и спиновым числом ms
(характеризующим одно из возможных
значений проекций спинового момента
на фиксированную ось). Возможны 2s+1
состояний с заданной волновой функцией,
отличающейся ориентацией спина.
Так как в отсутствие магнитного поля
энергия частицы не зависит от ориентации
спина, то наличие спина увеличивает
число квантовых состояний с заданной
энергией в 2s+1 раз. В
зависимости от того, является ли спин
целым или полуцелым, частицы делятся
на два класса: бозе-частицы, или бозоны
(с целым спином), и ферми-частицы, или
фермионы (с полуцелым спином). Бозонами
являются фотон (s=1), π- и
К-мезоны (s=0). Большинство
элементарных частиц (электроны, протоны,
нейтроны и др.) имеют спин s
=![]() и являются фермионами.
и являются фермионами.
Спин сложной частицы определяется числом входящих в нее фермионов. Если это число четное (Н, Н2, Не4), то сложная частица является бозоном, если нечетное (D, HD) – фермионом.
Волновая функция системы бозонов симметрична, а фермионов – антисимметрична относительно перестановки любой пары частиц. Волновая функция квантового идеального газа представляется произведением волновых функций отдельных частиц и полностью определяется заданием чисел заполнения nk каждого к-го одночастичного состояния. Требование антисимметрии волновой функции системы фермионов приводит к тому, что они удовлетворяют принципу Паули: в заданном квантовом состоянии может находиться не более одной частицы, т.е. nk=0; 1. В каждом одночастичном состоянии бозе-газа может находиться любое число частиц: nk=0;1;2,…N, где N – общее число частиц в системе.
Распределение частиц по одночастичным квантовым состояниям зависит от того, являются ли частицы бозонами или фермионами. В соответствии с этим существуют две квантовые статистики: статистика Бозе-Эйнштейна (для бозонов) и статистика Ферми-Дирака (для фермионов). Функция распределения по квантовым состояниям обоих классов частиц имеет вид:
![]() =
=![]()
![]() (nk)
=
(nk)
=![]()
![]() k
/
k
/
![]() k
1. Распределение бозе-частиц по
состояниям называется распределением
Бозе-Эйнштейна:
=
k
1. Распределение бозе-частиц по
состояниям называется распределением
Бозе-Эйнштейна:
=
 оно было установлено в 1924 г. Распределение
частиц по энергиям найдем, умножив
на число gk
микросостояний с энергией
оно было установлено в 1924 г. Распределение
частиц по энергиям найдем, умножив
на число gk
микросостояний с энергией
![]() :
(
)
=
:
(
)
= 2. Распределение Ферми-Дирака Среднее
число ферми-частиц в к-ом состоянии
равно:
=
2. Распределение Ферми-Дирака Среднее
число ферми-частиц в к-ом состоянии
равно:
=
 Распределение электронов по эгеогиям
(s=
)
будет
(
)
=
Распределение электронов по эгеогиям
(s=
)
будет
(
)
= сопоставление
распределений М-Б, Б-Э и Ф-Д: все эти
три функции распределения идеальных
газов можно записать в едином виде:
=
сопоставление
распределений М-Б, Б-Э и Ф-Д: все эти
три функции распределения идеальных
газов можно записать в едином виде:
=
 , (1) где
, (1) где
![]() для распределения М-Б,
для распределения М-Б,
![]() для распределения Ф-Д,
для распределения Ф-Д,
![]() для распределения Б-Э. На рис приведены
графики этих функций распределения. Из
(1 ) видно, что распределения Б-Э и Ф-Д
переходят в распределение М-Б, т.е. газ
становится классическим, если
для распределения Б-Э. На рис приведены
графики этих функций распределения. Из
(1 ) видно, что распределения Б-Э и Ф-Д
переходят в распределение М-Б, т.е. газ
становится классическим, если
![]() .
(2) Если
.
(2) Если
![]() ,
то функция распределения газа отличается
от максвелл-больщмановской и говорят,
что газ вырожден. Величина
,
то функция распределения газа отличается
от максвелл-больщмановской и говорят,
что газ вырожден. Величина
![]() называется фактором вырождения, выражение
(2) – критерием невырожденности, а
противоположные неравенства – критерием
сильного вырождения.
называется фактором вырождения, выражение
(2) – критерием невырожденности, а
противоположные неравенства – критерием
сильного вырождения.
Теплоемкость
твердых тел рассчитывается по формуле
Дюлонга и Пти:
![]() Твердое
тело рассматривается как совокупность
N независимых атомов,
колеблющихся с одной и той же частотой
ν. Однако средняя энергия, приходящаяся
на одну степень свободы, полагается
равной не КТ, а вычисляется по формуле
Планка для средней энергии линейного
осциллятора:
Твердое
тело рассматривается как совокупность
N независимых атомов,
колеблющихся с одной и той же частотой
ν. Однако средняя энергия, приходящаяся
на одну степень свободы, полагается
равной не КТ, а вычисляется по формуле
Планка для средней энергии линейного
осциллятора:
 (1)энергия грамм-атома, имеющего 3N
степеней свободы, равна:
(1)энергия грамм-атома, имеющего 3N
степеней свободы, равна:
 (2), величину
(2), величину
![]() ,
имеющего размерность температуры,
Эйнштейн назвал характеристической
температурой тела. Следовательно
,
имеющего размерность температуры,
Эйнштейн назвал характеристической
температурой тела. Следовательно
 ,
дифференцируя по температуре, получим
,
дифференцируя по температуре, получим

При
низких температурах (Т<<θ),
![]() ,
вследствие чего единицей в знаменателе
можно пренебречь и записать:
,
вследствие чего единицей в знаменателе
можно пренебречь и записать:
![]() При Т
При Т![]()
![]() ,
а
,
а
![]()
