
- •Введение.
- •Глава 1. Общие понятия и определения.
- •§1. Предмет и термодинамический метод исследования.
- •§2. Термодинамическое рабочее тело и его основные параметры состояния
- •Температура газа.
- •§3. Идеальный газ.
- •§4 Идеальные газовые смеси
- •Глава 2. Первый закон термодинамики.
- •§1 Внутренняя энергия системы.
- •§2 Первый закон термодинамики
- •1 Закон в конечном виде применим к конечному процессу 1-2:
- •§3 Анализ первого закона термодинамики.
- •§4 Связь количеств механического и теплового взаимодействий с основными параметрами газа.
- •Механическое взаимодействие:
- •Тепловое взаимодействие
- •§5 Теплоемкость идеального газа.
- •§6 Внутренняя энергия и энтальпия. Внутренняя энергия
- •Энтальпия
- •§7. Обратимые и необратимые процессы.
- •Глава 3. Газовые процессы.
- •§1Политропные методы исследования процесса.
- •§2 Порядок исследования политропного процесса.
- •А) Связь между начальными и конечными параметрами газа
- •Б) Связь между начальными и промежуточными параметрами.
- •В) Работа газа за процесс.
- •Д) Теплота, подводимая (отводимая) к газу за процесс
- •Е) Теплоемкость газа за процесс
- •Ж) Показатель политропы “n”
- •§3 Связь энтропии с основными параметрами газа
- •§4 Изотермический процесс.
- •§5 Изобарный процесс.
- •§6 Изохорный процесс.
- •§7 Адиабатический процесс.
- •§8 Обобщающие значения политропного процесса.
- •§9 Пример исследования политропного процесса.
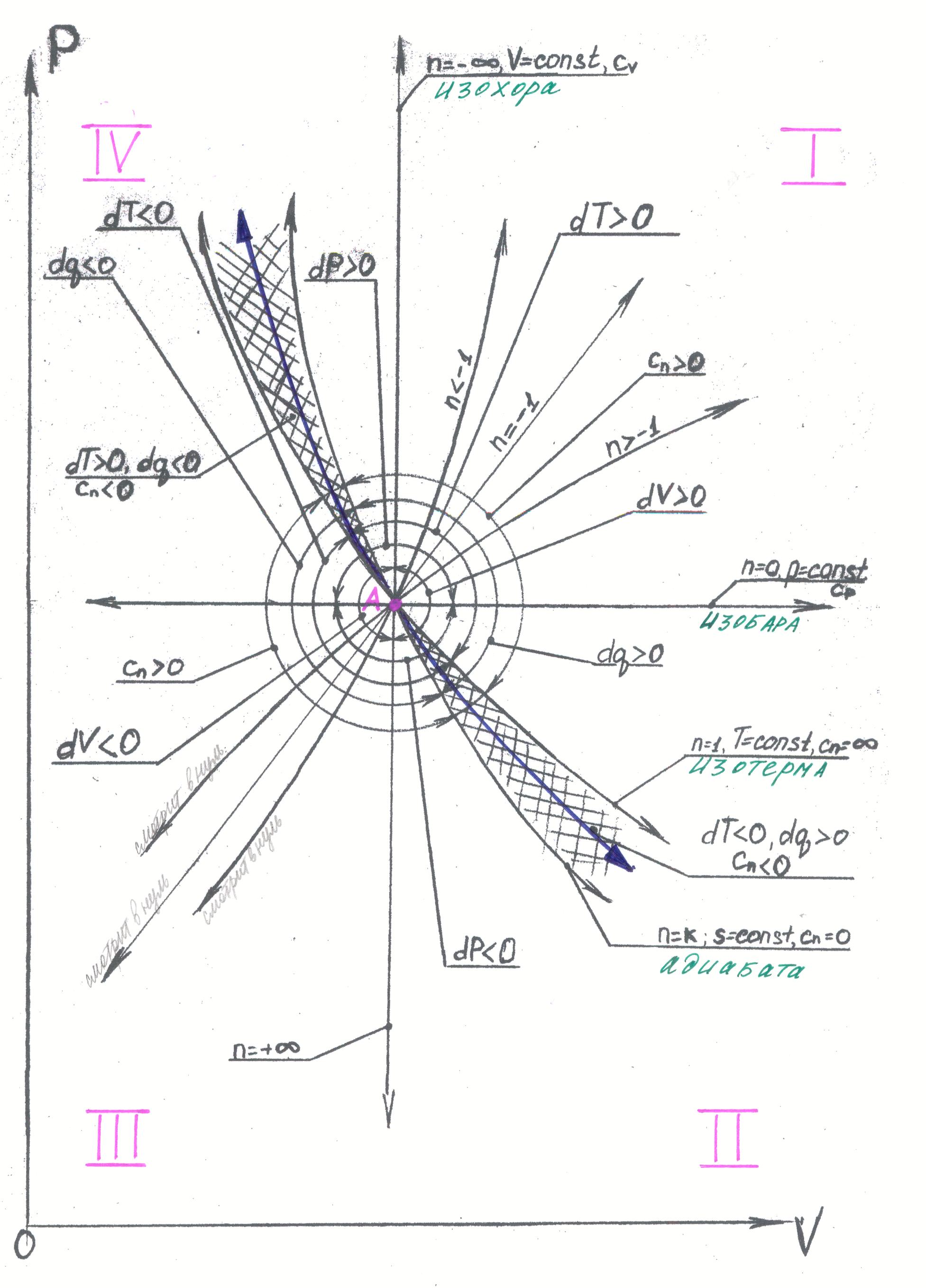
§8 Обобщающие значения политропного процесса.
Проведем через точку А изохору. Она все поле вокруг точки А делит на две области. Процессы, расположенные левее точки А, идут с понижением объема: dv<0; а процессы, расположенные правее точки А идут с повышением объема dv>0.
Проведем через точку А изобару. Процессы, расположенные ниже точки А идут с понижением давления dp<0; а процессы расположенные выше точки А, идут с повышением давления dp>0. Таким образом получили четыре квадранта.
В них лежат все политропные процессы. (см. Рис.)
pvn=const –∞ = n = +∞
Рассмотрим процессы, у которых показатель политропы - положительный
n>0; p=const/vn – гиперболы, которые лежат во 2м и 4м квадрантах
Рассмотрим равнобокую гиперболу:
n=1; р=const/v – изотерма (равнобокая гипербола)
Изотерма делит поле вокруг точки А на две области. Процессы, расположенные правее изотермы, протекают с увеличением температуры, левее - с уменьшением.
Рассмотрим адиабатный процесс:
n=k; р=const/vk – адиабата.
Адиабата делит поле вокруг точки А на две области. Процессы, находящиеся правее адиабаты, протекают с подводом тепла, левее - с отводом.
Рассмотрим, например, процесс изобарного расширения:
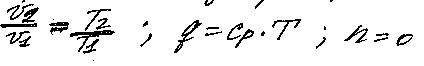
Рассмотрим процессы с отрицательным показателем политропы:
n<0; p=const/vn =v|n|const – параболы, которые лежат в 1м и 3м квадрантах
n= -1; p=v*const – уравнение прямой
n>-1;(например
n>-1/2)
p=![]() В
этих параболах функция растет медленнее
аргумента.
В
этих параболах функция растет медленнее
аргумента.
n<-1; (например n=-2) p=v2const - функция быстрее аргумента v.
Определим область положительных и отрицательных значений теплоемкости.
cn=dq/dT
cn>0 если a) dq>0, dT>0; b) dq<0, dT<0.
cn<0 если a) dq>0, dT<0; b) dq<0, dT>0 - заштрихованная область.
cn<0 при 1<n<k
§9 Пример исследования политропного процесса.
 Исследовать
идеальный и реальный процесс политропного
сжатия, протекающий при n=5.
Исследовать
идеальный и реальный процесс политропного
сжатия, протекающий при n=5.

Дано:
n=5;
pvn =const
dv<0 ;
pvn =const , p=const/vn → dp>0
dl=pdv → dl<0. В реальном процессе 1-2’ часть работы идет на преодоление силы трения между молекулами.
p2/p1=(T2/T1)n/(n-1) n/(n-1)>0 → dT>0
cn>0,т.к. теплоемкость отрицательна только в области 1<n<κ
dq=cndT → dq>0 ;
ds=dq/T → ds>0 (процесс должен идти с подводом тепла)
du=cvdT → du>0 ;
di=cpdT → di>0
Для
реального процесса:
![]()
 Исследовать
идеальный и реальный политропный
процесс, протекающий при n=1,2
и идущий с увеличением внутренней
энергии.
Исследовать
идеальный и реальный политропный
процесс, протекающий при n=1,2
и идущий с увеличением внутренней
энергии.

Дано:
n=1,2;
pvn =const
du>0 ;
du=cvdT → dT>0 ;
di=cpdT → di>0
cn<0,т.к. теплоемкость отрицательна в области 1<n<κ
dq=cndT → dq<0
ds=dq/T → ds<0
Для реального процесса:
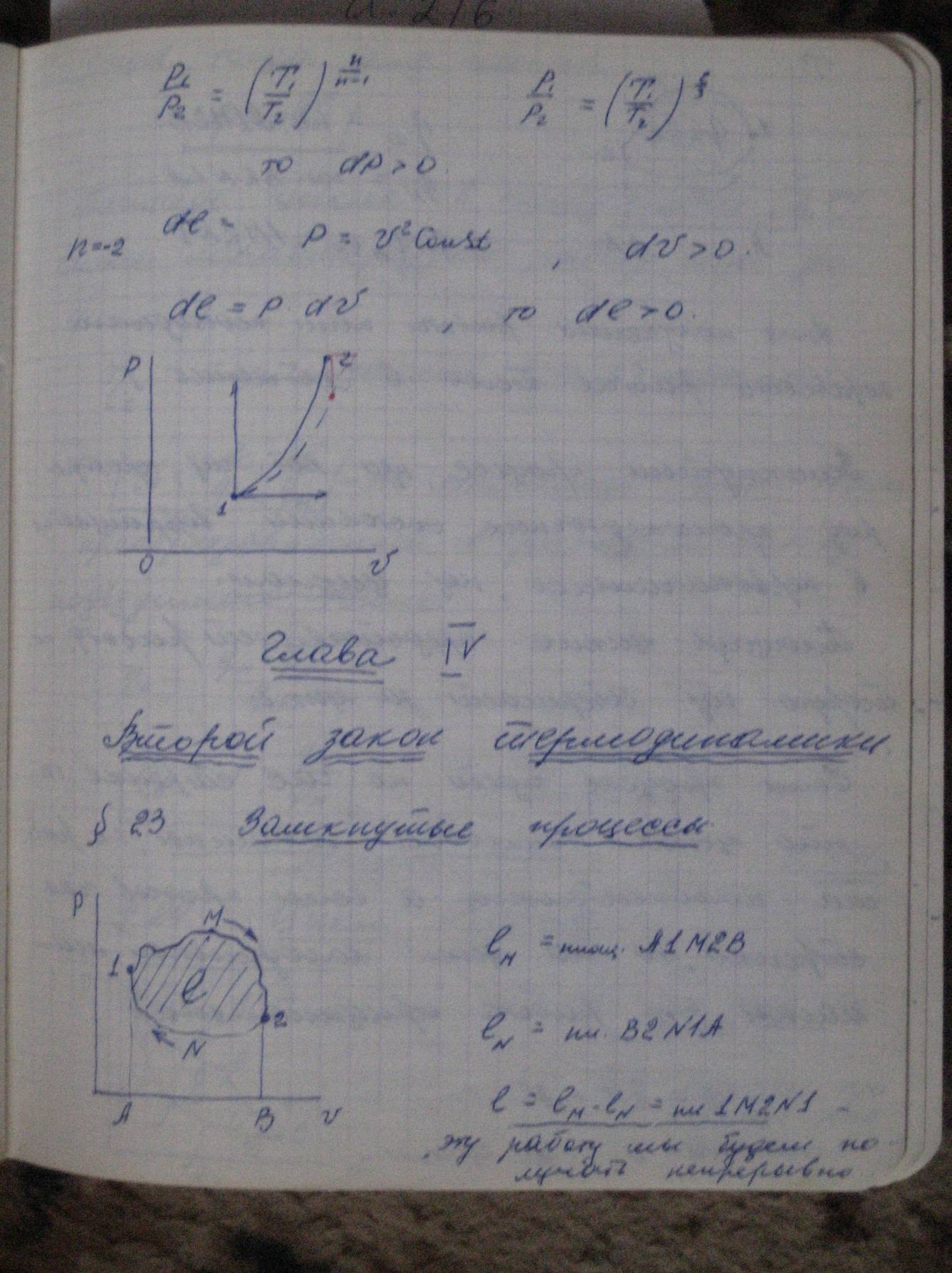
p2/p1=(T2/T1)n/(n-1) n/(n-1)>0 → dp>0
pvn =const , p=const/vn → dv<0
dl=pdv → dl<0.
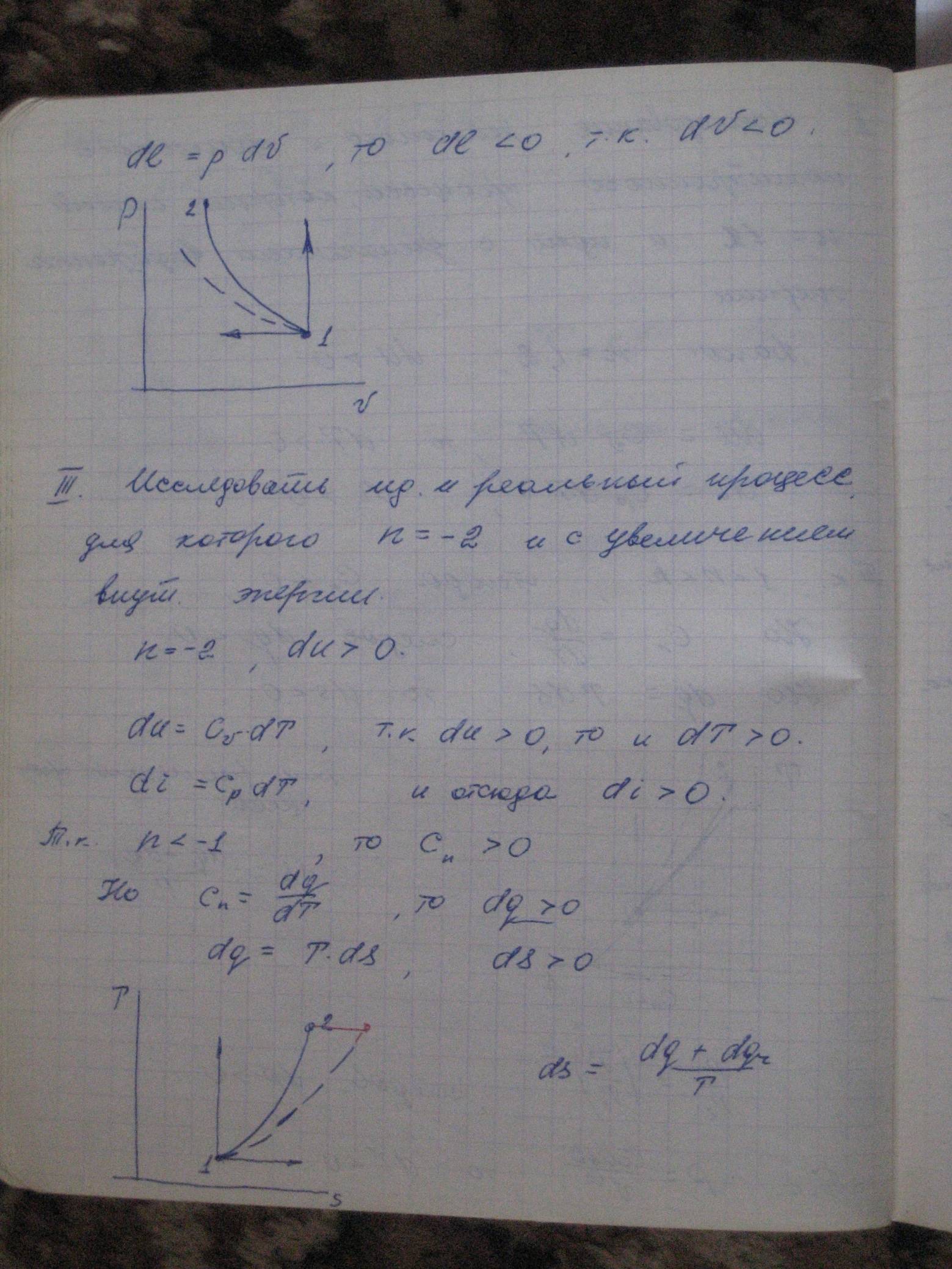
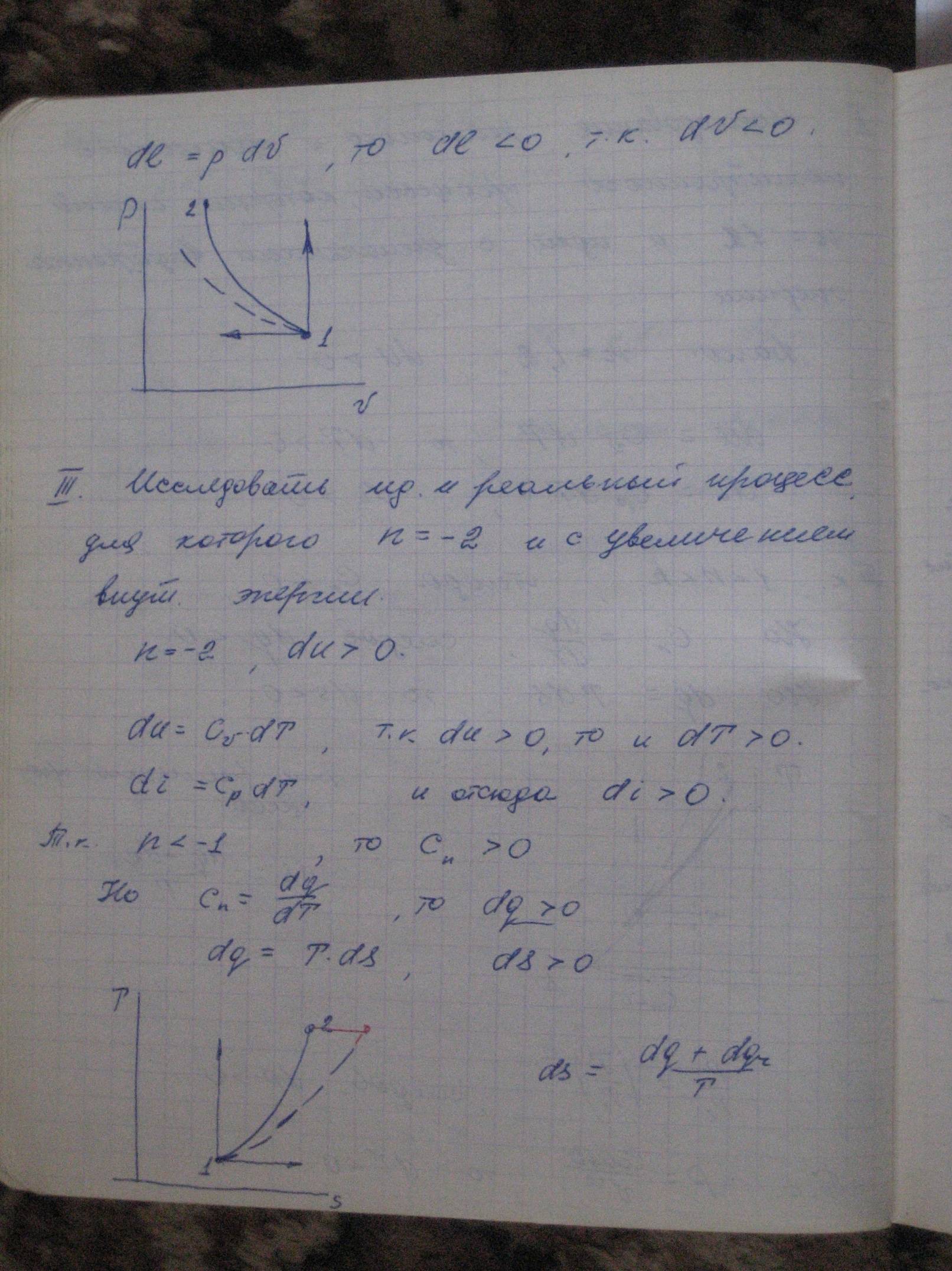 Исследовать
идеальный и реальный политропный
процесс, протекающий при n=-3
и идущий с увеличением внутренней
энергии.
Исследовать
идеальный и реальный политропный
процесс, протекающий при n=-3
и идущий с увеличением внутренней
энергии.
Дано:
n=-3;
pvn =const
du>0 ;
du=cvdT → dT>0 ;
di=cpdT → di>0
cn>0,т.к. теплоемкость отрицательна только в области 1<n<κ
dq=cndT → dq>0
ds=dq/T → ds>0
Для реального процесса:
p2/p1=(T2/T1)n/(n-1) n/(n-1)>0 → dp>0
pvn =const , p=const/vn → dv>0
dl=pdv → dl>0.
