
- •Миколаїв 2008
- •Рецензент: д.Ф.-м.Н., професор і.О. Муленко Вступ
- •1. Механіка
- •1.1 Кінематика поступального і обертального руху Система відліку. Траєкторія, шлях, переміщення.
- •Лінійна швидкість.
- •Лінійне прискорення.
- •Види поступального руху:
- •Кінематика обертального руху.
- •Зв'язок лінійних і кутових характеристик руху.
- •Приклади розв'язування задач.
- •Задачі для самостійної роботи.
- •1.2. Динаміка матеріальної точки. Перший закон Ньютона.
- •Механічні системи.
- •Імпульс.
- •Другий закон Ньютона.
- •Принцип незалежності дії сил.
- •Третій закон Ньютона.
- •Закон збереження імпульсу.
- •Закон руху центру мас.
- •Сили в механіці.
- •Робота, енергія, потужність.
- •Кінетична енергія.
- •Потенціальна енергія.
- •Закон збереження енергії.
- •Зіткнення.
- •Поле сил тяжіння.
- •Космічні швидкості.
- •Приклади розв'язування задач.
- •Задачі для самостійної роботи.
- •Робота сили. Закони збереження
- •1.3. Механіка твердого тіла Момент інерції.
- •Момент сили.
- •Момент імпульсу.
- •Основний закон динаміки обертального руху.
- •Кінетична енергія обертання.
- •Основні величини і співвідношення для поступального і обертального руху.
- •Приклади розв'язування задач.
- •Задачі для самостійної роботи. Основний закон динаміки твердого тіла.
- •Енергія обертального руху. Закони збереження
- •2. Молекулярна фізика та термодинаміка
- •2.1 Молекулярно-кінетична теорія ідеальних газів. Рівняння стану ідеального газу. Перший закон термодинаміки. Статистичний і термодинамічний методи дослідження.
- •Термодинамічна система.
- •Ідеальний газ.
- •Закон Бойля-Маріотта.
- •Закон Авогадро.
- •Закон Дальтона.
- •Закон Гей-Люссака.
- •Рівняння стану ідеального газу.
- •Основне рівняння молекулярно-кінетичної теорії ідеальних газів.
- •Закон Максвелла про розподіл молекул ідеального газу по швидкостям.
- •Барометрична формула.
- •Внутрішня енергія термодинамічної системи.
- •Число степенів вільності.
- •Перший закон термодинаміки.
- •Теплоємність.
- •Приклади розв'язання задач.
- •Задачі для самостійної роботи.
- •2.2 Адіабатний процес. Робота газу при різних процесах Явища переносу. Робота газу при його розширенні.
- •Адіабатичний процес. Рівняння Пуассона.
- •Робота газу в адіабатичному процесі.
- •Політропічні процеси.
- •Середня довжина вільного пробігу молекул.
- •Явища переносу.
- •Теплопровідність.
- •Дифузія.
- •Внутрішнє тертя (в’язкість).
- •К руговий процес (цикл).
- •Ккд кругового процесу. Цикл Карно.
- •Приклади розв'язання задач.
- •Задачі для самостійної роботи.
- •2.3 Другий закон термодинаміки. Рідини. Ентропія.
- •Статистичне тлумачення ентропії.
- •Другий закон термодинаміки.
- •Третій закон термодинаміки.
- •Реальні гази, рідини та тверді тіла.
- •Рівняння Ван-дер-Ваальса.
- •Внутрішня енергія реального газу.
- •Рідини та їх опис.
- •Поверхневий натяг.
- •Змочування.
- •Тиск під скривленою поверхнею рідини.
- •Капілярні явища.
- •Приклади розв'язання задач.
- •Задачі для самостійної роботи.
- •Додатки
- •1. Вектор.
- •9. Градієнт.
- •Основні фізичні постійні
Робота газу в адіабатичному процесі.
В
адіабатичному процесі
,
тому
![]() .
Якщо газ адіабатично розширюється від
об’єму V1
до V2,
то його температура зменшується від Т1
до Т2
і робота розширення ідеального газу
.
Якщо газ адіабатично розширюється від
об’єму V1
до V2,
то його температура зменшується від Т1
до Т2
і робота розширення ідеального газу
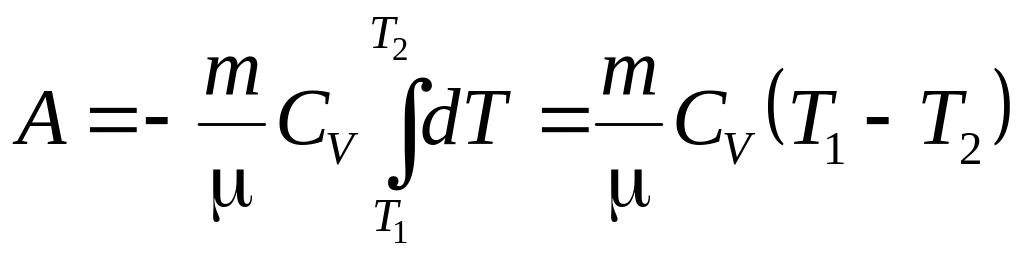
Звідки
отримуємо
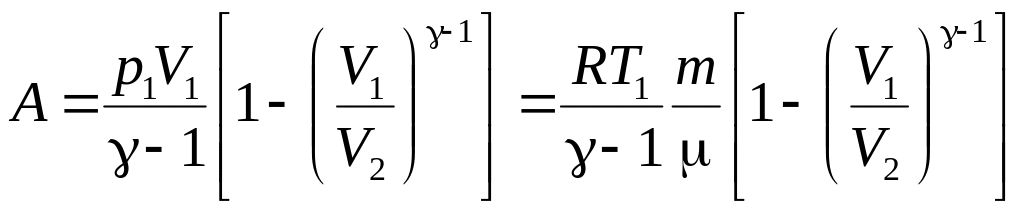 ,
використовуючи рівняння Менделєєва-Клапейрона
,
використовуючи рівняння Менделєєва-Клапейрона
![]() .
.
Робота адіабатичного розширення менше, чим при ізотермічному процесі. Це пояснюється тим, що при адіабатичному розширенні відбувається охолодження газу, тоді як при ізотермічному розширенні температура підтримується постійною за рахунок притоку ззовні еквівалентної кількості теплоти.
Політропічні процеси.
Узагальненням розглянутих вище процесів зміни стану ідеального газу є політропічний процес, який характеризується наступним рівнянням:
![]() ,
,
де
коефіцієнт
![]() називається показником політропи.
називається показником політропи.
Протягом політропічного процесу теплоємність залишається постійною (C = const). Ізохорний, ізотермічний, ізобарний і адіабатичний процеси є частинними випадками політропічного процесу.
Значення теплоємності і показника політропи для різних процесів наведені в таблиці.
Процес |
С |
n |
Адіабатичний |
С = 0 |
n = γ |
Ізотермічний |
С = ∞ |
n = 1 |
Ізобаричний |
С = Ср |
n = 0 |
Ізохорний |
С = СV |
n
=
|
Теплоємність
при ізотермічному процесі нескінченно
велика, оскільки dT
= 0,
в той час як
![]() .
.
Теплоємність
при адіабатичному процесі дорівнює
нулю, оскільки
![]() ,
в той час як
,
в той час як
![]() .
.
Середня довжина вільного пробігу молекул.
Відстань, яку в середньому проходять молекули між двома послідовними зіткненнями називається середньою довжиною вільного пробігу молекул . Величина є характеристикою всієї сукупності молекул газу, які задаються даними значеннями тиску та температури.
Мінімальна відстань, на яку зближуються при зіткненні центри двох молекул, називається ефективним діаметром молекули d.
Середнє число зіткнень, яке відбувається з однією молекулою газу за 1 с, можна виразити наступним чином:
![]() .
.
Звідки середня довжина вільного пробігу молекули
![]() ,
,
де n – концентрація молекул газу.
Явища переносу.
Однією з умов рівноважного стану термодинамічної системи є відсутність в ній потоків речовини та енергії. Якщо в газі існує просторова неоднорідність температури, густини або швидкості впорядкованого руху окремих шарів то виникають не обернені процеси спрямовані до вирівнювання вказаних неоднорідностей.
Явищами переносу називаються необоротні процеси в термодинамічно нерівноважних системах, в яких відбувається просторовий перенос енергії (теплопровідність), маси (дифузія), імпульсу (внутрішнє тертя).
Для спрощення обмежимося розглядом одномірних випадків, вибираючи ось OX таким чином, щоб вона була спрямована в напрямку переносу. Будемо розглядати потоки енергії, речовини і імпульсу впорядкованого руху частинок крізь площадку одиничної величини, розташовану перпендикулярну вісі OX, для ідеального газу густина якого ρ.
Теплопровідність.
Якщо в одній області газу середня кінетична енергія молекул більше, ніж в другій, то протягом часу внаслідок постійних зіткнень молекул відбувається процес вирівнювання середніх кінетичних енергій молекул – вирівнювання температур.
Перенос енергії (в формі теплоти) описується законом Фур’є:
![]() ,
,
де qE – густина потоку енергії – теплова енергія, яка переноситься за одиницю часу крізь одиничну площадку, перпендикулярну осі OX;
![]() – коефіцієнт
теплопровідності;
– коефіцієнт
теплопровідності;
![]() – градієнт
температури – швидкість зміни температури
на одиницю довжини OX
в
напрямку нормалі до цієї площадки;
– градієнт
температури – швидкість зміни температури
на одиницю довжини OX
в
напрямку нормалі до цієї площадки;
cV – питома теплоємність газу при постійному об’ємі;
