
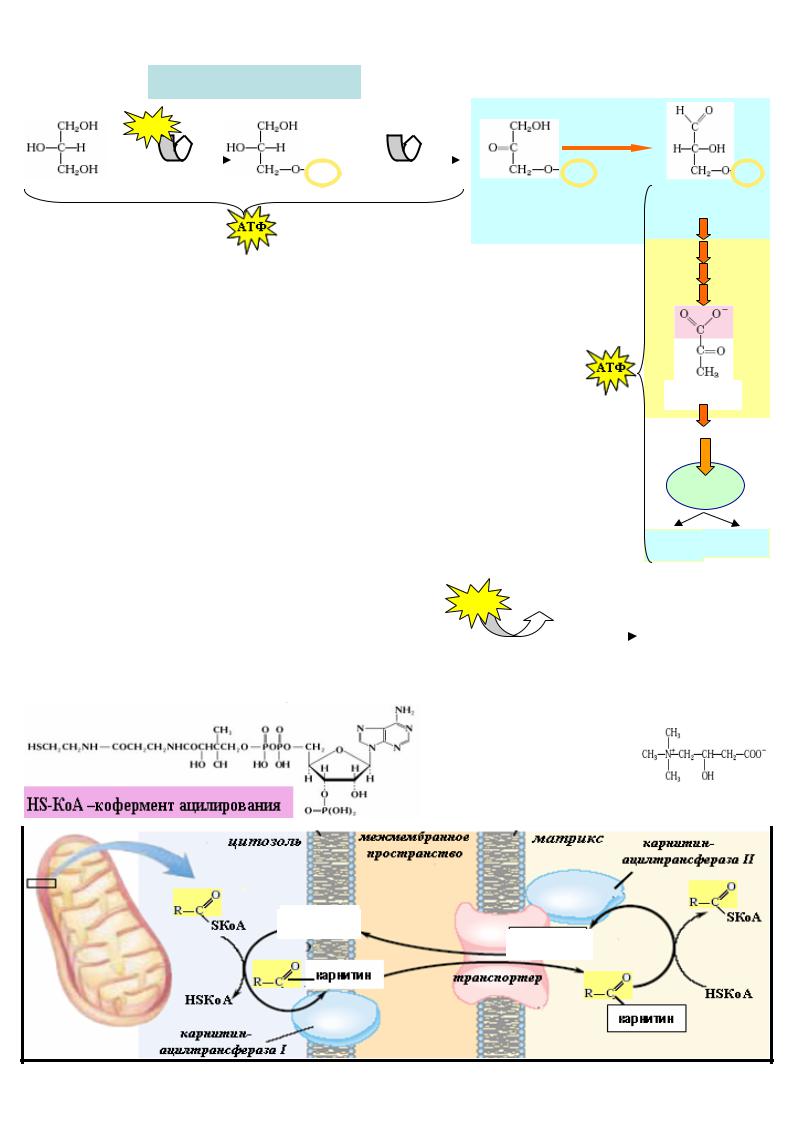
Окиснення гліцерину
|
|
АТФ АДФ |
|
|
|
|
НАД+ НАДН |
|
|
|||
|
|
|
|
|
P |
|
- |
P |
|
|||
|
|
гліцерол- |
|
|
фосфогліцерол |
|
||||||
гліцерин |
кіназа |
фосфогліцерол |
|
дегідрогеназа фосфодіоксі- |
|
|||||||
|
|
2 |
|
|
|
|
|
|
ацетон |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Гліцерин активується шляхом фосфорилювання (витрачається 1 |
|
|||||||||||
АТФ). Фосфогліцерол , що утворився , |
далі |
дегідрується з |
|
|||||||||
утворенням |
НАДН , котрий |
окиснюється у мітохондріальному |
|
|||||||||
дихальному ланцюзі . Окиснення НАДН поєднано зсинтезом |
|
20 |
||||||||||
3 АТФ . |
Фосфодіоксіацетон , метабол іт гл іколізу, перетво - |
|||||||||||
|
||||||||||||
рюється у 3-фосфогліцеральдегід , котрий окиснюється у другій |
|
|||||||||||
стадії гліколізу до пірувату . На даному етапі |
утворюється |
3 |
|
|||||||||
АТФ за рахунок окисного фосфорилювання і |
2 АТФ – шляхом |
|
||||||||||
субстратного фосфорилювання . У аеробних у мовах |
піруват |
|||||
окиснюється до ацетил -КоА з утворенням |
|
3 АТФ. Ацетил -КоА |
||||
«згорає» в ЦТК до СО |
2 і Н2О з утворенням 12 АТФ . Таким |
|||||
чином, при окис ненні |
гліцерину до к |
інцевих продукт ів |
||||
утворюється 22 АТФ. |
|
|
|
|
|
|
|
|
|
||||
|
Окиснення вищих жирних кислот |
|
|
|||
1. Активація ВЖК у цитозолі клітин: |
|
|
АТФ |
АМФ + ФФ |
||
|
RCOOH + HSKoA |
|
|
|
|
|
|
|
ацил-КоА-синтетаза |
||||
|
|
|
|
|
||
P
3-фосфогліцер- альдегид
піруват
ацетил -SКоА
ЦТ
К
Н2О СО2
R-CO- SKoA
2. Перенесення ацилКоА із цитозоля в матрикс мітохондрій за допомогою карнітину:
|
Окиснення ВЖК відбувається у мітохондріях, але |
|||||||
|
внутрішня мембрана мітохондрій непроникна |
|||||||
|
для ацил-КоА,тому ацил |
|
|
|
|
|
|
|
|
переноситься |
|
|
|
|
|
|
|
|
карнітином , котрий працює |
за |
|
|||||
|
човниковим принципом . |
|
|
|
|
|
|
|
|
|
карнітин |
|
|||||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
карнітін |
|
||||
|
міжмембранний |
|
|
|
||||
|
простір |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
карнітін
|
|
|
карнітін |
||
|
|
|
|
|
|
|
|
карнітін |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
карнітін |
|
карнітін |
|
|
|
81 |
|
|
|
|
|
||
|
|
|
|
||
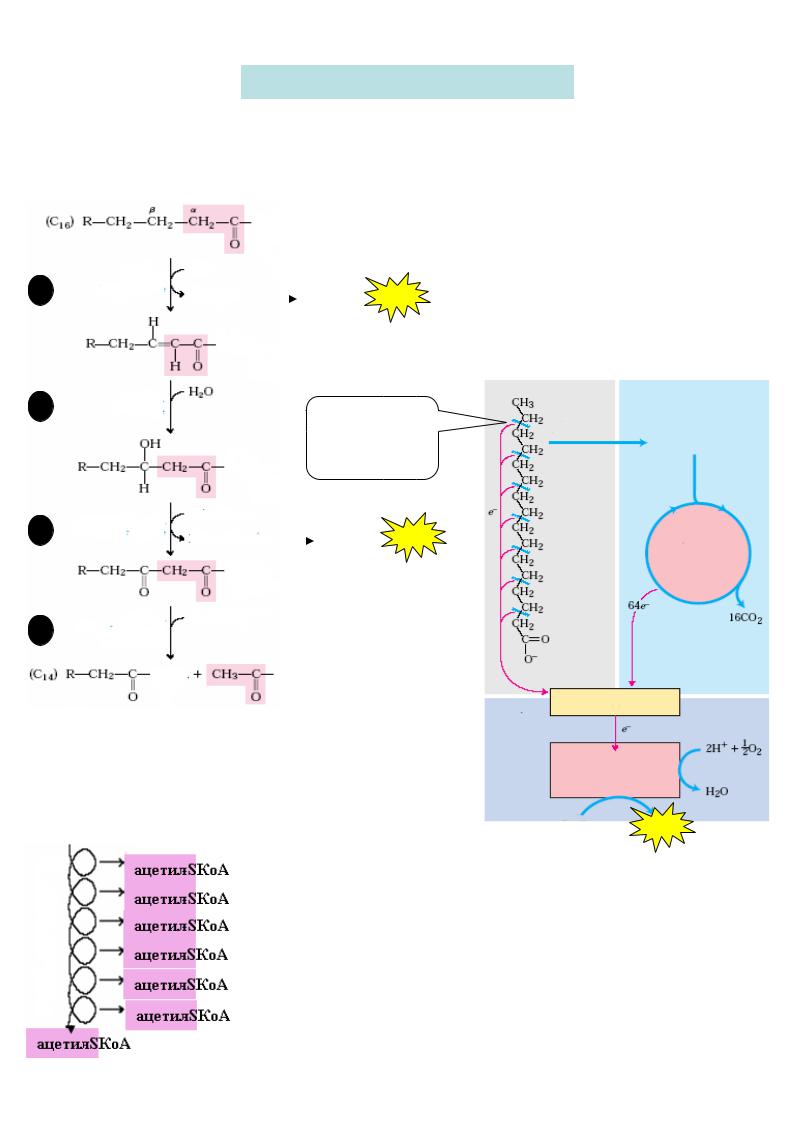
β-окиснення вищих жирних кислот
Мітохондріальне окиснення вищих жирних кислот(ВЖК) відбувається у три стадії. У 1 стадії (β-окиснення) ВЖК окиснюється з відщепленнямдвовуглецевого фрагменту у вигляді ацетил -SКоА, починаючи відкарбоксильного кінця ацилу, що окиснюється .
|
|
|
|
|
|
|
|
|
|
|
|
Наприклад, при оки |
|
сненні |
||||
|
|
|
|
|
|
|
|
|
|
|
|
пальмітинової кислот |
и |
(n=16) |
||||
|
|
|
S-КоА |
|
|
|
|
утворюється |
n/2=8 молекул ацетил - |
|||||||||
|
|
|
пальмітоїл- S-КоА |
|
SКоА, кот рі включаються у |
|
2 |
|||||||||||
1 |
ацил-SКоА- |
ФАД |
|
|
|
|
стадію окис нення ВЖК - цикл |
|
|
|||||||||
дегідрогеназа |
|
ФАДН2 |
|
|
|
|
в ЦПЭ 2АТФ |
Кребса . На цій стадії ацетиль |
ні |
|||||||||
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
групи окис |
нюються до СО |
2 |
і |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
S-КоА |
|
|
|
|
постачають |
атоми |
водню |
у |
|||||||
|
|
|
еноїл- S-КоА |
|
|
дихальний ланцюг. |
|
|
|
|
||||||||
2 |
еноїл-SКоА- |
|
|
|
|
|
|
|
|
кількість |
|
Стадія 1 |
Стадія 2 |
|
|
|||
гідратаза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
β-окиснення |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
циклів |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
8 ацетил -SКоА |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
S-КоА |
|
|
β-окиснення |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
(n/2-1)=7 |
|
|
|
|
|
|
|
||||||
β-оксіацил-SКоА- |
|
β-оксіацил- S-КоА |
|
|
|
|
|
|
|
|
||||||||
НАД+ |
|
|
|
|
|
|
|
|
|
|
|
|||||||
3 дегідрогеназа |
|
|
|
3АТФ |
|
|
|
|
|
|
|
|||||||
|
+ |
|
|
|
|
|
в ЦПЭ |
|
|
|
|
|
|
|
||||
|
|
|
НАДНН |
|
|
|
|
|
|
|
|
ЦТК |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
S-КоА |
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
β-кетоацил - |
|
|
|
|
|
|
|
|
|||||||
4 |
тіолаза |
НS-КоА |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
S-КоА |
|
S-КоА |
ацил-S-КоА |
|
|
ацетил |
-SКоА |
|
|
|
|
Ці чотири послідовні реакц ії (цикл β-окиснення) повторюються стільки разів, поки вся жирна кислота з парною кількістю атомів вуглецю (n), не перетвориться в n/2 молекул ацетил -SКоА:
НАДН , ФАДН2 Стадія 3
ланцюг
перенесення
електронів
АДФ+Ф АТФ
С14 |
У 3 стадії атоми водню від НАДН2 і ФАДН2 надходять у дихальний |
|||
С12 |
ланцюг і відновлюють кисень з утворенням води (жири – джерела |
|||
ендогенної води ). |
Енергія окиснення |
ВЖК конверт ується у |
||
|
||||
С10 |
молекули АТФ. При окис ненні 8 молекул ацетил -КоА утворюється |
|||
С8 |
8х12=96 молекул |
АТФ. Відбувається |
7 цикл ів окис нення |
|
пальмітинової кислоти .В кожному з них утворюються по 5 молекул |
||||
С6 |
АТФ за рахунок окиснення НАДН и ФАДН), тобто 7х5=35 молекул |
|||
АТФ. Сумарно : 141-1* = 140 АТФ. |
2 |
|||
|
||||
С4 |
|
|||
(* 1 молекула АТФвитрачена на активацію ВЖК). |
||||
82
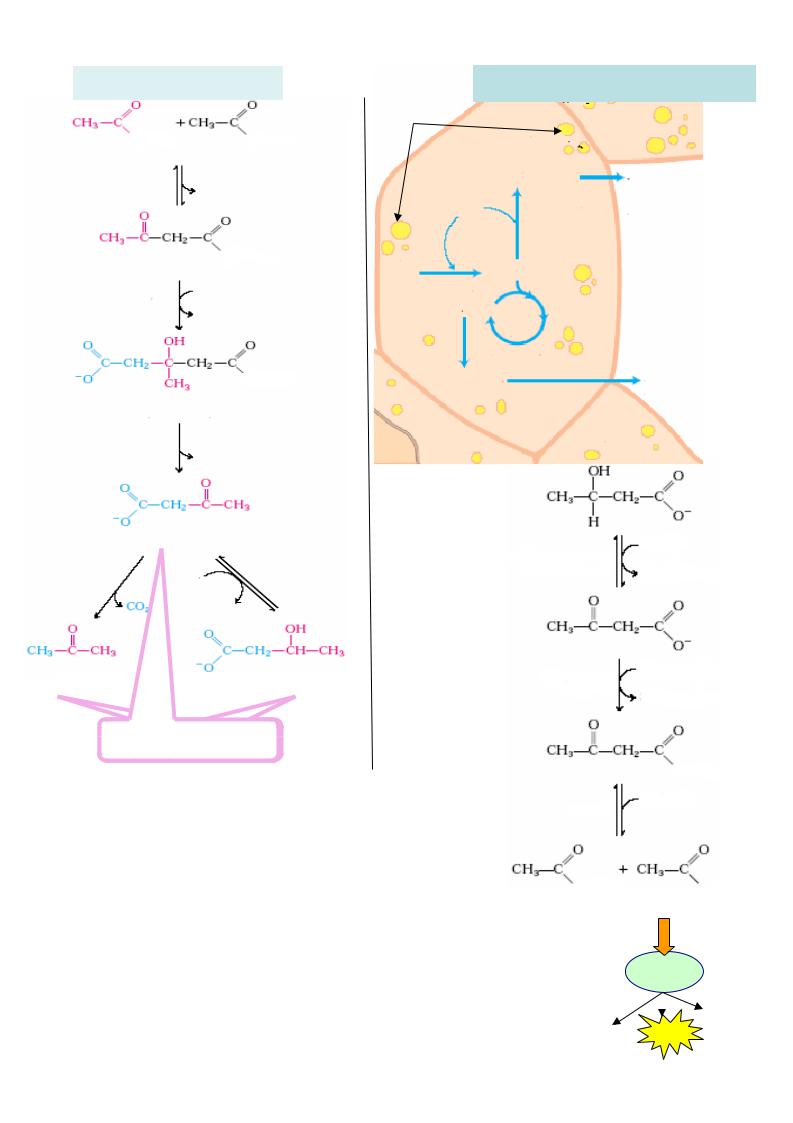
Синтез кетонових тіл
SКоА SКоА 2 ацетил -SКоА
тіолаза
НSКоА
SКоА ацетоацетил -SКоА
ОМГSКоА- ацетил -SКоА
синтетаза НSКоА
Метаболізм кетонових тіл
ліпідна
крапля
кетонові тіла
НSКоА
ВЖК ацетил -SКоА
оксалоацетат ЦТК
ацетоацетат і β- гідроксибутират
експортуються у якості джерел енергії для скелет -
них м’язів, серця, мозку.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
глюкоза |
|
||||
|
|
|
|
|
|
|
SКоА |
|
|
|
|
глюкоза |
експортується |
||||||||||||
β-окси-β-метилглутарил -SКоА(ОМГ-SКоА) |
|
|
гепатоцит |
|
у якості паль- |
||||||||||||||||||||
|
|
ного для мозку |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
ОМГSКоА- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
та інших |
|||||
|
|
ліаза |
ацетил -SКоА |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тканин |
|||||||
|
|
|
|
|
Утилізація |
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
кетонових тіл |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
ацетоацетат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
β-оксибутират |
|
|
|
|
|
НАД+ |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
НАДН |
β-оксибутират |
|
|
|
|
|
β-оксибутират |
|
|
|
НАДН |
|
||||||||
|
|
|
|
|
дегідрогеназа |
|
|
|
|
|
дегідрогеназа |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
НАД+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ацетоацетат |
|
сукцинілSКоА |
||||||||
|
ацетон |
|
|
|
|
β-оксибутират |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
β-кетоацилКоА |
сукцинат |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
трансфераза |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
ккетоновтоновыеітілатела |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Кетонові тіла синтезуются т |
ількі |
у |
печінці |
ацетоацетил -SКоА |
|
|
SКоА |
|
|||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||
(перша реакц ія – у цитозол і, інші – |
у мітохондріях |
|
тіолаза |
НSКоА |
|
||||||||||||||||||||
гепатоцитів), |
але вони ніколи не використовуються у |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
печінці. Кетонові тіла дифундують у |
кров і викорис - |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
товуються як |
альтернативне метаболічне паливо |
|
SКоА |
|
|
|
SКоА |
||||||||||||||||||
для позапечінкових |
|
органів і |
тканин: м |
іокарда, |
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
скелетних м ’язів, коркового шару наднирників та за |
|
|
|
2 ацетил -SКоА |
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
умов голодування - |
для мозку. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
У |
нормі концентрація кетонових тіл у крову невелика (10-20 мг/ |
ЦТ |
|
||||||||||||||||||||||
л), |
але вона суттєво |
|
підвищується при голод |
уванні та |
К |
|
|
|
|
||||||||||||||||
|
|
|
|
||||||||||||||||||||||
|
СО2 |
||||||||||||||||||||||||
цукровому діабеті. Це призводить до кетонемії, кетоацидозу та |
|
|
|
|
|||||||||||||||||||||
|
АТФ |
||||||||||||||||||||||||
кетонурії. |
|
|
|
|
|
|
|
|
|
|
|
|
Н2О |
|
|
83 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
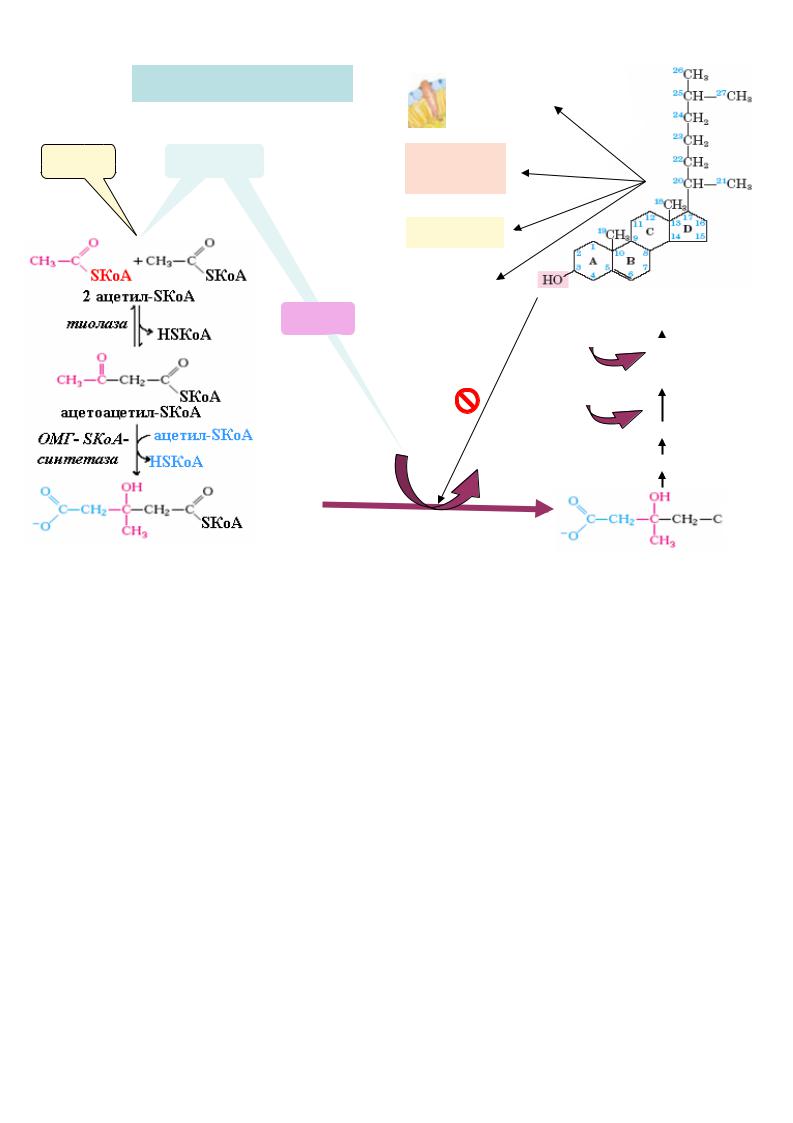
Синтез холестерину
біомембрани
ВЖК |
глюкоза |
стероїдні |
|
|
гормони |
вітамін D3
|
|
|
|
|
|
|
жовчні |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
холестерин |
|
||||||
|
|
|
ПФШ |
|
|
кислоти |
|
|
|
|
|
||||||
|
тіолаза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
НАДФН+ |
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
НАДФН+ |
ланостерин |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
сквален |
|||
|
|
|
|
|
|
2НАДФ+ |
ізопентенілдифосфат |
||||||||||
|
|
|
|
2(НАДФН+Н+) |
|||||||||||||
|
|
|
|
|
ОМГSКоАредуктаза |
|
|
|
|
|
Н2ОН |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
β-окси- β-метилглутарил -SКоА (ОМГ-SКоА) |
|
мевалонова |
кислота |
||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
Синтез |
ендогенного холестерин |
у переважно відбувається у |
печінці |
(50-80%), |
|||||||||||||
кишечнику (10-15%), а також у |
шкірі (до 5%), корі наднирників і репродуктивн их |
||||||||||||||||
органах . |
Біосинтез холестерин у |
починається з |
ацетил -КоА. |
Вуглецевий скелет |
|||||||||||||
С27стерину будується з С2- ланок у результаті складної послідовності реакцій. |
|||||||||||||||||
Біосинтез холестерину складається з чотирьох етапів. |
|
|
|
|
|
|
|
||||||||||
На першому етапі з трьох молекул ацетил -КоА утворюється мевалонат (С6). Перші реакції повністю співпадають із синтезом кетонов их т іл до ОМГSКоА, але вони локалізовані у цитозолі гепатоцитів. Далі ОМГ -SКоА відновлюється до мевалонової кислоти. Регуляторн ий фермент цього синтезу - ОМГ-SКоА-редуктаза ,коферментом котрого є НАДФН+Н+ (головне джерело НАДФН+Н+ - пентозофосфатн ий шлях окиснення глюкози). Активність цього ферменту інгібується холестерином і ЛПНЩ за принципом негативного зворотного зв’язку. Кім того, цей фермент також інгібується шляхом фосфорилювання (активна його дефосфорильована форма ).
На другому етапі мевалонат п еретворюється у |
« активний ізопрен » - |
ізопентенілдифосфат . |
|
На третьому етапі шість молекул ізопрену полімеризуються з утворенням сквалену
(С30).
На четвертому етапі сквален циклізується у ланостерин (С30), від котрого
|
відщеплюються три метильні групи та утворюється холестерин (С27). На схемі |
84 |
показани найбільш важливі проміжні продукти цього біосинтезу. |
|
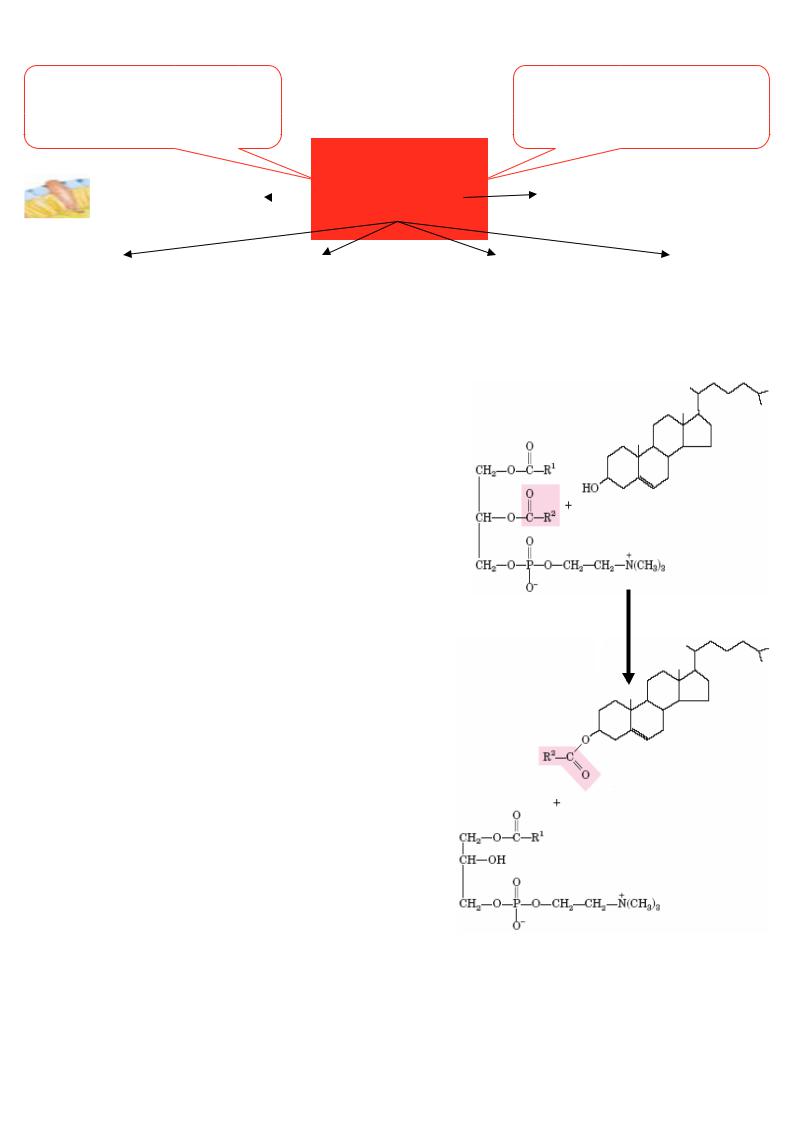
|
Надходження з їжею |
|
|
|
|
|
|
|
|
|
Синтез із ацетилКоА |
||||||||||
|
(екзогенний холестерин) |
|
|
|
|
|
|
|
|
(ендогенний холестерин) |
|||||||||||
|
0,3-0,5 г на добу |
|
|
|
|
|
|
|
|
|
|
|
до 1 на добу |
||||||||
|
|
|
|
|
|
|
фонд холестерину |
|
|
|
|
|
|
||||||||
|
структура мембран |
|
|
|
синтез стероїдних |
||||||||||||||||
|
|
|
|
|
в організмі |
|
|
||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
і ліпопротеїнів |
|
|
|
|
|
гормонів ~40 мг на добу |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
синтез |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
синтез |
|
||||
|
|
|
|
|
екскреція |
|
|
|
|
екскреція з |
|
|
|
|
|||||||
|
жовчних кислот |
|
|
|
з фекаліями |
|
|
шкіряним салом |
|
|
вітаміну D3 |
|
|||||||||
|
~ 1,0-1,3 г на добу |
|
~0,5-0,7 г на добу |
|
|
~ 0,1 г на добу |
|
|
~10мг на добу |
|
|||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
Фонд холестерину складається з: |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
вільного холестерину – найбільша |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
фракц ія, до котрої належать |
холестерин |
|
|
|
|
|
|
|
|
|||||||||||
мембран і оболонки |
ліпопротеїнів крові. |
|
|
|
|
|
|
|
|
||||||||||||
ефірів холестерину – гідрофобних молекул , |
|
|
|
|
|
|
|
|
|||||||||||||
|
котрі є запасною формою холестерину у |
|
|
|
|
|
|
|
|
||||||||||||
|
організмі. Вони знаходяться у ліпідних крап- |
|
|
|
|
|
|
холестерин |
|||||||||||||
лях цитозолю клітин і |
ядрах ліпопротеїнів . |
|
|
|
|
|
|
|
|
||||||||||||
|
Ефіри утворюються в реакції етерифікації |
|
|
|
|
|
|
|
|
||||||||||||
|
холестерину з ненасиченою жирною |
|
|
|
|
|
|
фосфатидилхолін (лецитин ) |
|||||||||||||
|
кислотою (із лецитину) за допомогою |
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
ферменту лецитинхолестеролацил- |
|
|
|
|
|
лецитинхолестерол - |
|
|
||||||||||||
|
трансферази (ЛХАТ) або в реакції ацилювання |
|
|
|
|||||||||||||||||
|
|
ацилтрансфераза |
|
|
|||||||||||||||||
|
холестерин у за допомогою |
|
ацил-КоА та |
|
(ЛХАТ) |
|
|
||||||||||||||
ацилхолестеролацилтрансферази (АХАТ). |
|
|
|
|
|
|
|
|
|||||||||||||
В организм і |
дорослої людини |
міститься |
|
|
|
|
|
|
|
|
|||||||||||
приблизно 140 г холестерин у, з |
|
котрих |
більш |
|
|
|
|
|
|
ефір |
|||||||||||
ніж 90% міститься у |
ткан инах, особ ливо у |
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
холестерину |
|||||||||||||||
нервовій, м’язовій, сполучній і жировій, а також |
|
|
|
|
|
|
|||||||||||||||
у наднирниках. До 10% холестерину міститься у |
|
|
|
|
|
|
|
|
|||||||||||||
плазмі кров і та |
лімфі у складі |
|
ліпопротеїнів |
|
|
|
|
|
|
|
|
||||||||||
(складова частка |
у |
вигляді ефірів ). |
З віком |
|
|
лізофосфатидилхолін |
|||||||||||||||
холестерин накопичується у организм і, |
тому у |
|
|
||||||||||||||||||
дорослих концентрац ія холестерин у |
у плазм і |
|
|
|
|
|
|
|
|
||||||||||||
крови вище у порівнянні з дітлахами і складає в |
|
|
|
|
|
|
|
|
|||||||||||||
нормі 3,88 – 6,46 |
ммоль /л. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Холестерин – дуже важлива сполука у організмі людини . Крім структурної функції (компонент клітинних мембран ), холестерин є попередником багатьох біологічно значущих речовин: стероїдних гормонів (кортикостероїдів, статевих гормонів ),
антирахітичного вітаміну D3, а та кож жовчних кислот , т обто |
усіх стеро їдів у |
організмі. |
85 |
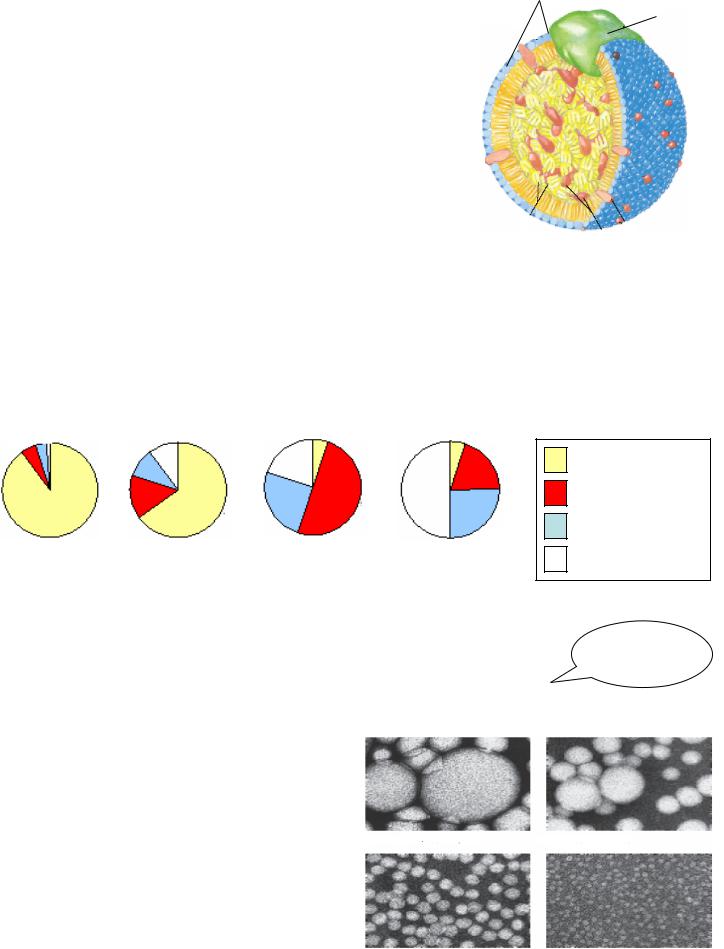
Ліпопротеїни – транспортні форми ліпідів |
|
фосфоліпіди |
|||||||||
|
|
|
|
|
|
|
|
|
|
апоВ-100 |
|
Усі ліпіди надходять у плазму у вигляді |
|
|
|
|
|||||||
|
|
|
|
|
|||||||
макромолекулярних |
комплексів , котрі називаються |
|
|
|
|||||||
ліпопротеїнами . |
Ліпопротеїни |
(ЛП) – |
це сферичні |
|
|
||||||
частинки, |
що складаються з |
гідрофобного ядра |
й |
|
|
||||||
амфіфільної оболо |
нки. Ядро |
|
містить неполярн |
і |
|
|
|||||
триацилгліцериди (ТАГ) та ефіри холестерину. Оболонка |
|
|
|||||||||
складається |
з полярн |
их л іпідів |
- |
холестерину |
та |
|
|
||||
фосфоліпідів. Заряджені кінці |
цих молекул |
спрямовані |
|
|
|||||||
назовні. Кр ім того, |
до складу |
оболо нки входят ь білки |
ТАГ |
холестерин |
|||||||
(апопротеїни ), нековалентно зв’язані з |
фосфоліпідами та |
||||||||||
ефіри холестерину |
|||||||||||
холестерином. Існують апопротеїни А, В, С, D і E. |
|
|
|
||||||||
Функції апопротеїнів: |
структурна, активація ЛП-ліпази, рецепторна . |
Циркулюючи у |
|||||||||
крові, ліпопротеїни обмінюються між собою поверхневими ліпідами та апопротеїнами. Апопротеїни служат ь "візитною карт кою" л іпопротеїнів, тому що ліпопротеїнові рецептори у різних тканинах та органах розпізнають тільки специфічні апопротеїни .
ХМ |
ЛПДНЩ |
ЛПНЩ |
ЛПВЩ |
|
|
|
|
|
|
ліпопротеїни |
ліпопротеїни |
хіломікрони |
ліпопротеїни |
||||||
|
|
дуже низької |
|
|
низької |
высокої |
|
|
|
|
|
|
|||
|
|
|
щільності |
|
|
щільності |
щільності |
|
|
|
|
|
|
|
|
транспорт |
|
|
транспорт |
|
|
транспорт |
транспорт |
ліпідів |
|
|
ліпідів, |
|
|
холестерину |
холестерину |
із клітин |
|
|
котрі син- |
|
|
до тканин |
із тканин у |
кишечника |
|
|
тезується |
|
|
атерогенні |
печінку |
|
|
|
у печінці |
|
|
антиатерогенні |
Існує декілька клас ів ліпопротеїнів в залежності від їхньої густини (визначається ультрацентрифугуванням) та електрофоретичною рухомістю . Щільність ліпопротеїнової частинки оцінюється за співвідношенням апопротеїни/ліпіди: чим більше білку , т им в ище густина. Електрофоретична рухомість за лежить від вмісту апопротеїнів і полярних 86 ліпідів.
Хіломікрони (х60000)
ЛПНЩ (х180000)
тригліцериди
холестерин
фосфоліпіди
апопротеїни
функції
ЛП
ЛПДНЩ (х180000)
ЛПВЩ (х180000)
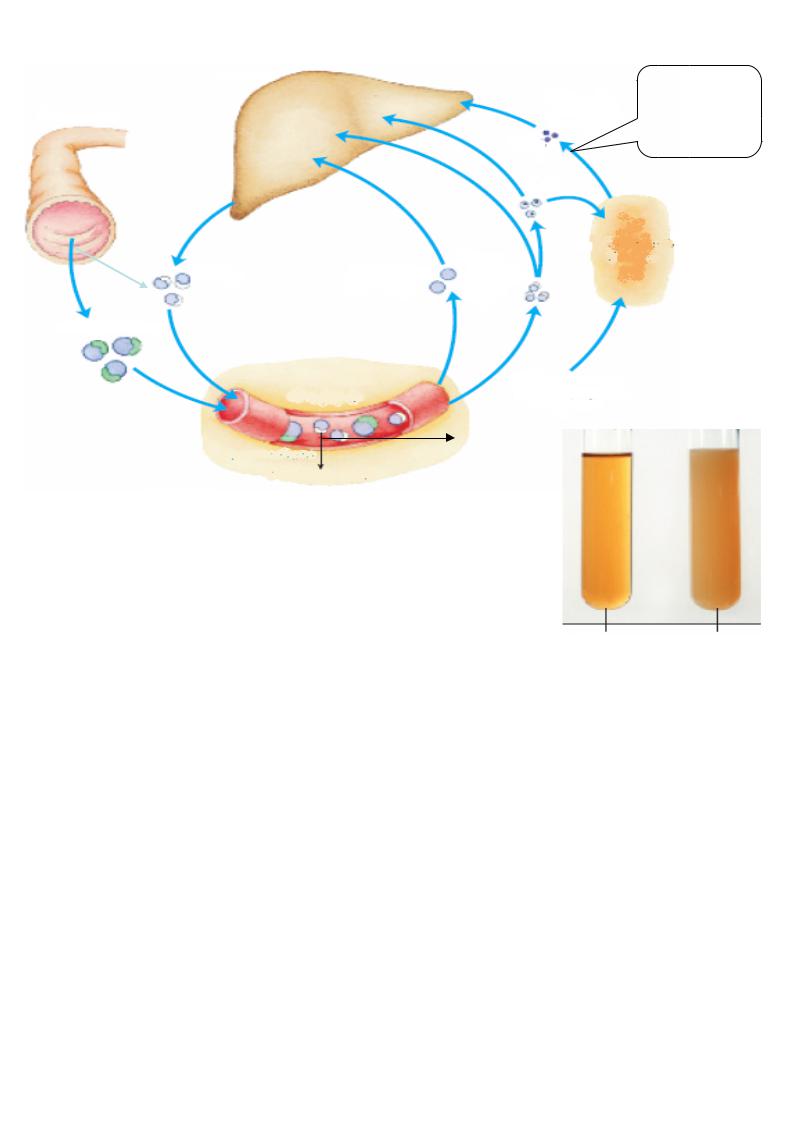
|
|
зворотний |
печінка |
|
транспорт |
|
ЛПВЩ холестерину |
|
кишечник |
|
до печінки |
|
|
|
|
|
ЛПНЩ |
|
|
поза- |
|
остат. |
печінкові |
ЛПДНЩ |
тканини |
|
ХМ |
остат. |
|
|
|
ЛПДНЩ |
ХМ |
|
попередники ЛПВЩ |
капіляр |
|
(із печінки та кишечника) |
ВЖК
ліпопротеїнліпаза жирова тканина, м’язи
Усі ліпопротеїни беруть участь у транспорті холестерину та його ефірів по крові та їхнім розподіленням по органам .
Хіломікрони транспортують екзогенний холестерин із кишечника до печінки.
ЛПДНЩ утворюються у печінці(в невеликій кількості – у
кишечнику) |
та транспорт |
ують екзота ендогенний |
холестерин |
(поряд із іншими |
ліпідами) до ткан ин. Обидві |
форми ліпопротеїнів (ХМ і ЛПДНЩ) швидко розпадаються (півперіод їхнього життя складає 1,5 – 2 години).
плазма крові |
плазма |
після |
крові після |
голодування |
прийому |
|
жирної їжі |
Ліпопротеїнліпаза (ЛП-ліпаза) розщеплює ТАГ у складі хіломікронів і ЛПДНЩ на поверхні ендотелію капілярів з наступним перетворенням цих частинок у остаткові хіломікрони та остаткові ЛПДНЩ, відповідно. Ці частинки поглинаються у печінці за механізмом ендоцитозу завдяки наявності специфічних рецепторів .
Далі ТАГ оста ткових ЛПДНЩ розщеплюються ЛП-ліпазою, після чого вони перетворюються у ЛПНЩ. ЛПНЩ відрізняються від своїх попередників не тільки збільшеним вмістом холестерин у (у вигляді ефірів), але й складом апопроте їнів. Це
основний клас ліпопротеїнів, котрі переносять холестерин не тільки до печінки, але й до позапечінкових тканин та органів для його подальшого використання . ЛПНЩ називаються атерогенними, тому що вони сприяють розвиткуатеросклерозу.
ЛПВЩ утворюються із своїх попередників у печінці та «дозрівають» у кров і. Завдяки своєї здатності «вытягати» на себ е із клітин мембранний холестерин , ЛПВЩ забезпечують його зворотний транспорт до печінки , тому вони називаються антиатерогенними ліпопротеїнами (перешкоджають розвитку атеросклерозу).
87
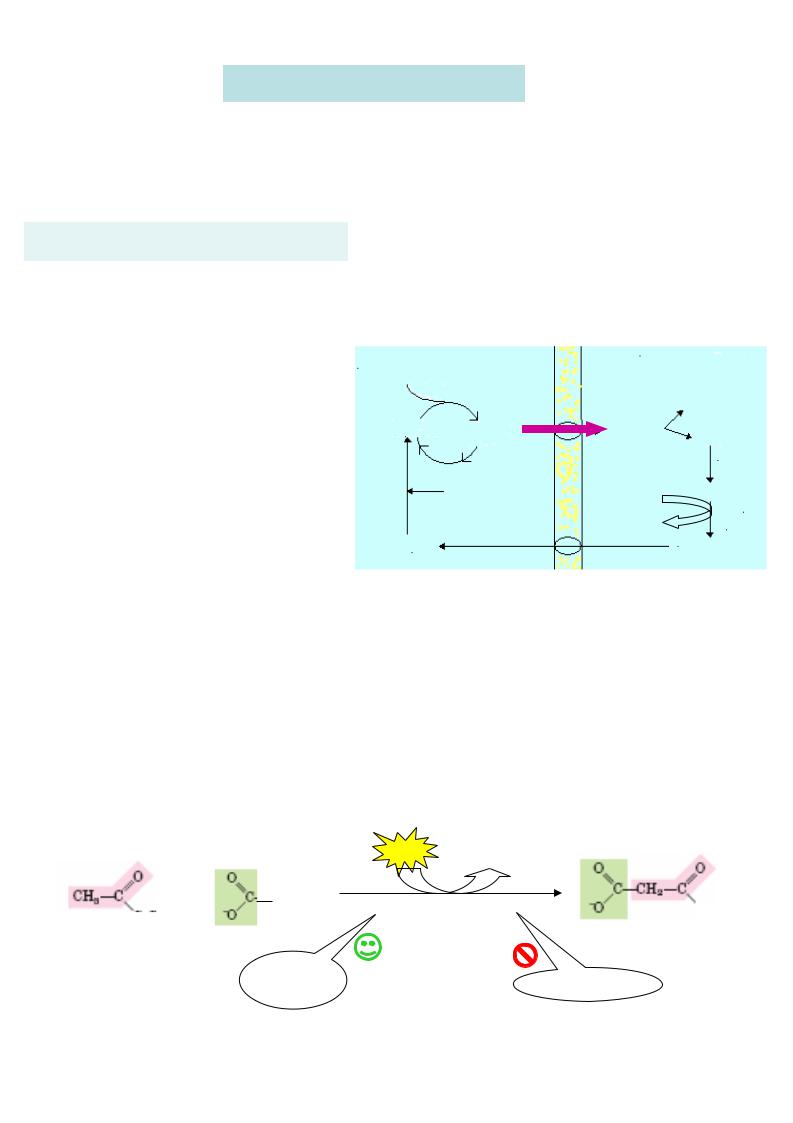
Біосинтез ліпідів - ліпогенез
Ліпогенез спрямований на акумуляцію у організмі людини резерв ів метабол ічного пального у вигляді триацилгліцеридів і на оновлення структурних компонентів біомембран шляхом синтез у фосфоліпідів, сф інголіпідів. Складовою частиною цього процесу є біосинтез жирних кислот, котрий найбільш активно відбувається у жировій тканині, печінці, молочній залозі пад час лактації.
Синтез вищих жирних кислот |
пальмітинова кислота (С16), |
В орган ізмі людини переважно синтезується |
безпосереднім донором дв овуглецевих фрагмент ів є ацетил -КоА, що утворюється при аеробному окисненні глюкози у мітохондріях клітин . Реакції синтезу локалізовані у цитозолі клітин, але внутрішня мембрана мітохондрій непроникнадля ацетил -КоА.
матрикс цитозоль
Перенесення |
ацетил у із |
|
ацетил -КоА |
|
|
|
|
|
|
|
|
|
|
ацетил -КоА |
|
||||||
мітохондрій у цитозоль здійсню - |
|
|
|
|
|
|||||
оксалоацетат цитрат |
|
|
|
|
|
|||||
|
|
|
|
|
||||||
ється за допомогою |
човникового |
цитрат |
оксалоацетат |
|||||||
механізму. Спочатку у мітохонд - |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|||
ріальному матриксі із ацетил -КоА і |
|
СО2 |
|
|
|
малат |
||||
оксалоацетату утворюється цитрат, |
|
НАДФ+ |
|
|||||||
|
|
|
|
|||||||
котрий проходи ть крізь |
мембрану |
|
|
|
НАДФН+ |
|
|
|
||
мітохондрій , |
і саме |
він є |
|
піруват |
|
|
|
піруват |
||
переносником ацетилу у цитозоль.
Оксалоацетат повертається у матрикс м ітохондрій також за допомогою човникової системи . Для цього він відновлюється у малат, кот рий проходить через мембрану . Іншим шляхом повернення оксалоацетату є його перетворення у піруват, для кот рого мембрана теж проникна . Перевагою цього шляху є утворення необхідного для відновного синтезу жирних кислот.
Умітохондріях цитрат є основним субстратом циклу Кребса , але він може залишати мітохондрії та виходити у цитозоль за умов посиленого вживання вуглеводів із їжею.
Упершій стадії відбуваєтьсякарбоксилювання ацетил -КоА з утворенням С3 молекули малоніл-КоА. Реакція каталізується ключ овим ферментом б іосинтезу – ацетил -КоА- карбоксилазою, простетична група цього фермента - біотин.
АТФ
|
|
|
АДФ+Ф |
|
|
SКоА |
+ |
біотин |
ацетилКоА -карбоксилаза |
SКоА |
|
|
|||||
ацетил -КоА |
|
|
( КоЕ – біотин) |
малоніл-КоА |
|
|
|
|
|||
|
|
цитрат |
|
пальмітоїл-КоА |
|
|
|
інсулін |
|
||
Біотин (вітамін Н) за участю АТФ утворює активний комплекс із вугільною |
|||||
88 кислотою – карбоксибіотин, який вводить карбоксильну групу в |
ацетил -КоА. |
||||
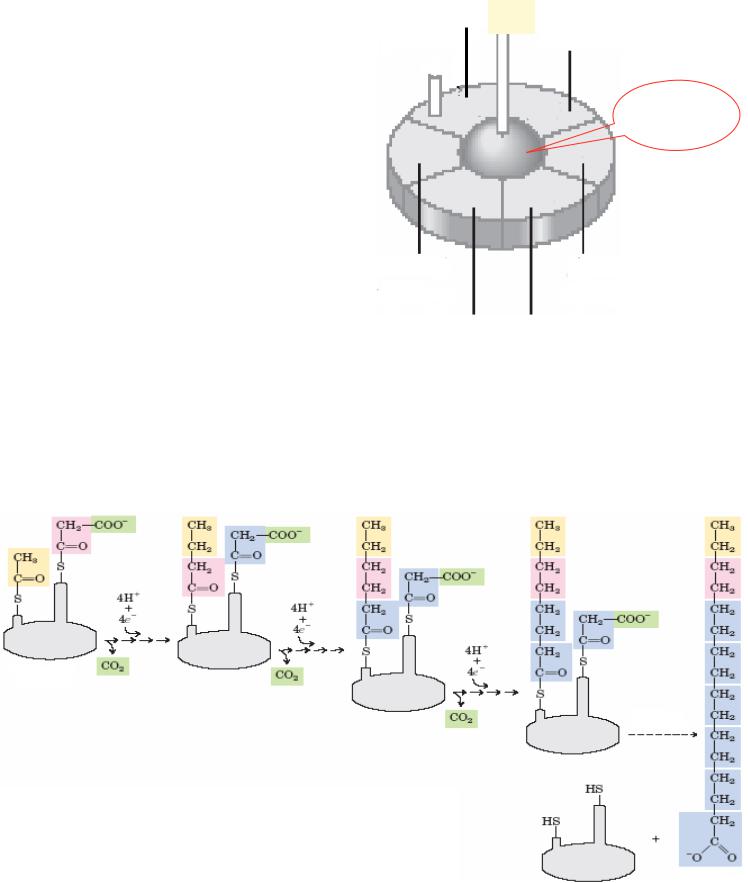
У синтез і жирн их кислот приймає участь мультиферментн ий комп -
лекс – синтаза жирн их кислот (пальмітатсинтаза), кот рий складається з декількох ферментів,
каталізуючих |
окремі реакц |
ії |
синтезу жирн |
их кислот , |
і з |
ацилтранспортуючого |
білку |
|
(АТБ). Цей комплекс має дві SH- |
||
групи: цистеїнового залишку (CysSH), що зв ’язує ацетильний залишок , і 4'-фосфопантотенової групи (Pan-SH), необхідної для зв’язування малонільного залиш -
ку. Ця частина ферменту функціонує як " довга рука", кот ра фіксує субстрат і передає його від одного ферменту реакції до іншого.
Синтаза жирних кислот (пальмітатсинтаза)
β-кетоацил -АТБ-
синтетаза SН Малоніл-КоА- АТБ-трансфераза
|
SН |
|
|
|
|
|
|
КС |
|
Ацил- |
|
|
|
МТ |
Транспортуючий |
||
|
|
|
|
Білок |
|
|
|
|
|
|
|
АТ |
|
АТБ |
|
КР |
|
ЕР ГД
Ацетил-КоА-АТБ- |
β-кетоацил - |
|
АТБ-редуктаза |
||
трансацетилаза |
||
|
||
Еноїл-АТБ- |
β-гідроксиацил -АТБ- |
|
редуктаза |
дегідратаза |
Просторове об’єднання декількох послідовних реакцій у такому мультиферментному комплексі має низку принцип ових переваг у порівнянні з окремими ферментами : запобігаються конкурентн і реакц ії, посл ідовні реакц ії узгоджені, як на конве єрі. Це сприяє найбільш ефективному перебігувсіх ферментативних реакцій.
Пальмітатсинтаза забезпечує |
|
|
|
послідовне зростання вуглецевого ланцюгу |
|
||
на два атоми вуглецю (С2, С4, С6 , тощо) до утворення |
|
||
16-вуглецевого ацильного залишку, зв’язаного з SН-групою |
|
||
АТБ. Відщеплення пальм |
ітилу від |
АТБ здійснюється |
|
шляхом гідролізу . При |
цьому утворюється вільна |
|
|
пальмітинова кислота С |
15Н31СООН |
та вивільняється |
89 |
пальмітатсинтаза . |
|
|
|
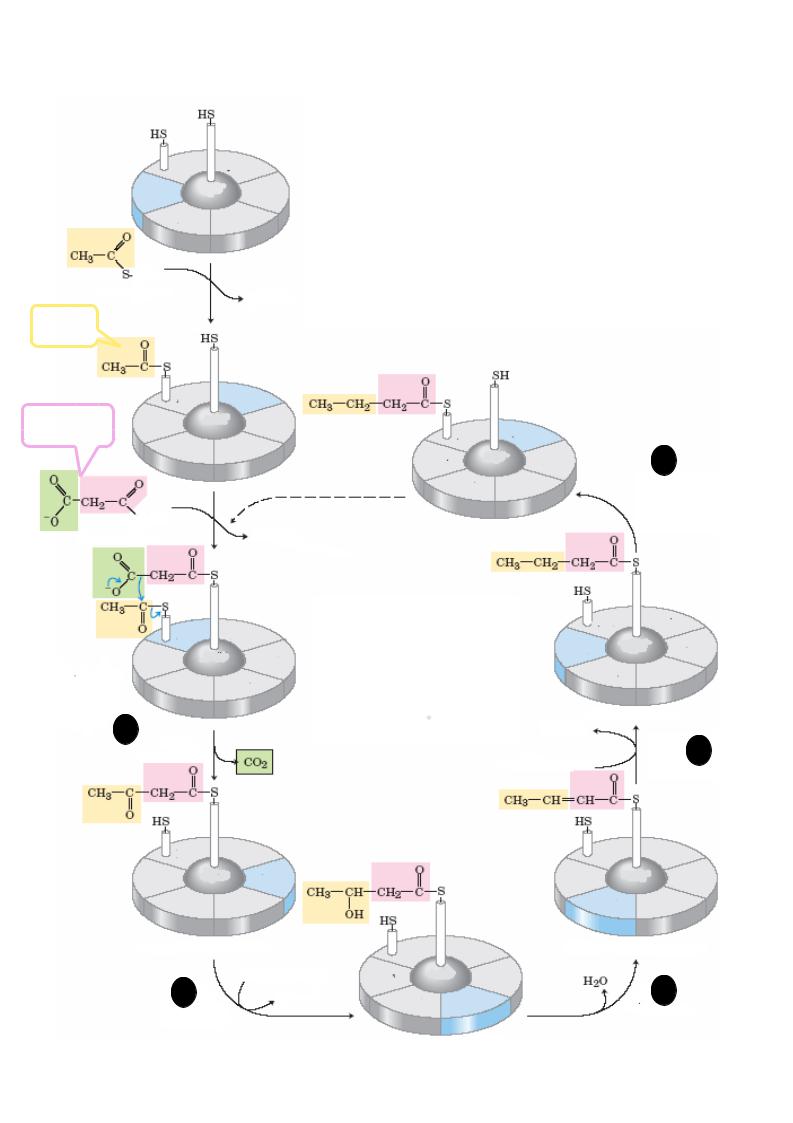
Послідовність ферментативних реакцій синтезу ВЖК |
|
||||||
|
|
|
|
|
|
||
|
|
|
|
|
На синтез однієї молекули |
||
|
|
КС |
|
|
пальмітату використовується: |
||
|
АТ |
МТ |
|
1 молекула ацетил -КоА; |
|||
|
АТБ |
КР |
|
7 молекул малоніл-КоА; |
|||
|
|
|
|
|
|
|
|
|
|
ЕР |
ГД |
|
|
|
+ |
|
|
|
14 молекул НАДФН + Н. |
||||
|
|
|
|
|
Внаслідок цього утворюється: |
||
|
КоА |
|
|
|
7 молекул СО2; |
|
|
ацетил -КоА |
|
НSКоА |
|
6 молекул H2O; |
|
||
перенос |
|
|
|
8 молекул НSКоА; |
|||
|
|
|
|
||||
ацетилу |
|
|
|
|
14 молекул НАДФН+Н+ |
||
перенос |
|
КС |
МТ |
|
|
|
|
АТ |
АТБ |
КР |
|
|
|
|
|
малонілу |
|
КС |
МТ |
|
|||
|
|
|
|||||
|
|
ЕР |
ГД |
АТ |
АТБ |
КР |
5 |
|
|
|
|
|
|||
|
|
|
|
|
ЕР |
ГД |
перенос бутирилу |
|
SКоА |
повторення циклів |
|
|
|
з SН-групи АТБ |
|
|
|
|
|
|
на SН-групу |
||
малоніл-КоА |
|
НSКоА |
|
|
|
||
|
|
|
|
ферменту КС |
|||
|
|
|
|
|
|
|
|
КС |
МТ |
синтаза жирних кислот |
КС |
|
МТ |
|
АТ |
АТБ |
КР |
||||
АТ АТБ |
КР |
|||||
з метильною та |
||||||
ЕР |
|
ГД |
||||
ЕР |
ГД |
малонільною групами |
|
|||
|
|
|
||||
1 |
|
|
бутирил-АТБ |
|||
|
|
НАДФ+ |
|
4 |
||
конденсація |
|
|
НАДФН+ |
|
||
|
|
|
|
|
||
відновлення
КС |
МТ |
|
КС |
МТ |
АТ АТБ |
КР |
|
АТ АТБ |
КР |
ЕР |
ГД |
|
ЕР |
ГД |
β-кетобутирил-АТБ |
КС |
МТ |
|
|
|
|
|
||
2
відновлення
90
НАДФН+ НАДФ+
АТ |
АТБ |
ГД |
КР |
3 |
ЕР |
|
|
||
|
|
дегідратація |
||
|
|
|
|
β-гідроксибутирил-АТБ
