
- •295 Основнi уявлення квантової механiки розділ 9. Елементи квантової механiки
- •Основнi уявлення квантової механiки
- •9.1.1. Мiсце квантової механiки в системi наук про рух тiл
- •9.1.2. Гiпотеза де Бройля
- •9.1.3. Спiввiдношення невизначеностей Гейзенберга
- •9.1.4. Основне рiвняння квантової механiки – рiвняння Шредiнгера
- •Знайдемо відповідні частиннi похiднi, а саме:
- •9.1.5. Рiвняння Шредiнгера для атома водню
- •9.1.6. Багатоелектроннi атоми
- •Випромiнювання та поглинання енергiї атомами та молекулами
- •9.2.1. Атомнi спектри
- •9.2.2. Молекулярні спектри
- •Люмiнесценцiя
- •9.3.1. Види люмінесценції
- •9.3.2. Фотолюмiнесценцiя, закон Стокса
- •9.3.3. Механізми люмінесценції
- •Індуковане випромінювання
- •9.4.1. Рівноважна та інверсна заселеність
- •9.4.2. Будова та принцип дiї лазера
- •Електронний парамагнiтний резонанс, ядерний магнiтний резонанс та їх медико-бiологiчнi застосування
- •9.5.1. Метод електронного парамагнiтного резонансу
- •9.5.2. Метод спiнових мiток (спiнових зондiв)
- •9.5.3. Спiн-iмунологiчний метод
- •9.5.4. Метод ядерного магнiтного резонансу
- •Практикум з квантової механіки
- •9.6.1. Практичне заняття “Основні уявлення квантової механіки”
- •Теоретичнi питання, що розглядаються на практичному занятті
- •Додаткова лiтература для пiдготовки до практичого заняття
- •Завдання для самостiйної роботи I самоконтролю
- •Типовi задачi з еталонами розв’язкiв
- •1. Хвильовi властивостi частинок. Формула де Бройля.
- •Розрахуємо довжину хвилi де Бойля для електрона
- •2. Електронний мiкроскоп, його межа розрiзнення.
- •3. Спiввiдношення невизначеностей Гейзенберга.
- •4. Квантовi числа, їх фiзичний змiст
- •5. Атомнi спектри
- •Завдання для перевiрки кiнцевого рiвня знань
- •Порядок виконання
- •Порядок виконання:
- •Контрольні питання
9.3.3. Механізми люмінесценції
Для пояснення спостерiгаємих закономiрностей розглянемо можливi механiзми виникнення фотолюмiнесценцiї.
1
Мал.
9.15. Механізм резонансної
флуоресценції.
Такий механiзм люмiнесценцiї зветься резонансною флуоресценцiєю. Найчастiше вiн реалiзується в одноатомних парах та газах.
2. Повернення атома або молекули зі збудженого стану в основний може вiдбуватися:
а) в результатi чергування випромiнювальних та безвипромiнювальних переходiв (мал. 9.16, а);
б) ступiнчато, в результатi випромiнювальних переходiв мiж промiжними енергетичними рiвнями (мал. 9.16, б). У таких випадках (hv)люм < (hv)зб або люм > зб, що i вiдображено в законi Стокса.
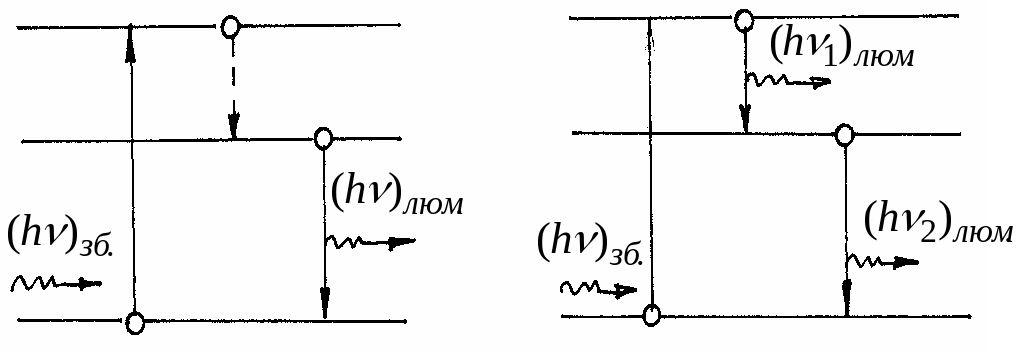
а) |
б) |
Мал. 9.16. Механізм люмінесценції відповідно до закону Стокса.
3
Мал.
9.17. Антистоксівське
випрмінювання (hv)люм
> (hv)зб
або люм
< зб.
4. Перехiд атома або молекули iз збудженого стану в основний може здiйснюватись через промiжний, так званий метастабiльний стан, перехiд з якого в основний стан є малоймовiрним в силу дiї правил заборони. Як приклад, розглянемо систему електронних рiвнiв бiомолекули (мал. 9.18), де S0 – енергетичний рiвень, що вiдповiдає основнiй електроннiй конфiгурацiї, S1, S2 – рiвнi, що вiдповiдають збудженим електронним конфiгурацiям. При поглинаннi збуджуючого випромiнювання може вiдбутися перехiд одного з електронiв iз заповненої орбiталi на одну з незаповнених з бiльш високою енергiєю. В результатi молекула опиниться в електроннозбудженому станi S1 або S2. Рiвнi S0, S1, S2 називаються синглетними – перехiд мiж ними вiдбувається без змiни орiєнтацiї спiна електрона. (Бiля кожного рiвня в клiтинах, що вiдповiдають орбiталям, показано напрямок спiна збудженого електрона по вiдношенню до спiна незбудженого).
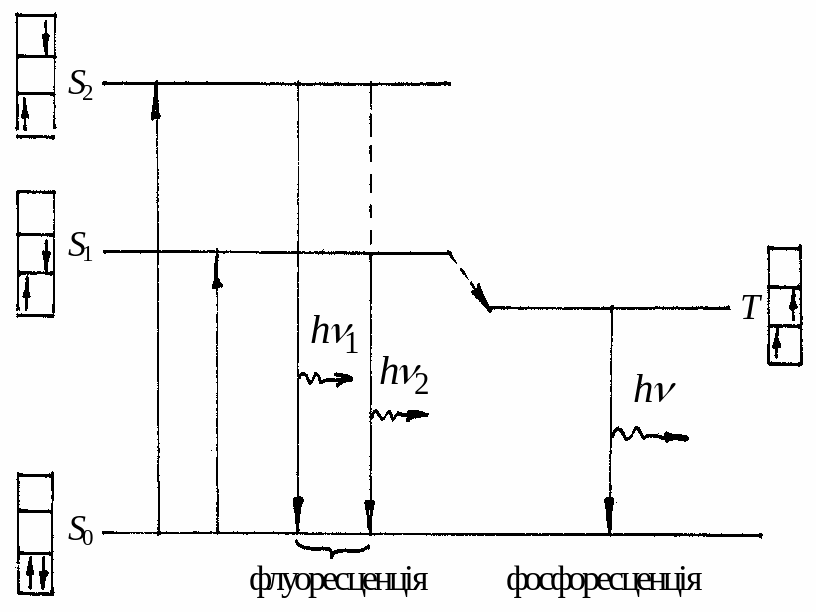
Мал. 9.18. Механізми виникнення флуоресцентного і фосфоресцентного випромінювань молекули.
Час життя молекули у збуджених станах S1 або S2 становить 10–8 с. Перехiд в основний енергетичний стан може здiйснюватись одним з розглянутих вище способiв: у результатi безвипромiнювальних переходiв або з випромiнюванням квантiв флуоресценцiї (короткочасного пiслясвiчення). З певною ймовiрнiстю можливе також обернення спiна збудженого електрона, тобто безвипромiнювальний перехiд молекули iз збудженого синглетного у збуджений триплетний стан.
Перехiд молекули iз триплетного в основний стан Т S0 заборонений по спiну (у вiдповiдностi з принципом Паулi). Таким чином, триплетний рiвень є метастабiльним.
В силу малої ймовiрностi переходу Т S0 в триплетному станi молекула може знаходитись достатньо довго (10–410 с). Перехiд Т S0 може здiйснитись як у результатi безвипромiнювального, так i випромiнювального переходiв. Випромiнювання, яке супроводжує перехiд Т S0, зветься фосфоресценцiєю. Фосфоресценцiя вiдрiзняється вiд флуоресценцiї тривалiстю пiслясвiчення. Ймовiрнiсть випромiнювального переходу атома або молекули з метастабiльного енергетичного рiвня на основний збiльшується при дiї на них зовнiшнього фотона, який має енергiю, що дорiвнює енергiї фотона, який випромiнюється самодовiльно. Такий випромiнювальний перехiд пiд дiєю зовнiшнього випромiнювання називається примусовим або iндукованим.
