
- •295 Основнi уявлення квантової механiки розділ 9. Елементи квантової механiки
- •Основнi уявлення квантової механiки
- •9.1.1. Мiсце квантової механiки в системi наук про рух тiл
- •9.1.2. Гiпотеза де Бройля
- •9.1.3. Спiввiдношення невизначеностей Гейзенберга
- •9.1.4. Основне рiвняння квантової механiки – рiвняння Шредiнгера
- •Знайдемо відповідні частиннi похiднi, а саме:
- •9.1.5. Рiвняння Шредiнгера для атома водню
- •9.1.6. Багатоелектроннi атоми
- •Випромiнювання та поглинання енергiї атомами та молекулами
- •9.2.1. Атомнi спектри
- •9.2.2. Молекулярні спектри
- •Люмiнесценцiя
- •9.3.1. Види люмінесценції
- •9.3.2. Фотолюмiнесценцiя, закон Стокса
- •9.3.3. Механізми люмінесценції
- •Індуковане випромінювання
- •9.4.1. Рівноважна та інверсна заселеність
- •9.4.2. Будова та принцип дiї лазера
- •Електронний парамагнiтний резонанс, ядерний магнiтний резонанс та їх медико-бiологiчнi застосування
- •9.5.1. Метод електронного парамагнiтного резонансу
- •9.5.2. Метод спiнових мiток (спiнових зондiв)
- •9.5.3. Спiн-iмунологiчний метод
- •9.5.4. Метод ядерного магнiтного резонансу
- •Практикум з квантової механіки
- •9.6.1. Практичне заняття “Основні уявлення квантової механіки”
- •Теоретичнi питання, що розглядаються на практичному занятті
- •Додаткова лiтература для пiдготовки до практичого заняття
- •Завдання для самостiйної роботи I самоконтролю
- •Типовi задачi з еталонами розв’язкiв
- •1. Хвильовi властивостi частинок. Формула де Бройля.
- •Розрахуємо довжину хвилi де Бойля для електрона
- •2. Електронний мiкроскоп, його межа розрiзнення.
- •3. Спiввiдношення невизначеностей Гейзенберга.
- •4. Квантовi числа, їх фiзичний змiст
- •5. Атомнi спектри
- •Завдання для перевiрки кiнцевого рiвня знань
- •Порядок виконання
- •Порядок виконання:
- •Контрольні питання
Випромiнювання та поглинання енергiї атомами та молекулами
9.2.1. Атомнi спектри
Якщо атом не зазнає зовнiшнiх впливів (зiткнень з iншими атомами, опромiнення тощо), то вiн знаходиться у станi з мiнiмальною енергiєю – в основному енергетичному станi. Змiна енергетичного стану атомiв при зовнiшнiх впливах обумовлена змiною їх електронних конфiгурацiй, тобто переходами електронiв мiж рiзними енергетичними рiвнями. Довжини хвиль або частоти, що їх випромiнюють або поглинають атоми при таких переходах, характеризують спектри випромiнювання та поглинання вiдповiдно.
Спектри випромiнювання та поглинання вiльних або слабо взаємодiючих атомiв, зумовленi переходами мiж енергетичними рiвнями зовнiшнiх (валентних) електронiв, називаються оптичними атомними спектрами. Закономiрностi, притаманнi атомним спектрам, розглянемо на прикладi спектра випромiнювання атомiв водню.
В результатi розв’язку рiвняння Шредiнгера були одержанi можливi значення енергiї атома водню
![]()
де R – стала Рiдберга.
Дiаграму енергетичних рiвнiв атома водню, розраховану за одержаною формулою, подано на мал. 9.6.
Надання атому енергії, як наслідок зовнiшнього впливу, приводить його до збудженого стану, що вiдповiдає переходу електрона з основного на бiльш високий енергетичний рiвень (на бiльш високоенергетичну орбiталь).
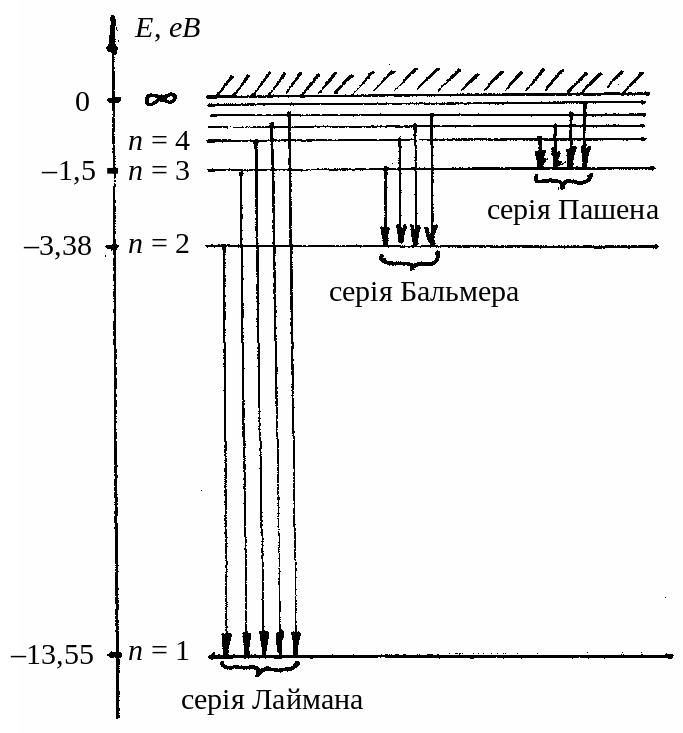
Мал. 9.6. Діаграма енергетичних рівнів атома водню.
Через промiжок часу 10–8 с (час життя атома в збудженому станi) атом повертається в основний енергетичний стан, випромiнюючи такі частоти:
![]() , (9.15)
, (9.15)
де ni та nk – головнi квантовi числа енергетичних рiвнiв, мiж якими вiдбувається перехiд, причому nk > ni .
Одержана формула не тiльки пояснює встановлений експериментально лiнiйчаcтий характер атомних спектрiв, але й дозволяє розрахувати набiр частот, якi вiдповiдають спостерiгаємим спектральним лiнiям.
Спектр випромiнювання атома водню складається з окремих груп лiнiй, якi називаються спектральними серiями. Кожнiй серiї вiдповiдає набiр частот, що випромiнюється атомами при переходi електрона на певний енергетичний рiвень з усiх вище розташованих рівнів (мал. 9.6).
При переходi електрона на основний енергетичний рівень (ni = 1) з усiх інших рівнів (nk = 2, 3, 4, …) випромiнюється серiя Лаймана, що лежить в ультрафiолетовiй областi. Частоти, якi вiдповiдають спектральним лiнiям цiєї серiї, легко одержати iз узагальненої формули (9. 15) при умовi ni = 1, nk = 2, 3, 4, …:
vЛ = R (1/12 – 1/nk2).
При переходi електрона на основний енергетичний рiвень з головним квантовим числом ni = 2 з бiльш високо розташованих рівнів випромiнюється серiя Бальмера, що лежить у видимiй та ближнiй ультрафiолетовiй областях:
vБ = R (1/22 – 1/nk2), nk = 3, 4, 5, … .
При переходi збудженого електрона на рiвень, що характеризується головним квантовим числом ni = 3, з усiх вище розташованих рівнів випромiнюється серiя Пашена, яка лежить в iнфрачервонiй областi:
vП = R (1/32 – 1/nk2), nk = 4, 5, 6, … .
Слiд вiдзначити, що в кожнiй серiї вiдстань мiж лiнiями зменшується при переходi до бiльш коротких хвиль. При цьому кожна серiя має короткохвильову границю, за межi якої вона не виходить. Ця границя називається “граничною лiнiєю” серiї, її частота визначається по узагальненiй формулi (9.15) при умовi nk = .
Атомнi оптичнi спектри багатоелектронних атомiв складнiшi за спектри атома водню, але їм теж притаманнi розглянуті вище закономiрностi.
