
- •1. Основные положения статистической термодинамики
- •1.1. Понятия и начала феноменологической термодинамики.
- •1.2. Микроскопическое (механическое) описание классических систем.
- •1.3. Особенности представления квантовых систем
- •1.4. Вероятность нахождения системы в элементе фазового пространства. Метод ансамблей Гиббса.
- •1.5. Макроскопические величины как фазовые средние
- •1.6. Распределение в системах с постоянным числом частиц
- •1.6.2. Распределения Гиббса.
- •1.6.3. Квазиклассическое приближение.
- •1.7. Свойства распределения Гиббса
- •1.8. Большое каноническое распределение Гиббса
- •2. Статистика идеального газа
- •2.1. Идеальный газ как модель статистической системы
- •2.2. Распределение Максвелла
- •2.3. Столкновения молекул со стенкой сосуда. Давление
- •2.4. Характерные величины идеального газа
- •2.5. Столкновение молекул между собой
- •2.6. Длина свободного пробега
- •2.7. Идеальный газ во внешнем поле
- •2.8. Число и функция состояний идеального газа
- •2.9. Классическая теория теплоемкости газа двухатомных молекул
- •2.10. Квантовая теория теплоемкости газа двухатомных молекул
- •2.11. Распределения в квантовых системах
- •3. Законы термодинамики
- •3.1. Статистическое обоснование первого начала термодинамики
- •3.2. Второе начало термодинамики
- •3.3. Вечный двигатель второго рода. Максимальная работа процессов
- •3.4. Полезная работа тепловых машин
- •3.5. Метод термодинамических потенциалов
- •3.6. Термодинамические коэффициенты. Критерии устойчивости равновесия
- •3.7. Статистическое вычисление термодинамических величин
- •3.8. Третье начало термодинамики (теорема Нернста)
- •3.9. Применения термодинамики
- •4. Статистика сложных систем.
- •4.1. Модель кристаллического твердого тела. Уравнение движения атомов
- •4.2. Дисперсионное уравнение нормальных колебаний кристалла
- •4.3. Кристалл как система линейных гармонических осцилляторов
- •4.4. Статистическая сумма и энергия кристалла (в гармоническом приближении)
- •4.5. Теория теплоемкости Дебая
- •4.6. Электронный газ в металлах
- •4.7. Зависимость энергии электрона от волнового вектора. Эффективная масса
- •4.8. Теория парамагнетизма. Природа и характеристики магнетизма.
- •4.9. Равновесное излучение.
- •4.10. Системы с кулоновским взаимодействием частиц.
- •5. Теория малых флуктуаций
- •5.1. Определение и значение флуктуаций
- •5.2. Мера вероятности и масштаб флуктуаций
- •5.3. Флуктуации термодинамических величин в однородной среде
- •5.4. Предельная чувствительность измерительных приборов
- •5.5. Рассеяния света флуктуациями
- •6. Элементы теории физической кинетики
- •6.1. Определения и характеристики необратимых процессов
- •6.2. Теория стационарных процессов в газе свободных электронов
- •6.3. Газокинетическое уравнение Больцмана
- •6.4. Приближение времени релаксации
- •Раздел 2
- •Раздел 2
- •Раздел 3
- •Раздел 4
- •Раздел 5
- •Раздел 6
- •Список Литературы
3.6. Термодинамические коэффициенты. Критерии устойчивости равновесия
3.6.1. Теплоемкости. Важную роль в термодинамике играет теплоемкость – количество тепла, необходимое для нагревания тела на один градус
 (3.50)
(3.50)
С учетом первого начала термодинамики для простых систем она может быть представлена в виде
 .
.
Неудобство такого определения для теоретических расчетов состоит в том, что внутренняя энергия – потенциал по отношению объема и энтропии, которая не относится к непосредственно измеряемым величинам. Здесь следует представить как функцию, например, объема и температуры
 .
.
Тогда
 . (3.51)
. (3.51)
Откуда видно, что
в общем случае теплоемкость является
сложной функцией как физических свойств
(через производные
 и
и
 ),
состояния системы (через давление и
производные), так и характера процесса.
),
состояния системы (через давление и
производные), так и характера процесса.
Проиллюстрируем
зависимость теплоемкости от характера
процесса. При изохорном процессе ( )
)
 (3.52)
(3.52)
Формула позволяет
вычислить
любой однородной системы, если известна
зависимость внутренней энергии от
параметров системы. Теплоемкость в
изотермическом процессе ( )
бесконечно большая. Это означает, что
количество тепла, подводимое к системе
не расходуется на повышение температуры.
В случае адиабатического процесса (
)
бесконечно большая. Это означает, что
количество тепла, подводимое к системе
не расходуется на повышение температуры.
В случае адиабатического процесса ( )
теплоемкость равна нулю (
)
теплоемкость равна нулю ( ).
Производная
имеет размерность давления. Она не
обращается в нуль, если внутренняя
энергия зависит от объема, иными словами,
лишь в том случае, когда в системе
действуют силы взаимодействия между
частицами, из которых она состоит.
).
Производная
имеет размерность давления. Она не
обращается в нуль, если внутренняя
энергия зависит от объема, иными словами,
лишь в том случае, когда в системе
действуют силы взаимодействия между
частицами, из которых она состоит.
Для квазистатического процесса из основного термодинамического равенства следует
 ,
,
где использовано соответствующее перекрестное соотношение (3.38). Подставляя эту частную производную в (3.51), получаем обобщающую формулу вычисления теплоемкости системы при произвольных фиксированных параметрах:
 . (3.53)
. (3.53)
Например, теплоемкость при постоянном давлении равна
 . (3.54)
. (3.54)
В случае
квазистатических процессов, используя
в (3.50) равенство
 и дифференциалы внутренней энергии и
энтальпии, соответственно, при постоянном
объеме и давлении находим
и дифференциалы внутренней энергии и
энтальпии, соответственно, при постоянном
объеме и давлении находим
 ;
;
 . (3.55)
. (3.55)
Выражения
 и
представляют собой производные
обобщенного параметра по сопряженной
ему обобщенной силе
и
представляют собой производные
обобщенного параметра по сопряженной
ему обобщенной силе
 и в дифференциальные соотношения не
входят. Поэтому теплоемкости относятся
к базовым параметрам термодинамики, их
анализ нельзя свести к исследованию
каких-либо других свойств вещества.
Здесь приходится прибегать к данным
непосредственного эксперимента и
строить
и в дифференциальные соотношения не
входят. Поэтому теплоемкости относятся
к базовым параметрам термодинамики, их
анализ нельзя свести к исследованию
каких-либо других свойств вещества.
Здесь приходится прибегать к данным
непосредственного эксперимента и
строить
 и
и
 в виде эмпирических формул.
в виде эмпирических формул.
3.6.2. Термические
и упругие коэффициенты. Помимо
теплоемкостей, свойства макроскопических
систем описываются термическими и
упругими коэффициентами. К группе первых
принадлежат коэффициент теплового
расширения
 и термический коэффициент давления
и термический коэффициент давления

 ;
;
 , (3.56)
, (3.56)
к группе вторых –
изотермическая
 и адиабатическая
и адиабатическая
 сжимаемости:
сжимаемости:
 ;
;
 , (3.57)
, (3.57)
Существует связь между этими коэффициентами и теплоемкостями. Она легко устанавливается с помощью якобиана преобразования. Например,
 . (3.58)
. (3.58)
Преобразуем с помощью якобиана преобразования производную
 .
.
После подстановки её в формулу (3.54) имеем
 . (3.59)
. (3.59)
Аналогичным образом можно получить и другие связи между термодинамическими параметрами.
3.6.3. Критерии
устойчивости равновесия однородной
системы. Пусть
однородная система, находится в термостате
с температурой
под постоянным давлением
.
Общим условием устойчивости равновесия
такой системы является минимум функции
(3.28) (см. раздел 3.5.1) Это означает, что
состояние системы в термостате при
данных
и
с обобщенными координатами
и
устойчиво, если при небольшом спонтанном
(изотермо-изобарным) изменении координат
 и
и
 функция
возрастает:
функция
возрастает:

Представим
 рядом до членов второго порядка малости
рядом до членов второго порядка малости


Но
 ,
,
 (3.32), и поскольку в равновесии температура
и давление системы и термостат совпадают
(
,
,
необходимые условия равновесия) имеет
место неравенство
(3.32), и поскольку в равновесии температура
и давление системы и термостат совпадают
(
,
,
необходимые условия равновесия) имеет
место неравенство
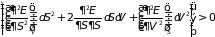 .
Оно выполняется при двух условиях:
достаточном для экстремума и необходимом
для минимума функции
:
.
Оно выполняется при двух условиях:
достаточном для экстремума и необходимом
для минимума функции
:
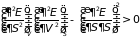 ;
;
 .
.
Так как температура
положительная величина
 ,
то теплоемкость при постоянном объеме
,
то теплоемкость при постоянном объеме
 . (3.60)
. (3.60)
Первое условие перепишем через якобиан преобразования
 .
.
Переходя к переменным и , имеем
 ,
,
 . (3.61)
. (3.61)
Увеличение объема при постоянной температуре всегда сопровождается уменьшением давления.
Формулы (3.60) и (3.61) определяют условия устойчивости равновесного состояния в однородных системах. В силу неравенства (3.61) из формулы (3.59) следует
 .
.
Положительность теплоемкостей означает, что внутренняя энергия и энтальпия – монотонно возрастающие функции температуры при постоянном объеме и давлении, соответственно.
