
- •Номенклатура
- •Химические свойства [править] Основные оксиды
- •[Править] Кислотные оксиды
- •[Править] Амфотерные оксиды
- •[Править] Получение
- •§5. Электронные облака - орбитали
- •Правило Хунда
- •[Править] Мнемоническое правило
- •Валентность
- •[Править] История возникновения понятия «валентность»
- •[Править] Современные представления о валентности
- •Химическая связь в молекулах и новая теория химической связи. Виды химической связи.
- •Химическая связь в молекулах объясняется только электрическим притяжением и отталкиванием.
- •Виды химической связи
- •При нашем способе расположения электронов отпадает необходимость в теории гибридизации орбиталей (да и вообще в самих орбиталях).
- •Откуда берётся деление химических элементов по периодам?
- •Новая теория химической связи, вытекающая непосредственно из устройства атомов
- •Химическая связь в металлах
- •Атом бора. Гидриды бора.
- •Строение молекулы бензола
- •Комплексные соединения платины
- •Функциональные группы и способ соединения в них атомов
- •Химические связи в группах. Карбоксильная группа и гидроксильная группа.
- •Химическая связь - история (то, что пишут в учебниках)
- •Важнейшие свойства химической связи
- •Тайна крещенской воды
- •3.2.4 Гибридизация атомных орбиталей
- •Силы Ван-дер-Ваальса
- •[Править] Классификация ван-дер-ваальсовых сил
- •Типы кристаллических решеток
- •Металлическая связь
- •[Править] Механизм металлической связи
- •[Править] Характерные кристаллические решётки
- •Водородная связь
- •[Править] Природа водородной связи
- •[Править] История
- •[Править] Свойства
- •[Править] Водородная связь в воде [править] Механизм Гротгуса
- •[Править] Водные кластеры
- •[Править] Водородная связь в нуклеиновых кислотах и белках
- •[Править] Водородная связь в полимерах
- •Структура воды
- •5) Термодинамическая фаза
- •[Править] Основные понятия
- •[Править] Термодинамические фазы на фазовой диаграмме
- •[Править] Термодинамические фазы и агрегатные состояния вещества
- •[Править] Выделение фаз
- •[Править] См. Также Внутренняя энергия
- •[Править] Идеальные газы
- •Термодинамика
- •[Править] Разделы термодинамики
- •[Править] Физический смысл термодинамики [править] Необходимость термодинамики
- •[Править] Законы — начала термодинамики
- •[Править] Основные формулы термодинамики [править] Условные обозначения
- •[Править] Формулы термодинамики идеального газа
- •[Править] Термодинамика сплошных сред
- •Закон Гесса
- •[Править] Следствия из закона Гесса
- •Термодинамическая энтропия
- •[Править] Термодинамическое определение энтропии
- •[Править] Статистическое определение энтропии: принцип Больцмана
- •[Править] Понимание энтропии как меры беспорядка
- •[Править] Границы применимости понимания энтропии как меры беспорядка
- •[Править] Энтропия в открытых системах
- •[Править] Измерение энтропии
- •[Править] Построение графика изменения энтропии
- •4.5. Энтропия
- •Энергия Гиббса
- •[Править] Определение
- •[Править] Связь с термодинамической устойчивостью системы
- •[Править] Применение в химии [править] Связь с химическим потенциалом
- •[Править] Энергия Гиббса и направление протекания реакции
- •2 Химическая кинетика и химическое равновесие
- •2.1 Кинетика химических реакций
- •Закон действующих масс
- •[Править] Закон действующих масс в химической кинетике
- •[Править] Закон действующих масс в химической термодинамике
- •6.1.3. Зависимость скорости реакции от температуры
- •Энергия активации
- •[Править] Математическое описание
- •[Править] Переходное состояние
- •5.2.Обратимые и необратимые процессы
- •Релаксация (физика)
- •[Править] Свойства и виды
- •[Править] Описание процесса релаксации [править] Для одноатомных газов
- •[Править] Для многоатомных газов
- •[Править] Для смесей газов
- •[Править] Для жидкостей
- •[Править] Для твёрдых тел и квантовых жидкостей
- •Динамические равновесия
- •Принцип Ле Шателье — Брауна
- •[Править] Влияние температуры
- •[Править] Влияние давления
- •Влияние инертных газов
- •5.1. Химическое равновесие в гомогенных системах
- •6. Растворы
- •6.1. Дисперсные системы. Растворы
- •Некоторые характеристики дисперсных систем
- •6.2. Процесс образования растворов. Тепловые эффекты при растворении
- •6.3. Растворимость
- •6.4. Способы выражения состава растворов
- •Способы выражения состава растворов
- •6.5. Разбавленные растворы неэлектролитов
- •6.5.1. Давление пара над растворами
- •6.5.2. Температура кипения и замерзания растворов
- •6.5.3. Осмотическое давление
- •6.6. Растворы электролитов. Основы теории электролитической диссоциации
- •6.6.1. Сильные и слабые электролиты
- •6.7. Равновесие в растворах слабых электролитов. Константа диссоциации
- •6.8. Основания, кислоты и соли в свете теории электролитической диссоциации
- •6.9. Ионное произведение воды
- •Окраска важнейших кислотно-основных индикаторов в различных средах
- •6.10. Произведение растворимости
- •6.11. Реакции обмена в растворах электролитов
- •6.12. Гидролиз солей
- •11. Химические свойства металлов
- •11.1. Общие положения
- •11.2. Физические свойства металлов
- •11.3. Получение металлов
- •11.3.1. Нахождение в природе
- •11.3.2. Общие методы получения металлов
- •11.3.3. Получение металлов высокой чистоты
- •11.4. Химические свойства металлов
- •11.4.1. Отношение металлов к окислителям - простым веществам
- •Щелочные металлы
- •[Править] Общая характеристика щелочных металлов
- •Некоторые свойства щелочных металлов
- •[Править] Химические свойства щелочных металлов
- •Окраска пламени щелочными металлами и их соединениями
- •[Править] Получение щелочных металлов
- •[Править] Соединения щелочных металлов [править] Гидроксиды
- •[Править] Карбонаты
- •[Править] Фотографии
- •[Править] Литература
- •[Править] Примечания
- •[Править] См. Также
- •[Править] Ссылки
- •13.Важнейшие классы неорганических веществ
- •13.1. Определения
- •13.2. Металлы
- •13.3. Неметаллы
- •13.4. Основные оксиды
- •13.5. Кислотные оксиды
- •13.6. Амфотерные оксиды
- •Окислительно-восстановительные реакции
- •[Править] Описание
- •[Править] Окисление
- •[Править] Восстановление
- •[Править] Виды окислительно-восстановительных реакций
- •[Править] Примеры [править] Окислительно-восстановительная реакция между водородом и фтором
- •[Править] Окисление, восстановление
- •[Править] Мнемонические правила
- •8. Электрохимические процессы
- •8.1. Гальванический элемент
- •8.2 Коррозия металлов
- •8.3. Электролиз
- •8.1. Гальванический элемент
- •8.1.1. Понятие об электродном потенциале
- •8.1.2. Гальванический элемент (гэ) даниэля-якоби
- •8.1.3. Напряжение гальванического элемента
- •8.1.4. Водородная шкала потенциалов
- •8.1.5. Потенциалы металлических электродов
- •8.1.6. Потенциалы газовых электродов
- •8.1.7.Поляризация в электрохимических процессах
- •8.2 Коррозия металлов
- •8.2.1.Химическая коррозия
- •8.2.2. Электрохимическая коррозия
- •Основные случаи возникновения коррозионных гальванических пар
- •8.2.3 Защита металлов от коррозии
- •8.3. Электролиз
- •8.3.1. Общие понятия
- •8.3.2. Электролиз расплавов электролитов
- •8.3.3. Электролиз растворов электролитов
- •8.3.4 Электролиз с растворимыми анодами
- •8.3.5. Законы электролиза
- •8.3.6. Применение электролиза
- •Электрохимическая коррозия
- •Газовая коррозия
- •Химическая коррозия в жидкостях-неэлектролитах
- •7.1.Коррозия металлов
- •7.2.Борьба с коррозией парогенераторов во время работы
- •7.3.Борьба со стояночной (кислородной) коррозией парогенераторов, находящихся в резерве или ремонте
- •7.4.Борьба с коррозией конденсатопроводов
- •7.5.Борьба с коррозией тепловых сетей
- •7.6.Защита от коррозии водоподготовительного оборудования
- •7.7.Удаление отложений
- •§ 36. Воздушная известь
- •А. Воздушные вяжущие вещества
- •Б. Гидравлические вяжущие вещества
При нашем способе расположения электронов отпадает необходимость в теории гибридизации орбиталей (да и вообще в самих орбиталях).
Становится
понятной причина равноценности всех
химических связей и симметричность
расположения их относительно центра у
таких молекул как CH4,
BF3 , BeCl2 .
Так же легко объясняются явления
пространственной изомерии и аллотропии.
Вы мне можете возразить, что такая
конфигурация электронов будет достаточно
неустойчивой. Согласен. Но напомню вам,
что между ядром и электронами действуют,
кроме электрических, ещё и гравитационные
силы.
Вот именно они и ответственны за появление
потенциальной ямы, в которой находятся
электроны. По величине энергии ионизации
атома можно понять, насколько глубока
эта яма.
 Замечу,
что расстояние от электрона до ядра
можно найти используя равенство между
собой двух сил. Силы электрического
притяжения между ядром и электроном и
силы электрического отталкивания между
одним электроном и всеми остальными,
составляющими электронную оболочку.
Замечу,
что расстояние от электрона до ядра
можно найти используя равенство между
собой двух сил. Силы электрического
притяжения между ядром и электроном и
силы электрического отталкивания между
одним электроном и всеми остальными,
составляющими электронную оболочку.
Откуда берётся деление химических элементов по периодам?
Два электрона располагаясь центрально симметрично относительно ядра, занимают всю сферическую область и третий электрон вынужден располагаться уже дальше от ядра. Так продолжается до тех пор, пока вся сферическая область следующего уровня не будет заполнена. Так как расстояние от ядра становится больше, то такая область может вместить уже восемь электронов. Свою роль в этом играет и возросший положительный заряд ядра.
Новая теория химической связи, вытекающая непосредственно из устройства атомов
Очевидны
всего два возможных способа образования
молекул. Но, что очень важно. Оба способа
объединения атомов становятся возможны
лишь при наличии
вакансий в
электронной оболочке реагентов. Вакансии
есть во всех атомах, кроме инертных
газов, скажете вы. Почему же не объединяются
в молекулу, допустим два атома бериллия.
Напомню, что мы во всём опираемся на
принцип непрерывности, из которого
следует, что уж если вакансии начали
заполняться, то процесс должен закончиться
лишь при заполнении всех имеющихся
вакансий. Так происходит, например с
двумя атомами кислорода.
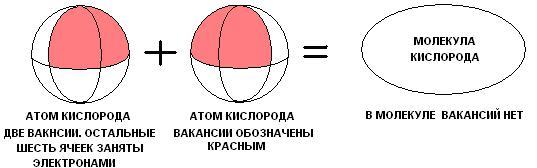 Рисунок
даёт представление об одном из возможных
видов химической связи. Так и будем для
простоты называть её вакантной связью
(В-В).
Второй вид химической связи возникает
в случае, когда у одного из реагентов
слишком большая вакантная область.
Тогда происходит следующее. Электроны
этого реагента будут представлять
своего рода возвышенности на теле атома,
назовём для краткости их пиками (показаны
на рисунке синим цветом). Так вот эти
пики при химической реакции будут
заполнять вакантные области второго
реагирующего атома. И конечно, по принципу
непрерывности, должны будут заполнить
все имеющиеся вакансии.
Рисунок
даёт представление об одном из возможных
видов химической связи. Так и будем для
простоты называть её вакантной связью
(В-В).
Второй вид химической связи возникает
в случае, когда у одного из реагентов
слишком большая вакантная область.
Тогда происходит следующее. Электроны
этого реагента будут представлять
своего рода возвышенности на теле атома,
назовём для краткости их пиками (показаны
на рисунке синим цветом). Так вот эти
пики при химической реакции будут
заполнять вакантные области второго
реагирующего атома. И конечно, по принципу
непрерывности, должны будут заполнить
все имеющиеся вакансии.
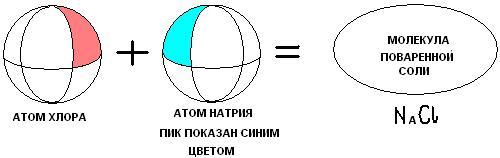 Назовём
такую связь вакантно-пиковой (В-П).
Назовём
такую связь вакантно-пиковой (В-П).
Покажем физическую сторону процессов химической связи атомов в молекулы.
Каждый атом будет представлять собой систему пространственного распределения положительной и отрицательной плотности электрического заряда. Покажем её на нескольких примерах (смотрите рисунок).
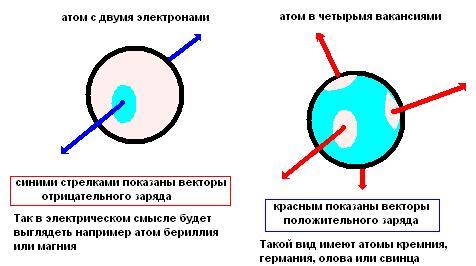 Зона
с частично положительным значением
заряда называется вакансией.
Таких зон в атоме может быть несколько.
Вакансии могут объединяться в одну
зону, или существовать обособленно.
Каждая
из зон с частично отрицательной плотностью
электрического заряда представляет
собой пик.
Пики могут объединиться в одну зону,
если электронов в атоме много, или
энергия атома велика. В наиболее низком
энергетическом состоянии пики равномерно
распределены по поверхности атома.
Зона
с частично положительным значением
заряда называется вакансией.
Таких зон в атоме может быть несколько.
Вакансии могут объединяться в одну
зону, или существовать обособленно.
Каждая
из зон с частично отрицательной плотностью
электрического заряда представляет
собой пик.
Пики могут объединиться в одну зону,
если электронов в атоме много, или
энергия атома велика. В наиболее низком
энергетическом состоянии пики равномерно
распределены по поверхности атома.
В результате химической реакции происходит взаимное обнуление зарядов (если представить атом в виде ежа, то его иголки будут векторами электрического заряда, и в результате реакции "иголки" одного атома должны равномерно распределиться между "иголок" второго). Чаще всего для реализации такого равномерного распределения требуется дополнительная энергия. Для этого применяются такие инструменты как нагревание и давление. Внесение катализатора также способствует облегчению процесса. Если же после соединения атомов суммарная энергия их в новой молекуле становится меньше, то избыток энергии выделяется, и реакция становится экзотермической. Я думаю, что вы прекрасно понимаете, что любой атом за исключением атомов инертных газов, можно представить двумя способами, показывая только отрицательные вектора, или только положительные.
Объяснением амфотерных свойств химических элементов будет являться то, что атом проявляет свои свойства по разному, в зависимости от того с чем он взаимодействует, то есть использует ли он для связи пики или вакансии.
Картина для атомов длинных периодов усложняется лишь тем, что количество ячеек, а, следовательно, и возможных пиков, возрастает до двадцати.
