
Журнал неврологии и психиатрии / 2009 / NEV_2009_09_20
.pdf
ЛЕКЦИЯ
Эффективность пирацетама в лечении головокружения
Д.м.н., проф. Э.И. МАЦНЕВ, к.м.н., с.н.с. Е.Э. СИГАЛЕВА
Efficacy of piracetam in vertigo
E.I. MATSNEV, Y.E. SIGALEVA
Отделение физиологии и патологии слуховой и вестибулярной систем Государственного научного центра РФ — Институт медико-
биологических проблем РАН, Москва
Ключевые слова: головокружение, лечение, пирацетам.
Key words: vertigo, treatment, piracetam.
Известно, что поддержание функции равновесия зависит от координированной деятельности различных сенсорных систем организма. Вестибулярная система (внутреннее ухо) с сенсорными волосковыми клетками обеспечивает восприятие движения и позицию головы в пространстве, органы зрения важны для поддержания равновесия и окуломоторного контроля, кожные рецепторы в области стопы (опора) сигнализируют о контакте с поверхностью земли, мышцы и суставы информируют ЦНС о положении туловища в пространстве.
Противоречивая или искаженная информация от сенсорных систем или нарушение центральной обработки этой информации приводят к развитию различных типов головокружения, нарушению равновесия и походки [8]. Головокружение или затруднения в ориентации могут существенно нарушать качество жизни (КЖ) больного и нередко представляют трудности для диагностики и лечения.
Патофизиологические механизмы, приводящие к расстройствам деятельности вестибулярного аппарата, и этиология головокружения до настоящего времени остаются недостаточно изученными [3]. В этой связи лечение головокружения с нарушением равновесия является в большей мере эмпирическим, направленным на ослабление симптомов этих расстройств. Принципы действия многих видов терапии головокружения не вполне объяснимы, так как не определены четкие критерии их назначения, а отдельные методы лечения не всегда эффективны. Например, использование седативных средств в общей схеме лечения головокружения приводит к нарушению процесса центральной компенсации и может повлиять на процесс реабилитации [40, 45].
Патофизиология головокружения и способность к компенсации при наличии этих расстройств зависит от состояния ЦНС. Важная роль в улучшении церебральных интегративных функций принадлежит ноотропным препаратам (пирацетам, или ноотропил), не обладающим седативными и психостимулирующими свойствами [22].
Патофизиология вестибулярной системы
Периферические вестибулярные рецепторы включают сенсорные клетки, чувствительные к угловым (воспринимаемым посредством полукружных каналов) и линейным (воспринимаемым отолитами — саккулюсом и утрикулюсом) ускорениям. Одновременно отолитовая система реагирует на изменения в гравито-инерциальных сдвигах, возникающих при изменении положения головы в пространстве.
Вестибулярные нервные сигналы проходят через вестибулярные нервы и достигают четырех основных ядер (латерального, верхнего, медиального и нижнего), образующих центральный вестибулярный ядерный комплекс в стволе головного мозга. Эти ядра составляют центр, где множественная модальность сенсорной информации (включая зрительный, соматосенсорный и вестибулярные «входы») интегрируется в виде основы для центральной реконструкции сигналов о скоростях движений головы в трехмерном пространстве [18, 19, 32]. Кроме того, вестибулярные ядра вовлечены в премоторные и преперцептивные функции. Они имеют важное значение для контролирования позы и равновесия, стабилизации головы и взора в пространстве, а также для выработки центрального представления о позиции тела и движения в пространстве [31].
Контроль равновесия и движений глаз частично обеспечивается посредством вестибулярных нейронов второго порядка с нисходящими (вестибулоспинальная система) и восходящими (вестибулоокулярная система) аксональными проекциями. Ответвления вестибулярных нейронов, влияющие на окуломоторные и спинальные нейроны, соучаствуют в стабилизации взора [31].
Вестибулокортикальные пути, проходящие через субъядра таламуса, участвуют в обеспечении большинства когнитивных функций, таких как ориентация тела в пространстве (субъективная вертикаль), восприятие тела (схема тела) и пространственная память [31]. Иными словами, вестибулярные корковые поля (парието-инсулярная
© Э.И. Мацнев, Е.Э. Сигалева, 2009 |
e-mail: e.matsnev@mail.ru |
Zh Nevrol Psikhiatr Im SS Korsakova 2009;109:9:90
90 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 9, 2009 |

ЛЕЧЕНИЕ ГОЛОВОКРУЖЕНИЯ
вестибулярная кора, поля 2v и 3a) и подкорковые структуры (нижняя олива, ретикулярная формация, мозжечок) модулируют вестибулярную ядерную активность и контроль вестибулярной активности [4, 20].
Поэтому периферический лабиринтный дефицит или одностороннее поражение вестибулярного нерва может быть причиной нескольких синдромов: связанных с равновесием (неустойчивость, падение, нарушение локомоторной траектории), с окуломоторными нарушениями (спонтанный нистагм, отклонение взора, осциллопсия) и перцепцией (головокружение, отклонение в восприятии вертикали). В этой связи различные формы вестибулоспинальных или окуломоторных синдромов присутствуют у значительного числа больных с вестибулярной дисфункцией. Компенсация статического и динамического вестибулярного дефицита является хорошей моделью для изучения пластичности ЦНС и изучения адаптивной способности мозга [30].
С одной стороны, в литературе [17, 42] описаны структурные изменения в вестибулярных ядрах после их поражения, а с другой — экспериментально продемонстрированы различные нейрофизиологические изменения в статических и динамических свойствах вестибулярных клеток и нейрохимические модификации (вверх или вниз направленная регуляция влияния аминокислот, ацетилхолина, нейропептидов или их рецепторов) в этих условиях.
Хорошо известно, что использование лекарственных средств может изменить течение компенсаторного процесса при вестибулярном дефиците путем ускорения (при использовании средств, стимулирующих деятельность ЦНС) или снижения (при использовании седативных средств) восстановительных процессов [31, 40]. Однако прием этих средств не должен быть длительным, так как они могут осложнить течение восстановительных процессов [7].
Ноотропил — альтернатива в лечении головокружения
Ноотропил (пирацетам) был первым в новом классе лекарств, названных ноотропами (препаратами, которые влияют на когнитивные функции, не вызывая седативного эффекта или стимуляции). Хотя ноотропил является циклическим дериватом гамма-аминомасляной кислоты (ГАМК), его механизм не связан с действием этого нейротрансмиттера. Важным фактором, определяющим основной принцип действия ноотропила, является его способность восстанавливать эластичность клеточной мембраны. Этот эффект не является специфическим ни по отношению к определенному органу, ни по отношению к клеткам. Ноотропил имеет различные точки приложения: его способность улучшать функциональное состояние мозга связана с воздействием как на нейрональном, так и на сосудистом уровнях. Восстановление эластичности клеточной мембраны положительно влияет на функцию таких мембранных белков, как рецепторы, что на нейрональном уровне проявляется в улучшении церебральной нейротрансмиссии и пластичности нейронов, а также в нейропротективном эффекте. Имеются сообщения [36], что на сосудистом уровне улучшается микроциркуляция и церебральная перфузия.
Пирацетам продемонстрировал эффективность при различных заболеваниях (лечение когнитивных нарушений, связанных с возрастом, кортикального миоклонуса,
серповидно-клеточной анемии, дислексии), в том числе при лечении периферического и центрального головокружения. При этом важно подчеркнуть, что пирацетам (ноотропил) значительно улучшает центральные церебральные интегративные функции при головокружении при отсутствии психостимулирующего и седативного эффекта [41].
Прием пирацетама в дозе 800 мг 3 раза в день у 25 здоровых добровольцев приводил к достоверному уменьшению продолжительности нистагменной реакции при синусоидальном маятниковом качании («пендул-тест») на вестибулометрическом кресле в пределах 15 мин после поступления в организм препарата [38, 39]. Эти результаты подтверждаются ранее проведенным исследованием влияния пирацетама на частоту, амплитуду и скорость медленной фазы (СМФ) поствращательного нистагма у 16 добровольцев после приема препарата по 800 мг 3 раза в день. Средняя частота, амплитуда и СМФ нистагма после приема пирацетама уменьшилась на 9, 34 и 14% соответственно.
Исследование влияния пирацетама на продолжительность и скорость медленной фазы калорического нистагма (стимуляция водой при температуре 44 °С в течение 40 с) у 10 здоровых добровольцев продемонстрировало достоверное уменьшение этих показателей, сохранявшееся от 24 ч до 8 дней после калоризации лабиринтов [6].
Таким образом, было доказано достоверное влияние пирацетама на состояние лабиринта, проявляющееся в торможении нистагменной реакции после адекватной стимуляции.
Фармакологическая активность пирацетама (ноотропила)
Оценивая фармакокинетику пирацетама, следует отметить его высокую растворимость в воде, почти полную абсорбцию (отсутствие взаимодействия с пищей, с другими лекарственными средствами, почти 100% биодоступность при приеме per os). Пирацетам не связывается с протеинами плазмы, избирательно накапливается в стволе головного мозга, в мозжечке и базальных ганглиях, практически не метаболизируется (95% препарата через 30 ч выводится почками).
У пирацетама нет клеточной специфичности, он активен как на клеточных, так и на внутриклеточных мембранах, увеличивая активность фосфолипидов. Как известно, фосфолипиды являются важной частью клеточных мембран. Они обеспечивают пластические свойства мембран клеток и клеточных органоидов, которые нарушаются с возрастом в связи с накоплением свободных радикалов, при токсических воздействиях. Для лечебной активности необходимо поддержание высоких доз пирацетама.
Препарат проявляет высокую реологическую активность, его антиагрегантные свойства сходны с аспирином. Он снижает вязкость крови, увеличивает кровоток и микроциркуляцию, способствует улучшению снабжения клетки кислородом и нутриентами.
На уровне нейронов ЦНС пирацетам восстанавливает нейрональный метаболизм и клеточные связи (функции практически всех нейротрансмиттеров). Фармакологический эффект пирацетама зависит от его способности улучшать процесс нейротрансмиссии. Препарат взаимодействует с большинством нейротрансмиттерных систем, не оказывая, однако, специфического агонистического или
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 9, 2009 |
91 |
ЛЕКЦИЯ |
|
|
|
|
Новые стратегии включают активацию обучения и биоло- |
|
|
гические процессы запоминания на основе процессуаль- |
|
|
ной памяти [5]. |
|
|
Одни фармакологические вещества способны замед- |
|
|
лить процесс вестибулярной адаптации (алкоголь, барби- |
|
|
тураты, фенотиазин, антигистаминные препараты, холи- |
|
|
номиметики, адренергические препараты, атропин, ско- |
|
|
поламин и др.). Другие улучшают физиологические про- |
|
|
цессы этой адаптации (кофеин, амфетамин, АКТГ, пира- |
|
|
цетам) [7, 24]. |
|
|
В ряде исследований показано, что пирацетам (ноо- |
|
|
тропил) проявляет высокую эффективность в лечении го- |
|
|
ловокружения периферического, центрального или сме- |
|
|
шанного характера [27, 29, 41]. |
|
|
В связи с тем, что центральная вестибулярная адапта- |
|
|
ция и компенсация зависят от улучшения передачи нерв- |
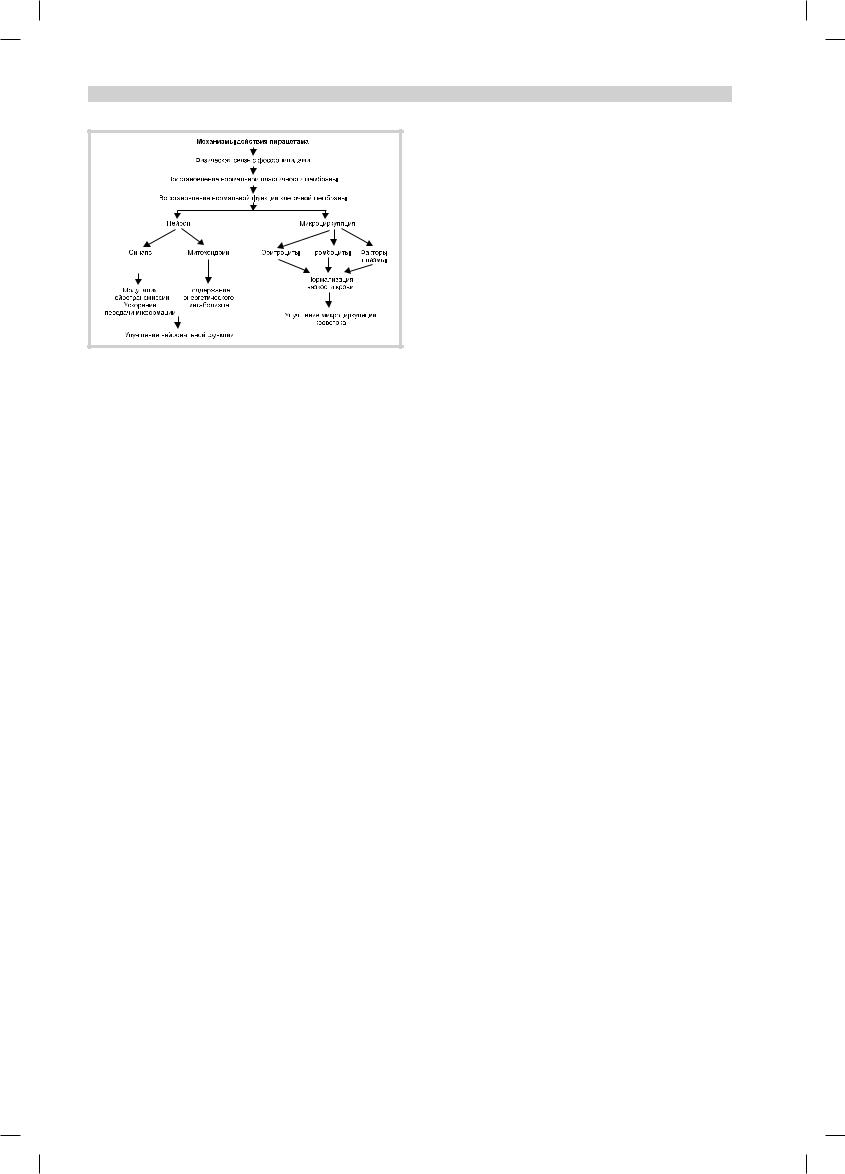
Механизмы действия пирацетама. |
ных импульсов, модулирующее действие пирацетама на |
|
|
|
холинергические, дофаминергические, норадренергиче- |
|
|
ские и глутаматергические системы способно ускорять |
антагонистического действия по отношению к тем или |
эти процессы. |
|
иным рецепторам. Он |
улучшает и модулирует нейро- |
Нейропластичность, по-видимому, имеет большое |
трансмиссию за счет увеличения плотности рецепторов и |
значение для вестибулярной адаптации, поскольку она |
|
усиления их функции. Это происходит в основном на |
важна для невральной перестройки. Согласно последним |
|
постсинаптическом уровне, т.е. за счет изменения актив- |
экспериментальным данным, пирацетам повышает ней- |
|
ности мембраны нервных клеток. В частности, действуя |
ропластичность. Важно подчеркнуть, что в этой связи эф- |
|
через восстановление числа и функции холинергических |
фективность пирацетама не зависит от этиологии голово- |
|
(мускариновых) и глутаматных рецепторов [36]. Таким |
кружения [25]. |
|
образом, влияние пирацетама на нейротрансмиссию в |
Пирацетам позитивно действует на центральные ме- |
|
большей мере связано с его способностью восстанавли- |
ханизмы нарушения равновесия [40]. Его эффект наибо- |
|
вать клеточную мембрану [35]. |
лее явно проявлялся у больных старших возрастных групп |
|
Основные механизмы фармакологического действия |
и при наличии гипоксии [9, 10, 22, 25, 43, 49]. |
|
пирацетама схематически представлены на рисунке. |
Клинические исследования [11, 16, 45, 46] показали, |
|
Клинические исследования |
что пирацетам может улучшать процесс обучения и эф- |
|
фективен при нарушении памяти. В последние годы по- |
||
У здоровых лиц «входные» вестибулярные, зритель- |
казана важная роль когнитивных процессов при расстрой- |
|
ные, проприоцептивные и другие сигналы от сенсорных |
ствах равновесия [25, 26]. Вместе с тем программирование |
|
систем интегрируются и «обрабатываются» в ЦНС в по- |
обучения является истинным когнитивным процессом |
|
рядке приоритетности (при участии нервного центра в |
[26]. В ряде исследований [27—29, 37, 38, 41] продемон- |
|
стволе головного мозга, получившего название — «компа- |
стрирована высокая эффективность пирацетама (ноотро- |
|
ратор»), но при ведущей роли информации от вестибуляр- |
пила) в лечении головокружения периферического, цен- |
|
ных органов [34]. |
|
трального или смешанного характера. |
При получении от «компаратора» выходной сенсор- |
Прием пирацетама в дозе 3,0 г/сут в течение 30 дней |
|
ной информации — противоречивой информации, сохра- |
обеспечивает улучшение социального и профессиональ- |
|
ненной в «памяти» мозга на основе предшествовавшего |
ного функционирования, а также КЖ у больных с голово- |
|
«сенсорного опыта», приобретенного организмом в про- |
кружением, причем переносимость этого курса лечения |
|
цессе развития, активируются нервные процессы, ини- |
большинством больных оценена как «хорошая» или |
|
циирующие так называемый «сенсорный конфликт» [34]. |
«очень хорошая» [13]. |
|
Последний может реализоваться в виде комплекса острых |
Лечение пирацетамом в дозе 2,4 г/сут у 50 больных с |
|
вестибулярных нарушений. Они проявляются симптома- |
периферическим (лабиринтным и ретролабиринтным) го- |
|
ми вестибуло-вегетативных расстройств (потливость, |
ловокружением в течение 60 дней привело к достоверному |
|
тошнота, рвота), оптомоторными нарушениями (ни- |
уменьшению числа эпизодов и интенсивности приступов |
|
стагм), пространственной дезориентацией, нарушением |
головокружения по сравнению с «плацебо» [28, 39]. |
|
восприятия вертикали |
(осциллопсия), расстройствами |
В исследовании U. Rosenhall и соавт. [41] c участием |
равновесия и другими нарушениями. |
143 больных с периферическим головокружением прием |
|
После острой вестибулярной дисфункции система |
пирацетама в аналогичной дозе в течение 8 нед достовер- |
|
равновесия нуждается в перестройке, на которую иногда |
но уменьшал нарушения равновесия и выраженность го- |
|
уходят многие дни и недели [7, 8, 12, 25, 26]. Основными |
ловокружения между их эпизодами по сравнению с пла- |
|
механизмами при этом процессе являются сенсорное за- |
цебо. |
|
мещение (или компенсация), выработка новых стратегий |
Эффект пирацетама был отмечен и у больных с голо- |
|
и процессы переобучения (или адаптация). Сенсорное за- |
вокружением, являющимся последствием черепно- |
|
мещение основано на нейрональной пластичности. В |
мозговой травмы и «хлыстовой» травмы шейного отдела |
|
основе адаптации преимущественно лежат механизмы |
позвоночника в результате дорожно-транспортных и бы- |
|
привыкания, хранения, обучения и модуляции [25, 26]. |
товых травм [1, 2, 29]. По современным представлениям, |
|
92 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 9, 2009 |

ЛЕЧЕНИЕ ГОЛОВОКРУЖЕНИЯ
постконтузионный синдром (ПКС) является комплексом соматических, когнитивных и эмоциональных нарушений. Головокружение является одним из ведущих проявлений ПКС в виде периферической, центральной или комбинированной вестибулярной дисфункции [26]. В основе ПКС лежат органические и псевдоорганические процессы: диффузное микроскопическое аксональное повреждение, макроскопические изменения во фронтальной, височной областях и глубоких слоях белого вещества, клеточные повреждения и метаболические нарушения в белом веществе фронтальной области, нарушения регионарного кровотока в паренхиме головного мозга и др. [26].
Большинство пациентов с ПКС полностью выздоравливают в течение 3 мес после травмы, хотя приблизительно у 1/3 больных ряд симптомов сохраняется на более длительный срок. Приблизительно у 8% пациентов симптомы ПКС могут сохраняться в течение года (хроническая фаза), иногда пожизненно [26]. Прогноз и ход реабилитации пациентов в подострой фазе этого синдрома определяют такие факторы, как тяжесть травмы и длительность потери сознания. Особенно частым осложнением ПКС, снижающим качество жизни пострадавших, является головокружение, по поводу которого нередко проводят судебномедицинское освидетельствование. Многие из этих пациентов частично или полностью утрачивают способность к труду. Существуют факты, доказывающие органическую основу повторяющегося головокружения после травмы головы, независимо от обращения за компенсацией ущерба [14].
По данным литературы, ряд психостимуляторов холинергических, дофаминергических препаратов и антидепрессантов могут оказывать определенный благоприятный эффект при лечении когнитивных и поведенческих проявлений травматического повреждения головного мозга. Однако для пациентов с головокружением после сотрясения мозга комплексных рекомендаций не существует [26].
Использование ноотропила в постконтузионном периоде способствует адаптации, а также улучшает микроциркуляцию внутреннего уха [37]. При дозах 2,4—4,8 г/сут препарат достоверно и быстро (2—6 нед), ослаблял головокружение и головную боль, уменьшал вестибулярные проявления (тормозил нистагм), способствовал восстановлению функции вестибулярного аппарата, повышал функцию равновесия и значимо уменьшал степень выраженности этих расстройств в период между приступами головокружения. Препарат повышал КЖ у больных с ПКС с наличием упорных головокружений [26].
Результаты 3 независимых исследований [1, 15, 29, 47, 48] по изучению эффективности курсового приема пирацетама при ПКС (8-недельный курс в дозе 2,4 или 4,8 г/ сут) с использованием двойного слепого метода выявили уменьшение симптомов или прекращение головокружения у достоверно большего числа пациентов по сравнению с плацебо.
Пирацетам показал высокую эффективность в лечении центрального головокружения сосудистой природы. Как известно, у лиц старше 60 лет головокружение, связанное с дефицитом кровоснабжения вестибулярного ядерного комплекса в стволе головного мозга, превалирует среди других причин головокружения [21, 23]. У 28 больных (средний возраст 65 лет) с хроническим сосудистым головокружением продолжительностью более 1 года прием пирацетама в дозе 800 мг 3 раза в сутки в течение 8 нед обеспечил достоверное уменьшение головокружения и улучшение показателей вестибулярной функции (по данным отоневрологического обследования) по сравнению с «плацебо» [21]. Отмеченный эффект пирацетама, по мнению автора, может быть связан с активацией процесса нейротрансмиссии, ускорением метаболических процессов и улучшением кровотока. В более ранних экспериментальных исследованиях было показано, что пирацетам в дозе 400 мг достоверно улучшал кохлеарный кровоток у морских свинок [33].
Заключение
Представленные данные свидетельствуют о том, что ноотропил (пирацетам) может ускорять процесс спонтанного восстановления у больных с острым головокружением, а также усиливать и стабилизировать адаптацию при хроническом головокружении. Таким образом, пирацетам способен усиливать нормальный процесс вестибулярной компенсации, восстанавливать окуломоторную и постуральную функцию у больных с периферическим и центральным головокружением [37].
Прием ноотропила в дозе 3,0 г/сут в течение 30 дней обеспечивает улучшение социального и профессионального функционирования, а также качества жизни у больных с головокружением [13]. Причем переносимость этого курса лечения 20 больных оценили как «хорошую» или «очень хорошую» [13]. Аналогичную оценку дали и другие 50 больных с головокружением, получавших курс лечения пирацетамом в дозе 2,4 г/сут в течение 60 дней [28]. В лечении больных с головокружением пирацетам хорошо сочетается с реабилитационной терапией [47].
Противопоказанием к приему препарата у больных с головокружением являются непереносимость пирацетама или других производных пирролидона, а также церебральные геморрагии.
Представленные данные свидетельствуют о том, что более чем 30-летний опыт мировой клинической медицины подтверждает фармакологические и клинические доказательства эффективности. Препарат эффективен при периферических, центральных, смешанных и постконтузионных головокружениях. Использование ноотропила является логическим подходом к симптоматическому лечению головокружения, что выгодно отличает его от ряда фармакологических средств, в частности вестибулярных супрессантов [41].
ЛИТЕРАТУРА
1.Aantaa E., Meurman O.H. The effect of piracetam (Nootropil 6215) upon the late symptoms of patienta with head injures. J Int Ved Res 1975;3:5:352— 353.
2.Aantaa E. et al. The effect of piracetam upon the late symptoms of patients with head injures. J Int Med Res 1975;3:354—355.
3.Baloh R.W. Vertigo. Lancet 1998;352:1841—846.
4.Bertoz A. How does the cerebral cortex process and utilize vestibular signals? In: Disorders of the vestibular system. Eds. R.W. Balow, G.M. Halmagyi. New York: Oxford University Press 1996;113—125.
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 9, 2009 |
93 |

ЛЕКЦИЯ
5.Berthoz A. Neural basis of spatial orientation and memory of routes: topokinetic memory or topokinesthesic memory. Rev Neurol (Paris) 2001;157(8— 9 Pt 1):779—789.
6.Boniver R. Acta Oto-laryngologica Belgica 1974;28:293—299.
7.Brandt Th.N. Vertigo: its multisensory syndromes. London: Springer-Verlag 1991;1—24.
ноотропы». Часть 2. «Ноотропил в лечении головокружения. Афины (Греция) 2007; 2—6.
27.Haguenauer J.P. Clinical study of piracetam in the treatment of vertigo. Les Cahiers d’ ORL 1986;21:460—466.
28.Haguenauer J.P. Essai clinique du piracetam dans le traitement des vertiges. Etude controlee versus placebo. Les Cahiers d’ ORL 1988;21:6:460—466.
8.Brandt T., Dieterich M., Strupp M. Vertigo and Dizziness — common com29. Hakkarainen H., Hakamies L. Piracetam in the treatment of postcontus-
plaints. London: Springer 2005.
9.Canonico P.L., Aronica E., Aleppe G. et al. Repeated injections of piracetam improve spatial learning and increase the stimulation of inositol phospholipids hydrolysis by excitatory amino acid in aged rats. Funct Neurol 1991;6:2:107—111.
10.Cohen S.A., Muller W.E. Effects of piracetam on N-methyl-d-aspartate receptor properties in the aged mouse brain. Pharmacology 1993;47:217— 222.
11.Croisile B., Trillet M., Fondarai J. et al. Long-term and high-dose piracetam treatment of Alzheimer’s disease. Neurology 1993;43:301—305.
12.Curthoys I.S., Halmagyi G.M. Vestibular compensation: a review of the oculomotor, neural, and clinical consequences of unilateral vestibular loss. J Vest Res 1995;5:67—107.
13.Dauman R., Billardon M., Fondarai J. Preliminary, double-blind, comparative study of the efficacy of Nootropyl (piracetam) versus placebo, in the treatment of vertigo. Les Cahiers d’ ORL 1995;4:241—248.
14.Davies R.A. et al. Dizziness following head injury: a neuro-otological study. J Neurol 1995;242:222—230.
15.Deza Bringas L. Treatment of the subjective post-traumatic syndrome with piracetam. Revista de Neuro-Psiquiatria 1984;47:74—86.
16.Diamond S.J., Brouwer E.Y.M. Increase in the power of human memory in normal man through the use of drugs. Psychopharmacologia 1976;49:307— 309.
17.Dieringer N. Vestibular compensation: neural plasticity and its relations to functional recovery after labyrinthine lesions in frogs and other vertebrates. Prog Neurobiol 1995;46:97—129.
18.Fernandez C., Goldberg J.M. Responses of peripheral vestibular neurons to angular and linear acceleration in the squirrel monkey. Acta Оtolaryngol 1975;80:101—110.
19.Fernandez C., Goldberg J.M. Physiology of peripheral neurons innervating otolith organs of the squirrel monkey. J Neurophysiol 1976;39:996—1008.
20.Furukushima K. Corticovestibular interactions: anatomy, electrophysiology, and functional considerations. Exp Brain Res 1997;117:1—16.
21.Gavalas G. Piracetam in the treatment of central vertigo of vascular origin. In. Abstract Symposium at Piracetam: 5 Years Progress in Pharmacology and Clinics. Athens (Greece) 1990;39—43.
22.Giurgea C. Piracetam: nootropic pharmacology of neurointegrative activity. Curr Develop Psychopharmacol 1976;3:222—273.
23.Giurgea C., Mouravieff-Lesuisse F. Central hypoxia models and correlations with aging brain. Neuropsychopharmacology 1978;2:1923—1931.
24.Goebel J.A. Management options for acute versus chronic vertigo. Otolaryngol Clin North Am 2000;33:483—493.
25.Guidetti G. (еd.) Rehabilitative management of the dizzy patient. Milano: Excerpta Medica 2000.
26.Guidetti G. Центральная роль когнитивных процессов при расстройстве равновесия. Материалы конгресса «Когнитивные функции и
sional syndrome. A double-blind study. Eur Neurol 1978;17:50—55.
30.Lacour M., Toupet M., Denise P. et al. Vestibular compensation. Fact, theories and clinical perspectives. Paris: Elsevier 1989;308.
31.Lacour M., Sterkers O. Histamine and Betahistine in the Treatmen of Vertigo. Elucidation of mechanisms of Action. CNS Drugs 2001;15:11:853— 870.
32.Lacour M. Restoration of vestibular function: basic aspects and practical advances for rehabilitation. Curr Мed Res Opin 2006;22:9:1651—1659.
33.Maass B., Soetanto R. Laryng Rhinol Otol 1988;67:132—135.
34.Matsnev E.I., Sigaleva E.E. Efficacy of histaminergic drugs in experimental motion sickness. J Vestibular Res 2007;17:313—321.
35.Muller W.E., Hartmann H., Koch S. Neurotransmission in aging — therapeutic aspects. In: Recent advances in the treatment of neurodegenerative disorders and cognitive dysfunction. International Academy for Biomedical and Drugs Research. Eds. G. Racagni, N. Brunello, S. Langer. Basel: Karger 1994;7:166—173.
36.Nootropil. Monograph UCB Pharma, 2004.
37.Norre M.E. Dysfunction and cerebral adaptation. In: Posture in otoneurology. Acta Otorhinolaryngol (Belg) 1990;44:2(II):139—181.
38.Oosterveld W.J. The efficacy of piracetam in vertigo. A double-blind study in patients with vertigo of central origin. Arzeimittel Forschung 1980;30(II):11: 1947—1949.
39.Oosterveld W.J. Piracetam in vertigo: a review. UCB Report 2000.
40.Peppard S.B. Effect of drug therapy on compensation from vestibular injury. Laryngoscope 1986;96:878—898.
41.Rosenhall U., Deberdt W., Friberg U. et al. Piracetam in patients with chronic vertigo. Results of a double-blind, placebo-controlled study. Clin Drug Invest 1996;11:51:251—260.
42.Smith P.H., Darlington C.L. Neurochemical mechanisms of recovery from peripheral vestibular lesions (vestibular compensation). Brain Res Brain Res Rev 1991;16:117—113.
43.Stoll L., Schubert T., Muller W.E. Age related deficits of cerebral muscarinic receptor function in the moose: partial restoration by chronic piracetam treatment. Neurobiol Aging 1991;13:39—44.
44.Vernon M.W., Sorkin E.M. Piracetam — an overview of its pharmacologic properties and a review of its pharmacologic properties and a review of its therapeutic use in senile cognitive disorders. Drugs Aging 1991;1:1:17—35.
45.Vibert P.D.,Terra H., Hausler E.R. Ie traitment medicamenteux des vertiges. Rev Med de la Romande 1993;113:685—688.
46.Wilsher C. Piracetam and dislexia — effects on reading tests. J Clin Psychopharmacol 1987;7:4:230—237.
47.Winblad B. Piracetam: a review of pharmacological properties and clinical uses. CNS Drug Rev 2005;11:169—182.
48.Wustmann Ch., Fischer H.D., Schmidt J. The effect of piracetam on posthypoxic dopamine release inhibition. Acta Biol Med German 1982;41:729— 732.
94 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 9, 2009 |
