
- •Краткий курс
- •Карбоновые кислоты и их производные
- •1. Способы получения карбоновых кислот
- •1.1. Реакции окисления
- •1.2. Синтез карбоновых кислот из галогенопроизводных
- •1.2.1.Синтез карбоновых кислот через нитрилы
- •1.2.2. Синтез карбоновых кислот реакцией Гриньяра
- •1.3. Гидролиз производных карбоновых кислот
- •2. Химические свойства карбоновых кислот
- •2.1. Кислотно-основные свойства
- •2.2. Декарбоксилирование карбоновых кислот
- •2.3. Галогенирование карбоновых кислот
- •3. Производные карбоновых кислот
- •3.1. Реакции нуклеофильного замещения: механизм и реакционная способность
- •3.2. Сложные эфиры
- •3.1.1. Способы получения
- •3.1.2. Химические свойства
- •3.3. Галогенангидриды
- •3.4. Ангидриды
- •3.5. Амиды
- •3.5.1. Способы получения
- •3.5.2. Химические свойства
- •3.6. Нитрилы
- •4. Α,β-Ненасыщенные карбоновые кислоты
- •4.1. Способы получения
- •4.2. Химические свойства
- •5. Дикарбоновые кислоты
- •5.1. Способы получения
- •5.2. Свойства дикарбоновых кислот
- •5.3. Малоновый эфир
- •6. Задачи и упражнения
- •1. Способы получения
- •1.1. Восстановление азотсодержащих соединений
- •1.2. Алкилирование аммиака и аминов
- •2. Химические свойства
- •2.1. Основность аминов
- •2.2. Амины как нуклеофилы
- •2.2.1. Алкилирование и ацилирование аминов
- •2.2.2. Взаимодействие первичных и вторичных аминов с альдегидами и кетонами
- •2.2.3. Взаимодействие аминов с азотистой кислотой
- •2.3. Особенности химического поведения ароматических аминов
- •2.3.1. Реакции электрофильного замещения
- •2.3.2. Превращения первичных ароматических аминов через соли арилдиазония
- •3. Задачи и упражнения
3.1.2. Химические свойства
Гидролиз
Сложные эфиры гидролизуются до карбоновых кислот и спиртов как в кислой, так и в щелочной среде. Кислотный гидролиз обратим, это обратная реакция этерификации. Механизм кислотного гидролиза можно изобразить, рассмотрев механизм этерификации с конца.
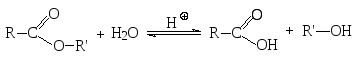
Щелочной гидролиз необратим, поскольку в результате реакции образуется не сама карбоновая кислота, а ее соль, совершенно неактивная в реакции с нуклеофильным спиртом, поэтому обратная реакция не идет.

Необратимый щелочной гидролиз называют омылением, поскольку этой реакцией с давних пор из животных жиров, которые представляют собой сложные эфиры глицерина и так называемых жирных кислот, получали соли этих кислот, обладающие поверхностной активностью и использовавшиеся в качестве мыла.
Аммонолиз
Сложные эфиры при взаимодействии с аммиаком или аминами выступают как ацилирующие агенты. Продуктами этих реакций являются амиды карбоновых кислот, например:
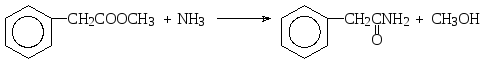
метилфенилацетат фенилацетамид

этилформиат N,N-диметилформамид
3.3. Галогенангидриды
Галогенангидриды карбоновых кислот, или ацилгалогениды, представляют собой производные карбоновых кислот, в которых вместо гидроксильной группы находится атом галогена. Названия галогенопроизводных производятся заменой суффикса и окончания –овая кислотав названии карбоновой кислоты на суффикс–оилгалогенид.Например, хлоранигидрид уксусной кислоты называется этаноилхлорид (или ацетилхлорид), а хлорангидрид 2-метилпентановой кислоты – 2-метилпентаноилхлорид.
Из всех галогенопроизводных карбоновых кислот наибольшее значение имеют хлорангидриды. Их получают из карбоновых кислот действием тионилхлорида или пентахлорида фосфора.
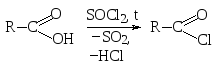

Хлорангидриды карбоновых кислот имеют большое значение в органической химии, поскольку они являются сильнейшими ацилирующими агентами, способными ацилировать практически любые нуклеофилы:
С-нуклеофилы, например, арены в реакциях ацилирования по Фриделю-Крафтсу до ароматических кетонов

О-нуклеофилы, например, воду или гидроксид-анион в реакциях нейтрального или щелочного гидролиза хлорангидридов до карбоновых кислот или их солей, спирты и фенолы или алкоголяты и феноляты до сложных эфиров, соли карбоновых кислот до ангидридов карбоновых кислот. Например, при взаимодействии бензоилхлорида с бензоатом натрия образуется ангидрид бензойной кислоты (бензойный ангидрид).

N-нуклеофилы, например, аммиак или первичные и вторичные амины при получении амидов карбоновых кислот. Так, при ацилировании метиламина пропаноилхлоридом в присутствии основания (например, щелочи) образуется N-метилпропанамид. Щелочь выступает в данной реакции не как катализатор, а как реагент, нейтрализующий выделяющийся хлороводород, который мог бы в противном случае реагировать с метиламином как основанием и дезактивировать его нуклеофильные свойства.

Эта реакция, как и другие реакции ацилирования О- и N-нуклеофилов, протекает по механизму нуклеофильного замещения.

