
- •Краткий курс
- •Карбоновые кислоты и их производные
- •1. Способы получения карбоновых кислот
- •1.1. Реакции окисления
- •1.2. Синтез карбоновых кислот из галогенопроизводных
- •1.2.1.Синтез карбоновых кислот через нитрилы
- •1.2.2. Синтез карбоновых кислот реакцией Гриньяра
- •1.3. Гидролиз производных карбоновых кислот
- •2. Химические свойства карбоновых кислот
- •2.1. Кислотно-основные свойства
- •2.2. Декарбоксилирование карбоновых кислот
- •2.3. Галогенирование карбоновых кислот
- •3. Производные карбоновых кислот
- •3.1. Реакции нуклеофильного замещения: механизм и реакционная способность
- •3.2. Сложные эфиры
- •3.1.1. Способы получения
- •3.1.2. Химические свойства
- •3.3. Галогенангидриды
- •3.4. Ангидриды
- •3.5. Амиды
- •3.5.1. Способы получения
- •3.5.2. Химические свойства
- •3.6. Нитрилы
- •4. Α,β-Ненасыщенные карбоновые кислоты
- •4.1. Способы получения
- •4.2. Химические свойства
- •5. Дикарбоновые кислоты
- •5.1. Способы получения
- •5.2. Свойства дикарбоновых кислот
- •5.3. Малоновый эфир
- •6. Задачи и упражнения
- •1. Способы получения
- •1.1. Восстановление азотсодержащих соединений
- •1.2. Алкилирование аммиака и аминов
- •2. Химические свойства
- •2.1. Основность аминов
- •2.2. Амины как нуклеофилы
- •2.2.1. Алкилирование и ацилирование аминов
- •2.2.2. Взаимодействие первичных и вторичных аминов с альдегидами и кетонами
- •2.2.3. Взаимодействие аминов с азотистой кислотой
- •2.3. Особенности химического поведения ароматических аминов
- •2.3.1. Реакции электрофильного замещения
- •2.3.2. Превращения первичных ароматических аминов через соли арилдиазония
- •3. Задачи и упражнения
2.3. Особенности химического поведения ароматических аминов
2.3.1. Реакции электрофильного замещения
Выше уже отмечались некоторые особенности ароматических аминов:
взаимодействие с азотистой кислотой первичных ароматических аминов в отличие от первичных алифатических аминов приводит к образованию солей арилдиазония;
взаимодействие третичных ароматических аминов с азотистой кислотой протекает как электрофильное нитрозирование в ароматическое ядро.
Кроме реакции нитрозирования, ароматические амины легко вступают и в обычные реакции электрофильного замещения в ароматическое ядро. Аминогруппа, обладая положительным мезомерным эффектом, который превышает воздействие отрицательного индуктивного эффекта, является одним из самых сильных электронодонорных заместителей, активируя молекулу и направляя замещение в орто- ипара-положения. Реакционная способность ароматических аминов в реакциях электрофильного замещения настолько высока по сравнению с бензолом и его гомологами, что некоторые реакции могут быть осуществлены в более мягких условиях и не требуют катализа. Однако, основный характер и склонность первичных ароматических аминов к окислению делает условия проведения некоторых реакций ароматического электрофильного замещения для них неприемлемыми, так как некоторые реагенты являются сильными кислотами и окислителями. Кислоты, протонируя аминогруппу, превращают ее из активирующего заместителя в сильный дезактивирующий заместитель:
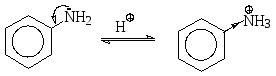
+М>-I только –I-эффект
(активирущий, 1-го рода) (дезактивирующий, 2-го рода)
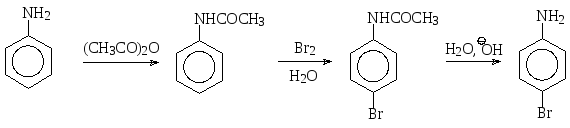
Бромирование. При взаимодействии анилина с бромной водой происходит электрофильное бромирование, причем реакционная способность анилина при введении одного атома брома, который является электроноакцепторным заместителем, в бензольное кольцо понижается незначительно, так что бромирование идет дальше до образования 2,4,6-триброманилина.

Для понижения реакционной способности анилина и получения монобромзамещенного анилина используют предварительное ацетилирование до ацетанилида, в котором сохраняется ориентирующее действие заместителя (+М-эффект по-прежнему больше –I-эффекта), но из-за сопряжения неподеленной пары электронов на атоме азота не только с бензольным кольцом, но и с карбонильной группой донорные свойства заместителя уменьшаются. Ацетанилид подвергают действию бромной воды, при этом образуется практически только один продукт – пара-бромацетанилид, который гидролизом (в кислой или щелочной среде) может быть превращен впара-броманилин.
Сульфирование. Анилин при взаимодействии с концентрированной серной кислотой превращается в гидросульфат фениламмония, который при нагревании до 200ОС в результате электрофильного сульфирования превращается впара-аминобензолсульфокислоту, илисульфаниловую кислоту.

Нитрование.Нитрование ароматических соединения обычно осуществляют смесью концентрированных азотной и серной кислот. Анилин в такой смеси существует практически полностью в виде соли фениламмония, поэтому его нитрование, если и происходит, то идет очень медленно и приводит к продуктумета-замещения. Однако при этом взаимодействии весьма существенными оказываются процессы деструктивного окисления анилина, что бывает заметно по обильному выделению оксидов азота. Поэтому нитрование анилина производят, предварительно «защитив» аминогруппу от воздействия кислой среды и окислителя ацетильной группой, которая резко понижает основность атома азота и предотвращает протонирование и окисление. После нитрования в обычных условиях образующийся как основной продуктпара-нитроацетанилид гидролизуют в кислой или щелочной среде допара-нитроанилина.

