- •Краткий курс
- •Карбоновые кислоты и их производные
- •1. Способы получения карбоновых кислот
- •1.1. Реакции окисления
- •1.2. Синтез карбоновых кислот из галогенопроизводных
- •1.2.1.Синтез карбоновых кислот через нитрилы
- •1.2.2. Синтез карбоновых кислот реакцией Гриньяра
- •1.3. Гидролиз производных карбоновых кислот
- •2. Химические свойства карбоновых кислот
- •2.1. Кислотно-основные свойства
- •2.2. Декарбоксилирование карбоновых кислот
- •2.3. Галогенирование карбоновых кислот
- •3. Производные карбоновых кислот
- •3.1. Реакции нуклеофильного замещения: механизм и реакционная способность
- •3.2. Сложные эфиры
- •3.1.1. Способы получения
- •3.1.2. Химические свойства
- •3.3. Галогенангидриды
- •3.4. Ангидриды
- •3.5. Амиды
- •3.5.1. Способы получения
- •3.5.2. Химические свойства
- •3.6. Нитрилы
- •4. Α,β-Ненасыщенные карбоновые кислоты
- •4.1. Способы получения
- •4.2. Химические свойства
- •5. Дикарбоновые кислоты
- •5.1. Способы получения
- •5.2. Свойства дикарбоновых кислот
- •5.3. Малоновый эфир
- •6. Задачи и упражнения
- •1. Способы получения
- •1.1. Восстановление азотсодержащих соединений
- •1.2. Алкилирование аммиака и аминов
- •2. Химические свойства
- •2.1. Основность аминов
- •2.2. Амины как нуклеофилы
- •2.2.1. Алкилирование и ацилирование аминов
- •2.2.2. Взаимодействие первичных и вторичных аминов с альдегидами и кетонами
- •2.2.3. Взаимодействие аминов с азотистой кислотой
- •2.3. Особенности химического поведения ароматических аминов
- •2.3.1. Реакции электрофильного замещения
- •2.3.2. Превращения первичных ароматических аминов через соли арилдиазония
- •3. Задачи и упражнения
2.2. Амины как нуклеофилы
2.2.1. Алкилирование и ацилирование аминов
Как нуклеофилы, амины могут реагировать с реагентами, имеющими электрофильные центры. При этом могут протекать как реакции замещения, так и реакции присоединения. Взаимодействиями первого типа являются реакции алкилирования и ацилирования аминов.
При алкилированииаминов галогенопроизводными углеводородов реакция может идти по одному из известных механизмов нуклеофильного замещения. В результате образуется соль аммония, которую можно перевести в «свободный» амин действием основания (см. способы получения аминов). Так, алкилированием первичного амина можно получить вторичный амин, алкилированием вторичного амина – третичный, а при алкилировании третичного амина образуется четвертичная соль аммония. Например, взаимодействием бензиламина с этилбромидом получают Ν-этилбензиламин, а последовательное метилирование метиламина с помощью метилиодида приводит к иодиду тетраметиламмония в качестве конечного продукта. Этот же продукт можно получить и при взаимодействии метиламина с тремя эквивалентами метилиодида.
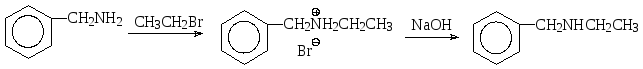
бромид бензилэтиламмония
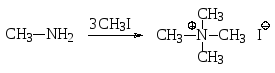
иодид тетраметиламмония
Ацилированиеаминов до амидов карбоновых кислот осуществляют такими производными карбоновых кислот, как галогенангидриды и ангидриды. Например, взаимодействием пропиламина с бензоилхлоридом в присутствии щелочи получают Ν-пропиламид бензойной кислоты (Ν-пропилбензамид), а реакция анилина с ангидридом уксусной кислоты приводит к Ν-фенилацетамиду.
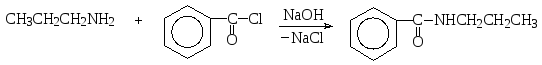
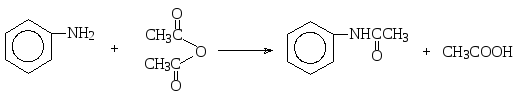
2.2.2. Взаимодействие первичных и вторичных аминов с альдегидами и кетонами
С альдегидами и кетонами первичные и вторичные амины реагируют по механизму нуклеофильного присоединения. С первичными аминами образуются азометины (основания Шиффа):
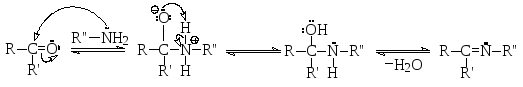
Так, например, анилин реагирует с бензальдегидом с образованием безилиденанилина.
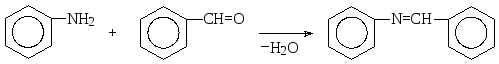
Вторичные амины с альдегидами и кетонами, имеющими атом водорода в α-положении, дают аддукт, который стабилизируется также в результате дегидратации, однако, поскольку при атоме азота в этом аддукте нет атома водорода, происходит отщепление воды с образованием двойной связи между бывшим карбонильным атомом углерода и α-атомом углерода. Такие продукты называют енаминами. Рассмотрим эту реакцию на примере взаимодействия циклогексанона с диметиламином с образованием 1-(Ν,Ν-диметиламино)циклогексена.
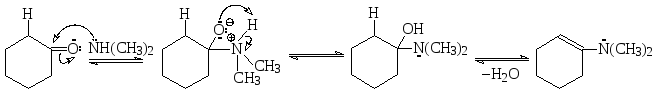
2.2.3. Взаимодействие аминов с азотистой кислотой
Взаимодействие аминов с азотистой кислотой осуществляют, действуя на амины нитритом щелочного металла в кислой среде, чаще всего в соляной кислоте. При этом используется избыток кислоты, необходимый для образования электрофильной частицы – нитрозил-катиона, который и реагирует с амином, находящимся в равновесии с его протонированной формой.
Первичные алифатические амины реагируют с нитритом натрия в избытке соляной кислоты по механизму, который можно рассмотреть на конкретном примере пропиламина.
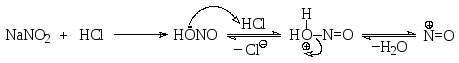
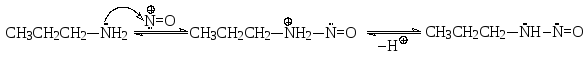
О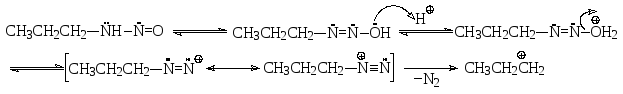 бразовавшийся
при взаимодействии амина с нитрозил-катионом
Ν-нитрозопропиламин находится в
равновесии с его таутомером (таутомеры
– структурные изомеры, находящиеся в
динамическом равновесии и превращающиеся
друг в друга в результате перемещения
какого-либо атома или группы атомов,
чаще всего – атома водорода, см. Альдегиды
и кетоны), из которого после протонирования
и отщепления воды образуется катион
пропилдиазония, чрезвычайно неустойчивый,
как и все алифатические диазониевый
катионы.
бразовавшийся
при взаимодействии амина с нитрозил-катионом
Ν-нитрозопропиламин находится в
равновесии с его таутомером (таутомеры
– структурные изомеры, находящиеся в
динамическом равновесии и превращающиеся
друг в друга в результате перемещения
какого-либо атома или группы атомов,
чаще всего – атома водорода, см. Альдегиды
и кетоны), из которого после протонирования
и отщепления воды образуется катион
пропилдиазония, чрезвычайно неустойчивый,
как и все алифатические диазониевый
катионы.
Этот катион с отщеплением молекулы азота превращается в карбокатион, с которым могут происходить различные превращения: присоединение воды с образованием спирта, присоединение хлорид-аниона с образованием пропилхлорида, отщепление протона с образованием пропена, а также изомеризация в изопропилкатион и образование изопропилового спирта и изопропилхлорида. В качестве основного продукта при взаимодействии первичных алифатических аминов с азотистой кислотой получаются спирты, поскольку реакция проходит в большом избытке воды.
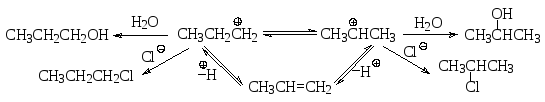
Первичные ароматические аминыреагируют с азотистой кислотой аналогично первичным алифатическим аминам, однако образующиеся катионы арилдиазония в отличие от соответствующих алифатических катионов достаточно устойчивы, особенно при низкой температуре. Таким образом, при взаимодействии первичного ароматического амина с азотистой кислотой при 5-10ОС в качестве продукта реакции образуетсясоль арилдиазония. Эта реакция получила названиереакциидиазотирования. Для анилина уравнение этой реакции выглядит следующим образом:
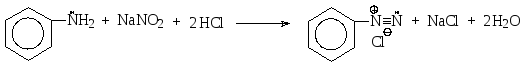
хлорид фенилдиазония
Вторичные аминылюбого строения с азотистой кислотой вступают в реакцию, которая заканчивается на стадии нитрозирования атома азота. При этом образуются Ν-нитрозоамины.
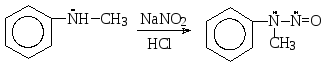
Ν-метиланилин Ν-метил-Ν-нитрозоанилин
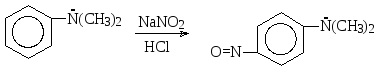
Третичные алифатические амины с азотистой кислотой не взаимодействуют. Но третичные ароматические аминывступают с азотистой кислотой в реакцию электрофильного замещения в бензольное кольцо, причем электрофильной частицей в этой реакции является нитрозил-катион. В результате образуется продукт замещения атома водорода впара-положении на нитрозогруппу, т.е. происходит нитрозирование по атому углерода ароматического кольца. Так, например, при взаимодействии Ν,Ν-диметиланилина с нитритом натрия в соляной кислоте образуетсяпара-нитрозо-Ν,Ν-диметиланилин: