
А Е Щеголев Органическая химия 2016 / 12 Гетероциклические соединения
.pdf
Глава 12. ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
Гетероциклические соединения — это вещества, молекулы которых содержат циклы, построенные из атомов разных химических элементов. Обычно такими гетероатомами являются азот, кислород, сера, но могут быть фосфор, кремний, селен, бор и др. Циклы могут быть ароматическими, насыщенными и ненасыщенными.
Гетероциклические соединения чрезвычайно распространены как в животном, так и в растительном мире. Очень многие биологически важные вещества содержат в своѐм составе гетероциклические фрагменты.
12.1. КЛАССИФИКАЦИЯ И НОМЕНКЛАТУРА
Гетероциклические соединения могут быть классифицированы:
1)по размеру цикла,
2)по природе гетероатома,
3)по числу гетероатомов в цикле.
Тривиальные названия здесь широко распространены. Примерами гетероциклических соединений (и их тривиальных названий), относящихся к разным группам, являются следующие вещества:
|
|
|
N |
N |
N |
S |
N |
H |
H |
|
H |
пиррол |
пирролидин |
тиофен |
имидазол |
|
|
H |
|
|
N |
N |
O |
N |
N |
N |
N |
|
|
H |
H |
пиридин |
пиразин |
пиперазин |
морфолин |
Согласно номенклатурным правилам ИЮПАК (номенклатура гетероциклических соединений) присутствие гетероатома в цикле указывается приставками окс(а)- (О), ти(а)- (S), селен(а)- (Se), аз(а)- (N), фосф(а)- (Р),
арс(а)- (As), сил(а)- (Si). (Буква «а» может быть опущена для благозвучия.) Число одинаковых гетероатомов обозначается количественными приставками ди-, три-, тетра- и т.д. Если в гетероцикле несколько разных гете-
600

роатомов, то их называют в определѐнной последовательности: окса-,
тиа-, селена-, аза-, фосфа-, арса-, сила-.
Размер цикла обозначается с помощью корня слова: трѐхчленные циклы — -ир, четырѐхчленные — -ет, пятичленные — -ол, шестичленные
—-ин, семичленные — -епин.
Вназвании гетероциклических соединений отражают и степень гидрирования (насыщенности) атомов гетероцикла. Основное название (без суффиксов) относится к соединению с максимально возможным числом двойных связей в цикле, но исключение составляют трѐхчленные циклы
—для обозначения их ненасыщенности добавляется суффикс -ен (для азотосодержащих — -ин).
Полностью гидрированное соединение обозначают суффиксами -идин (для азотосодержащих гетероциклов) или -ан (для кислородо- и серосодержащих гетероциклов), но для циклов с числом атомов 6 и более может быть использована приставка пергидро-. Для частично гидрированных соединений используют приставки дигидро-, тетрагидро-, при этом цифровыми локантами указываются атомы цикла, к которым присоединены атомы водорода. Если водородный атом присоединѐн только к одному из гетероатомов, это обозначается буквой Н и цифрой, указывающей гидрированный атом.
Для названия производных гетероциклических соединений необходимо пронумеровать атомы цикла. Обычно нумерация начинается с гетероатома. Если имеется несколько гетероатомов, то используют ряд убы-
вающего старшинства: O, S, Se, Te, N, P, As, Sb, Bi, Si, Ge, Sn, Pb, B, Hg.
Для некоторых гетероциклических соединений сохраняется особый вид нумерации. Примеры названий некоторых соединений:
|
|
|
|
|
N |
|
N |
N |
N |
O |
N |
N |
|
O |
||||||
H |
|
H |
|
H |
||
|
|
|
||||
азирин |
2Н-азирин |
азиридин |
оксиран |
1,3-диазол 1,2-оксазол |
||
|
|
N |
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
O |
O |
||
|
S |
|
|
N |
S |
H3C |
Si CH3 |
||||
4,5-дигидро-1,3-тиазол |
1,3-диазин |
тиепин |
2,2-диметилпергидро- |
||||||||
|
|
|
|
|
|
|
|
-1,3,2-диоксасилин |
|||
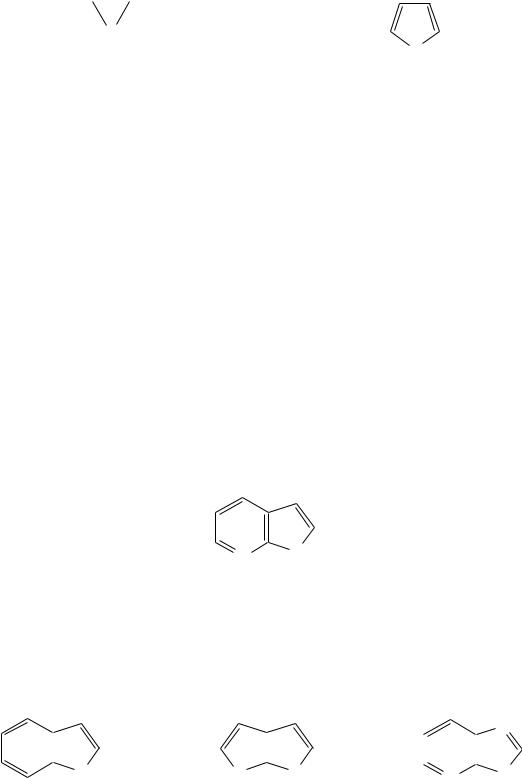
Гетероциклы могут быть названы и по заменительной номенклатуре. При этом заменительные приставки окса-, тиа-, аза- и др. присоединяются к названию карбоциклического соединения, например:
601
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
||
|
|
N |
S |
|||||||
|
|
H |
|
|
||||||
|
|
|
|
|
|
|
||||
1-азациклопроп-2-ен 1-азациклобут-1,3-диен |
1-тиациклопент-2,4-диен |
|||||||||
Названия гетероциклических соединений с двумя и более конденсированными циклами строятся по следующим правилам.
1.Выбирают главный цикл. При этом старшинство циклических систем определяется по следующим критериям (в порядке убывания приоритета):
а) при наличии карбоциклической и гетероциклической систем выбирается цикл, содержащий гетероатом;
б) при наличии гетероциклов с разными гетероатомами выбирается цикл, содержащий наиболее электроотрицательный гетероатом;
в) если циклы имеют разный размер, выбирается цикл большего размера;
г) если гетероциклы содержат разное число гетероатомов, выбирается цикл, содержащий наибольшее число гетероатомов.
2.Для указания места сочленения циклов в главном цикле связи обозначают буквами a, b, c, d и т.д., начиная со связи гетероатом—углерод. В младшем цикле место сочленения циклов указывается с помощью цифровых локантов. Например:
d |
c 3 |
4 |
|
|
|
e |
b 2 |
5 |
f N a NH1
3.Название младшего цикла даѐтся приставкой бензо-, пирро-, имидазо- и др. по названию бензольного, пиррольного или имидазольного циклов соответственно. Примеры названий конденсированных систем (часто используются тривиальные названия циклов):
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
3 |
|
|
|
|
|
4 |
N |
||
|
|
b |
|
|
|
|
b |
|
b |
|
|
2 |
|
|
|
a O |
S |
|
|
|
a O |
|
N a |
|
5 |
N 1 |
|
|
|
2 |
|
|
|
||||||||
|
|
|
1 |
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
бензо[b]фуран |
тиено[2,3-b]фуран |
имидазо[4,5-b]пиридин |
|||||||||||
602
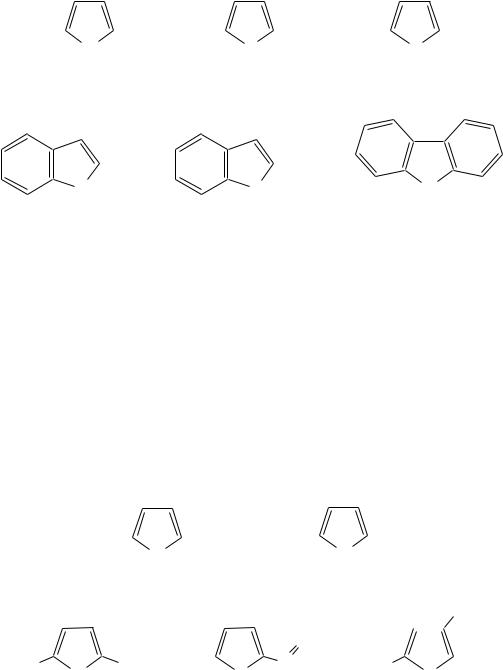
12.2. ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ С ОДНИМ ГЕТЕРОАТОМОМ
Наиболее важны в практическом отношении такие пятичленные гетероциклы, как пиррол, фуран, тиофен и конденсированные системы на их основе: индол, кумарон и карбазол.
N |
O |
S |
H |
|
|
пиррол |
фуран |
тиофен |
|
N |
O |
N |
|
H |
|
H |
индол |
кумарон |
|
карбазол |
12.2.1.НОМЕНКЛАТУРА ПИРРОЛА, ФУРАНА И ТИОФЕНА И ИХ ПРОИЗВОДНЫХ
Пиррол, фуран и тиофен могут иметь систематические названия по номенклатуре гетероциклов азол, оксол и тиол, но такие систематические названия практически не используются, и в качестве родоначальных названий этих гетероциклов рекомендуются тривиальные названия.
Положение заместителей указывается греческими буквами или цифровыми локантами:
4 |
3 |
|
|
5 |
2 |
|
|
|
X |
|
X |
|
1 |
|
|
Например:
|
|
|
|
|
|
|
CH3 |
|
|
|
|
O |
|
|
|
Br |
N |
CH3 |
O |
C |
H3C |
S |
|
|
H |
||||||
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2-бром-5-метилпиррол |
2-фуранкарбальдегид |
2,4-диметилтиофен |
|||||
-бром- ’-метилпиррол |
-фуранкарбальдегид |
,’-диметилтиофен |
|||||
|
|
|
фурфурол |
|
|
|
|
603
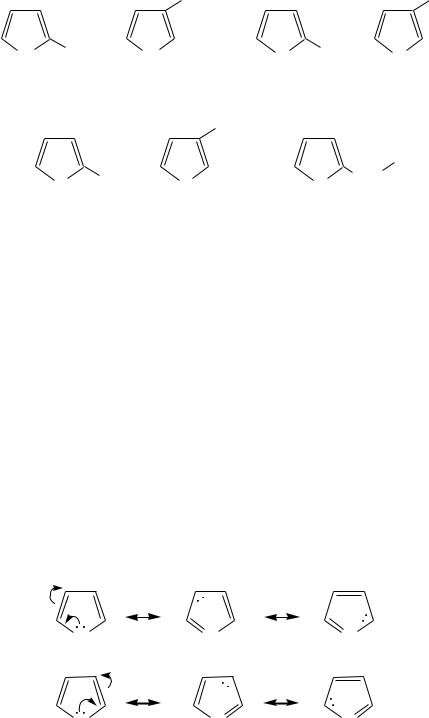
Радикалы, образованные от пиррола, фурана, тиофена и их производных, имеют следующие тривиальные названия:
N |
N |
S |
S |
H |
H |
|
|
-пиррил |
-пиррил |
-тиенил |
-тиенил |
O |
O |
O CH2 |
-фурил |
-фурил |
фурфурил |
12.2.2. СТРОЕНИЕ ПИРРОЛА, ФУРАНА И ТИОФЕНА
Молекулы пиррола, фурана и тиофена содержат систему сопряжѐнных связей и атом с неподелѐнной электронной парой. В результате образуется циклическая сопряжѐнная система с шестью -электронами (четыре-электрона от двух двойных связей и два — от гетероатома). Поэтому данные соединения имеют ароматический характер.
За счѐт неподелѐнной электронной пары гетероатом в этом кольце является электронодонором, на углеродных атомах электронная плотность повышена (по сравнению с бензолом), и пятичленные гетероциклы в целом являются -избыточными ароматическими системами. Циклическую делокализацию неподелѐнной пары электронов гетероатома можно показать с помощью граничных структур:
|
- |
|
|
|
+ |
+ |
- |
|
|
||
X |
X |
X |
|
|
|
- |
|
|
+ |
- |
+ |
|
|
||
X |
X |
|
X |
Квантово-химическими расчѐтами показано, что величина электронной плотности в -положении больше, чем в -положении.
В пространстве молекула такого соединения представляет плоский пятиугольник, однако длины связей и валентные углы неодинаковы. Это связано с неравномерностью распределения -электронной плотности в
604
кольце и зависит от природы гетероатома. Чем электроотрицательнее гетероатом, тем более неравномерно распределена электронная плотность и, следовательно, меньшей ароматичностью обладает система. Поэтому ряд уменьшения ароматичности (по сравнению с бензолом) можно показать следующим образом (в скобках приведена энергия делокализации ароматической системы в кДж/моль):
бензол (151) > тиофен (122) > пиррол (90) > фуран (68).
12.2.3.ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА ПИРРОЛА, ФУРАНА И ТИОФЕНА
Пиррол, фуран и тиофен являются бесцветными жидкостями с приятным запахом, практически нерастворимы в воде.
Химические свойства пятичленных гетероциклических соединений определяются как наличием ароматического цикла, так и наличием гетероатома.
12.2.3.1. Кислотно-оснόвные свойства
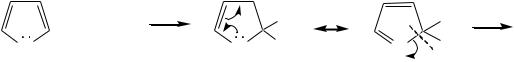
Пиррол, фуран и тиофен взаимодействуют с сильными кислотами. В случае пиррола, фурана и их алкилпроизводных обычно происходит «осмоление» (олигомеризация и полимеризация), тиофеновое кольцо к разрушению под действием холодных кислот устойчиво. Данное свойство пиррола, фурана и отчасти тиофена и их производных называется ацидофобностью. Ацидофобность связана с присоединением протона в большинстве случаев к -углеродному атому, разрушением ароматической системы и дальнейшим превращением активной диеновой системы:
|
+ |
|
|
|
|
+ H+ |
H |
+ |
H |
. . . |
|
X |
X H |
H |
|||
X |
|
Наибольшей основностью обладает пиррол, он легче всего протонируется. Самым слабым основанием из рассматриваемых гетероциклов является тиофен, он наиболее трудно протонируется, поэтому он наименее ацидофобен.
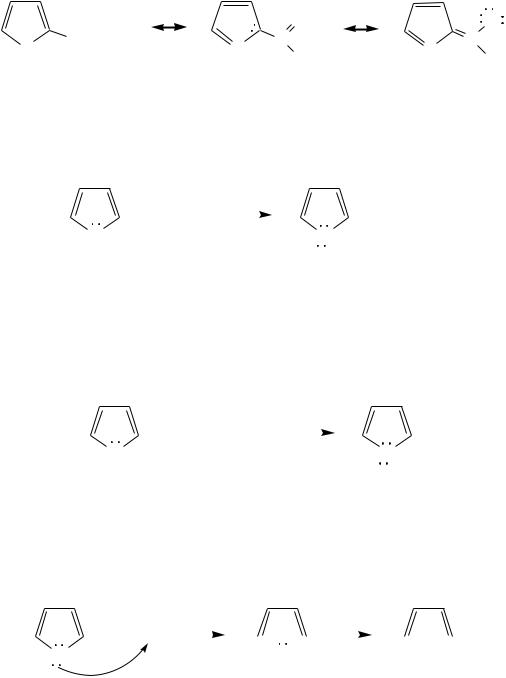
Введение в молекулу электроноакцепторных заместителей уменьшает электронную плотность на ароматическом кольце и тем самым снижает ацидофобность. При наличии сильных электроноакцепторов в гетероциклическом кольце соединение может и вовсе быть устойчиво к действию кислот, как, например, молекула пирослизевой кислоты:
605
|
|
- |
O |
|
O- |
O |
COOH |
+ |
C |
+ |
C |
|
O |
OH |
O |
OH |
|
|
|
|
|
пирослизевая кислота
К действию оснований фуран и тиофен устойчивы, так как не содержат подвижных атомов водорода, а пиррол является слабой NH-кислотой (рКа = 17.5) и при сплавлении со щелочами образует соли:
+ KOH |
|
T |
- |
+ H2O |
|
|
|||
N |
|
N K+ |
|
|
H |
|
|
|
|
пирролид калия
По кислотности пиррол сравним со спиртами, и поэтому для получения его солей могут использоваться также алкоголяты или металлорганические соединения, как, например, при взаимодействии с реактивом Гриньяра:
+ |
CH3MgBr |
|
|
|
|
|
-CH4 |
|
|||
N |
|
|
N |
||
H |
|
|
|
|
MgBr |
бромид-пирролид магния
Соли пиррола используются для алкилирования (и ацилирования) молекулы пиррола соответствующими алкилгалогенидами (или ацилгалогенидами). Реакция протекает по азоту или по -углеродному атому:
- |
|
+ R-I |
|
|
|
|
-KI |
||
N |
K+ |
|
|
|
|
|
|
to
 N
N 

 N
N 
 R R H
R R H
12.2.3.2. Реакции электрофильного замещения
В общем случае электрофильное замещение для пиррола, фурана и тиофена протекает легче, чем для бензола в связи с большей величиной - электронной плотности в молекуле гетероциклов. При этом на атомах углерода в наибольшей степени повышена электронная плотность в кольце пиррола по причине большего +М-эффекта атома азота по сравнению с другими гетероатомами. Поэтому реакционная способность по отношению к электрофилам будет увеличиваться в ряду:
бензол < тиофен < фуран < пиррол.
606
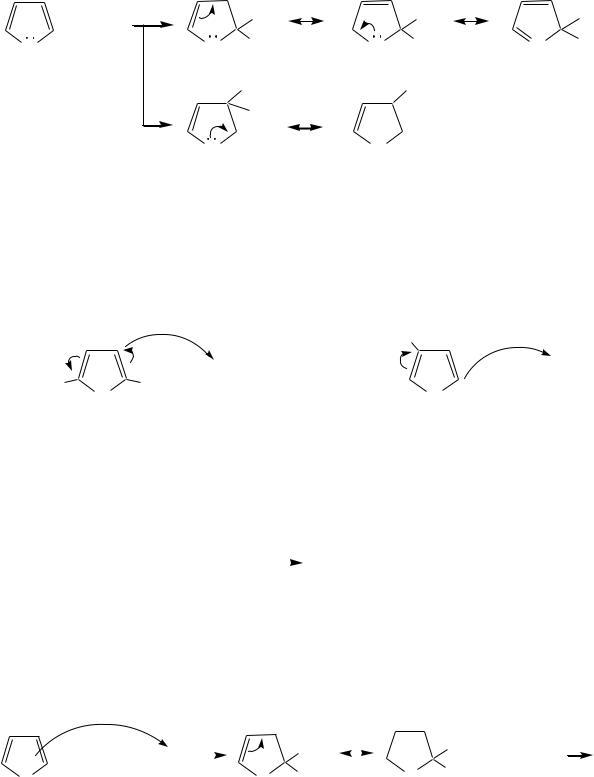
Электрофильное замещение в пирроле, фуране и тиофене протекает селективно в -положение, но когда оно занято, то реакция идѐт по-углеродному атому. Направление реакции в -положение объясняется сравнением устойчивости образующихся -комплексов (и подтверждается
квантово-химическими расчѐтами):
|
|
+ |
+ |
E+ |
E |
|
||
X |
|
X H |
|
|
E |
|
|
H |
|
|
+ |
|
|
X |
|
E |
|
E |
+ |
H |
+ |
H |
X |
X |
E
 H
H
+
X
Влияние заместителей в гетероциклическом кольце на направление электрофильного замещения проявляется только в том случае, если оба-положения заняты, либо оба -положения свободны, а заместитель находится в -положении. В этих случаях электрофильная атака протекает в соответствии с влиянием заместителей на распределение электронной плотности в данном ароматическом кольце. Например:
|
|
|
O2N |
|
|
|
+ E+ |
+ E+ |
|
O2N |
|
CH3 |
|
|
X |
X |
|||
|
|
Для нитрования пиррола, фурана и тиофена азотная кислота не используется по причине ацидофобности этих соединений. Нитрование фурана и тиофена проводят ацетилнитратом CH3COONO2, для чего используют раствор азотной кислоты в уксусном ангидриде:
O O |
|
O |
|||||||
|
|
|
|
|
|
|
|
|
|
CH3-C-O-C-CH3 + HO-NO2 |
|
|
CH3-C-O-NO2 + CH3COOH , |
||||||
|
|
||||||||
хотя возможно использование и других смешанных ангидридов или эфиров азотной кислоты. При этом фуран первоначально образует продукт присоединения ввиду своего выраженного диенового характера, а затем отщепляет молекулу уксусной кислоты (обычно под действием органического основания) и превращается в продукт замещения:
|
|
|
+ |
|
|
|
|
|
|
|
|
|||
|
|
|
|
+ |
NO2 |
|
|
|
NO2 |
- |
||||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
+ |
CH3-C-O-NO2 |
|
|
|
|
|
|
+ |
|
|
CH3COO |
|||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
O |
|
|
|
|
|
|
|
O H |
|
|
O |
H |
|
|
O |
|
|
|
|
||||||||||
|
|
|
|
|
||||||||||
607
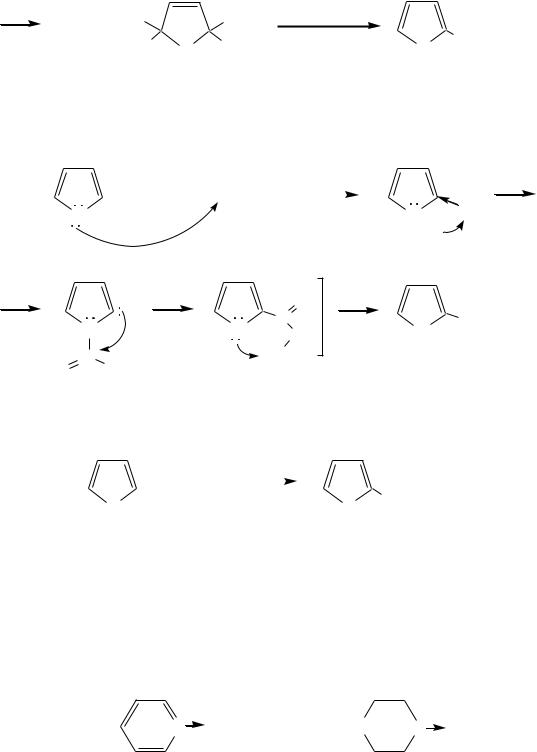
CH COO |
NO2 |
|
|
|
3 |
|
|
|
|
H |
O H |
-CH3COOH |
O |
NO |
|
2 |
|||
|
|
|
|
2-нитрофуран
-Нитропиррол в отличие от нитропроизводных фурана и тиофена получают через соли пиррола. Например, при использовании этилнитрата:
|
|
+ |
|
|
|
|
|
|
- |
|
+ H5C2O-NO2 |
|
|
|
|
|
|
|
|
-C2H5OK |
|
|
|
H |
||
N |
K+ |
|
|
|
|
N |
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
NO2 |
|
|
|
|
|
|
|
|
|
|
- |
- |
+ |
O |
|
|
|
|
N |
|
|
NO2 |
||
N |
N |
O |
N |
|||
|
|
|||||
+ |
|
H |
|
H |
|
|
O N OH |
|
|
|
|||
|
|
|
|
|
2-нитропиррол
Сульфировать серной кислотой можно только тиофен:
+ H2SO4 |
|
|
+ H2O |
|
|
||
S |
|
S SO3H |
|
|
|
|
тиофен-2-сульфокислота |
(Механизм сульфирования здесь такой же, как и механизм взаимодействия с холодной концентрированной серной кислотой бензола и его производных.)
Для сульфирования пиррола и фурана по причине их ацидофобности используют комплексы триоксида серы с электронодонорами, обычно пиридинсульфотриоксид или диоксансульфотриоксид:
N SO3 |
O |
O SO3 |
пиридинсульфотриоксид диоксансульфотриоксид
Механизм сульфирования такими комплексами аналогичен механизму сульфирования триоксидом серы:
608

|
|
O + |
|
|
O |
O- |
+ |
N: SO3 |
S |
O |
+ |
S |
|
|
|
|||||
|
|
|
|
|
|
|
X |
- N: |
X O |
|
X H O |
|
|
N: |
|
+ |
|
|
|
|
|
SO - + |
NH |
|
|
|
|
X |
|
|
|
|
|
|
3 |
|
|
|
|
|
|
Пиридин (или диоксан) в качестве донора электронной пары необходим для связывания отщепляющегося протона.
Галогенирование (хлорирование, бромирование, йодирование) пиррола и тиофена протекает настолько легко, что если специальным образом не контролировать течение реакции, образуются тетрагалогенопроизводные. Так, например, бромирование пиррола раствором брома в этаноле при 0 С даѐт тетрабромпиррол:
|
|
|
|
Br |
|
Br |
|
|
+ 4Br2 |
C2H5OH |
|
|
+ 4HBr |
||
|
|
|
|||||
N |
|
|
Br |
N |
Br |
||
|
|
|
|
||||
|
|
|
|
|
|
||
H |
|
|
|
|
H |
|
|
Получение монобромпиррола ( -изомер) представляет определѐнную трудность, и для этих целей обычно используют специальные бромирующие агенты. Для получения монобромтиофена применяют достаточно низкие температуры (-5 -15 С). Для хлорирования используют сульфурилхлорид SO2Cl2 или тетрахлорид олова SnCl4. Йодирование осуществляется молекулярным йодом (или KI + H2O2) в присутствии кислотного катализатора.
Галогенирование фурана протекает через реакцию присоединения (с последующим отщеплением галогеноводорода) — в этом проявляется диеновый характер этого гетероцикла. Здесь возможно хлорирование (газообразным хлором) или бромирование с образованием полигалогенопроизводных, но не йодирование. Фуран не реагирует с йодом.
Ацилирование пиррола, фурана и тиофена осуществляют ангидридами (реже галогенангидридами) карбоновых кислот.
Алкилирование фурана и пиррола не проводят, так как вероятные продукты этой реакции ещѐ более ацидофобны и полимеризуются за счѐт выделяющегося галогеноводорода.
Высокая активность пиррола иллюстрируется его способностью реагировать со слабыми электрофилами, например с солями арендиазония, диоксидом углерода, альдегидами. Скорость азосочетания сильно зависит от рН среды. При значениях рН ниже 8 в реакцию сочетания с катионом бензолдиазония вступает нейтральная молекула пиррола, а при значениях
609
