
А Е Щеголев Органическая химия 2016 / 12 Гетероциклические соединения
.pdf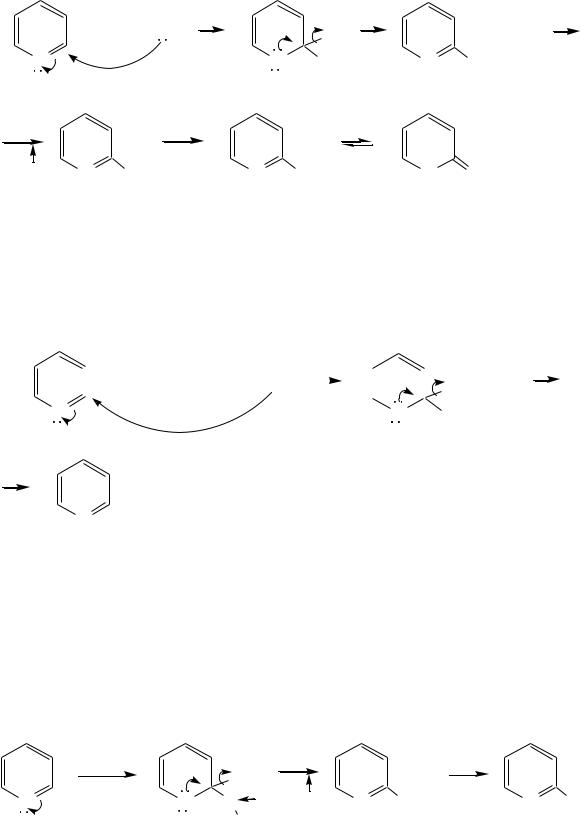
+ |
K+ -OH |
H |
|
+ KH |
|
+ |
|
- |
OH |
|
|
N |
|
N |
N |
OH |
|
|
|
K |
+ |
|
|
|
|
H+ |
|
|
|
-H2 |
OK |
-K+ |
OH |
|
O |
N |
N |
N |
|||
|
|
|
|
H |
|
|
|
-гидроксипиридин |
-пиридон |
|
|
Алкилирование и арилирование проводятся литийорганическими соединениями R-Li или Ar-Li при температуре 100 С. Эти реакции также селективно приводят к образованию -замещѐнных пиридинов. Например, взаимодействие с бутиллитием осуществляется по следующей схеме:
|
- |
|
|
|
|
|
|
|
+ CH3CH2CH2CH2: Li + |
|
|
|
|
|
H |
|
|
|
|
|
|
||
|
+ |
|
|
- |
|
||
N |
|
|
|
N (CH2)3CH3 |
|||
|
|
|
|
|
|
Li+ |
|
+ LiH
N  (CH2)3CH3
(CH2)3CH3
-бутилпиридин
Для отщепления гидрид-иона на стадии превращения -комплекса в продукты реакции может быть использовано окисление кислородом воздуха; тогда вместо гидрида лития образуется LiOH.
Аминирование пиридина и родственных гетероциклических соединений (реакция А.Е. Чичибабина*) осуществляется амидом натрия в апротонных растворителях при 100 С (или в жидком аммиаке при -33 С). Замещение осуществляется селективно в -положение.
|
NaNH2 |
|
H |
|
|
H2O |
|
+ |
- |
|
-H2 |
- |
-NaOH |
|
|
|
|
|
|||||
N |
N |
+ |
N H |
|
N NHNa+ |
N NH2 |
|
|
|
H |
|
|
|
|
|
|
Na |
|
|
|
|
||
Но если оба -положения заняты, то замещается водород в -положении. При нагревании с избытком амида натрия можно получить пиридин-2,6- диамин.
640
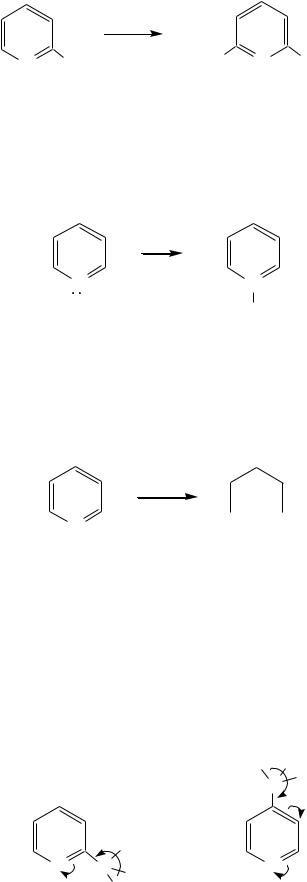
NaNH2
N |
NH |
H N N NH2 |
|
2 |
2 |
12.4.3.5. Реакции окисления и восстановления
Пиридиновый цикл устойчив к окислителям. Окисление может протекать по атому азота, например, действием пероксида водорода или пероксикислот (H2SO5):
[O]
+
N N O-
пиридин-N-оксид
Восстановление пиридина водородом на никелевом катализаторе приводит к полному гидрированию цикла. Реакция гидрирования пиридина протекает трудно, в условиях, аналогичных гидрированию бензола
(гл. 9.5.1.2).
[H]
N  N
N  H
H
пиперидин
12.4.4.ОСОБЕННОСТИ ХИМИЧЕСКОГО ПОВЕДЕНИЯ ПИКОЛИНОВ И ФУНКЦИОНАЛЬНЫХ ПРОИЗВОДНЫХ ПИРИДИНА
Пиколины с метильной группой в - и -положениях обладают повышенной СН-кислотностью за счѐт акцепторного влияния атома азота:
|
|
|
H |
|
H |
|
|
|
|
|
C |
H |
|
|
+ |
|
|
|
||
|
|
|
|
|
||
|
|
|
|
+ |
|
|
+ |
+ |
H |
+ |
|
+ |
|
N |
C H |
N |
||||
|
|
|
||||
|
|
H |
|
|
|
|
|
-пиколин |
-пиколин |
||||
641
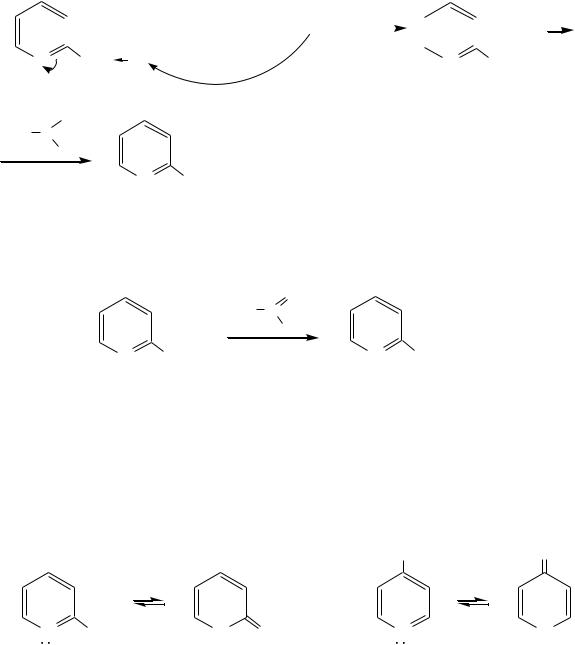
Это проявляется при образовании ими металлорганических соединений, например, при взаимодействии с бутиллитием, которые затем могут быть использованы в качестве реагентов в нуклеофильных реакциях:
|
|
|
|
+ CH3CH2CH2CH2: Li |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
-C4H10 |
|
|
|
||
|
|
|
|
|
|
|
|
|||
N CH2 |
|
H |
|
|
|
|
|
N CH2Li |
||
|
|
|
|
|||||||
O
H C  H
H
N CH2CH2OLi
или же сами - и -метилпиридины могут вступать в реакции нуклеофильного присоединения с альдегидами в присутствии оснóвного (реже кислотного) катализатора:
|
O |
R |
C |
|
H |
N CH3 |
N CH=CH-R |
Кислотные свойства -пиколина близки к таковым для толуола, и в целом химические свойства -изомера с участием метильной группы аналогичны свойствам толуола.
Из гидроксипиридинов - и -изомеры в обычных условиях существуют в виде - и -пиридонов, образующихся в результате таутомерных превращений:
OH |
O |
N OH |
N O |
N |
N |
|
H |
|
H |
-гидроксипиридин |
-пиридон |
-гидроксипиридин |
-пиридон |
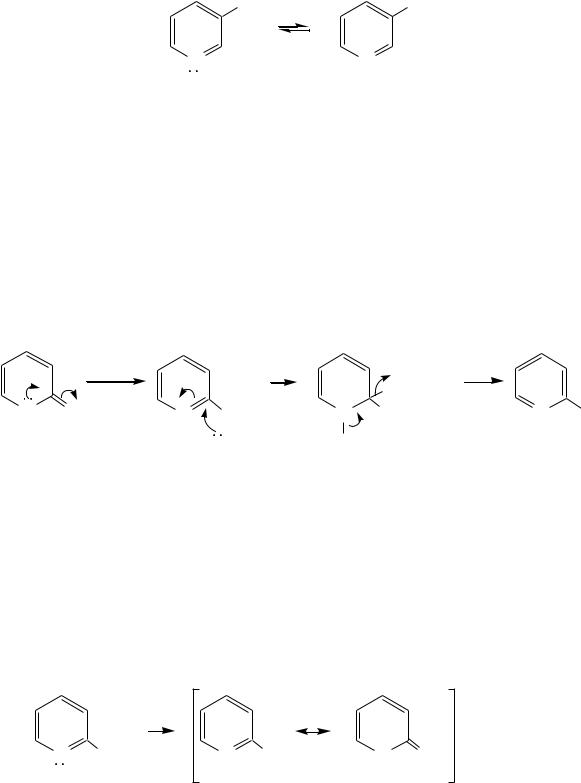
а -изомер существует в равновесии с биполярной формой (в водном растворе обе формы находятся примерно в равных количествах):
642
OH |
O- |
|
+ |
N |
N |
H
-гидроксипиридин
Все гидроксипиридины являются слабыми основаниями и слабыми кислотами. В наибольшей степени кислотные свойства проявляются у-изомера (рКа = 8.7), для него характерны типичные свойства фенолов (нитруется и бромируется легко, реагирует с формальдегидом, с солями диазония — SE-реакции идут преимущественно в положение 2).
Кислотные свойства - и -изомеров выражены значительно слабее (рКа 11), для них становятся возможны реакции спиртов, не характерные для фенолов, в частности, замещение гидроксогруппы в 2-гидрокси- пиридине (или, что то же самое, атома кислорода в 2-пиридоне):
|
POCl3/T |
|
|
|
H2O |
|
|
|
|
- |
+ |
|
OPOCl2 |
-2HCl |
|
|
|
N O |
OPOCl2 |
N Cl |
-HPO3 |
N |
Cl |
|||
N |
||||||||
|
|
|||||||
H |
|
H |
Cl- |
H |
|
|
|
|
|
|
|
|
|
Алкилирование гидроксипиридинов может протекать по атому азота (например, CH3I, (CH3)2SO4) или по атому кислорода (например, диазометаном CH2N2).
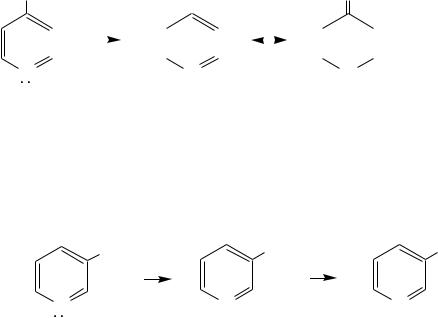
Все изомерные аминопиридины проявляют оснóвные свойства в большей степени, чем незамещѐнный пиридин, и образуют при протонировании по кольцевому атому азота кристаллические соли. Производные пиридина с аминогруппами в - и -положениях одноосновны, так как положительный заряд делокализуется между двумя атомами азота, что препятствует повторному протонированию.
|
H+ |
|
|
|
|
+ |
|
+ |
pKb = 6.8 |
N NH2 |
N |
NH2 |
N NH2 |
|
|
H |
|
H |
|
643
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
||||||
NH2 |
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
NH2 |
|
|||||||
H+ |
|
|
|
|
|
|
|
|
|
|
|
|
pKb = 4.9 |
|||||||||
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
N |
|
|
|
|
|
|
N |
|
|
|
|
|
|
N |
|
|||||||
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
H |
|
|
|||||
У -изомера основность выражена слабее, что объясняется отсутствием донорного мезомерного влияния аминогруппы в -положении на кольцевой атом азота (рКb = 7.4), но в сильнокислых средах пиридин-3- амин способен дважды протонироваться с образованием дикатиона.
|
|
|
+ |
|
NH2 |
NH2 |
NH3 |
|
H+ |
|
H+ |
|
+ |
|
+ |
N |
N |
|
N |
|
H |
|
H |
Алкилирование аминопиридинов протекает по кольцевому атому азота, а ацилирование — по азоту аминогруппы. Все аминопиридины легко вступают в SE-реакции по кольцу, причѐм место вступления электрофила определяется ориентацией аминогруппы.
-Аминопиридин при взаимодействии с азотистой кислотой превращается в соответствующую соль диазония. В случае - и -амино- пиридинов соли диазония легко гидролизуются в пиридоны. Причиной тому можно считать высокие эффективные положительные заряды на - и-атомах пиридинового кольца, создаваемые акцепторным влиянием азота, что в свою очередь приводит к дестабилизации катиона диазония. Здесь, как и в гидроксильных производных пиридина, -изомер в большей степени проявляет свойства функциональных производных ароматического ряда, чем - и -производные.
Свойства галогенопроизводных пиридина также в значительной степени зависят от положения атома галогена в пиридиновом кольце. В - и-положениях нуклеофильное замещение протекает значительно легче (возможна прямая нуклеофильная атака по этим атомам углерода — механизм SN2), а галоген в -положении, как и в неактивированном бензольном кольце, может замещаться только в очень жѐстких условиях, по ариновому механизму. Например, для 2,3-дихлорпиридина нагревание с метиламином даѐт исключительно продукт замещения по -атому:
644

|
Cl |
|
|
Cl |
- |
||
|
|
:NH2CH3/ T |
|
|
+ |
||
|
+ |
|
|
|
|
+ [NH3CH3] |
Cl |
|
|
|
|
|
|||
N Cl |
|
N NH-CH3 |
|
||||
Пиридинкарбоновые кислоты (пиколиновая, никотиновая и изоникотиновая) во многом представляют собой типичные ароматические карбоновые кислоты. Однако из-за наличия в их молекулах атома азота в качестве основного центра они могут существовать и в виде внутренней соли (как типичные аминокислоты).
Различия в свойствах карбоксильных групп, находящихся в различных положениях пиридинового цикла, проявляются по отношению к нагреванию, и это можно проиллюстрировать следующим примером:
|
COOH |
|
|
|
COOH |
|
|
|
|||||||||
|
|
|
COOH |
|
|
|
|
|
|
|
COOH |
|
|
COOH |
|||
|
|
|
|
|
|||||||||||||
|
|
|
|
|
450 K |
|
|
|
|
|
|
|
|
510 K |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-CO2 |
|
|
|
|
|
|
|
|
-CO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
N COOH |
2 |
|
|
N |
|
N |
||||||||||
|
|
|
|
|
|||||||||||||
пиридин-2,3,4-трикарбоновая |
пиридин-3,4-дикарбоновая |
|
никотиновая |
||||||||||||||
|
|
кислота |
|
(цинхомеровая) |
|
кислота |
|||||||||||
|
|
|
|
|
|
кислота |
|
|
|
||||||||
12.4.5. ХИНОЛИН И ИЗОХИНОЛИН
Хинолин и изохинолин — это конденсированные системы, состоящие из пиридинового цикла и бензольного кольца. Поэтому их названия как конденсированных систем:
ba |
cb a N |
N |
|
хинолин |
изохинолин |
(бензо[b]азин) |
(бензо[c]азин) |
Хинолин и изохинолин являются азотоаналогами нафталина, и нумерация атомов в их молекулах проводится так же, как и в молекуле нафталина: в хинолине, начиная с гетероатома, а в изохинолине атом азота имеет номер 2.
645

5 |
4 |
5 |
4 |
6 |
3 |
6 |
3 |
|
|
7 |
N |
2 |
7 |
N 2 |
|
||||
8 |
|
8 |
1 |
|
1 |
|
Хинолин, изохинолин и их производные — это бесцветные жидкости и низкоплавкие вещества, малорастворимые в воде и имеющие своеобразный запах.
12.4.5.1. Строение
Хинолин и изохинолин, так же, как и их углеродный аналог нафталин, представляют бициклические сопряжѐнные системы из 10 -элек- тронов. Присутствие атома азота значительно изменяет распределение электронной плотности. Электроноакцепторное влияние атома азота главным образом распространяется на цикл пиридина. Поэтому электронная плотность на бензольном кольце понижена в незначительной степени, а наибольший положительный заряд возникает в положении 2 молекулы хинолина и в положении 1 изохинолина:
+ |
N |
N |
+ |
|
12.4.5.2. Химические свойства
Как и пиридин, хинолин и изохинолин являются типичными основаниями с константами основности, близкими к таковым для пиридина. Образование солей протекает аналогично пиридину. Например, для хинолина:
|
HCl |
Cl- |
|
+ |
|
N |
N |
|
H
хлорид хинолиния
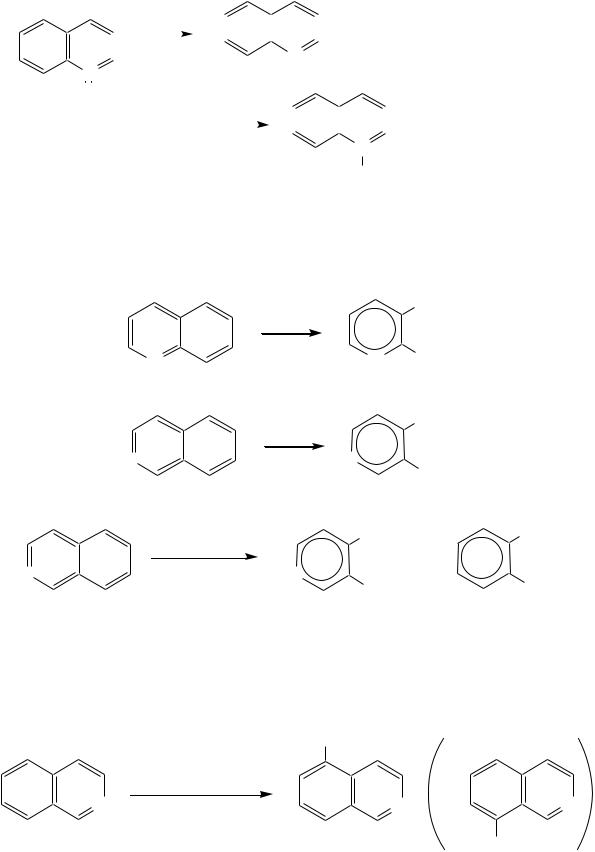
Реакции алкилирования и окисления по атому азота протекают в тех же условиях и при участии тех же реагентов, что и для пиридина. Например, для хинолина:
646
|
|
|
+ RI |
|
|
|
|
|
I- |
|
|
||||
|
|
|
|
|
|
|
|
+ |
|
|
йодид N-алкилхинолиния |
||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|||||||||
N |
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
H2O2 / CH3COOH |
|
|
|
|
+ |
|
хинолин-N-оксид |
|||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
O -
Однако хинолин и изохинолин могут окисляться под действием сильных окислителей (KMnO4, HNO3) с разрушением одного цикла, обычно бензольного. Но окисление изохинолина щелочным раствором перманганата калия приводит к смеси двух кислот.
|
HNO3,to |
COOH |
|
|
|
N |
|
N COOH |
|
хинолиновая кислота |
|
|
HNO3,to |
COOH |
|
|
|
N |
N |
COOH |
|
|
|
|
цинхомеровая кислота |
|
- |
o |
|
COOH |
COOH |
KMnO4 / OH ,t |
|
|
|
+ |
N |
|
N |
|
|
|
COOH |
COOH |
||
|
|
|
Реакции электрофильного замещения для обоих соединений протекают по бензольному кольцу, обычно по атомам С5 и С8. Но если при нитровании хинолина образуется примерно эквимолярная смесь 5- и 8-нит- рохинолинов, то нитрование изохинолина даѐт преимущественно 5-нитро-
производное:
NO2
|
HNO3 / H2SO4,273 K |
+ |
N |
N |
N |
|
|
NO2 |
|
5-нитроизохинолин |
8-нитроизохинолин |
|
90% |
10% |
|
647 |
|
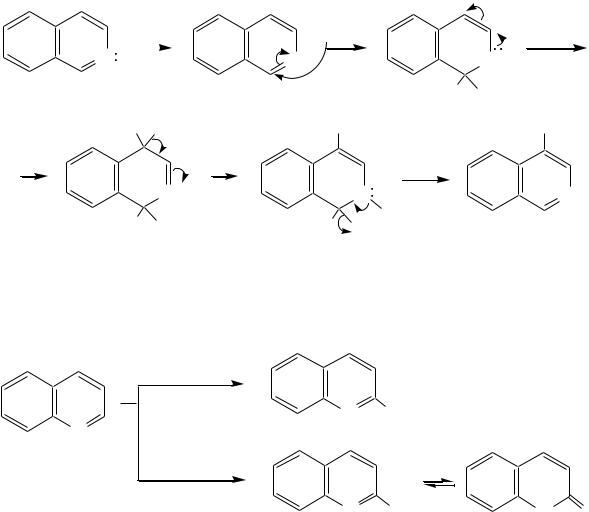
Сульфирование при обычных температурах (90 230 С) также приводит к образованию хинолин-5-сульфокислоты и хинолин-8-сульфокислоты (главным образом, 8-производного), но эти изомеры при нагревании выше 260 С переходят в более термодинамически стабильную 6-сульфоновую кислоту.
Галогенирование хинолина и изохинолина в условиях реакции электрофильного замещения (в присутствии кислотных катализаторов) также приводит к 5- и 8-производным. Введение атома галогена в пиридиновое кольцо происходит в значительно более мягких условиях. Так, бромирование хинолина и изохинолина в присутствии незначительных количеств HCl даѐт 3-бромхинолин и 4-бромизохинолин соответственно. Механизм процесса на примере изохинолина можно представить в следующем виде:
|
|
|
|
:Br- |
+ |
- |
HCl |
|
+ |
Br :Br |
|||
N -Cl- |
|
|
NH -Br- |
|||
|
NH |
|
||||
|
|
|
|
H |
Br |
|
Br |
H |
|
|
Br |
Br |
|
|
+ |
-H+ |
|
|
|
|
|
NH |
|
N -HBr |
|
N |
|
H |
Br |
|
|
H Br H |
|
|
4-бромизохинолин
Нуклеофильное замещение атома водорода идѐт наиболее легко в положение С2 хинолина и С1 изохинолина. Так, например, протекают реакция А.Е. Чичибабина и взаимодействие со щѐлочью для хинолина:
NaNH2 / NH3
N NH2
N
KOH,513 K
N OH |
N O |
|
H |
|
хинолин-2-он |
Для хинолина и изохинолина возможно гидрирование как пиридинового цикла, так и бензольного кольца. Восстановить пиридиновый цикл до тетрагидропиридинового можно боргидридами металлов или каталити-
648
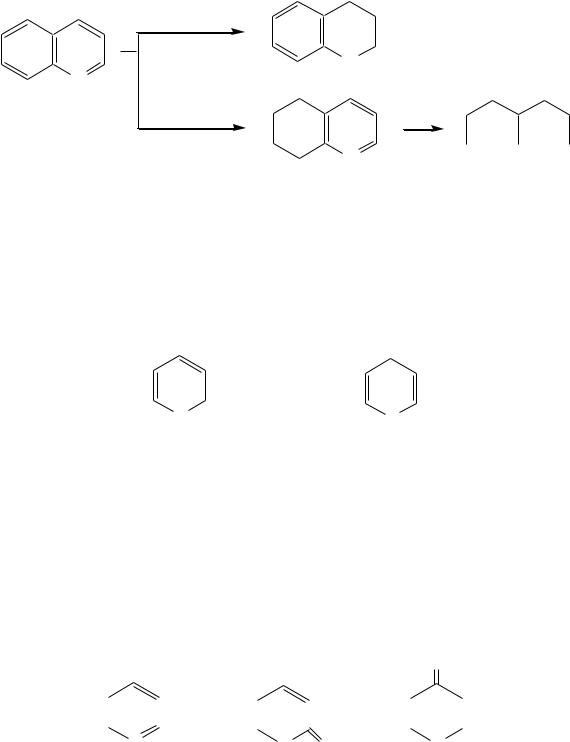
чески водородом в метаноле. Однако каталитическое гидрирование в растворе сильных кислот приводит к первоначальному селективному восстановлению бензольного кольца, а затем — к продукту исчерпывающего гидрирования — декагидропроизводному. Например, для хинолина:
|
H2 / Pt, CH3OH |
|
N |
N |
H |
H2 / Pt, HCl
N 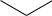
 N
N 
H
12.4.6. -ПИРАН И -ПИРАН И ИХ ПРОИЗВОДНЫЕ
Пираны — это ненасыщенные гетероциклические кислородосодержащие соединения. Возможно существование двух таких изомеров —-пирана и -пирана (или, соответственно 2Н-пиран и 4Н-пиран):
O |
O |
-пиран |
-пиран |
2Н-пиран |
4Н-пиран |
Циклы пиранов содержат один насыщенный атом углерода ( -атом в-пиране и, соответственно, -атом в -пиране), поэтому в их молекулах отсутствует полное циклическое сопряжение и эти соединения не могут относиться к ароматическим.
Пираны широкого распространения и практического использования не имеют. Однако более распространены соли катиона пирилия и оксопроизводные пиранов — пироны:
O
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
O |
|
O O |
|
|
O |
|||
пирилий-катион |
|
-пирон |
-пирон |
|||||||
649
