
Методички 3-й курс 1-й семестр / ДЛЯ ТЕХ КТО МЕТРОЛОГИЮ ЗАВАЛИЛ / sergeev_a_g_metrologiya_istoriya_sovremennost_p
.pdf
Глава 7. Воспроизведение эталонной базы СИ
с 1989 г. по настоящее время: температурная шкала в диапазоне 0,5–10 К (устройства для реперных точек на сверхпроводниках) (МТШ-90). Здесь буква «П» («практическая») опущена, поскольку разница между практической и теоретической (термодинамической) температурами ничтожно мала. Тем самым область определения
МТШ-90 увеличена на разность ТÌÒØ-90 – ÒÌÒØ-68.
Единица термодинамической температуры в МТШ-90 не изменилась (кельвин, или К). Без изменений также осталась связь температуры Кельвина с температурой Цельсия t, осуществляемая известным соотношением t = T – 273,15 K. Существующие значительные расхождения между значениями ТÌÒØ-90 è ÒÌÏÒØ-68 учитываются при анализе результатов измерений температуры с помощью средств измерений, проградуированных по разным шкалам.
Можно выделить четыре основные группы различий шкал МТШ-90 и МПТШ-68, касающихся:
Øобласти определения шкал;
Øсредств воспроизведения единицы температуры;
Øспециальных требований;
Øинтерполяционных зависимостей.
Государственные первичные эталоны России воспроизводят МТШ-90 в двух поддиапазонах: 0,8–273,16 К и 273,16–2773 К.
Âсостав первого эталона в качестве основной его части входят две группы железородиевых и платиновых термометров сопротивления. Каждая группа содержит два платиновых и два железородиевых термометра, постоянно находящихся в блоке сравнения – массивном цилиндре с четырьмя продольными каналами для термометров. Передача шкалы термометрам, вторичным и рабочим эталонам, осуществляется приведением их в тепловой контакт с эталонным блоком сравнения и сличением в криостате. Среднеквадратическая погрешность эталона лежит в пределах 0,3–1 мК, а неисключенная систематическая погрешность – в пределах 0,4–1,5 мК для любого значения температуры поддиапазона. Наименьшие значения соответствуют точке 0,8 К.
Âсостав второго эталона входят платиновые термометры сопротивления, температурные лампы, аппаратура воспроизведения реперных точек в диапазоне 271,16–1355,77 К. Среднеквадратическая
234

7.5. Эталон единицы температуры
погрешность этого эталона лежит в пределах 5·10–5–1·10–2; неисключенная систематическая погрешность – 1·10–4–5·10–3 (в относительных значениях).
В английской и американской научной литературе иногда встре- чается абсолютная термодинамическая шкала шотландца У. Ранкина (R), одного из создателей технической термодинамики. Ее нулевая точка совпадает с 0 К, а градус Ранкина (°R) по величине равен градусу Фаренгейта. Точка таяния льда 491,67°R , кипения воды 671,67°R. Перевод в температуру Кельвина выполняется по уравне-
íèþ ÒÊ = 5/9tR.
До нашего времени из всего множества температурных шкал дошли всего четыре, хотя и это явно многовато. В науке температуру выражают в кельвинах, а в жизни мы используем градусы Цельсия и изредка встречаем шкалы Реомюра и Фаренгейта. Выражения для взаимного перевода интервальных практических шкал Фаренгейта, Реомюра и Цельсия, включая и термодинамическую, можно представить в следующем виде:
Øшкала Цельсия: °С = 1 К; Т = tÖ + 273,15, где Т – температура Кельвина; tÖ – температура Цельсия;
Øшкала Реомюра: 1°Rе = 1,25 °С; tÖ = 1,25tRå, ãäå tRå – температура Реомюра; Т = 1,25tRå + 273,15;
Øшкала Фаренгейта: 1°F = 5/9 °С = 5/9 К; tÖ = 5/9(tF – 32), ãäå tF – температура Фаренгейта; Т = 5/9(tF – 32) + 273,15.
Соотношения между шкалами приведены в табл. 7.6.
Следует иметь в виду, что, нагревая изолированное тело, можно суммировать приращение его термодинамической температуры. Например, тело было нагрето до 100 К, нагрели еще на 50 К, в итоге получили 150 К. Если температура кипения одной жидкости 100 К, а другой – 50 К, то справедливо утверждать, что первое зна- чение в 2 раза больше второго. Но суммировать термодинамические температуры различных тел нельзя, это бессмысленно и равносильно известной шутке о средней температуре в больнице.
Особенно осторожно следует поступать со шкалами Цельсия, Реомюра, Фаренгейта, поскольку они начинаются с условных нулей. Скажем, по Цельсию иногда можно найти среднее арифметическое значение, измерив температуру воздуха в разных точках помещения
235

Глава 7. Воспроизведение эталонной базы СИ
Таблица 7.6
Соотношения между шкалами
Шкала |
|
Цельсия, |
|
|
Кельвина, |
Фаренгейта, |
|
|
Реомюра, |
Ранкина, |
|||||||||||||||||||||||||||||
|
|
|
|
|
°Ñ |
|
|
|
|
|
|
|
Ê |
|
|
|
°F |
|
|
|
|
|
|
|
|
°Re |
|
|
|
|
|
|
°R |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Цельсия, °С |
|
|
|
|
|
1 |
Ò |
|
– 273,15 |
|
5 |
(T − 32) |
|
|
|
|
|
|
|
5 |
T |
|
5 |
T |
|
|
− 273,15 |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Ê |
|
|
|
9 |
F |
|
|
|
|
|
|
|
4 |
|
Re |
9 |
|
R |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Кельвина, К |
Ò |
|
|
– 273,15 |
|
|
|
|
|
|
|
1 |
|
5 |
T |
+ 255,37 |
|
|
5 |
T |
|
|
+ 273,15 |
|
|
|
|
|
5 |
T |
|||||||||
|
Ñ |
|
|
|
|
|
|
|
9 |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
F |
|
|
4 Re |
|
|
|
|
|
|
|
9 R |
||||||||||||
Фаренгейта, |
|
|
|
9 |
T + 32 |
|
|
9 |
T |
|
− 459,67 |
|
|
|
1 |
|
|
|
|
|
9 |
T |
|
+ 32 |
Ò |
|
|
– 273,15 |
|||||||||||
°F |
|
|
5 |
|
C |
5 |
|
K |
|
|
|
|
|
|
4 |
|
|
Re |
|
|
|
R |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Реомюра,°Re |
|
|
|
|
|
4 |
T |
|
4 |
(T |
|
− 273,15) |
|
|
4 |
(T − 32) |
|
|
|
|
|
|
|
|
|
1 |
|
9 |
T |
|
|
− 218,52 |
|||||||
|
|
|
|
|
|
5 C |
5 |
|
|
K |
|
|
9 |
F |
|
|
|
|
|
|
|
|
|
|
|
4 |
|
R |
|
|
|
||||||||
Ранкина, °R |
|
9 |
T |
|
+ 491,67 |
|
|
|
|
|
|
|
9 |
T |
Ò |
– 273,15 |
|
9 |
T |
|
+ 491,67 |
|
|
|
|
|
|
1 |
|||||||||||
|
5 |
|
C |
|
|
|
|
|
|
|
|
|
5 K |
|
|
F |
|
|
4 Re |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
и определив среднюю температуру в нем. Можно найти среднесуточную (среднемесячную, среднегодовую) температуру в данной точке Земли. Но если вчера термометр показывал +15 °С, а сегодня +30 °С, то нельзя говорить, что на улице стало вдвое теплее. Это не так. Чтобы оценить значение перепада температуры, нужно перейти к термодинамической шкале. В нашем случае температура приблизительно увеличилась с 273 + 15 = 288 К до 273 + 30 = 303 К, т. е. всего на 5%.
7.6. Эталон единицы силы света
Видимый свет – часть электромагнитного спектра в диапазоне длины волн λ = (380 – 780) нм. Свет можно характеризовать яркостью, воспринимаемой человеческим глазом. В XIX в. с возникновением светотехники появилась потребность в количественной оценке освещенности и источников света.
Процесс восприятия света глазом весьма сложен, в него вклю- чены не только отдельные части глаза (сетчатку, зрительный нерв), но и головной мозг, физиологические и психологические процессы.
236

7.6. Эталон единицы силы света
Поэтому свет оценивается глазом избирательно и индивидуально (субъективно), а световые измерения, строго говоря, не вполне объективны.
Энергетическая теория света, описанная уравнениями Максвелла, определяет плотность потока энергии (интенсивности) излуче- ния источника света. Существует спектральное распределение энергетической яркости. Энергетической силе света соответствует фотометрическая сила света, а энергетической яркости – яркость фотометрическая.
Со времен возникновения фотометрии делались попытки создать эталонный источник света. В 1881 г. впервые было предложено в качестве такой единицы использовать виоль – тепловое излу- чение платиновой поверхности в точке плавления. В 1886 г. появилась дециметровая свеча. Наряду с ней появились свеча Гефнера – Альтенека, основанная на излучении амилацетатного пламени, и ряд других конструкций из разных материалов.
Значения предложенных единиц были различны: карсельская лампа превосходила по силе света лампу Гефнера – Альтенека в 10,9 раза, спермацетовая свеча составляла 1,14, парафиновая – 1,22 и десятичная Виола – 1,13 значения свечи той же лампы. Все это были светильники с открытым пламенем. И только в 1915 г. была предложена так называемая международная свеча, состоявшая уже из электрических ламп накаливания, а в 1921 г. создан международный эталон силы света в виде групп постоянно возобновляемых электрических ламп накаливания с угольной нитью (ламп Эдисона).
В России самостоятельной работы по созданию единиц силы света почти не проводили. До конца XIX в. не было также общепринятой единицы, хотя можно, по-видимому, считать, что в последней четверти XIX в. до появления лампы Гефнера – Альтенека доминировала спермацетовая свеча. Специфической русской единицей силы света была стеариновая свеча Невского завода, «четвериковая» свеча, называемая так потому, что ее начальный вес равнялся четверти фунта. Постепенно лампа Гефнера – Альтенека, официально принятая в Германии и Австро-Венгрии в качестве единицы силы света, вытеснила в России прочие единицы. Она использовалась также для метрологических целей, в частности потому, что герман-
237

Глава 7. Воспроизведение эталонной базы СИ
ский Физико-технический институт воспроизводил ее в достаточно совершенной форме. В Главной палате мер и весов для воспроизведения единицы силы света имелись четыре лампы Гефнера– Альтенека, аттестованные в германском Физико-техническом институте,
àтакже электрическая лампа сравнения с силой света около 1 све- чи, поверенная по лампе Гефнера – Альтенека и служившая для непосредственной поверки светоизмерительных ламп и определения силы света различных источников.
Ê1937 г. в качестве основного эталона был разработан черный излучатель, работающий при температуре затвердевания платины,
àв 1967 г. на XIII Генеральной конференции по мерам и весам было дано определение единицы силы света – канделы (от лат. candela – свеча). Кандела (кд) – сила света, испускаемого с площади 1/600 000 м2 сечения полного излучателя в перпендикулярном к этому сечению направлении при температуре излучателя, равной температуре затвердевания платины при давлении 101 325 Па.
Надо сказать, что единице силы света особенно не повезло с определениями. Они принимались в 1860, 1869, 1881, 1893, 1915, 1921, 1948, 1967 и 1979 гг. И, самое главное, каждый раз изменялся и размер единицы. Причиной изменений определений в 1948, 1967 и 1979 гг. была необходимость сделать однозначной связь световых и энергетических величин, связать канделу с ваттом. Эта связь осуществляется через величину, называемую максимальной световой эффективностью с размерностью люмен на ватт. В 1979 г. было принято решение, аналогичное принятому в отношении скорости света, считать ее постоянной величиной. Наиболее достоверное зна- чение этой величины, равное 683 лм/Вт, было возведено в ранг абсолютно точных, не имеющих погрешности метрологических констант.
В 1979 г. на XVI ГКМВ было принято новое, ныне действующее определение: кандела – сила света в заданном направлении источ- ника, испускающего монохроматическое излучение частотой 540 · 1012 Гц, энергетическая сила света которого в этом направлении составляет 1/683 Вт/ср. Частота 540 · 1012 Гц находится в зеленой области видимого света и соответствует максимуму чувствительности глаза.
238

7.6. Эталон единицы силы света
Заметим, что за период с 1967 по 1979 г. значение максимальной световой эффективности, используемое при определении размера канделы, изменилось с 673 до 683 лм/Вт, т. е. почти на 1,5%. Следовательно, на столько же мог измениться и размер канделы. Для основной единицы системы ситуация беспрецедентная.
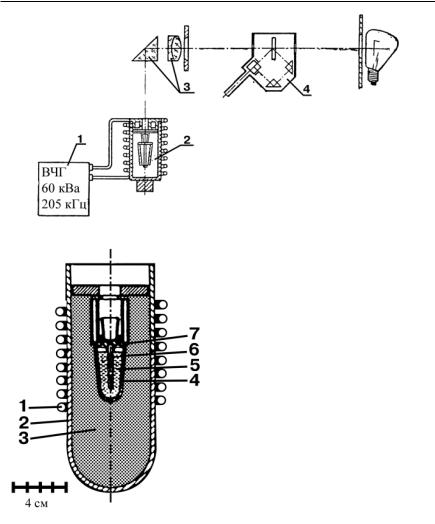
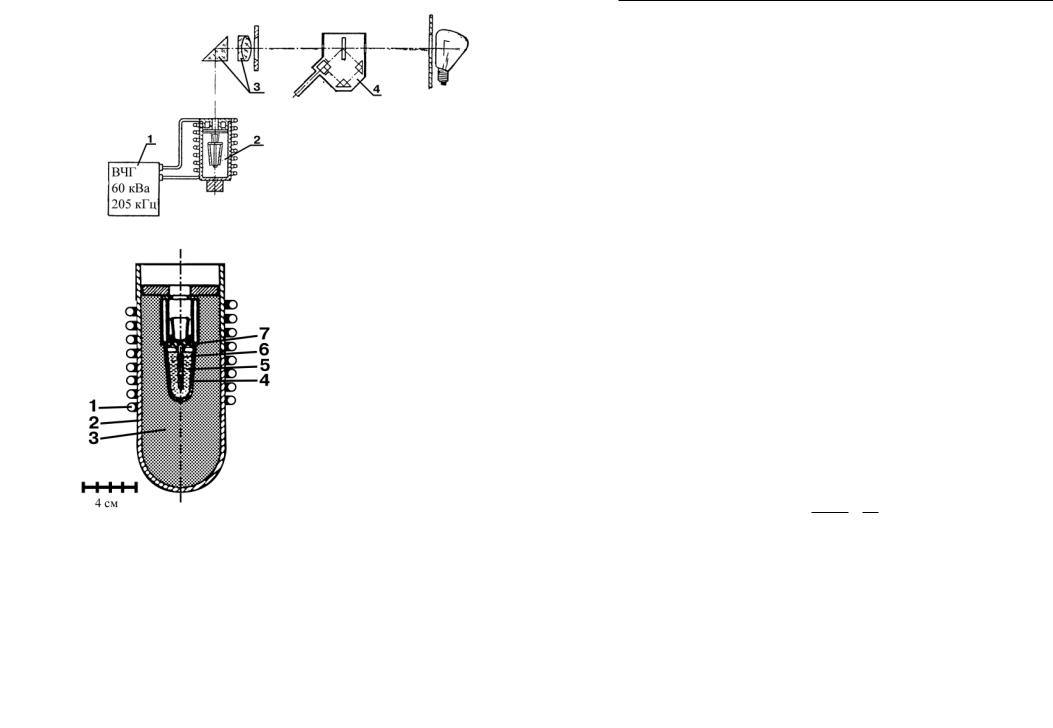
Кандела наиболее точно воспроизводится при помощи эталонного устройства – полного излучателя. Для реализации канделы используют черный излучатель при температуре плавления платины. Иногда его называют абсолютно черным телом. Он состоит из закрытой снизу керамической трубки (диаметром до 2 мм и длиной 40 мм), которая вертикально погружена в тигель для расплава, заполненный чистой платиной (рис. 7.17,а). Трубка и тигель для расплава закрыты крышкой с отверстием, диаметр которого немного меньше диаметра трубки. С целью термоизоляции тигель для расплава помещен в сосуд, заполненный порошком тория. При нагревании в индукционной печи платина расплавляется, при охлаждении она затвердевает, ее температура устанавливается и сохраняется на значении TPt = 2045 K. С помощью отклоняющей призмы и линзы объемное излучение, ограниченное диафрагмой, проецируется на поверхность, играющую роль фотометра (рис. 7.17,б). Свет излучается из полости трубочки через отверстие в верхней ее части. Яркость полного излучателя при температуре затвердевания платины сравнивается с помощью фотометра с яркостью особых ламп накаливания, используемых в качестве вторичных эталонов.
От измерительной диафрагмы зависит эффективная поверхность излучателя, погрешности в ее определении влияют на точ- ность установления единицы силы света. Существуют и другие при- чины погрешностей:
1)излучающая полость имеет конечное отверстие (коэффициент излучения меньше единицы), поэтому нельзя полностью достичь идеальных условий для верного излучателя;
2)вследствие теплопроводности и отражения температура излу- чающей полости несколько ниже температуры платиновой ванны. Платина затвердевает неоднородно;
3)при прохождении через оптическую систему теряется часть света. Необходимые в связи с этим поправки составляют около 1%, что вносит новые погрешности в определение канделы.
239
Глава 7. Воспроизведение эталонной базы СИ
à)
Рис. 7.17. Устройство для реализации канделы:
а – полный излучатель (1 – высоко- частотный генератор; 2 – полный излучатель; 3 – призма полного внутреннего отражения; 4 – фотометр; 5 – эталонная лампа накаливания); б – платиновый объемный излучатель (1 – индукционная печь; 2 – керамический сосуд; 3 – терми- чески изолированный наполнитель; 4 – керамический тигель;
5 – платиновая ванна; 6 – керами- ческая трубка; 7 – крышка тигля)
á)
Государственный эталон единицы силы света – канделы – ГЭТ 5-90, находящийся во ВНИИОФИ, воспроизводит ее значение в диапазоне 30–15 000 кд с относительной погрешностью 0,1 · 10–2– 0,25 · 10–2.
240
7.7.Эталон количества вещества
7.7.Эталон количества вещества
Âатомистической концепции строения материи вместо массы возникает еще одно представление о количестве вещества как числе частиц этого вещества. В системе СИ в качестве базисной вели- чины было принято количество вещества, измеряемое в молях; 1 моль – это такое количество вещества, в котором содержится точ- но столько структурных частиц (атомов, молекул, ионов или других частиц), сколько атомов содержится в 12 г углерода 12С. Это число
частиц называют числом, или постоянной, Авогадро NÀ. Оно может быть найдено, если известна масса одного атома 12Ñ (ma) :
NA = (12 ã/ìîëü) ma.
Углерод 12С выбран по нескольким причинам. Главная из них состоит в том, что он входит в огромное число химических соединений, с помощью которых становится возможным установление точных соотношений между атомными характеристиками этих элементов.
Число Авогадро обладает размерностью (количество вещества)–1 и измеряется в единицах моль–1. При этом макроскопическую массу количества вещества 1 моль можно выразить как M =NAma, ãäå [M] = 1 ã·ìîëü–1 (или 1 кг/кмоль). Величина M называется молярной массой. Наилучшее в настоящее время определение числа NA дает значение (6,0220921 ± 0,0000062)·1023 ìîëü–1.
Если взято произвольное количество вещества, имеющее массу (выраженную в килограммах или граммах), можно непосредственно указать соответствующее ей количество вещества:
V = maN = m , maN A M
причем [V ] = [m] [M ] = 1 ìîëü.
[M ] = 1 ìîëü.
Индивидуальные характеристики веществ часто указываются как удельные величины, т. е. величины, отнесенные к единице массы, например удельный объем (V/m), удельная (массовая) теплоемкость (Q/m), удельная радиоактивность (N/m) и т. д. Совершенно аналогично вводятся и молярные величины, отнесенные к единице
241

Глава 7. Воспроизведение эталонной базы СИ
количества вещества: молярный объем (объем одного моля), молярная теплоемкость (теплоемкость одного моля) и др.
Чтобы представить или реализовать единицу количества вещества 1 моль, уже нельзя опираться на соотношение, определяющее NA. Определить NA можно путем макроскопических измерений на монокристалле кремния (Si). Масса атома очень мала, а ее точное определение затруднительно. Однако при современном уровне развития измерительной техники сравнительно просто измерять относительные атомные массы. В 1960 г. было решено принять за основу в этом определении 1/12 массы атома углерода 12С. При этом относительные атомные массы (называвшиеся ранее атомными весами) равны:
A = |
ma |
= |
|
maN A |
= 12 |
Ma |
. |
|
|
|
|
||||
r |
1/12m(12C) |
|
1/12m(12C)NA |
|
M (12C) |
||
Эти величины представляют собой неименованные числа (так как являются отношениями). Например, для 12С имеем:
Ar = 12 12 ã / ìîëü−1 /12 ã ìîëü−1 = 12.
И вообще, если известна (из таблиц) относительная атомная масса, то можно указать молярную массу Ma для любого соответствующего вещества:
Ma = Ar 121 M (12C) = Ar ã ìîëü−1.
Отсюда по формуле v = m /Ma можно найти количество вещества путем одного только взвешивания.
Взаимозависимость атомной массы и NA очевидна из определения атомной единицы массы (а.е.м.):
1 à.å.ì. = |
|
1 |
m(12C) = |
|
1 |
|
M (12C) |
= |
1ã |
= |
|
|
12 |
12 |
N |
A |
6,0220921 10−23 ìîëü−1 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
= 1,6605525 10−27 êã.
Вначале молярная масса вещества измерялась масс-спектрогра- фическим методом. Позже для высокоточных измерений стали использовать параметры выхода энергии при ядерных реакциях.
242

7.7. Эталон количества вещества
Введение этой единицы было встречено научной общественностью очень неоднозначно. Дело в том, что при введении моля был допущен ряд отступлений от принципов образования систем физи- ческих величин. Во-первых, не было дано четкого и однозначного определения основополагающего понятия «количество вещества». Под количеством вещества можно понимать как массу того или иного вещества, так и количество структурных единиц, содержащихся в данном веществе. Во-вторых, из определения моля не ясно, каким образом при помощи измерений возможно получение объективно количественной информации о физической величине (ФВ).
Надо сказать, что понятие «моль» в 1902 г. ввел О. Оствальд для теоретической химии. Нельзя забывать, что в 1960 г. XI Генеральная конференция по мерам и весам приняла окончательно единую Международную систему единиц, базирующуюся на шести единицах основных физических величин. Седьмая основная единица – моль – была дополнительно введена в СИ на XIV ГКМВ в 1971 г., т. е. спустя 11 лет. В этой связи возникает вопрос о функции, выполняемой молем среди основных единиц СИ.
Любая основная единица призвана осуществлять две функции. Воспроизведенная в виде эталона, она обеспечивает единство измерений не только собственной физической величины, но и производных, в формировании размерности которых она участвует. С формальных позиций при образовании удельных величин моль входит в их размерность. Тем не менее удельную величину не следует отождествлять с производной ФВ. Удельные величины отличаются от соответствующих ФВ только количественно. Они представляют тот же количественный аспект измеряемого свойства, но только отнесенный либо к единице массы, либо к единице объема, либо, в рассматриваемом случае, к молю. Отсюда следует, что моль не выполняет одну из самых главных функций единицы основной ФВ. Не выполняет моль и функции обеспечения единства измерений количества вещества. В большинстве публикаций подчеркивается, что он является расчетной единицей и эталона для его воспроизведения не существует. Нет также ни одного метода и средства, предназначенного для измерения моля в соответствии с его определением. Все это свидетельствует о том, что следует ожидать исключения моля из числа основных единиц ФВ.
243
