
- •Военно-медицинская академия имени с. М. Кирова военная токсикология, радиобиология и медицинская защита
- •Рекомендуется Учебно-методическим объединением по медицинскому и фармацевтическому образованию вузов России в качестве учебного пособия для студентов медицинских вузов
- •Печатается согласно редакционно-иэдательскону плану Военно-медицинской академии имени с. М. Кирова, утвержденному начальником Главного военно-медицинского управления Министерства обороны рф
- •Оглавление
- •Часть I токсикология
- •Раздел I. Общая токсикология
- •Глава 1. Предмет, цель, задачи и структура токсикологии
- •Глава 2. Основные понятия токсикологии
- •Часть I. Luiwnisujiwi nn
- •Часть I. I wivwnivwjivi ил
- •Глава 1. Предмет, цель, задачи и структура токсикологии 21
- •Глава 3. Токсикометрия
- •Основные значения ответа группы на токсикант сосредоточены вокруг среднего значения
- •Влияние способа введения на токсичность зарина и атропина для лабораторных животных
- •Глава 3. Токсикометрия
- •Глава 4. Токсикокинетика
- •Характеристики различных биологических барьеров
- •Признаки специфического транспорта
- •Примеры биотрансформации ксенобиотиков с образованием активных промежуточных продуктов в ходе I фазы метаболизма
- •Глава 4. Токсикокинетика
- •А. Реакции, протекающие при участии активированных форм присоединяемых агентов
- •Дальнейший метаболизм экскреция
- •Глава 5. Токсикодинамика
- •Глава 5. Юкиикидиндми
- •5.214. Нарушение гомеостаза внутриклеточного кальция
- •Глава 6. Антидоты. Общие принципы оказания неотложной помощи отравленным
- •Глава 7. Основные понятия военной токсикологии
- •Глава 8. Отравляющие и высокотоксичные вещества раздражающего действия
- •8.Ц. Основные проявления поражения
- •Глава 9. Отравляющие и высокотоксичные вещества пульмонотоксического действия
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •Кофактор
- •Диметиламинфенол
- •Способность некоторых ароматических аминов вызывать образование метгемоглобина у разных экспериментальных животных
- •Глава 11. Отравляющие и высокотоксичные вещества цитотоксического действия
- •Сравнительная характеристика поражения кожи люизитом и ипритом
- •Основные свойства фенилдихлорарсина
- •Глава 1. Предмет, цель, задачи и структура токсикологии 21
- •Глава 1. Предмет, цель, задачи и структура токсикологии 21
- •Унитиол
- •Глава 12. Отравляющие и высокотоксичные вещества нейротоксического действия
- •Предполагаемые потери живой силы в районе применения отравляющего вещества VX из выливных авиационных приборов, % (по в. В. Мясникову, 1989)
- •Вещества нервно-паралитического действия
- •Классификация нервно-паралитических овтв в соответствии с особенностями их токсического действия на организм
- •Возможные общие механизмы генерации судорожного синдрома
- •Классификация нервно-паралитических овтв в соответствии с механизмами токсического действия на организм
- •Глава 1. Предмет, цель, задачи и структура токсикологии 21
- •Глава 1. Предмет, цель, задачи и структура токсикологии 21
- •100 Дней; pH 13 — 16 мин, pH 14 — 1,3 мин
- •006 Г/человека
- •Признаки острого поражения фос и механизмы их развития
- •Основные направления разработки средств медицинской защиты от фосфорорганических отравляющих веществ (по с. Н. Голикову и соавт., 1972)
- •Норборнан
- •Дисульфотетразоадамантан
- •Распределение ионов внутри и вне возбудимых клеток, мМ/л (по Katz, 1971)
- •Степени тяжести и фазы течения интоксикаций атропиноподобными препаратами (по с. С. Крылову и соавт., 1999)
- •Глава 13. Предмет, цель и задачи радиобиологии
- •Глава 14. Виды ионизирующих излучений и их свойства
- •Относительная биологическая эффективность ионизирующих излучений для клеток
- •Ориентировочные значения поглощенной дозы излучения при некоторых медицинских процедурах
- •Глава 15. Радионуклиды как источник радиационной опасности
- •Глава 16.
- •Нестохастические эффекты
- •Стохастические эффекты
- •Глава 17. Факторы, вызывающие поражения личного состава войск при ядерных взрывах и радиационных авариях
- •Глава 18. Лучевые поражения в результате внешнего облучения
- •Глава 19. Лучевые поражения в результате общего (тотального)облучения
- •Реконструкция дозы общего однократного равномерного внешнего у-облучения организма по некоторым проявлениям поражения в период общей первичной реакции на облучение
- •Глава 20. Медицинская защита от внешнего облучения
- •Фид Cfls° с пРепаРатом (опыт)
- •Глава 21.
- •Глава 22. Поражения в результате внутреннего радиоактивного заражения
- •Глава 1. Предмет, цель, задачи и структура токсикологии 21
- •Ожидаемая частота и характеристика радиационно индуцированной эметической реакции при комбинированных радиационных поражениях (по Бритуну а. И. И др., 1992)
- •Глава 1. Предмет, цель, задачи и структура токсикологии 21
- •И объема первой помощи
- •Глава 25. Специальная обработка в подразделениях и частях медицинской службы
- •Глава 25. Специальная обработка в подразделениях и частях медицинской службы
- •Глава 25. Специальная обработка в подразделениях и частях медицинской службы
- •Глава 25. Специальная обработка в подразделениях и частнх медицинскои службы
- •Глава 25. Специальная обработка в подказдьльнинх и чашНл мьдициникии службы
- •Глава 25. Специальная обработка в подразделениях и частях медицинскои службы
- •Глава 26. Радиационная и химическая разведка в частях и подразделениях медицинской службы
- •26.1. Средства и методы радиационной разведки и контроля
- •26Д. Организация и проведение контроля доз облучения личного состава, раненых и больных на этапах медицинской эвакуации
- •26.5. Организация и проведение экспертизы воды и продовольствия на зараженность отравляющими, высокотоксичными и радиоактивными веществами
- •Учебное издание
- •Учебник Под редакцией профессора с. А. Куценко
- •190020, Санкт-Петербург, Нарвский пр., 18, оф. 501 тел./факс: (812) 325-39-86, 186-72-36 e-mail: foliant@peterlink. Ru
Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
Общеядовитым называется действие химических веществ на организм, сопровождающееся повреждением биологических механизмов энергетического обеспечения процессов жизнедеятельности.
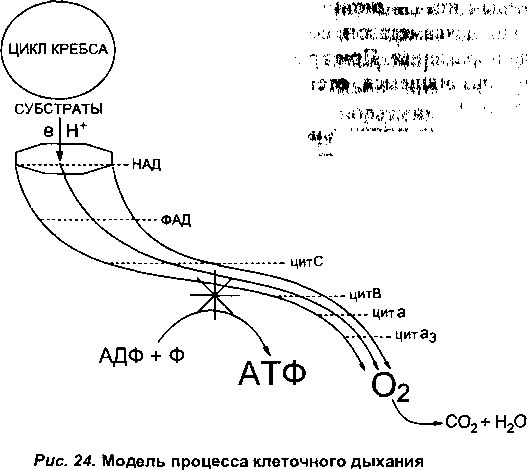
Как указывалось ранее (см. раздел «Общая токсикология»), основным содержанием биоэнергетических процессов в организме является непрерывный синтез в клетках и поддержание на постоянном уровне концентрации богатых энергией (макроэргических) соединений, в частности, аденозинтрифосфорной кислоты (АТФ). Источником, запасаемой в форме АТФ энергии, является биологическое окисление субстратов, образующихся в ходе метаболизма питательных веществ, поступающих из окружающей среды (рис. 24).
БЕЛКИ
ЖИРЫ УГЛЕВОДЫ
АцКоА
"■л.?
тжь!i
I лава 1U. UI РАШ 1НГиЩИС VI Doivvrvv I цш^ппрц; ОСЩСОI DM I wi v-» M^rtv I twin
Энергия, запасенная в субстратах, образуемых в цикле Кребса, при их окислении (движение электронов и протонов по цепи дыхательных ферментов к кислороду) обеспечивает работу сопряженного механизма синтеза макроэргов путем фосфорилирования их предшественников (в частности, превращение аденозиндифосфорной кислоты в аденозинтрифосфорную).
Практически любой токсикант, вызывая тяжелую, острую интоксикацию, в той или иной степени нарушает энергетический обмен, т. е. оказывает общеядовитое действие. Однако в большинстве случаев нарушение биоэнергетики является лишь звеном в патогенезе токсического процесса, инициированного за счет иных механизмов. Вместе с тем имеются вещества, способные первично повреждать систему энергообеспечения клеток, нарушая:
механизмы транспорта кислорода кровью;
механизмы биологического окисления;
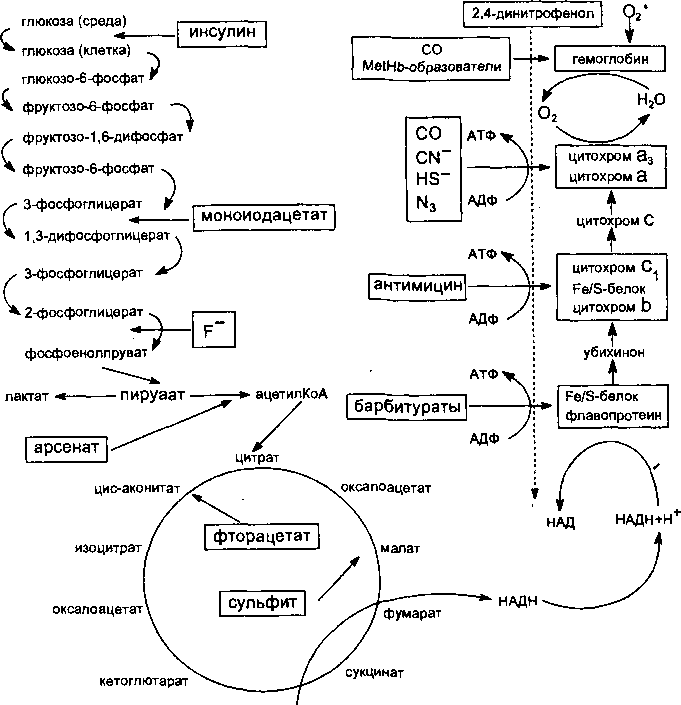
механизмы сопряжения биологического окисления и синтеза макроэргов (фосфорилирования) (рис. 25).
НАД
Рис.
25.
Механизмы действия некоторых токсикантов
на биоэнергетические процессы
Токсиканты, основным (первичным) механизмом повреждающего действия которых на организм является нарушение биоэнергетики, могут быть объединены в группу веществ общеядовитого действия.
Важными особенностями токсического процесса, развивающегося при отравлении такими веществами, являются:
быстрота развития острой интоксикации (короткий скрытый период, бурное течение токсического процесса);
функциональный характер нарушений со стороны вовлеченных в токсический процесс органов и систем, отсутствие грубых структурно-морфологических изменений в тканях отравленных;
вовлечение в патологический процесс преимущественно органов и систем с интенсивным энергообменом и, прежде всего, центральной нервной системы;
закономерный характер развития нарушений со стороны ЦНС: возбуждение, переходящее в состояние гиперактивации, а затем глубокого угнетения (изменение сознания, судороги, кома и т. д.).
Ряд веществ-ингибиторов энергетического обмена при экстремальных ситуациях могут стать причиной групповых и массовых поражений людей и потому представляют интерес для военной медицины.
Классифицировать ОВТВ рассматриваемой группы можно в соответствии с особенностями механизма их токсического действия:
ОВТВ, нарушающие кислородтранслортные функции крови:
Нарушающие функции гемоглобина:
Образующие карбоксигемоглобин (монооксид углерода, карбонилы металлов).
Образующие метгемоглобин (оксиды азота, ароматические нитро- и аминосоединения, нитриты и др.).
Разрушающие эритроциты (мышьяковистый водород).
ОВТВ, нарушающие тканевые процессы биоэнергетики:
Ингибиторы ферментов цикла Кребса (производные фторкарбоновых кислот).
Ингибиторы цепи дыхательных ферментов (синильная кислота и ее соединения).
Разобщители тканевого дыхания и фосфорилирования (динитро-орто-крезол, динитрофенол).
Наряду с общими чертами, патологические процессы, развивающиеся при острых отравлениях ОВТВ с различными механизмами общеядовитого действия, имеют и свою специфику.
ОВТВ, нарушающие кислородтранспортные функции крови
ОВТВ, нарушающие функции гемоглобина
Одна из важнейших функций крови — транспорт кислорода от легких к тканям. Транспорт кислорода осуществляется двумя способами:
гемоглобином — в форме соединения;
плазмой — в форме раствора.
В растворенном состоянии плазмой крови переносится около 0,2 мл
на 100 мл крови. В связанной с гемоглобином форме эритроциты переносят в 100 раз больше кислорода (20 мл на 100 мл крови). 1 г гемоглобина способен обратимо связать около 1,5 мл 02, а в 100 мл крови содержится около 14—16 г гемоглобина.
%
НЬО (У)
20 40 60 80 ЮО
р02
мм рт. ст. (х),
К+1 КХп
НЬ
+ О
к_, 1
+ X"
К
= К+1/К_,
п
— константа Хила, в норме равна 3 Рис.
26. Кривая насыщения гемоглобина
кислородом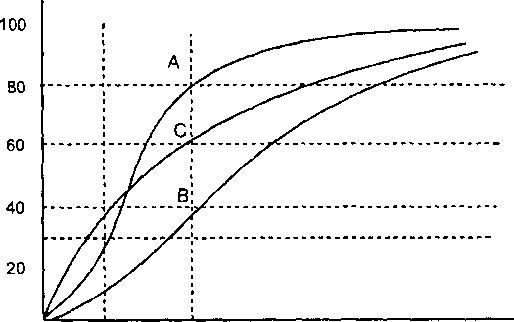
""
" НЬО у=
”
А — pH 7,4 В —pH 7,0
С — в присутствии СО
При повышении парциального давления кислорода (сатурация крови в легких) содержание НЬО увеличивается и при р02 100 мм рт. ст. приближается к 100%. При понижении парциального давления Ог (в тканях) НЬО распадается, при этом выделяющийся кислород утилизируется тка
нями организма. Процесс насыщения гемоглобина О2 и рассыщения ок- сигемоглобина описывается S-образной кривой (см. рис. 26). Такая форма зависимости между р02 и % НЬО есть следствие явления взаимодействия четырех субъединиц гемоглобина в молекулярном комплексе (гем-гем взаимодействие). Физиологический смысл явления — обеспечение максимально возможного выделения кислорода в ткани при незначительном различии парциального давления газа в крови и тканях (при р02 в крови около 40 мм рт. ст. и р02 в тканях около 20 мм рт. ст. гемоглобин высвобождает около 50% связанного кислорода).
В норме на сродство кислорода к гемоглобину влияют многочисленные факторы. Среди основных: pH, рС02 (эффект Бора), биорегуляторы процесса диссоциации оксигемоглобина (2,3-дифосфоглицерат и др.). При повышении pH, рС02 и содержания 2,3-дифосфоглицерата в эритроцитах сродство гемоглобина к кислороду снижается — отдача кислорода тканям возрастает.
Из сказанного ясно, что вещества, взаимодействующие с гемоглобином и нарушающие его свойства, будут существенно изменять кислород- транспортные свойства крови, вызывая развитие гипоксии гемического типа.
Кислородное голодание плохо переносится человеком и другими млекопитающими и в тяжелых случаях может привести к серьезным нарушениям со стороны различных органов и систем. Особенно чувствительными к гипоксии являются клетки органов с интенсивным энергообменом — сердечной мышцы, почек и головного мозга (табл. 27).
Таблица
27
Потребление
кислорода различными органами крысы
(по Field
et al., 1939)
Орган
Скорость
потребления кислорода, мл/г ткани а
минуту
Скелетная
мускулатура
0,875
Кожа
0,416
Кости
0,153
Кровь
0,025
Печень
2,010
Почки
4,120
Мозг
1,840
Легкие
1,250
Сердце
1,930
Функциональная состоятельность мозга целиком зависит от непрерывного снабжения его кислородом. Так, при полной аноксии «местных» запасов кислорода (7—10 мл) хватает лишь на 10 с. Мозг, составляя по массе 2—3% от массы тела, потребляет около 20% всего потребляемого
организмом кислорода. Нормальная скорость кровотока составляет 50—60 мл/мин/100 г ткани, а скорость поглощения 02 — 3,5 мл/мин/100 г ткани. Собственно нервные клетки составляют 5% от общей массы мозга, но потребляют 25% 02, потребляемого мозгом (нейрон — 350—450 мкл Оз/мин; глиальные клетки — 60 мкл Oj/mhh). До 90% вырабатываемой и потребляемой энергии расходуется на поддержание электрохимического градиента возбудимых мембран и метаболизм биологически активных веществ, участвующих в передаче нервных импульсов. Неудивительно, что сознание, как функциональный феномен, утрачивается уже в течение несколько секунд полной аноксии мозга. Необратимые изменения нейронов наступают позже, спустя 4—5 мин после полного прекращения снабжения мозга кислородом. Другие органы и ткани, расходующие энергию в основном на обеспечение пластического обмена (процессы синтеза и разрушения структурных элементов живого), способны переживать (хотя и с нарушениями функций) нехватку кислорода в течение нескольких часов.
Токсиканты, избирательно нарушающие кислородтранспортные функции крови, обладают высокой токсичностью.
ОВТВ, образующие карбоксигемоглобин
Карбоксигемоглобин образуется при действии на организм монооксида углерода (СО), так называемого угарного газа, а также при отравлении некоторыми карбонилами металлов, которые, попав в организм, разрушаются с образованием СО. В недалеком прошлом тетракарбонил никеля [Ni(CO)4] и пентакарбонил железа [Fe(CO)s] изучались на предмет возможности создания на их основе боевых отравляющих веществ.
10.1*1.1.1* Карбонилы металлов
Соединения металлов с СО называются карбонилами металлов. Их применяют в некоторых областях химической промышленности. Из множества соединений особый интерес представляют пентакарбонил железа и тетракарбонил никеля — вещества, легко разлагающиеся с образованием СО. Оба токсиканта представляют собой бесцветные летучие жидкости (максимальная концентрация в воздухе — более 300 г/м3), пары которых примерно в 6 раз тяжелее воздуха (могут образовывать нестойкие зоны заражения). Плохо растворяются в воде; хорошо — в липидах.
Действуют как ингаляционно, так и через неповрежденную кожу (в крови разрушаются с образованием СО).
В зонах заражения возможны два варианта поражения — собственно веществами и продуктами их разложения. Собственно вещества обладают свойствами пульмонотоксикантов (см. выше). Тяжелое поражение сопровождается развитием (в течение 10—15 ч) токсического отека легких. Токсичным продуктом разложения веществ является оксид углерода, особенности действия которого представлены ниже.
Оксид углерода (СО)
Оксид углерода является продуктом неполного сгорания углерода. Он образуется в качестве примеси везде, где происходит горение углеродсодержащего топлива (топка печей, эксплуатация двигателей внутреннего сгорания и т. д.). Массовые поражение угарным газом возможны в очагах пожаров и при накоплении вещества в плохо вентилируемых пространствах — помещениях, туннелях, шахтах и т. д., где действует источник его образования.
Физико-химические свойства
СО — бесцветный газ, не имеющий запаха, с низкой плотностью по воздуху (0,97). Кипит при -191,5° С и замерзает при —205,1° С. В воде и плазме крови растворяется мало (около 2% по объему), лучше в спирте. Смесь СО с воздухом способна взрываться. Плохо сорбируется активированным углем и другими пористыми материалами. Оксид углерода как соединение с двухвалентным атомом углерода является восстановителем и может вступать в реакции окисления. На воздухе горит синим пламенем с образованием диоксида углерода. При нормальной температуре превращение СО в СО2 идет при участии катализаторов, например гопкалита [смеси двуокиси марганца (60%) и окиси меди (40%)]. Поскольку газ легче воздуха, зоны нестойкого химического заражения на открытом пространстве могут формироваться лишь в очагах обширных пожаров.
Токсичность
Чувствительность людей к оксиду углерода колеблется в довольно широких пределах. Она зависит от многих факторов: от длительности экспозиции, степени физической нагрузки в момент действия яда, от температуры внешней среды и состояния организма. Отравление наступает быстрее и протекает тяжелее при анемиях, авитаминозах, у истощенных людей. Пребывание в атмосфере, содержащей 0,01 об. % СО (0,2 мг/л), при физической нагрузке допустимо не долее 1 ч. После этого появляются признаки отравления. Отчетливая клиническая картина острого поражения развивается при содержании СО в воздухе более 0,1 об. %.
Токсикокинетика
Единственный способ поступления газа в организм — ингаляционный. Оксид углерода, при вдыхании зараженного им воздуха, легко преодолевает легочно-капиллярную мембрану альвеол и проникает в кровь. Скорость насыщения крови оксидом углерода увеличивается при повышении его парциального давления во вдыхаемом воздухе, усилении внешнего дыхания и интенсификации легочного кровообращения (увеличиваются при физических нагрузках). По мере увеличения концентрации яда в крови скорость резорбции замедляется. При достижении равновесия в содержании СО в альвеолярном воздухе и в крови дальнейшее поступление его в организм прекращается.
Выделение оксида углерода из организма при обычных условиях происходит в неизмененном состоянии также через легкие. Период полувы- ведения составляет 2—4 ч.
Основные проявления интоксикации
Раздражающим действием оксид углерода не обладает. Контакт с веществом проходит незамеченным. Тяжесть клинической картины отравления угарным газом определяется содержанием СО во вдыхаемом воздухе, длительностью воздействия, потребностью организма в кислороде, интенсивностью физической активности пострадавшего. По степени тяжести интоксикации принято делить на легкие, средние и тяжелые.
Легкая степень отравления формируется при действии относительно невысоких концентраций яда. Она развивается медленно (порой в течение нескольких часов) и характеризуется сильной головной болью, головокружением, шумом в ушах, потемнением в глазах, понижением слуха, ощущением «пульсации височных артерий», тошнотой, иногда рвотой. Нарушается психическая деятельность: пораженные теряют ориентировку во времени и пространстве, могут совершать немотивированные поступки. Отмечается повышение сухожильных рефлексов. У отравленного развиваются тахикардия, аритмия, повышается артериальное давление. Возникает одышка — признак компенсаторной реакции организма на развивающуюся гипоксию. Однако в результате одышки увеличивается количество выдыхаемого диоксида углерода (С02), развивается газовый алкалоз. Кроме того, учащение дыхания при нахождении человека в отравленной зоне является дополнительным фактором, ускоряющим поступление оксида углерода в организм.
Легко пораженный СО утрачивает боеспособность. Однако при прекращении поступления яда в организм все перечисленные симптомы отравления в течение нескольких часов проходят без каких-либо последствий.
При продолжительном поступлении оксида углерода в организм или при действии его в более высоких концентрациях развивается отравление средней степени тяжести, характеризующееся более выраженными проявлениями интоксикации, большей скоростью их развития. Нарушается координация движений. Сознание затемняется, развиваются сонливость и безразличие к окружающей обстановке, появляется выраженная мышечная слабость. Слизистые оболочки и кожа приобретают розовую окраску. Могут развиваться фибриллярные подергиваний мышц лица. Возможно повышение температуры тела до 38—40° С. Одышка усиливается, пульс учащается. Артериальное давление после кратковременного подъема, связанного с возбуждением симпатико-адреналовой системы и выбросом катехоламинов из надпочечников, снижается. Этот эффект объясняют прямым действием СО и рефлекторной реакцией (с хеморецепторов каротидного синуса) на центры регуляции сосудистого тонуса.
Прогрессирующая гипоксия активирует процессы анаэробного гликолиза, о чем свидетельствует активация ряда ферментов (альдолазы, дегид- рогеназы-3-фосфоглицеринового альдегида, лактатдегидрогеназы). В результате в организме накапливаются молочная и пировиноградная кислоты.
Это способствует развитию метаболического ацидоза, который приходит на смену газовому алкалозу.
При отравлении средней степени тяжести в большинстве случаев через несколько часов (до суток) после прекращения действия яда состояние пострадавших существенно улучшается, однако довольно долго сохраняются тошнота, головная боль, сонливость, склонность к головокружению, шаткая походка.
Тяжелое отравление характеризуется быстрой потерей сознания, появлением признаков гипертонуса мышц туловища, конечностей, шеи и лица (ригидность затылочных мышц, тризм жевательной мускулатуры). На высоте токсического процесса могут развиться судороги клонико-то- нического характера. Кожные покровы и слизистые оболочки приобретают ярко-розовый цвет (признак высокого содержания карбоксигемогло- бина в крови). Если в этот период пострадавший не погибает, судороги прекращаются, но развивается кома: утрачиваются рефлексы, мышцы расслабляются. Дыхание становится поверхностным, неправильным. Зрачки расширены, на свет не реагируют. Пульс частый, слабого наполнения, артериальное давление резко снижено. При регистрации биоэлектрической активности сердца на электрокардиограмме определяются экстрасистолия, нарушение внутрисердечной проводимости, признаки диффузных и очаговых мышечных изменений, острой коронарной недостаточности. Изменения в мышце сердца, регистрируемые на ЭКГ, отчасти обусловлены изменением электролитного состава крови: увеличивается содержание кальция и магния, уменьшается содержание натрия и калия. В связи с сужением периферических сосудов происходит переполнение кровью внутренних органов и полых вен. Развиваются застойные явления, затрудняющие работу сердца.
В крови, вследствие рефлекторного сокращения селезенки, увеличивается до 6—7 • 1012/л количество эритроцитов, развиваются лейкоцитоз со сдвигом формулы крови влево, относительная лимфопения и эозино- пения. Растет содержание мочевины в крови. В таком состоянии отравленный может пребывать несколько часов, и при нарастающем угнетении дыхания с прогрессирующим падением сердечной деятельности наступает смертельный исход. При благоприятном течении отравления и своевременном оказании медицинской помощи симптомы интоксикации исчезают, и через 3—5 дней состояние пострадавшего нормализуется. Изменения ЭКГ при тяжелых отравлениях порой выявляются в течение нескольких недель и даже месяцев.
В случае высокого содержания во вдыхаемом воздухе оксида углерода (до нескольких процентов) на фоне пониженного парциального давления С>2 (до 17—14%) при выполнении физической нагрузки, сопровождающейся усиленным газообменом (ситуация, возникающая при пожарах, взрывах боеприпасов в замкнутых пространствах и т. д.), развивается молниеносная форма отравления (Другов Ю. В., 1959). Пораженные быстро теряют сознание. Возможны кратковременные судороги, за которыми наступает смерть или развивается тяжелая кома. Прогноз неблагоприятный, если коматозное состояние продолжается более двух суток.
Выделяют также синкопальную форму интоксикации. По данным Б. И. Предтеченского, эта разновидность поражения составляет до 10—20% всех случаев отравления и развивается у лиц с нарушенными механизмами регуляции гемодинамики. При этом варианте течения отравления наблюдается резкое снижение артериального давления, сознание быстро утрачивается, кожные покровы и слизистые оболочки становятся бледными («белая асфиксия»). Развившееся коллаптоидное состояние может продолжаться несколько часов. Возможен смертельный исход от паралича дыхательного центра.
Осложнения острой интоксикации
При отравлениях тяжелой степени могут наблюдаться осложнения, которые снижают дееспособность или полностью лишают человека работоспособности в течение длительного времени. Чаще эти осложнения развиваются не сразу после отравления, а по прошествии нескольких дней или даже недель. К таким осложнениям относятся деструктивные процессы в ткани мозга, приводящие к формированию стойких нарушений функций центральной нервной системы (ослабление памяти, неспособность к умственному напряжению, изменения психической деятельности). Нарушения со стороны периферической нервной системы характеризуются невритами, радикулитами, парестезий. Иногда развиваются параличи и парезы конечностей. Возможны расстройства зрения, слуха, обоняния и вкуса. Тяжелое отравление часто осложняется пневмонией и отеком легких, вследствие нарушения легочного кровообращения и сердечной недостаточности, а также рабдомиолизом с последующей острой почечной недостаточностью.
Механизм токсического действия
Оксид углерода in vitro активно взаимодействует с многочисленными гем-содержащими протеидами (гемоглобин, миоглобин, цитохромы и т. д.) при условии, что железо, входящее в структуру порфиринового кольца их простетической группы, находится в двухвалентном состоянии. Связь двухвалентного железа с СО — обратима. С трехвалентным железом вещество не взаимодействует.
Оксид углерода, проникший в кровь, вступает во взаимодействие с гемоглобином (НЬ) эритроцитов, образуя карбоксигемоглобин (НЬСО), не способный к транспорту кислорода. Развивается гемический тип гипоксии. Оксид углерода способен взаимодействовать как с восстановленной (НЬ), так и с окисленной (НЬО) формой гемоглобина, поскольку в обеих формах железо двухвалентно.
К+,
НЬО + СО =5=ъ= НЬСО + о К-1
К* = К+1/К_1 — Константа Дугласа; К*= 300
Степень сродства токсиканта к гемоглобину может быть охарактеризована константой равновесия реакции взаимодействия (константа Дугласа). Установлено, что у человека, хотя скорость присоединения СО к гемоглобину в 10 раз ниже скорости присоединения кислорода, скорость диссоциации карбоксигемоглобина приблизительно в 3600 раз меньше соответствующей скорости для оксигемоглобина. Поэтому относительное сродство НЬ к СО примерно в 300 раз выше, чем к кислороду. Величина константы Дугласа у животных разных видов различна (у лошади — 240, канарейки — 100, кролика — 40). В состоянии равновесия СО, в концентрации 1 объемная часть на 1000 объемных частей воздуха, превращает 50% гемоглобина крови человека в карбоксигемоглобин. Как правило, в реальных условиях концентрация 0,1% СО во вдыхаемом воздухе обусловливает образование около 10% карбоксигемоглобина в крови.
Количество карбоксигемоглобина, образовавшегося в крови в начале воздействия яда, может быть рассчитано по формуле Лилиенталя (1946):
% НЬСО = (рССИ*МОД)«0,05,
где рСО — парциальное давление СО во вдыхаемом воздухе в мм рт. ст.;
t — время экспозиции в минутах;
МОД — минутный объем дыхания в литрах.
Поскольку карбоксигемоглобин не в состоянии переносить кислород от легких к тканям, существует тесная корреляция между его уровнем в крови и выраженностью клинической картины отравления. Экспозиция
5% СО в течение часа при умеренной физической активности сопровождается образованием 20% карбоксигемоглобина, при этом пострадавший начинает испытывать неприятные ощущения, предъявляет жалобы на головную боль. Интоксикация средней степени тяжести развивается при содержании крабоксигемоглобина 30—50%, тяжелая — около 60% и j выше. Смертельные исходы при отравлении СО в эксперименте на животных наблюдаются при уровне НЬСО в крови — 60—70%. Вместе с тем механическое удаление 70% гемоглобина или ингаляция воздуха с пониженным парциальным давлением О2 (и снижение тем самым содержания 1 НЮ до уровня 30%) к смерти экспериментальных животных не приводят. Это наблюдение косвенно указывает на наличие дополнительных механизмов токсического действия СО. По существующим представлениям они состоят в следующем.
Во-первых, оксид углерода не только выключает из транспорта О2 часть гемоглобина, но также нарушает явление гем-гем взаимодействия, затрудняя тем самым процесс диссоциации НЮ в крови отравленного и передачу транспортируемого кислорода тканям (Л. А. Тиунов, В. В. Кустов, 1969). Эффект еще более усиливается по мере развития интоксикации и понижения парциального давления СО2 в крови и тканях (эффект Бора).
Во-вторых, СО взаимодействует не только с гемоглобином, но также с целым рядом различных цитохромов (цитохромом «а», цитохромом «С», цитохромом Р-450 и т. д.), угнетая тем самым биоэнергетические процессы в тканях (развивается гистотоксический тип гипоксии — см. ниже).
Поскольку валентность железа тканевых цитохромов переменна, они становятся уязвимыми для действия токсиканта при переходе в состояние Fe+2. Это состояние наиболее вероятно в условиях снижения парциального давления кислорода в тканях (при гипоксии). Так, установлено, что экспериментальные животные, находящиеся под воздействием газовой смеси 3 атм. кислорода и 1 атм. оксида углерода, не погибают, хотя при этих условиях практически весь НЬ превращается в НЬСО. Тем не менее тканевые цитохромы резистентны к действию СО (железо находится преимущественно в трехвалентной форме), а растворенного в плазме крови кислорода оказывается достаточно, чтобы удовлетворить потребность в нем тканей. При изменении соотношения газовой смеси — 3 атм. кислорода и 2 атм. оксида углерода — животные погибают, несмотря на то что количество растворенного в плазме крови кислорода остается таким же, как в первом опыте. Развитие интоксикации в этом случае можно объяснить угнетением системы цитохромов — нарушением тканевого дыхания.
Наконец, СО активно взаимодействует с миоглобином (сродстро в 14—50 раз выше, чем к кислороду), пероксидазой, медь-содержащими ферментами (тирозиназа) тканей. Миоглобин (мышечный пигмент — аналог гемоглобина, состоящий из одной молекулы глобина, связанной с гемом) в организме выполняет функцию депо кислорода, а также значительно ускоряет диффузию кислорода в мышечной ткани. Взаимодействие оксида углерода с миоглобином приводит к образованию карбокси- миоглобина. Нарушается обеспечение работающих мышц кислородом. Этим отчасти объясняют развитие у отравленных выраженной мышечной слабости.
Определение карбоксигемоглобина в крови
Для уточнения диагноза отравления оксидом углерода производится определение НЬСО в крови различными физико-химическими и химическими методами.
Существуют довольно простые экспресс-методы определения содержания НЬСО в крови: проба с разведением, проба с кипячением, проба со щелочью, проба с медным купоросом, проба с формалином. Принцип методов основан на большей устойчивости НЬСО (сохраняет розовую окраску в растворе), в сравнении с НЬО, к денатурирующим воздействиям. Их чувствительность находится в пределах 25—40% НЬСО.
Количественное определение содержания НЬСО в крови производят спектрометрическими, фотометрическими, колориметрическими и газоаналитическими методами. Наиболее чувствительны фотометрический и спектрофотометрический методы, позволяющие определять НЬСО в крови начиная с 0,5—1%.
При необходимости направления проб в лабораторию для определения наличия НЬСО необходимо исключить контакт содержимого пробирок с воздухом, например, путем наслаивания вазелинового масла.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
» использование индивидуальных технических средств защиты (средства защиты органов дыхания; при применении карбонилов металлов — средства защиты органов дыхания и кожи) в зоне химического заражения.
Специальные профилактические медицинские мероприятия: ш применение антидота перед входом в зону пожара;
проведение санитарной обработки пораженных карбонилами металлов на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
» своевременное выявление пораженных;
применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
подготовка и проведение эвакуации.
Медицинские средства защиты
Сразу после удаления пораженного из зараженной атмосферы начинается процесс спонтанного выведения СО из организма, постепенно восстанавливаются свойства гемоглобина и тканевых ферментов. Специфическими противоядиями при отравлении СО являются вещества, ускоряющие этот процесс: кислород (Н. Н. Савицкий и др.) и ацизол (J1. А. Тиунов и др.).
Кислород. В связи с тем что СО обратимо связывается с гемоглобином и при этом конкурирует за участок связывания (двухвалентное железо гема) с кислородом, увеличение парциального давления последнего во вдыхаемой смеси (вдыхание чистого кислорода) способствует ускорению диссоциации образовавшегося карбоксигемоглобина и усиленному выведению яда из организма отравленного (скорость элиминации возрастает в 3—4 раза). При ингаляции О2 под повышенным давлением (0,5—2 атмосферы избыточной), кроме того, увеличивается количество кислорода, транспортируемого плазмой крови в форме раствора, снижается чувствительность тканевых цитохромов к ингибиторному действию СО, что также способствует устранению явлений кислородного голодания, нормализации энергетического обмена.
Ингаляцию кислорода (или кислородо-воздушных смесей) с помощью имеющихся на снабжении технических средств (кислородные ингаляторы) следует начинать как можно раньше. В первые минуты рекомендуют вдыхать 100% кислород, затем в течение 1—3 ч — 80—90% кислородо-воздуш- ную смесь, затем — 40—50% смесь кислорода с воздухом. Продолжительность мероприятия определяется степенью тяжести пострадавшего.
Бессознательное состояние, признаки ишемии миокарда, уровень карбоксигемоглобина в крови выше 60%, дыхательная недостаточность — показания к проведению гипербарической оксигенации (при наличии технических средств).
Ацизол — бис-(1-виниламидазол)-цинкдиацетат — комплексное соединение цинка, которое при действии на гемоглобин уменьшает его сродство к оксиду углерода (константа Хила процесса взаимодействия уменьшается с 2,3 до 1,8). Препарат рекомендуют применять внутримышечно в форме 6% раствора на 0,5% растворе новокаина в объеме 1,0 мл на человека в возможно более ранние сроки после воздействия СО. В случае тяжелого отравления допускается повторное введение ацизола в той же дозе не ранее чем через 1 ч после первой инъекции.
Симптоматические средства. При легких и средней степени тяжести поражениях позитивный эффект на состояние пострадавших оказывает назначение, наряду с ингаляцией кислорода, средств, возбуждающих дыхание и сердечную деятельность: кордиамин — 1 мл (п/к), кофеин 10% —
2 мл (п/к), вдыхание паров нашатырного спирта. Применение таких средств у тяжелопораженных без одновременно проводимой кислородотера- пии — противопоказано.
При поражении карбонилами металлов, кроме указанного выше, при угрозе развития токсического отека легких необходимо использование средств и методов, применяемых при отравлениях ОВТВ удушающего действия (см. гл. 9. «Отравляющие и высокотоксичные вещества пульмонотоксического действия».).
ОВТВ, образующие метгемоглобин
Как уже указывалось, железо, входящее в структуру гемоглобина, — двухвалентно, не зависимо от того, связан пигмент крови с кислородом (НЬО) или нет (НЬ). Более того, только находясь в двухвалентном состоянии (Fe+2), железо обладает необходимым для осуществления транспортных функций сродством к кислороду.
В нормальных условиях спонтанно и под влиянием различных патогенных факторов, в том числе химической природы, двухвалентное железо гемоглобина окисляется, переходя в трехвалентную форму. Образуется так называемый метгемоглобин (MetHb). Метгемоглобин не участвует в переносе кислорода от легких к тканям, поэтому значительное повышение его содержания в крови представляет опасность. Эволюционно сформировались механизмы обратного превращения метгемоглобина в гемоглобин. Благодаря этим механизмам у здорового человека уровень метгемоглобина в крови не превышает 0,5—2%. Существуют два основных механизма защиты железа гемоглобина от окисления.
Первый связан с «обезвреживанием» проникающих в эритроциты ксенобиотиков-окислителей до момента их действия на гемоглобин. Так, в присутствии энзима глутатионпероксидазы (ГПО) восстановленный глутатион взаимодействует с молекулами-окислителями, попавшими в клетки крови, предотвращая их метгемоглобинообразующее действие.
Несостоятельность этого механизма (снижение активности глугатионпе- роксидазы, содержания восстановленного глутатиона в эритроцитах) может привести к умеренной метгемоглобинемии и появлению в крови телец Гейнца (продукты денатурации гемоглобина).
Второй механизм обеспечивает восстановление уже образовавшегося в крови метгемоглобина при участии двух ферментативных систем: НАДН-зависимой и НАДФН-зависимой метгемоглобинредуктаз. В одной из них донорами электронов (восстанавливающих агентов) являются продукты анаэробного этапа метаболизма глюкозы (НАДН), в другой — гексозомонофосфатного превращения (НАДФН) (рис. 27).
Гексозомонофосфатный шунт
НАДФИ-MetHbRed
НАДФН + HbFe(+3)-OH ► HbFe(+2) + НАДФ + HgO
