
Posobie_dlya_podgotovki_k_zanyatiam
.pdfотделяемого измеряют и записывают в историю болезни. Больные с наружными свищами органов пищеварения требуют особого ухода. Их, как правило, перевязывают один или несколько раз в сутки в перевязочной.
Дежурной медсестре нередко, особенно в вечернее и ночное время, приходится менять повязку, промокшую кишечным содержимым или желчью. При смене повязки необходимо тщательно соблюдать все правила асептики и особенно стараться не сместить дренажные трубки, которые часто фиксируют полоской бинта вокруг тела больного. При перевязках больных с желчными или панкреатическими свищами смена повязки должна производиться в присутствии врача, так как при этом можно вместе с повязкой удалить дренаж из раны. Нередко при желчных или панкреатических свищах имеется мацерация окружающей кожи от раздражения желчью и панкреатическим соком. Раздраженную кожу обмывают теплым раствором фурацилина, просушивают стерильным шариком, после чего наносят на нее толстый слой цинковой пасты или пасты Лассара. Обычно накладывают сухую асептическую повязку из нескольких слоев больших марлевых салфеток с разрезом до середины (штанишки) так , чтобы можно было через разрез пропустить дренаж. Вторую салфетку укладывают в противоположном направлении, следя за тем, чтобы разрезанная часть верхней салфетки легла на целую часть нижней.
Смена повязок у больных со свищами двенадцатиперстной и тонкой кишки производится также, как описано выше. Однако у этих пациентов чаще возникает сильная мацерация кожи. При обширном поражении кожи больные испытывают постоянную жгучую боль, причем малейшее прикосновение к разъеденной коже очень болезненно. Поэтому перед перевязкой больному целесообразно ввести обезболивающие средства. Удаляя пинцетом повязку, нужно действовать аккуратно, стараясь не причинять боль. Туалет кожи вокруг свища выполняют обмыванием теплым раствором фурацилина. Смазывать спиртом или иодом мацерированную кожу нельзя - это вызовет очень сильную боль. После обмывания кожу просушивают и наносят слой пасты с помощью стерильного шпателя. Затем свищ укрывают новой повязкой. Сформированные свищи толстой кишки обычно доставляют меньше забот. Оформленный кал легко убирается кусочками ваты, а кожа моется обычной водой с мылом. Загрязненный калоприемник меняют на чистый. Необходимо научить больного правильно пользоваться калоприемником и самостоятельно выполнять все гигиенические мероприятия. Не нужно забывать, что сам калоприемник подлежит ежедневному мытью и дезинфекции. При уходе за больными с гастростомой, то есть свищем желудка, нужно следить за чистотой кожи вокруг трубки и за ее хорошей фиксацией.
Борьба с болью является одной из наиболее важных задач в послеоперационном периоде. Эффективное обезболивание способствует ранней реабилитации больного, снижает частоту возникновения послеоперационных осложнений и хронических болевых синдромов. В настоящее время имеется широкий выбор лекарственных препаратов и методов немедикаментозного обезболивания, однако многочисленные исследования, проведенные в разных странах, выявили недостаточную анальгезию раннего послеоперационного периода почти у 50% больных [6,7,11]. Поэтому знание современных принципов обезболивания после операции имеет большое практическое значение.
Этапами адекватного обезболивания являются:
1. Предоперационная оценка интенсивности и длительности болевого синдрома (табл. 1, табл. 2).
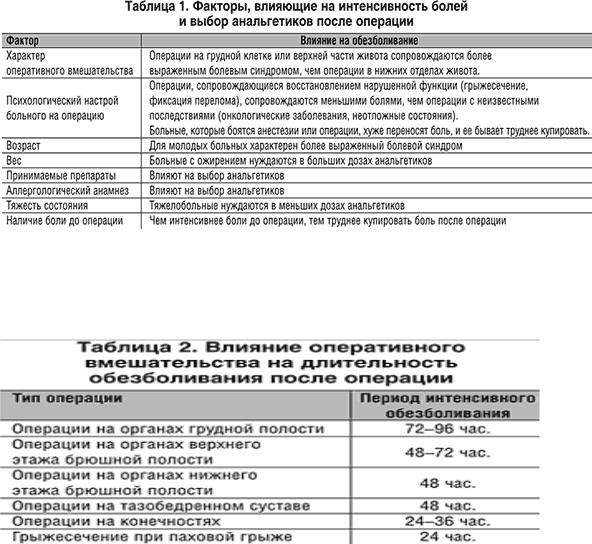
2.Построение плана лечения боли (анальгетик(и), пути введения, частота и т.д.) (табл. 3).
3.Лечение боли.

4. Послеоперационная оценка эффективности обезболивания (для корректировки плана лечения боли при недостаточном обезболивании). Для определения качества обезболивания после операции наибольшее распространение получила визуальная аналоговая шкала (рис. 1). Больной ставит на линии вертикальную отметку, соответствующую уровню боли. Обезболивание признается адекватным, если больной не отмечает болей в покое, а при движении, кашле возникает умеренная боль, не ограничивающая их.
Рис. 1. Визуальная аналоговая шкала
Опиоидные анальгетики реализуют свое действие через опиатные рецепторы, расположенные на спинальном и супраспинальном уровнях, и являются основной группой лекарственных средств для лечения боли в послеоперационном периоде.
В то же время после обширных внутриполостных хирургических вмешательств для достижения адекватного обезболивания у каждого третьего больного требуется введение опиоидов в дозах, превышающих стандартно рекомендуемые [3]. Увеличение дозы опиоидных анальгетиков сопровождается выраженными побочными реакциями (сонливостью, угнетением дыхания, тошнотой, рвотой, парезом желудочно–кишечного тракта, нарушениями мочеиспускания), поэтому в настоящее время признано, что монотерапия опиоидными анальгетиками не всегда достаточно эффективна, а иногда даже опасна.
Кроме того, при традиционном подкожном и внутримышечном введении трудно поддерживать оптимальную концентрацию опиоидов в плазме, что может сопровождаться либо угнетением дыхания, либо недостаточным обезболиванием.
Болюсное введение опиоидных анальгетиков интратекально или эпидурально обеспечивает хорошее обезболивание до 24 часов, однако даже небольшие дозы вводимых препаратов (в десятки раз меньше, чем при внутримышечном введении) могут сопровождаться побочными и токсическими эффектами.
Трамадол (Трамал) – это опиоидный агонист, стоящий особняком среди всех представителей опиоидов этого класса, прежде всего потому, что в отличие от них он не принадлежит к наркотическим средствам. Это подтверждено обширным клиническим опытом его использования во всем мире и специальными научными исследованиями его наркотического потенциала.
Вотличие от других опиоидных агонистов трамадол имеет двойной механизм действия. Установлено, что анальгезия, вызванная трамадолом, полностью не устраняется опиоидным антагонистом налоксоном и наряду с опиоидным механизмом реализуется путем дополнительного торможения болевой импульсации с участием серотонин– и адренергической систем. Т.е. по механизму анальгетического действия трамадол не полностью идентичен другим опиоидным агонистам.
Анальгетический потенциал трамадола по данным разных авторов, составляет от 0,1 до 0,2 от потенциала морфина, он равен или несколько превосходит потенциал кодеина; по эффективности 50 мг трамадола эквивалентны 1000 мг метамизола, т.е. трамадол принадлежит к анальгетикам, предназначаемым для лечения боли сильной и умеренной интенсивности.
Вмногочисленных исследованиях не установлено значимого угнетения дыхания у послеоперационных пациентов под влиянием Трамала в диапазоне терапевтических доз от 0,5 до 2 мг на 1 кг массы тела даже при внутривенном болюсном введении, тогда как морфин в терапевтической дозе 0,14 мг/кг статистически достоверно и значительно снижает частоту дыхания и повышает напряжение СО2 в выдыхаемом воздухе.
Нестероидные противовоспалительные препараты (НПВП) обладают анальгетическими и противовоспалительными свойствами. Механизм действия связан с ингибированием циклооксигеназы, которая катализирует расщепление арахидоновой кислоты на различные простагландины, являющиеся основными медиаторами воспаления. Кроме того, НПВП оказывают влияние на проведение болевых импульсов в центральной нервной системе. НПВП считаются эффективными анальгетиками при легкой или умеренной боли. Побочные эффекты связаны с основным действием НПВП – подавлением синтеза простагландинов и развиваются, как правило, при длительном применении. К ним относят НПВП–гастродуоденопатию (диспептические расстройства, эрозии и язвы желудка и двенадцатиперстной кишки); нефротоксичность; нарушение
свертывающей активности крови (торможение аггрегации тромбоцитов и образования протромбина в печени); гематотоксичность (снижение количества эритроцитов и лейкоцитов в крови). Выраженность побочных эффектов уменьшается при использовании селективных ингибиторов циклооксигеназы–2 [8].
Методы регионарной анестезии широко применяются при выполнении оперативных вмешательств для уменьшения побочных эффектов системного обезболивания и могут быть использованы в послеоперационном периоде.
Существует несколько способов применения местных анестетиков:
–инфильтрационная анестезия ран;
–блокада периферических нервов и сплетений;
–эпидуральная или интратекальная (спинномозговая, спинальная) анестезия. Инфузия местных анестетиков позволяет обеспечить эффективную анальгезию,
однако может сопровождаться артериальной гипотензией, моторным блоком, тошнотой и расстройствами мочеиспускания.
При выраженном болевом синдроме применяют катетеризацию эпидурального пространства для многократного введения анальгетика – длительная эпидуральная анестезия (реже применяется длительная спинальная анестезия).
Клонидин является агонистом a–норадренергических рецепторов и тормозит передачу болевых импульсов за счет воздействия на постсинаптические рецепторы.
Кетамин и сульфат магния снижают проведение болевых импульсов и препятствуют возбудимости нейронов на различных уровнях центральной нервной системы (ЦНС).
Несмотря на большое число обезболивающих препаратов, применение каждого из них сопряжено с риском развития побочных эффектов, поэтому в настоящее время одним из основных принципов послеоперационного обезболивания является принцип сбалансированного обезболивания, когда используется комбинация опиоидных анальгетиков, нестероидных противовоспалительных средств, местных анестетиков и препаратов других групп (кетамин, сульфат магния).
Одновременное применение препаратов разных групп (трамадол и ацетаминофен (Залдиар)) позволяет блокировать проведение ноцицептивных (болевых) импульсов на всех уровнях, уменьшает дозу каждого из анальгетиков, улучшает качество обезболивания и значительно снижает число побочных эффектов. Препарат может применяться после малотравматичных оперативных вмешательств (грыжечение, секторальная резекция молочной железы, резекция щитовидной железы и т.д.), при этом многие авторы до сих пор полагают, что монотерапия НПВП достаточна для эффективного обезболивания
[3,12].
При более травматичных операциях (большинство полостных операций) наиболее оптимальным является сочетание НПВП с опиоидными анальгетиками (Залдиар). Синергизм анальгетического действия опиоидов и НПВП позволяет на 20–60%. снизить потребность в опиоидных анальгетиках и уменьшить их побочные эффекты (улучшение функции внешнего дыхания, быстрое восстановление моторики желудочно–кишечного тракта) [5,6,9].
Трамадол и ацетаминофен (парацетамол) – два анальгетика, доказавшие свою эффективность при широком спектре заболеваний, и послужили основой для создания комбинированного препарата Залдиар (трамадол 37,5 мг/ацетаминофен 325 мг). Использование такой комбинации препаратов оправдано, в первую очередь, с точки зрения фармакокинетических и фармакодинамических особенностей препаратов.
Механизм действия ацетаминофена (парацетамола) недостаточно понятен. Предполагают, что он имеет центральное действие, при этом анальгезия достигается за счет повышения порога боли, а антипиретическое действие – через торможение простагландин–синтетазы в гипоталамусе. Ацетаминофен назначают при слабых и умеренных болях, чаще при артрозе крупных суставов при небольшой выраженности воспаления.
Время достижения максимальной концентрации в сыворотке крови (Тmax) у ацетаминофена и у трамадола различные. Исходя из фармакокинетических особенностей, применение комбинации препаратов является обоснованным: ацетаминофен развивает ранний аналгетический эффект, в то время как трамадол реализует свое действие позже, и, обладая большим периодом полувыведения, обеспечивает пролонгацию аналгезии. Использование указанной комбинации лекарственных средств проявило большую клиническую эффективность, чем прием трамадола 75 мг в качестве монотерапии.
По результатам проведенного рандомизированного двойного слепого плацебо– контролируемого исследования у 1783 больных (одонтогенный болевой с–м, послеоперационные больные ортопедического, гинекологического профиля), комбинация трамадол/ацетаминофен оказалась более эффективна, чем применение обоих препаратов в отдельности [6]. По данным других авторов, применение 2 таблеток Залдиара (трамадол 75 мг + ацетаминофен 750 мг) у больных при одонтогенных оперативных вмешательствах оказывало более быстрый и длительный эффект, чем монотерапия трамадолом. Наиболее часто принцип сбалансированной анальгезии применяется после хирургических вмешательств, сопровождающихся большой травматичностью (расширенные онкологические операции с лимфаденэктомией; операции, выполняемые торакоабдоминальным доступом; резекция пищевода с пластикой желудочной трубкой или толстой кишкой; обширные резекции печени и т.д.). Для повышения качества послеоперационного обезболивания в последние годы применяется методика контролируемой пациентом анальгезии (КПА). Устройство для КПА представляет собой автоматический шприц с микропроцессорным управлением, приводимый в действие кнопкой, находящейся в руках больного. Применение КПА позволяет снизить дозу анальгетиков (и их побочных и токсических эффектов) и нивелировать индивидуальные особенности действия препаратов у различных больных. КПА на основе внутривенного введения морфина показана больным с низким риском развития сердечно–легочных осложнений и требуется введение опиоидных анальгетиков, как минимум, в течение 2 суток после операции. В данной методике нуждаются от 10 до 30% больных [6].
Условием проведения КПА являются восстановление сознания и адекватность больного, а также обязательное мониторирование жизненно важных функций, что вместе с высокой стоимостью устройств для КПА ограничивает применение метода. Традиционная концепция послеоперационного обезболивания предполагала использование анальгетиков только после появления сильных болей. Однако в настоящее время доказано, что обезболивания достичь гораздо труднее, если ощущение боли уже сформировалось. Во время оперативного вмешательства возникает травма тканей, которая сопровождается формированием большого количества ноцицептивных (болевых) импульсов. Затем из поврежденных тканей выделяются медиаторы воспаления и другие биологически активные вещества, которые, взаимодействуя с мембраной нервных окончаний ноцицептивных рецепторов, повышают их чувствительность к механическим и термическим факторам. Развивается сенситизация (повышение чувствительности) ноцицепторов в области повреждения, что проявляется снижением порога их активации (периферическая сенситизация) [1,2]. Поток ноцицептивных импульсов, возросший вследствие периферической сенситизации, приводит к увеличению возбудимости спинальных нейронов, участвующих в проведении болевых импульсов (центральная сенситизация).
При возникновении состояния сенситизации стимулы, которые в норме не вызвали бы боли, начинают восприниматься, как болевые, а болевые стимулы начинают восприниматься, как гиперболевые (гиперальгезия).
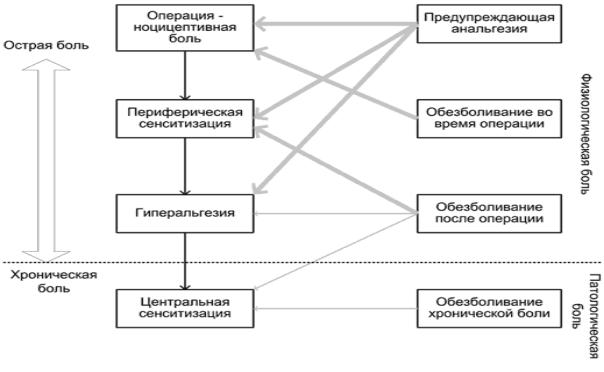
Возникшая вследствие повреждения тканей сенситизация ноцицептивных нейронов ЦНС может сохраняться несколько часов или дней после прекращения поступления ноцицептивных импульсов с периферии.
Принцип предупреждающего обезболивания (профилактика боли) заключается в применении анальгетиков (как правило, НПВП) до начала операции, что позволяет предотвратить возникновение периферической и центральной сенситизации (рис. 2)
[4,10].
Рис. 2. Стратегия лечения боли (цит. по Kissin I., 2000 с изменениями) Толщина стрелок соответствует эффективности воздействия
Оптимального метода послеоперационного обезболивания в настоящее время не существует. Выбор лекарственных препаратов и методов обезболивания определяется опытом анестезиолога, материальными возможностями и другими факторами.
Приводим пример возможной схемы обезболивания при операции гастрэктомии с расширенной лимфаденэктомией в объеме D2.
Премедикация – накануне операции в 22:00 и за 20–60 минут до операции внутримышечно вводится мидазолам (0,07–0,1 мг/кг) и 100 мг кетопрофена. Катетеризация эпидурального пространства осуществляется на уровне ThVII–ThIX. Начальная доза местного анестетика составляет 6–10 мл ропивакаина (или бупивакаина 0,25%) с добавлением 50–100 мг фентанила, затем постоянная инфузия ропивакаина (8–12 мл/час) и фентанила (2–2,5 мкг/кг/час). Поддержание анестезии осуществляется любым доступным способом (нейролептоанестезия, тотальная внутривенная анестезия). В послеоперационном периоде для эпидуральной анестезии применяются меньшие концентрации местных анестетиков (0,2% ропивакаин или 0,2% бупивакаин). Минимально эффективная доза подбирается путем титрования (скорость инфузии при этом может варьировать от 4 до 12 мл в час). При недостаточной анальгезии не следует увеличивать скорость инфузии или концентрацию анестетика, а необходимо применить НПВП, другие ненаркотические анальгетики или опиоиды.
Важно отметить, что некупирующийся болевой синдром в послеоперационном периоде требует исключения осложнений после операции (несостоятельности швов, панкреонекроза и др.).
Уход за роженицами и родильницами.
Медицинские сестры в акушерско-гинекологических учреждениях выполняют назначения врача, раздают больным лекарства, производят внутримышечные и подкожные инъекции, обеспечивают тщательное наблюдение за больными в послеродовом и послеоперационном периодах, готовят больных к различным процедурам и операциям.
Медицинским сестрам приходится выполнять и более простые работы: участвовать в приеме больных, рожениц и родильниц, осуществлять наблюдение и уход за больными, производить утренний туалет и уборку больных в течение суток, следить за чистотой постели (вовремя оправлять ее, менять постельное и нательное белье), кормить и поить больных, обеспечивать уборку палат и чистоту в них, ставить очистительные клизмы, подавать больным судна и выносить их, следить за чистотой предметов ухода за больными (судна, пузыри для льда, подкладные клеенки, наконечники для клизм, термометры, грелки, газоотводные трубки и др.), доставлять больных на перевязку, сопровождать на процедуры и консультации к специалистам, в рентгенкабинет и др.
При уходе необходимо обеспечить роженице, родильнице или гинекологической больной соответствующий санитарно-гигиенический режим, спокойную обстановку, не допускать шума, принимать меры для охраны нервно-психического состояния больных, внимательно относиться к их жалобам и просьбам, следить за чистотой постели, отсутствием складок в постельном белье, перекладывать больных несколько раз в день, регулярно следить за кожей, не допускать у тяжелобольных пролежней, протирать кожу камфорным спиртом, а при первой возможности организовать мытье больной под душем или в ванне).
Необходимо наблюдать за функцией желудочно-кишечного тракта (своевременно ставить очистительные клизмы, давать слабительные по указанию врача), обеспечить правильный туалет полости рта (регулярное полоскание или протирание ее). Особенно важны тщательное наблюдение и уход за тяжелобольными.
Гигиена роженицы, родильницы, гинекологической больной включает комплекс мероприятий, способствующих профилактике заболеваний и высокой эффективности лечения. Больных, поступающих в акушерско-гинекологические учреждения, подвергают тщательному осмотру и санитарной обработке (ванна, душ или влажное обтирание). Уход за кожей начинается с приемного отделения, куда поступают больные. Если характер заболевания позволяет произвести санитарную обработку, то в первую очередь следует вымыть больную. У некоторых женщин, поступающих по скорой помощи, санитарная обработка упрощается (производится обмывание наиболее загрязненных мест – ног и промежности). Беременные и роженицы, поступающие в родильный дом в удовлетворительном состоянии, моются под душем. Если состояние роженицы не позволяет принять душ, ограничиваются влажным обтиранием тела, мытьем ног и подмыванием (после сбривания волос в области лобка и наружных половых органов). Гинекологические больные (если нет противопоказаний) при поступлении принимают гигиеническую ванну. У больных и рожениц при поступлении коротко подстригают ногти на руках и ногах. В туалетных комнатах для гинекологических больных должны быть условия для выполнения всех гигиенических процедур. Тяжелобольным в выполнении гигиенических процедур помогает младший медицинский персонал. Гигиенический душ или ванна рекомендуются в плановом порядке один раз в 7-10 дней с последующей сменой нательного и постельного белья. При необходимости (повышенное потоотделение, загрязнение кожи и постели выделениями, рвотными массами и др.) врач может назначить душ или ванну в любой день, а также перед операцией.
Гигиенический уход за женщинами имеет свои особенности. На коже могут скапливаться бактерии, которые у полных женщин могут вызвать раздражение в складках кожи под молочными железами, в паху и в области наружных половых органов. Раздражение, как правило, порождает зуд. Присоединение гноеродной инфекции может
повлечь за собой появление гнойничков, фурункулов. В связи с этим особое внимание при уходе следует обращать на состояние кожи, в толще которой располагаются сальные и потовые железы, выделяющие на поверхность кожи жир, пот и другие продукты обмена веществ. Наружные половые органы ходячие больные подмывают сами в душевой или в ванной либо в специальной комнате личной гигиены. Перед этим следует помочиться. Чисто вымытыми руками, поливая струей воды, обмывают не реже одного раза в день (а в дни менструации – 2 раза в день) наружные половые органы и кожу внутренней поверхности бедер. По окончании обмывания наружных половых органов тщательно обмывают область заднего прохода, а затем чистой салфеткой или отдельным полотенцем обсушивают кожу. Необходимо обучить женщину правильно совершать этот туалет.
Лежачим больным наружные половые органы подмывают ежедневно один раз (если подмывание не назначено более часто). Перед подмыванием больная должна помочиться и опорожнить кишечник. Под больную подставляют судно и ватным шариком, захваченным корнцангом, поливая из кувшина, тщательно обмывают наружные половые органы, включая область клитора. Для подмывания рекомендуется пользоваться слабым (1:5000) раствором калия перманганата или 1 % водным раствором лизоформа. Медицинская сестра должна следить за чистотой и своих рук. Частое мытье рук с мылом и теплой водой (с применением щеток) с последующим ополаскиванием их раствором хлорамина дает возможность сохранить руки в чистоте. Он начинается с момента рождения последа и кончается через 6–8 недель. Симптомы: матка после родов хорошо сокращается, стенки ее утолщаются, она плотной консистенции, очень подвижная из за растяжения связочного аппарата.
При переполнении соседних органов (мочевого пузыря, прямой кишки) матка поднимается. С каждым днем послеродового периода матка становится все меньше, о чем можно судить по высоте стояния дна матки – в течение первых 10–12 дней после родов дно матки опускается ежедневно на один поперечный палец. На 1-2-й день дно матки стоит на уровне пупка (при опорожненном мочевом пузыре), а на 10-12 день дно матки обычно скрывается за лоном.
Шейка матки формируется изнутри кнаружи. Сразу после родов шейка имеет вид тонкостенного мешка, канал ее свободно пропускает кисть. Сначала закрывается внутренний зев, потом – наружный. Внутренний зев закрывается на 7-10 день, наружный
– на 18-21 день после родов. Внутренняя поверхность матки после родов представляет собой сплошную раневую поверхность с обрывками эпителия, донышек желез матки и стромы базального слоя эндометрия. Отсюда и происходит регенерация слизистой оболочки. Слизистая оболочка на всей внутренней поверхности матки восстанавливается на 7-10-й день, а в области плацентарной площадки – к концу 3-й недели.
При восстановлении эндометрия образуются послеродовые выделения – лохии, представляющие собой раневой секрет. В первые 3–4 дня лохии кровянистые, в следующие 3–4 дня – серозно-кровянистые, к 7-8 дню уже не содержат примеси крови, становятся светлыми. С 3-й недели они становятся скудными, а к 5-6 неделе послеродового периода выделения прекращаются. Если выделения и после 7-8 дня с примесью крови, это указывает на замедленное обратное развитие матки, что бывает при плохом сокращении ее, наличии в матке остатков плацентарной ткани, воспаления и т. д. Иногда выделения отсутствуют, лохии скапливаются в матке.
При нормальном течении послеродового периода состояние родильницы хорошее, дыхание глубокое, пульс ритмичный, 70–76 в минуту, нередко замедлен, температура нормальная. Учащение пульса и повышение температуры указывают на осложнение послеродового периода, чаще всего на развитие послеродовой инфекции.
Мочеотделение обычно нормальное, лишь изредка возникает затрудненное мочеиспускание. После родов может наблюдаться задержка стула, обусловленная атонией кишечника. Атонии способствует расслабление брюшного пресса и ограничение движений после родов.
На 3-4-й день после родов молочные железы начинают отделять молоко. Они набухают, становятся чувствительными, нередко при сильном набухании возникают распирающие боли. Иногда на 3-4-й день самочувствие родильницы может ухудшаться из за сильного нагрубания молочных желез, хотя молока продуцируется немного в эти дни, поэтому сцеживание при нагрубании бесполезно и вредно. В послеродовом периоде родильнице необходимо создать режим, способствующий правильному обратному развитию половых органов, заживлению раневых поверхностей, нормальной функции организма.
Раневые поверхности в матке и других отделах родовых путей являются входными воротами для легкого проникновения инфекции. Поэтому основным правилом в организации ухода за родильницей является строгое соблюдение всех правил асептики и антисептики.
Уход за родильницей. Главное: наблюдение за общим состоянием и самочувствием, контроль пульса не менее 2 раз в день и температурой тела. Кроме того, следят за состоянием молочных желез (нет ли трещин на сосках). Ежедневно измеряют высоту стояния дна матки, ее консистенцию, форму, чувствительность; осматривают наружные половые органы, определяют характер и количество лохии. Следят за отправлением кишечника и мочевого пузыря. Все эти данные записывают в историю родов. При болезненных послеродовых схватках можно назначить амидопирин, антипирин (по 0,3– 0,5 г). При замедленной инволюции матки применяют средства, усиливающие сокращение матки. При затруднении мочеиспускания проводят ряд соответствующих мероприятий. При задержке стула на 3-й день делают очистительную клизму, или назначают слабительное (касторовое или вазелиновое масло).
Если послеродовой период протекает без осложнений и нет разрывов промежности, родильнице на 2-е сутки разрешают сидеть, а на 3-4-е – ходить. Раннее вставание способствует лучшему опорожнению мочевого пузыря, кишечника, более быстрому сокращению матки. Не противопоказано раннее вставание и при разрывах промежности I– II степени (при этом не следует садиться). Здоровые родильницы со 2-го дня после родов начинают занятия лечебной гимнастикой. Занятия проводят в первой половине дня, лучше через 2 ч после завтрака, летом – при открытых окнах, зимой – после тщательного проветривания палаты. Занятия способствуют усилению обмена веществ, углублению дыхания, укреплению мышц брюшной стенки и промежности. Упражнения выполняют в медленном темпе. Продолжительность занятия 5-15 мин. Каждой родильнице, выписывающейся домой, надо разъяснить необходимость продолжения лечебной гимнастики и дома. Перед каждым кормлением родильница должна мыть руки, ежедневно менять рубашку, не реже 2 раз в день производить туалет наружных половых органов. Молочные железы следует обмывать 0,5 % раствором нашатырного спирта или теплой водой с мылом утром и вечером после кормления. Соски обмывают 1 % раствором борной кислоты и обсушивают стерильной ватой. При значительном нагрубании молочных желез ограничивают питье, назначают слабительные средства.
Если при сосании молочная железа опорожняется не полностью, после каждого кормления необходимо сцеживать молоко молокоотсосом. Утром и вечером проводят воздушные ванны длительностью 15 мин. В особом питании родильница не нуждается. К обычному питанию следует добавить 0,5 л кефира, 100–200 г творога, свежие фрукты, ягоды, овощи. Из рациона следует исключить острые и жирные блюда, консервы. Алкоголь противопоказан. Родильниц с повышенной температурой, катаром верхних дыхательных путей, послеродовыми заболеваниями необходимо изолировать от здоровых родильниц, для чего заболевших переводят в другое акушерское отделение или отдельную палату. При нормальном течении послеродового периода родильницу выписывают через 7–8 сут после родов.
