
- •1.4.1. Процеживание
- •1.4.2. Отстаивание
- •4.3. Фильтрование
- •1.5.1.1. Электрокоагуляция
- •Усреднители
- •Песколовки
- •1.5.2. Флотация
- •1.5.2.1. Флотация с выделением воздуха из раствора
- •1.5.2.2. Флотация с механическим диспергированием воздуха
- •Необходимое число флотационных камер определяется из соотношения
- •1.5.2.3. Флотация с подачей воздуха через пористые материалы
- •1.5.2.4. Электрофлотация
- •1.5.2.5. Биологическая и химическая флотация
- •1.5.3. Сорбция
- •1.5.4. Экстракция
- •Таблица 1.3
- •1.5.6. Мембранные процессы
- •Таблица 1.4
- •Расход реагентов для нейтрализации 100 % кислот и щелочей
- •Расход реагентов, требуемых для удаления металлов
- •Реагенты
- •Вода
- •Известь
- •Осадок
- •Рис. 1.50. Нейтрализатор дымовых вод щелочными газами
- •Продукция
- •Производство
- •Асбест
- •Вода
- •В атмосферу
- •Выпуск отработанного воздуха
- •Рис. 1.56. Контактные аппараты для озонирования:
- •Осадок
- •Сточная
- •NaHSO2
- •Азота диоксид (газ)
- •Углерода оксид (газ)
- •Циклогексан (пары)
- •3. Переработка отходов производства и потребления
- •3.2. Способы утилизации промышленных отходов
- •3.3. Отходы потребления
- •3.4. Методы утилизации отходов производства и потребления
- •3.5. Переработка твердых бытовых отходов компостированием
- •СПИСОК ЛИТЕРАТУРЫ
- •Приемный корпус
вается не сразу, а по истечении некоторого времени – 10÷15 мин. Сказанное выше относится к сточным водам, содержащим сильные кислоты (H2SO4, H2SO4), кальциевые соли которых труднорастворимы в воде [1].
При нейтрализации сточных вод, содержащих серную кислоту (H2SO4), реакция в зависимости от применяемого реагента протекает по уравнениям:
H2SO4+Ca (OH)2 = CaSO4+2H2O,
H2SO4+CaCO3=CaSO4+CO2.
Образующийся в результате нейтрализации сульфат кальция (гипс) кристаллизуется из разбавленных растворов в виде CaSO4·2H2O. Растворимость этой соли при температуре 0-40 0С колеблется от 1,76 до 2,11 г/л.
При более высокой концентрации сульфат кальция выпадает в осадок, поэтому при нейтрализации сильных кислот, кальциевые соли которых труднорастворимы в воде, необходимо устраивать отстойники-шламонакопители. Существенным недостатком метода нейтрализации серной кислоты известью является образование пресыщенного раствора гипса
(коэффициент пресыщения может достигать 4÷6), выделение которого из сточной воды может продолжаться несколько суток, что приводит к зарастанию трубопроводов и аппаратуры. Присутствие в сточных водах многих химических производств высокомолекулярных органических соединений усиливает устойчивость пресыщенных растворов гипса, поскольку эти соединения сорбируются на гранях кристаллов сульфата кальция и препятствуют их дальнейшему росту.
Для уменьшения коэффициента пресыщения используется метод рециркуляции образующегося в результате нейтрализации осадка сульфата кальция. Концентрация ионов кальция в сточной воде уменьшается при увеличении дозы рециркулирующего осадка: продол-
жительность перемешивания этой воды должна быть не менее 20÷30 мин. Для уменьшения зарастания трубопроводов, по которым транспортируются нейтрализованные известью сернокислотные стоки, применяют методы промывки, увеличивают скорость транспортирования, а также заменяют металлические трубопроводы на пластмассовые.
Поскольку в кислых и щелочных сточных водах практически всегда присутствуют ионы тяжелых металлов, то дозу реагентов следует определять с учетом выделений в осадок тяжелых металлов.
Количество реагента, необходимого для нейтрализации сточных вод определяется по формуле
G = k 100B Q A a,
где k – коэффициент запаса расхода реагента по сравнению с теоретическим k = 1,1 – для известкового молока, k = 1,5 – для известкового теста и сухой извести; В – количество активной части в товарном продукте, %; Q – количество сточных вод подлежащих нейтрализации, м3; а – расход реагента для нейтрализации (табл. 1.7), г/кг
Расход реагентов для нейтрализации 100 % кислот и щелочей |
Таблица 1.7 |
||||
|
|||||
Щелочь, кг |
|
Кислоты |
|
|
|
Серная |
Соляная |
|
Азотная |
Уксусная |
|
|
|
||||
Известь: |
|
|
|
|
|
негашеная |
0,56/1,79 |
0,77/1,3 |
|
0,46/2,2 |
0,47/2,15 |
гашеная |
0,76/1,32 |
1,01/0,99 |
|
0,59/1,7 |
0,62/1,62 |
|
|
|
|
|
|
Сода: |
|
|
|
|
|
кальцинированная |
1,08/0,93 |
1,45/0,69 |
|
0,84/1,19 |
0,98/1,14 |
каустическая |
0,82/1,22 |
1,1/0,91 |
|
0,64/1,57 |
0,67/1,5 |
|
|
|
|
|
|
84
Аммиак |
0,35/2,88 |
0,47/2,12 |
0,27/3,71 |
– |
|
|
|
|
|
При нейтрализации кислых и щелочных сточных вод содержащих соли тяжелых металлов, количество реагента будет определяться по формуле
G = k 100B Q (a A +b1 C1 +b2 C2 + ...+bnCn ),
где С1, С2,...,Сn – концентрации металлов в сточных водах, кг/м; b1, b2,...,bn, – концентрации реагентов, требуемых для перевода металла из растворенного состояния в осадок (табл. 1.8), кг/кг.
|
Расход реагентов, требуемых для удаления металлов |
Таблица 1.8 |
|||
|
|
||||
Металл |
|
|
Реагент |
|
|
|
|
|
|
|
|
СаО |
Са(ОН)2 |
|
Na2CO3 |
NaOH |
|
|
|
||||
|
|
|
|
|
|
Цинк |
0,85 |
1,13 |
|
1,6 |
1,22 |
|
|
|
|
|
|
Никель |
0,95 |
1,26 |
|
1,8 |
1,36 |
Медь |
0,88 |
1,16 |
|
1,66 |
1,26 |
|
|
|
|
|
|
Железо |
1 |
1,32 |
|
1,9 |
1,43 |
Свинец |
0,27 |
0,36 |
|
0,51 |
0,38 |
|
|
|
|
|
|
Например, при нейтрализации гашеной известью сточных вод, поступающих после травления черных металлов серной кислотой происходят следующие реакции:
с серной кислотой: |
H2SO4+ Са(ОН )2 = CaSO4+ 2H2O |
||||
|
98 |
|
74 |
136 |
36 |
с сульфатом железа: |
FeSO4+ Ca(OH)2 = CaSO4+ Fe(OH)2 |
||||
|
152 |
74 |
136 |
|
90 |
На основании приведенных выше реакций или данных в табл. 1.7 и 1.8, а также по содержанию серной кислоты и железа в отработанных травильных растворах можно определить количество гашеной извести, необходимой для нейтрализации кислых сточных вод и осаждения железа
G = k 100B Q (0,76 A +1,32 C),
где А – содержание серной кислоты, кг/м3; С – содержание железа, кг/м3.
Количество сухого вещества, которое образуется при нейтрализации 1м3 сточной воды, содержащей свободную серную кислоту и соли тяжелых металлов, определяется по формуле
M = 100B− B (x1 + x2 )+ x3 +(y1 − y2 − 2),
где М – масса сухого вещества, кг; В – содержание активного вещества в используемой извести, %; х1, х2 – количество активного вещества, необходимое соотвественно для осаждения металла и для нейтрализациии свободной серной кислоты, кг; х3 – количество образующихся гидроксидов металлов, кг; у1, у2 – количество сульфата кальция, образующиеся соответственно при осаждении металла и при нейтрализации свободной серной кислоты, кг.
Если значение третьего члена в приведенной формуле отрицательно, то он не учитывается.
Объем осадка, образующегося при нейтрализации сточной воды можно найти по уравнению
85
V = 100М ,
ос |
100 −Wвл |
|
где Wвл – влажность осадка, %.
Для нейтрализации кислых вод могут быть использованы: NaOH, КОН, Na2CO3. NH4OH (аммиачная вода), СаСО3. доломит (СаСО3. MgСО3 ) цемент. Однако наиболее дешевым реагентом является гидроксид кальция (известковое молоко) с содержанием активной извести
Са(ОН)2 5÷10 %. Соду и гидроксид натрия следует использовать, если они являются отходами производства. Иногда для нейтрализации применяют различные отходы производства. Например, шлаки сталеплавильного, феррохромового и доменного производств используют для нейтрализации вод, содержащих серную кислоту.
Реагенты выбирают в зависимости от состава и концентрации кислой сточной воды. При этом учитывают, будет ли в процессе образовываться осадок или нет. Различают три вида кислотосодержащих сточных вод: 1) воды, содержащие слабые кислоты (Н2СО3, СН3СООН); 2) воды, содержащие сильные кислоты (НСl, HNO3). Для их нейтрализации может быть использован любой названный выше реагент. Соли этих кислот хорошо растворимы в воде; 3) воды, содержащие серную и сернистую кислоты. Кальциевые соли этих кислот плохо растворимы в воде и выпадают в осадок.
Известь для нейтрализации вводят в сточную воду в виде гидроксида кальция (известкового молока; «мокрое» дозирование) или в виде сухого порошка («сухое» дозирование). Схема установки для нейтрализации кислых вод известковым молоком показана на рис. 1.49.
Для гашения извести используют шаровые мельницы мокрого помола, в которых одновременно происходят тонкое измельчение и гашение. Для смешения сточных вод с известковым молоком применяют гидравлические смесители различных типов: дырчатые, перегородчатые, вихревые, с механическими мешалками или барботажные с расходом воздуха 5-10 м3/ч на 1 м2 свободной поверхности.
Известь
Вода
 3
3
2
 4
4
Сточная
вода
5
1 |
Очищенная |
|
|
|
вода |
Осадок |
6 |
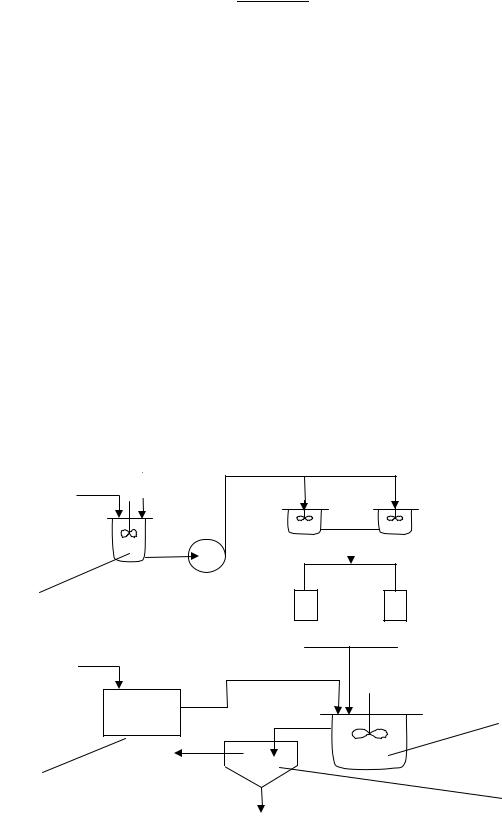
Рис. 1.49. Схема установки нейтрализации кислых вод гидроксидом кальция:
1 – усреднитель; 2 – аппарат для гашения; 3 – растворные баки; 4 – дозаторы; 5 – нейтрализатор; 6 – отстойник
При нейтрализации сточных вод, содержащих серную кислоту, известковым молоком в осадок выпадает гипс CaSO4·2H:2O. Растворимость гипса мало меняется с температурой. При перемещении таких растворов происходит отложение гипса на стенках трубопроводов и их
86
забивка. Для устранения забивки трубопровода необходимо промывать их чистой водой или добавлять в сточные воды специальные умягчители, например гексаметафосфат. Увеличение скорости движения нейтрализованных вод способствует уменьшению отложений гипса на стенках трубопровода.
Для нейтрализации щелочных сточных вод используют различные кислоты или кислые газы. Метод реагентной нейтрализации кислых и щелочных сточных вод широко используется на предприятиях химической промышленности.
Нейтрализация кислых вод фильтрованием через нейтрализующие материалы. В
этом случае для нейтрализации кислых вод проводят фильтрование их через слой магнезита, доломита, известняка, мела, мрамора, твердых отходов (шлак, зола) и др. Процесс ведут в фильтрах-нейтрализаторах, которые могут быть горизонтальными или вертикальными круп-
ность фракций материала загрузки 3÷8 мм. Для вертикальных фильтров используют куски
известняка или доломита размером 30÷80 мм. При высоте слоя материала 0,85÷1,2 м скорость должна быть не более 5 м/с и зависит от вида загрузочного материала, а продолжительность контакта не менее 10 мин. У горизонтальных фильтров скорость течения сточных
вод 1÷3 м/с. Нейтрализация соляно- и азотнокислых, а также сернокислых сточных вод при концентрации серной кислоты не более 1,5 г/л происходит на непрерывно действующих фильтрах.
Применение таких фильтров возможно при условии отсутствия в кислых сточных водах солей металлов, поскольку при рН > 7 они будут выпадать в осадок в виде труднорастворимых соединений, которые полностью забивают поры фильтра. Ограничивается применение нейтрализующих фильтров при подаче на них сернокислых сточных вод с концентрацией серной кислоты более 1,5 г/л. В этом случае количество образующегося сульфата кальция превышает его растворимость ( << 2 г/л) и он начинает выпадать в осадок, который покрывает поверхность нейтрализующей загрузки, затрудняет доступ к ней кислоты, в результате чего нейтрализация прекращается.
Если загрузка выполняется из карбоната магния, это ограничение снимается, поскольку растворимость сульфата магния достаточно высока – 355 г/л (MgSO4·7H2O).
Нейтрализация кислыми газами. Для нейтрализации щелочных сточных вод в последнее время начинают использовать отходящие газы, содержащие СО2, SO2, NO2 и др. Применение кислых газов позволяет не только нейтрализовать сточные воды, но и одновременно производить высокоэффективное очистку самих газов от вредных компонентов.
Использование для нейтрализации щелочных сточных вод диоксида углерода имеет ряд преимуществ по сравнению с применением серной или соляной кислот позволяет резко снизить стоимость процесса нейтрализации. Вследствие плохой растворимости СО2 уменьшается опасность переокисления нейтрализованных растворов. Образующиеся карбонаты находят большее применение по сравнению с сульфатами или хлоридами, кроме того, коррозионные и токсичные воздействия СО3:2– ионов в воде меньше, чем ионов SO42 и С132–.
Процесс нейтрализации может быть проведен в реакторах с мешалкой, в распылительных, пленочных и тарельчатых колоннах.
Дымовые газы вентилятором подают в кольцевое пространство вокруг вала мешалки и распределяют мешалкой в виде пузырьков и струй в сточной воде, поступающей внутрь реактора. Благодаря большой поверхности контакта между водой и газами происходит быстрая нейтрализация сточной воды. Присутствие в газах SO2 способствует нейтрализации щелочных сточных вод.
При проведении процесса в тарельчатых колоннах степень нейтрализации увеличивается с ростом скорости газа и уменьшением плотности орошения.
Количество кислого газа, необходимого для нейтрализации, может быть определено по уравнению массоотдачи
М = К вЖ F ∆C
где М – количество кислого газа, необходимого для нейтрализации; К – фактор ускорения; вЖ – коэффициент массоотдачи в жидкой фазе; F – поверхность контакта фаз; ∆С – движущая
87
