
- •1.4.1. Процеживание
- •1.4.2. Отстаивание
- •4.3. Фильтрование
- •1.5.1.1. Электрокоагуляция
- •Усреднители
- •Песколовки
- •1.5.2. Флотация
- •1.5.2.1. Флотация с выделением воздуха из раствора
- •1.5.2.2. Флотация с механическим диспергированием воздуха
- •Необходимое число флотационных камер определяется из соотношения
- •1.5.2.3. Флотация с подачей воздуха через пористые материалы
- •1.5.2.4. Электрофлотация
- •1.5.2.5. Биологическая и химическая флотация
- •1.5.3. Сорбция
- •1.5.4. Экстракция
- •Таблица 1.3
- •1.5.6. Мембранные процессы
- •Таблица 1.4
- •Расход реагентов для нейтрализации 100 % кислот и щелочей
- •Расход реагентов, требуемых для удаления металлов
- •Реагенты
- •Вода
- •Известь
- •Осадок
- •Рис. 1.50. Нейтрализатор дымовых вод щелочными газами
- •Продукция
- •Производство
- •Асбест
- •Вода
- •В атмосферу
- •Выпуск отработанного воздуха
- •Рис. 1.56. Контактные аппараты для озонирования:
- •Осадок
- •Сточная
- •NaHSO2
- •Азота диоксид (газ)
- •Углерода оксид (газ)
- •Циклогексан (пары)
- •3. Переработка отходов производства и потребления
- •3.2. Способы утилизации промышленных отходов
- •3.3. Отходы потребления
- •3.4. Методы утилизации отходов производства и потребления
- •3.5. Переработка твердых бытовых отходов компостированием
- •СПИСОК ЛИТЕРАТУРЫ
- •Приемный корпус
сферу весьма разнообразен и определяется технологическим процессом производства. В таблице 2.1 приводится состав наиболее значительной части выбросов в атмосферу химического предприятия, аналогичного по технологическому процессу ПО «Азот».
Таблица 2.1
Вещества, выбрасываемые в атмосферу предприятием химической промышленности (ПО «Азот»)
|
|
Выброс |
|
Наименование |
загрязняющих веществ в атмосферу |
||
вещества |
|
|
|
|
г/сек |
|
т/год |
Ванадия пятиокись (аэрозоль) |
0,035 |
|
0,368 |
Сода кальцинированная (пыль) |
41,618 |
|
952,90 |
Известь (аэрозоль) |
0,695 |
|
5,234 |
Азота диоксид (газ) |
59,097 |
|
1296,39 |
Аммиак (газ) |
70,060 |
|
1585,616 |
Аммиачная селитра (аэрозоль) |
32,409 |
|
357,237 |
Серная кислота (аэрозоль) |
0,517 |
|
14,078 |
Сернистый ангидрид (газ) |
33,007 |
|
517,594 |
Пыль серы |
0,011 |
|
0,074 |
Сероводород (газ) |
0,009 |
|
0,262 |
Углерода оксид (газ) |
1942,96 |
|
2442,506 |
Циклогексан (пары) |
38,369 |
|
631,915 |
Бензол (пары) |
3,245 |
|
43,339 |
Циклогексанол (пары) |
4,917 |
|
84,309 |
Циклогексанон (пары) |
6,919 |
|
107,893 |
Карбамид (аэрозоль) |
28,397 |
|
558,760 |
Многочисленные загрязнения атмосферы из различных источников можно объединить в три группы:
1)аэродисперсные системы, состоящие из твердых или жидких дисперсных частиц взвешенных в воздушной среде (пыль, дым, туман);
2)газообразные вещества (SO2 , SO3 , H2S, оксиды азота, оксиды углерода, аммиак и др.);
3)пары веществ (летучие растворители, углеводороды и их галогенопроизводные, ароматические углеводороды и др.).
Аэродисперсные системы Пыль образуется при многих технологических процессах, связанных с измельчение
твердых материалов; состоит из твердых частиц, находящихся в воздухе во взвешенном состоянии. В инженерной практике пылью называют также сами твердые пылевые частицы, в том числе осевшие или выделенные каким-либо способом в виде порошка. Твердые частицы пыли имеют различные размеры, неправильную форму. Размеры частиц пыли характеризуют величиной эффективного диаметра d, который определяется как диаметр сферической частицы того же объема, что и частица пыли. Пыль – полидисперсная система, размеры частиц могут сильно различаться.
В зависимости от размеров, частицы пыли по-разному ведут себя в атмосфере. Частицы диаметра более 75 мкм быстро осаждаются вблизи источника выбросов. Частицы диамет-
ра 5÷75 мкм медленно осаждаются, могут переноситься воздушными массами на относительно большие расстояния от источника выбросов, границы зоны рассеивания зависят от атмосферных условий, а также технических условий выброса в атмосферу (от высоты трубы, температуры, скорости ветра и т.п.). Частицы диаметра менее 5 мкм переносятся с воздуш-
125
ными массами на большие расстояния от источника выбросов, долгое время могут оставаться в атмосфере [6].
Дымом называют аэрозоли, в которых дисперсной фазой являются твердые частицы, а дисперсионной средой – атмосферный воздух. Дымы образуются, например, при плавке металлов и их сварке в результате конденсации паров, при возгонке органических и неорганических веществ. Дым может содержать некоторое количество жидких аэрозольных частиц. Например, при сгорании топлива образуется дым, содержащий как твердые частицы, так и мельчайшие капли воды.
Туманом называют аэрозоли с жидкими частицами дисперсной фазы, взвешенными в дисперсионной среде – атмосферном воздухе. Туманы могут образоваться при конденсации пересыщенных паров жидкостей или при распылении жидкостей, например, при помощи форсунок. Смесь дыма, тумана, паров воды и газообразных загрязняющих веществ в атмосфере принято обозначать термином «смог».
Газообразные вещества и пары
К газообразным загрязняющим веществам относят вещества, которые при температурах и давлениях, обычных для приземного слоя атмосферы, находятся в газообразном состоянии. Основными газообразными загрязнениями являются оксиды серы SO2 , SO3 , сероводород H2S, оксиды азота NO, NO2 , оксиды углерода СО, СO2 , аммиак NH3.
Ватмосфере загрязняющие вещества могут взаимодействовать с кислородом, водой, между собой с образованием опасных для биосферы продуктов. В частности, такое явление, как кислотные дожди (кислотные осадки), обусловлено присутствием в атмосфере главным образом оксидов серы и азота. Болезни и усыхания лесов при воздействии кислотных дождей наблюдались еще в 1841 году в районе промышленного центра Германии – города Рура. Термин «кислотные дожди» впервые применил в 1872 году английский химик Смит, изучавший выбросы промышленных предприятий в районе Манчестера. В настоящее время более широким является термин «кислотные осадки».
Вотсутствие любых загрязнений у дождевой воды обычно слабо кислая реакция (рН=5,6), что обусловлено растворением в ней углекислого газа из воздуха с образованием
слабой угольной кислоты: СO2 + Н2О = Н2СО3
Оксиды серы и азота в загрязненной атмосфере постепенно реагируют с парами воды, образуя кислоты, которые выпадают на поверхность земли в виде кислотных осадков:
4NO2 + O2 + 2Н2О = 4НNO3
2SO2 + O2 = 2SO3 SO3 + Н2О = Н2 SO4
Кислотными называют любые осадки – дожди, туманы, снег, рН которых имеет значение 5,5 и менее. Обычно кислотность осадков на две трети обусловлена серной кислотой и на одну треть – азотной кислотой. Значение рН осадков зависит от количества как кислот, так и воды, в которой они растворены. Туман и роса могут быть более кислыми, чем дождь. В туманах кислоты растворены в относительно небольшом количестве влаги. К кислотным осадкам относят также выпадение из атмосферы сухих кислых частиц. Так кислоты могут адсорбироваться на частицах оседающей пыли. Если такие сухие отложения накапливаются на поверхности растений, то при смачивании небольшим количеством влаги, например при выпадении росы, на загрязненной поверхности образуются сильные кислоты. Потому к кислотным осадкам можно отнести и кислотную росу.
Присутствие в атмосфере аммиака приводит к подщелачиванию осадков вследствие образования слабого основания – гидроксида аммония: NH3 + Н2О = NH4ОН
Продукты реакций, образующиеся при взаимодействия загрязнений в атмосфере (вторичные загрязнения), в результате течения различных биосферных процессов переносятся в другие природные среды, воздействуют на живые организмы, являются часто причиной экологических кризисов. Загрязненный атмосферный воздух является значимым экологическим фактором, оказывающим глубокое влияние на состояние растительных организмов. Иссле-
126
дования разных авторов позволяют расположить некоторые из изученных газообразных загрязнений в следующий ряд по мере увеличения их негативного воздействия на растения:
СО2 < СО < NxOy < SO2 < CI2 < F2.
Газообразные загрязняющие вещества и пары ряда органических веществ при попадании в атмосферу могут вызывать разрушение озонового экрана – тонкого слоя озона, находящегося в стратосфере на высоте около 25 км от поверхности земли. Озоновый экран защищает поверхность земли от воздействия ультрафиолетового излучения. Если бы все ультрафиолетовое излучение, падающее на верхние слои атмосферы, достигало поверхности Земли, то вряд ли на ней сохранилась бы жизнь. К азоноразрушающим загрязнениям относится оксид азота NO:
NO + O2 → NO2 + O
O + O3 → 2 O2
Разрушение озона может также проходить при попадании в атмосферу хлорфторуглеводороды (фреонов), широко используемых в технике и быту.
2.2.Техника защиты окружающей среды от пыли. Принцип действия аппаратов обеспыливания газов (пылеосадительные камеры, циклоны, фильтры, скрубберы)
Аэрозоли воздушных выбросов промышленных предприятий характеризуются большим разнообразием дисперсного состава и других физико-химических свойств. В связи с этим разработаны различные методы очистки и типы пылеуловителей - аппаратов, предназначенных для очистки выбросов от пыли (и других аэрозолей).
Методы очистки промышленных газовых выбросов от пыли можно разделить на две группы: методы улавливания пыли «сухим» способом и методы улавливания пыли «мокрым» способом. Аппараты обеспыливания газов включают: пылеосадительные камеры, циклоны, пористые фильтры, электрофильтры, скрубберы и др.
Сухие механические обеспыливающие аппараты. К таким аппаратам относятся пылеосадительные камеры, циклоны, пористые фильтры. Применение того или иного аппарата обуславливается свойствами и группой дисперсности пыли [6]:
Ι - очень крупнодисперсная пыль, d50 > 140 мкм, ΙΙ- крупнодисперсная пыль, d50 = 40 - 140 мкм,
ΙΙΙ- среднедисперсная пыль, d50 = 10 - 40 мкм, ΙΥ- мелкодисперсная пыль, d50 = 1 - 10 мкм,
Υ- очень мелкодисперсная пыль, d50 < 1 мкм.
d50 - среднее значение эффективного диаметра 50 частиц пыли.
Пылеосадительные камеры и циклоны большой пропускной способности применяют для улавливания пыли первой и второй групп (крупнодисперсной), тканевые фильтры - для улавливания пыли третьей и четвертой групп (средне- и мелкодисперсной), электрофильтры эффективны для улавливания пыли пятой группы (очень мелкодисперсной).
Пылеосадительные камеры. Аппарат этого типа представляет собой пустотелый или с горизонтальными полками во внутренней полости короб, в нижней части которого имеется бункер для сбора пыли (рис. 2.1). Поток запыленного газа вводится в камеру через отверстие сравнительно небольшого диаметра, но при этом газ должен полность заполнять поперечное сечение камеры. Для соблюдения этого условия в конструкции камеры предусматриваются специальные устройства (полки, перегородки). Загрязненный пылью газ 1
пропускается через камеру со скоростью 0,2÷1,5 м/с, частицы пыли оседают под действием силы тяжести в нижней части аппарата. Степень очистки газа в камерах не превышает
40÷50%. Обеспыленный газ 2 выводится из камеры и далее либо выбрасывается в атмосферу, либо подается в другие аппараты для более глубокой очистки.
127

1 |
2 |
Пыль |
Пыль |
Рис. 2.1 Пылеосадительная камера
Циклоны различных типов получили широкое применение для сухой очистки газов. Это механические обеспыливающие устройства, в которых очистка газа основана на ис-
пользовании инерционных свойств частиц пыли. Циклоны являются наиболее характер-
ными представителями сухих инерционных пылеуловителей. Они, как правило, имеют простую конструкцию, обладают большой пропускной способностью и несложны в эксплуатации. Общая схема одной из конструкций циклона представлена на рис. 2.3. Запыленный воздух вводится тангенциально в верхнюю часть циклона. Здесь формируется вращающийся поток, который затем опускается по кольцевому пространству, образованному цилиндрической частью циклона и выхлопной трубой. Продолжая вращаться, воздушный поток выходит из циклона через выхлопную трубу. Отделение загрязнений происходит следующим образом. При входе в циклон частицы дисперсной фазы по инерции движутся прямолинейно. Затем центробежные силы искривляют траекторию их движения. Те из частиц, масса которых достаточно велика, достигают стенок циклона, под действием силы тяжести опускаются в нижнюю часть аппарата, далее через пылевыпускное отверстие проходят в бункер, где и оседают.
Очищенный газ
патрубок для ввода  загрязненного газа
загрязненного газа
корпус
циклона
бункер для пыли
пыль
Рис. 2.3. Циклон
Для очистки больших объемов воздуха циклоны могут компоноваться в группы, объединенные общим пылесборником и коллектором очищенного воздуха.
Фильтры с пористыми перегородками различных типов широко используют для очистки загрязненных газовых выбросов. Процесс фильтрования состоит в пропускании аэро-
128

дисперсной системы (газа, загрязненного пылью или частицами аэрозолей) через пористый материал фильтра. Частицы дисперсной фазы, размеры которых превышают диаметр пор фильтровального материала, отделяются от газового потока. В промышленности используются фильтры различных конструкций с различными фильтрующими элементами. По типу фильтрующей перегородки фильтры бывают:
1)с зернистыми неподвижными слоями, состоящими из свободно насыпанных зернистых материалов;
2)с зернистыми псевдоожиженными слоями;
3)с гибкими пористыми перегородками из ткани, войлока, полимерных материалов, губчатой резины и т.п.;
4)с полужесткими пористыми перегородками из вязаной и тканой сетки, стружки;
5)с жесткими пористыми перегородками из пористой керамики, пористых металлов и других подобных материалов.
Фильтрующие зернистые слои используют для очистки газов от крупнодисперсных частиц загрязнений. Для очистки газов от пылей механического происхождения (от дробилок, сушилок, мельниц) часто используют фильтры из гравия.
Для тонкой очистки газов от аэрозолей и мелкодисперсной пыли применяют войлоки из синтетических волокон (лавсана, ПВХ, капрона). Хорошими фильтрующими свойствами обладают хлопчатобумажные и шерстяные ткани, но они менее прочны и химически стойки, чем синтетические. Проволочные сетки, изготовленные из специальных марок сталей, меди,
латуни, бронзы, никеля могут работать в широком интервале температур (0ОС÷800ОС), в химически агрессивных средах. Фильтрующие элементы из пористой керамики, пористых металлов обладают высокой прочностью, коррозионной и термостойкостью.
Загрязненный |
очищенный |
газ |
газ |
фильтрующая пористая перегородка
Рис. 2.4. Схема фильтра с пористым фильтрующим элементом
Конструкционное оформление газовых фильтров может быть различным. Наибольшее распространение получили рукавные фильтры. Поток загрязненного газа проходит через фильтрующие тканевые рукава, пыль задерживается на внутренней поверхности рукавов. Отделение пыли и регенерация фильтров может проводиться одним из следующих методов: механическим встряхиванием, обратной продувкой воздухом, импульсной продувкой сжатым воздухом. Главным достоинством рукавных фильтров является высокая эффективность очистки для всех размеров частиц.
Электрофильтры. В основе работы электрофильтра лежит явление электризации взвешенных в газе частиц дисперсной фазы с последующим осаждением их на электроде с зарядом, противоположным по знаку заряду частиц загрязнений (осадительном электроде). По конструкции электрофильтры подразделяют на трубчатые и пластинчатые. В трубчатых
электрофильтрах загрязненный газ пропускается по вертикальным трубам диаметром 20÷25 см, по центру которых натянута проволока. Скорость движения газа в трубке составляет
0,5÷2 м/с. Газ находится в трубке 6÷8 с. Постоянный ток напряжением 50 – 100 кВ подается на электроды. Электродами являются стенки трубки (осадительный электрод) и проволока (каронирующий электрод).
В пластинчатых электрофильтрах осадительными электродами являются пластинки, между которыми натянута проволока – коронирующий электрод. Для увеличения степени
129
очистки электроды могут смачивать водой. В таком случае электрофильтр будет относиться к мокрым.
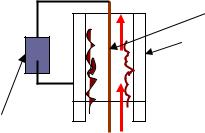
Процесс очистки газа от частиц пыли происходит следующим образом. Молекулы газов воздуха, проходящего в пространстве между двумя электродами (рис. 2.5), при определенной напряженности электрического поля между электродами ионизируются. Образующиеся ионы движутся к соответствующему электроду (стенке трубки), сталкиваются при движении с частицами пыли (или жидкими частицами аэрозоля), передают им свой заряд – ионизируют частицы. Далее заряженные частицы пыли движутся к электроду с противоположным по знаку зарядом (к стенке трубки), осаждаются на поверхности этого электрода. Очищенный газ выводится из трубки. Накапливающийся на поверхности осадительного электрода слой пыли периодически удаляют сухим (вибрация) или мокрым (отмывка) способом. Пыль собирается в бункера в виде сухого порошка или в виде пульпы (взвеси) в нижней части аппарата. Электрофильтры применяют для тонкой очистки газов от частиц аэрозолей. Выбор той или иной конструкции электрофильтра определяется условиями работы: составом и свойствами очищаемых газов, требуемой эффективностью очистки.
очищенный газ
1
2
(+)
3
(-)
загрязненный газ
Рис. 2.5. Схема элемента трубчатого электрофильтра:
1 – коронирующий электрод; 2 – осадительный электрод; 3 – выпрямитель
Мокрые пылеулавливающие аппараты работают по принципу улавливания частиц пыли поверхностью или объемом жидкости (воды). Эти аппараты характеризуются высокой степенью очистки от мелкодисперсной пыли. С их помощью можно очищать от пыли горячие и взрывоопасные газы. Эффективность работы аппаратов мокрой очистки зависит от смачиваемости пыли, площади соприкосновения запыленного потока газа с поверхность жидкости. Если пыль плохо смачивается водой, то в воду добавляют поверхностно активные вещества (ПАВ). Для увеличения поверхности контакта в аппараты мокрой очистки вводят специальные насадки из материалов инертных по отношению к воде и загрязнениям (в промывных башнях) или воду распыляют при помощи форсунок (форсуночные скрубберы).
На рис. 2.6 приведены схемы двух аппаратов мокрой очистки – промывной башни (а) и форсуночного скруббера (б). Промывная башня является простейшим аппаратом мокрой очистки газов от пыли. Она представляет собой колонну, заполненную кольцами Рашига или каким-либо другим инертным материалом.
Промывную воду и запыленный газовый поток подаются в колонну противотоком. По мере продвижения газового потока снизу вверх колонны пыль захватывается водной поверхностью, вода загрязняется твердыми частицами, растворимыми веществами и в виде шлама выводится из нижней части колонны.
В форсуночных скрубберах запыленный газовый поток подается через патрубок в нижней части скруббера и направляется на зеркало воды, где отделяются наиболее крупные частицы пыли. Далее газовый поток, содержащий мелкодисперсную пыль, распределяется по всему сечению аппарата, поднимается вверх навстречу потоку капель воды, подаваемых через форсуночные пояса. По мере продвижения газового потока снизу вверх аппарата пыль захватывается каплями воды, опускается в нижнюю часть аппарата и выводится в виде шла-
130
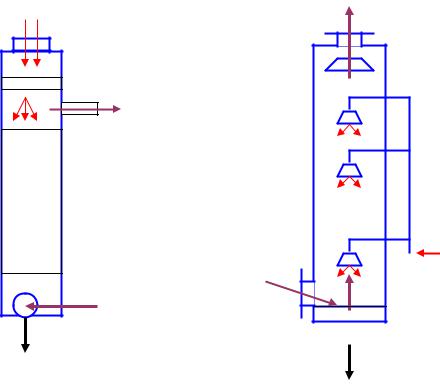
ма.
К недостаткам мокрых пылеулавливающих аппаратов относятся: образование шлама, требующего дополнительных специальных систем для его переработки; вынос в атмосферу водяных паров; повышенная коррозия аппаратов и газоходов; ухудшение условий рассеивания загрязнений через заводские трубы.
а) |
б) |
2 |
|
Вода |
|
|
2 |
|
вода
1
1
шлам 
 шлам
шлам
Рис. 2.6. Схема аппаратов мокрой очистки газов
2.3.Техника защиты окружающей природной среды от техногенных газообразных и парообразных загрязнений. Общая характеристика методов, процессов и аппаратов
Промышленные газовые выбросы могут содержать токсичные для биоты неорганические и органические вещества. Среди них наиболее опасны для биоты оксиды серы, азота, углерода (СО), аммиак, хлористый водород, фтористый водород, хлор, пары летучих органических соединений: ацетона, бензола, толуола, ксилола, фенола, метилэтилкетона, низших спиртов, гептана, сероуглерода, эфиров, галогенуглеводородов (фтор- и хлорпроизводных),
бензина. Общим для всех загрязнений данной группы является то, что при обычных
атмосферных условиях (давление, температура) эти вещества находятся в газообразном состоянии в потоке очищаемого газа. Эти загрязнения отличаются по растворимости в воде и другим физико-химическим и химическим свойствам, что используется при выборе метода очистки.
В зависимости от типа процесса, методы очистки промышленных газовых выбросов от газообразных загрязнений и паров подразделяются на пять основных групп (таблица 2.2), каждой из которых соответствуют определенные аппараты:
Таблица 2 Методы очистки промышленных газовых выбросов от газообразных и парообразных
загрязнений
Методы очистки |
тип процесса |
аппараты |
131
абсорбционные |
поглощение загрязнений растворителем |
насадочные |
башни; |
|||
|
(водой) с образованием раствора |
скрубберы; |
|
|
||
|
|
|
барботажно-пенные |
|
||
|
|
|
аппараты и др. |
|
||
хемосорбционные |
химическое взаимодействие загрязнений |
насадочные |
башни; |
|||
|
с жидкими сорбентами (поглотителями) |
скрубберы; |
распыли- |
|||
|
с образованием малолетучих или мало- |
тельные |
аппараты |
и |
||
|
растворимых химических соединений |
др. |
|
|
|
|
адсорбционные |
адсорбция загрязнений |
на поверхности |
адсорберы |
|
|
|
|
твердого вещества |
|
|
|
|
|
термические |
окисление загрязнений кислородом воз- |
камеры |
сжигания |
и |
||
|
духа при высоких температурах с обра- |
др. |
|
|
|
|
|
зованием нетоксичных (менее токсич- |
|
|
|
|
|
|
ных) соединений |
|
|
|
|
|
каталитические |
каталитическая химическая реакция за- |
каталитические |
и |
|||
|
грязнений с другими загрязнениями или |
термокаталитические |
||||
|
добавленными веществами с образова- |
реакторы |
|
|
|
|
|
нием нетоксичных (менее токсичных) |
|
|
|
|
|
|
соединений |
|
|
|
|
|
биохимические |
трансформация загрязнений под воздей- |
биофильтры; |
био- |
|||
|
ствием ферментов, |
вырабатываемых |
скрубберы |
|
|
|
|
микроорганизмами |
|
|
|
|
|
Абсорбционные методы основаны на различиях в растворимости веществ в определенных растворителях. При контакте загрязненного газового потока с жидким растворителем пары определенных загрязнений поглощаются растворителем – абсорбентом с образованием раствора. Наиболее дешевым и доступным в промышленных условиях растворителем является вода. Процесс поглощения таких загрязнений растворителем (водой) проводится одним из следующих способов. Загрязненный газовый поток:
а) пропускается через насадочную колонну, орошаемую растворителем (водой); б) контактирует с каплями жидкости, распыляемой форсунками; в) барботируется через слой жидкости.
Чистый растворитель вводится в верхнюю часть аппаратов абсорбционной очистки, а из нижней части аппаратов отбирают отработанный раствор. Очищенный газ из верхней части аппаратов выводится в атмосферу. Полученный раствор подвергают обычно регенерации, т.е. очищают от загрязнений и снова возвращают в аппарат. Концентрат загрязняющих веществ используют в качестве ВМР – вторичного материального ресурса или отхода. Таким образом, в атмосферу загрязнения не поступают, но могут загрязнять почву в виде твердых отходов или поступать в водоемы в составе сточной воды, если не применяются в производственном процессе малоотходные или безотходные технологии.
Хемосорбционные методы основаны на химическом взаимодействии газообразных или парообразных загрязнений с твердыми или жидкими поглотителями с образованием малолетучих или малорастворимых химических соединений. Используемые в методе реакции, как правило, обратимы. Потому при определенных условиях возможно смещение равновесия в сторону обратной реакции, т.е. десорбция поглощаемого вещества, регенерация хемосорбента. Аппараты хемосорбционной очистки похожи на аппараты абсорбционной очистки.
Общим недостатком этих аппаратов является образование большого количества отходов.
Адсорбционные методы основаны на явлении избирательной адсорбции (поглощения и концентрирования) загрязнений на поверхности твердых тел. В адсорбционных методах очистки используются сорбенты, имеющие пористую структуру и, как следствие, большую удельную поверхность. Например, удельная поверхность единицы массы активирован-
132
ного угля достигает 106 м2/кг. Такие сорбенты применяют для очистки газов от паров органических растворителей, удаления неприятных запахов и др. Основными промышленными сорбентами являются активированный уголь, активированный глинозем, силикагель, синтетические цеолиты. При выборе адсорбента основное внимание уделяется его селективности и адсорбционной способности по отношению к извлекаемому компоненту.
Аппараты для адсорбционной очистки газов представляют собой вертикальные , горизонтальные или кольцевые емкости, заполненные пористым адсорбентом, через слой которого пропускается поток очищаемого газа. За время контакта загрязнения задерживаются поверхностью адсорбента, а из аппарата выводится газ, который может содержать инертные примеси, не взаимодействующие с адсорбентом или незначительно им поглощаемые. Регенерацию адсорбента проводят продувкой нагретым водяным паром.
Термическая нейтрализация загрязненных газовых выбросов основана на окислении загрязнений кислородом воздуха при высоких температурах до менее токсичных соединений. Метод применим для очистки газовых выбросов, содержащих пары органических соединений, но не содержащих таких загрязнений, как галогены, сера, фосфор и их соединения. Ограничение обусловлено тем, что при горении указанных соединений образуются, как правило, продукты, превышающие по токсичности исходные загрязнения.
Процесс очистки может проводиться: прямым сжиганием загрязнений в пламени с температурой 600÷800ОС в присутствии катализаторов или без них, окислением при темпе-
ратурах 250÷450ОС. Прямое сжигание (факел) применяют для горючих газообразных отходов технологического процесса. Например, если отходящие газы содержат водород, летучие углеводороды, метан в больших концентрациях и температура их достаточна для горения, то такая газовая смесь будет гореть. В пламени проходит окисление других примесей.
Термическое окисление при более низких температурах проводят в тех случаях, когда концентрация горючих примесей мала и они не обеспечивают требуемой высокой температуры газового потока, или в газовой смеси недостаточно кислорода для горения.
Каталитическое окисление проводят для того, чтобы получить менее токсичные продукты горения за счет образования определенных промежуточных соединений веществ газовой смеси с катализатором. В очищаемый газ при необходимости могут вводиться дополнительные вещества, участвующие в каталитической реакции с веществами-загрязнениями с образованием менее токсичных промежуточных продуктов. В промышленности в качестве катализаторов чаще применяются химически инертные металлы: платина, палладий. Процесс проводится в каталитических и термокаталитических реакторах.
Биохимические методы очистки газовых выбросов от загрязнений – это по существу также каталитические методы, но отличающиеся тем, что катализаторы процессов превращения загрязняющих веществ в менее токсичные «поставляются» живыми микроорганизмами. Следовательно, для успешной реализации этих методов необходимо обеспечить такие условия, при которых возможна жизнедеятельность микроорганизмов. Процесс может проводиться в биофильтрах и биоскрубберах. Принципиальное отличие биофильтров от аналогичного типа аппаратов других методов газоочистки заключается в том, что фильтрующим
элементом является почва, торф или другой – материал, на поверхности и в объеме создаются условия для поддержания жизнедеятельности сообщества микроорганизмов.
Основное отличие биоскрубберов состоит в том, что поток газа контактирует не с каплями жидкости, а с каплями суспензии активного ила. Биохимический метод пока широкого применения не находит из-за сложности обеспечения стабильной жизнедеятельности сообщества микроорганизмов. Но по своей сущности это наиболее экологичный метод очистки, обеспечивающий при должном подборе видов микроорганизмов наиболее эффективную очистку по отношению к биоте.
2.4.Очистка промышленных выбросов от оксидов углерода, азота, серы (сорбционные методы, реагентные методы)
2.4.1. Очистка газов от оксидов углерода СО2 и СО
133
Оксиды углерода СО2 и СО в воздухе присутствуют в газообразном состоянии. Продолжительность их пребывания в приземном слое атмосферы определяется свойствами оксидов и параметрами среды (температура, давление, влажность и т.п.). Оксид углерода СО2 значительно легче, чем СО, выводится из атмосферы в процессе ее самоочищения. Оксид углерода СО чрезвычайно токсичен, переносится на большие расстояния от источников выброса, долго может находиться в неизменном виде в приземном слое атмосферы. Очистка промышленных газов от СО2 и СО основана на их физических и химических свойствах (табл.
2.3).
Оксид углерода (ΙΥ) – это бесцветный газ со слегка кисловатым запахом и вкусом. В воде СО2 растворим довольно хорошо (приблизительно 1:1 по объему). По химической природе это кислотный оксид, взаимодействующий с водой при растворении в ней, основаниями (щелочами), основными оксидами. При растворении СО2 в воде образуется слабая угольная кислота:
Н2О + СО2 = Н2 СО3 .
Н2О + СО2 = Н2 СО3 = Н+ + НСО3¯ = 2 Н+ + СО3 2 ¯
При нагревании СО2 улетучивается и равновесия смещаются влево. При добавлении щелочи или щелочных реагентов равновесия смещаются вправо. Образующиеся карбонаты и гидрокарбонаты имеют различную растворимость в воде, не токсичны.
Оксид углерода (ΙΙ) – бесцветный газ, не имеющий запаха и вкуса, плохо растворим в воде. Газ сильно токсичен, его ПДК в воздухе населенных мест 1 мг/м3. Основная опасность СО для животных и человека обусловлена его способностью связываться с гемоглобином крови легче, чем кислород. Большая токсичность СО обусловливает необходимость тщательной очистки от него промышленных газов, выбрасываемых в атмосферу. При очистке загрязненных газов от СО используются следующие его свойства: возможность окисления СО до СО2; способность СО вступать в реакции комплексообразования.
Таблица 3
Методы очистки газов от оксидов углерода
метод |
основные процессы метода |
Абсорбция СО2 водой |
абсорбция: |
|
СО2 + Н2О = Н2СО3 |
|
регенерация сорбента: |
|
Н2СО3 = Н2О + СО2 |
Абсорбция СО2 этанола- |
абсорбция: |
мином |
(RNH3)2 СО3 + СО2 + Н2О = 2 (RNH3)НСО3 |
|
регенерация сорбента: |
|
2 (RNH3)НСО3 = (RNH3)2 СО3 + СО2 + Н2О |
Метанирование СО и СО2 |
СО + 3 Н2 = СН4 + Н2О |
|
СО2 + 4 Н2 = СН4 + 2 Н2О |
|
(катализатор на основе оксидов NiO, Al2O3) |
Абсорбция медноаммиач- |
абсорбция: |
ным раствором СО и СО2 |
[Cu(NH3)2]+ + CO + NH3 = [ Cu(NH3)3CO]+ |
|
регенерация сорбента: |
|
[Cu(NH3)3CO]+ = [ Cu(NH3)2]+ + CO + NH3 |
|
NH3 + Н2О = NH4OH |
|
2NH4OH + СО2 = (NH4)2 CO3 + Н2О |
|
(NH4)2 CO3 + СО2 + Н2О = 2NH4HCO3 |
Конверсия СО с водяным |
СО + Н2О = СО2 + Н2 |
|
134 |
паром |
(катализатор на основе оксидов железа) |
Абсорбция СО2 водой - один из простейших методов очистки газообразных выбро-
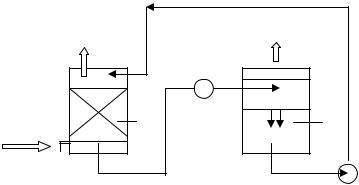
сов от оксида углерода (ΙΥ) (рис. 2.7). Максимальная поглотительная способность воды 8 кг СО2 на 100 кг воды. Очищенный газ выводится в атмосферу. Раствор СО2 в воде перекачивается в дегазатор, где СО2 выделяется из раствора и выводится из аппарата для дальнейшего использования или химической переработки. Вода из дегазатора подается в поглотительную колонну для использования в следующем аналогичном цикле.
|
Н2О |
|
газ |
|
СО2 |
|
|
2 |
газ+ СО2 |
1 |
3 |
2
Н2О + СО2 |
Н2О |
Рис. 2.7. Схема абсорбционной очистки газов от СО2:
1 – колонна высокого давления; 2 – устройства для перекачки жидкостей (вода, раствор); 3 – дегазатор
Основные преимущества данного метода заключаются в следующем: отсутствие токсичных отходов, выбрасываемых в природные среды; экономичность; доступность растворителя – воды, относительная простота технологического процесса и применяемых аппаратов. К существенным недостаткам метода относится небольшая поглотительная емкость воды по СО2, недостаточная чистота выделяемого СО2.
Абсорбция СО2 этаноламинами обладает рядом преимуществ по сравнению с абсорбцией СО2 водой и является наиболее распространенным методом очистки промышленных газообразных выбросов от этого компонента. Большая по сравнению с водой эффективность этаноламинов обусловлена, прежде всего, наличием щелочных свойств у моно-, ди- и триэтаноламинов (МЭА, ДЭА, ТЭА). Как следствие, данные растворители способны эффективно поглощать из загрязненных газовых сред не только СО2 , но и другие загрязнения, обладающие кислотными свойствами, например, сероводород. Моноэтаноламин хорошо по-
глощает также оксид углерода (ΙΙ).
2 RNH2 + 2 Н+ + СО3 2 ¯ = (RNH3 )2 СО3 (RNH3 )2 СО3 + СО2 + Н2О = 2 (RNH3 )НСО3 2 RNH2 + Н2S = (RNH3 )2 S
(RNH3 )2 S + Н2S = 2 (RNH3 )HS
где RNH2 − моноэтаноламин (МЭА, R – этил С2Н5 ); R2NH − диэтаноламин (ДЭА); R3N − триэтаноламин (ТЭА).
В промышленности чаще применяют моноэтаноламин как абсорбент, эффективный по отношению к нескольким компонентам, недорогой, легко поддающийся регенерации. Технологическая схема процесса обычная для абсорбционных процессов.
Метанирование СО и СО2 применяется для очистки газов, содержащих небольшие остаточные количества СО. Очистка газов основана на экзотермической реакции гидрирования СО в присутствии катализаторов. Одновременно из очищаемого газа удаляется СО2 и
135
кислород. Образующийся метан может далее сжигаться, если не используется в технологическом процессе.
Абсорбция СО и СО2 медноаммиачным раствором используется для глубокой очи-
стки газов от СО. Процесс основан на способности комплексного медно-аммиачного соединения поглощать СО под высоким давлением с образованием соответствующего комплексного соединения [Cu(NH3)3CO]+. При нагревании последнего СО легко удаляется, что объясняет возможность легкой регенерации поглотительного раствора. Улавливаемы оксид углерода СО следует далее на другие ступени очистки (например, на окисление до СО2). Процесс абсорбции проводят при высоком давлении и температуре, близкой к 0ОС. Десорбцию СО
проводят при атмосферном давлении и температуре ≈ 80ОС. Технологическая схема процесса обычная для абсорбционных процессов.
Конверсия СО с водяным паром. Окисление СО до СО2 в промышленных условиях проводится с использованием различных реагентов, но наиболее распространенными реагентами являются водяной пар и метан. Конверсия СО с водяным паром проводится в присутствии железных окисных катализаторов (Fe2O3 + Cr2O3), реакция СО + Н2О = СО2 + Н2 экзотермична.
2.4.2. Очистка газов от сероводорода
Сероводород – бесцветный газ с характерным запахом, хорошо растворим в воде. Один объем воды растворяет в обычных условиях около 3 объемов сероводорода. В водном растворе сероводород ведет себя как слабая кислота, она несколько слабее угольной кислоты. При нагревании растворимость сероводорода в воде понижается.
Сероводород сильно токсичен. При концентрации сероводорода в воздухе 0,004 мг/л ощущается сильный запах. При более высоких концентрациях этого газа в воздухе возможны сильные отравления у людей, вплоть до летальных исходов из-за остановки дыхания. Предельно допустимая концентрация (ПДК) сероводорода в воздухе рабочей зоны составляет 10 мг/м3, а в присутствии углеводородов – 3 мг/м3. Максимальная разовая и среднесуточная ПДК в атмосферном воздухе населенных пунктов равна 0,008 мг/м3
Методы очистки газовых выбросов от сероводорода основаны таких его свойствах, как хорошая растворимость в воде с образованием слабой кислоты, способности окисляться с образованием различных продуктов (табл. 2.4). Сероводород может гореть на воздухе с образованием серы или оксида серы в зависимости от условий проведения процесса:
2Н2S + 3 О2 = 2 Н2О + 2 S О2 (в избытке кислорода)
2Н2S + О2 = 2 Н2О + 2 S (при недостатке кислорода)
Очистка промышленных газовых выбросов от сероводорода может проводиться как мокрым, так и сухим способами. В мокрых методах очистки содержащие сероводород газы контактируют с поглотительными растворами, в состав которых входят компонеты, способные химически взаимодействовать с сероводородом. В сухих способах очистки газов от сероводорода используются сорбенты различной природы. Поглощение сероводорода происходит в результате течения обратимых химических реакций и процессов сорбции – десорбции.
Таблица 2.4
Методы очистки газов от сероводорода
метод |
|
основные процессы метода |
Мышьяково-содовый |
метод |
абсорбция: |
очистки газов от Н2S |
|
Na4As2S5O2 + H2S = Na4As2S6O + H2O |
|
|
регенерация сорбента: |
136

|
Na4As2S6O + ½ O2 = Na4As2S5O2 + S |
|
Фосфатный метод очистки га- |
Н2S + К3РО4 = К2НРО4 + КНS |
|
зов от Н2S |
|
|
Железо-содовый метод очист- |
абсорбция: |
|
ки газов от Н2S |
Н2S + Na2CO3 = NaНS + NaНCO3 |
|
|
3NaНS + 2Fe(OH)3 = Fe2S3 + 3 NaОН + 3Н2О |
|
|
3NaНS+2Fe(OH)3 =2 FeS + S + 3NaОН+3Н2О |
|
|
регенерация сорбента: |
|
|
2 Fe2S3 + 6 Н2О + 3 О2 = 4 Fe(OH)3 |
+ 6 S |
|
4 FeS + 6 Н2О + 3 О2 = 4 Fe(OH)3 |
+ 4S |
Адсорбция Н2S цеолитами. |
адсорбция: |
|
|
Н2S + NaA → Н2S(NaA) |
|
|
регенерация сорбента: |
|
|
Н2S(NaA) → Н2S + NaA |
|
Адсорбция Н2S активирован- |
адсорбция: |
|
ным углем |
Н2S + (уголь) + О2 |
|
|
каталитическое окисление: |
|
|
2 Н2S + О2 = 2 Н2О + 2 S |
|
Мышьяково-содовый метод очистки газов от Н2S основан на хемосорбции серово-
дорода тиоарсенатом натрия. Химизм процесса сложен, результирующие реакции могут быть представлены в виде следующих схем:
Na−S |
|
|
S−Na |
Na−S |
S−Na |
|
|
As−S−As |
+ Н2S → |
As−S−As |
+ Н2О |
||
Na−S |
|| |
|| |
S−Na |
Na−S || |
|| S−Na |
|
|
O |
O |
|
O |
S |
|
|
Раствор А |
|
Раствор Б |
|
||
Na−S |
|
S−Na |
Na−S |
|
S−Na |
|
|
As−S−As |
+ ½ O2 → |
As−S−As |
+ S |
||
Na−S |
|| |
|| |
S−Na |
Na−S || |
|| |
S−Na |
|
O |
S |
|
O |
O |
|
Абсорбцию и регенерацию сероводорода проводят при температуре 40÷45ОС в скрубберах различной конструкции. Абсорбцию и регенерацию сероводорода проводят при тем-
пературах 40÷45ОС.
К достоинствам метода относится селективность очистки по отношению к сероводороду, высокая эффективность очистки: степень выделения сероводорода достигает 98%.
Фосфатный метод очистки газов от Н2S основан на хемосорбции сероводорода раствором фосфата калия. Данный метод очистки газов от сероводорода обладает определенными преимуществами по сравнению с мышьяково-содовым методом: нелетучесть фосфата калия позволяет проводить процесс при более высоких температурах, используемый поглотительный раствор позволяет селективно выделять сероводород из загрязненных газов, где его концентрация относительно высока и присутствует в значительных количествах СО2. Фосфат калия может взаимодействовать с очищаемым газом с выделением в аппаратах очистки нерастворимых карбонатов, потому при повышенном содержании в промышленных газах СО2 процесс проводят с использованием 35% раствора фосфата калия. Степень очистки газов от сероводорода в фосфатном методе несколько ниже, чем в мышьяково-содовым, остаточное содержание сероводорода около 1,5 г/м3.
137
Железо-содовый процесс очистки газов от Н2S проводится на ряде химических предприятий. В основе метода лежит процесс поглощения сероводорода суспензией гидроксида железа Fe(OH)3 в растворе соды Na2CO3 в щелочной среде (рН 8,5 – 9,0).
При регенерации поглотительного раствора сульфиды железа окисляются кислородом воздуха с выделением элементарной серы, которая представляет собой товарный продукт.
Очистка газов от Н2S цеолитами. Цеолиты NaA, CaA являются эффективными сорбентами, отличающимися высокой адсорбционной способностью и селективностью по отношению к сероводороду. Процесс можно проводить в присутствии СО2, который хоть и сорбируется вместе с сероводородом, но значительно легче десорбируется. На начальной стадии очистки из загрязненного газа извлекаются как сероводород, так и СО2. Затем сероводород вытесняет из сорбента СО2 и содержание последнего в выходящем из адсорбера газе начинает возрастать. Процесс может быть остановлен при любом экономически и технологически оправданном содержании СО2 в очищаемой газовой смеси. Наилучшими эксплуатационными свойствами обладают цеолиты типа СаА.
Очистка газов от Н2S активированным углем состоит в адсорбции сероводорода на поверхности угля и последующем окислении Н2S кислородом воздуха до элементарной серы. Активированный уголь одновременно является адсорбентом и катализатором окисления сероводорода. Каталитические свойства сорбента усиливают путем нанесения на его поверхность других веществ - катализаторов окисления сероводорода, например, иода, иодистого калия. Образующаяся на поверхности и в объеме пор сорбента элементарная сера снижает его активность, поэтому периодически проводят регенерацию угля. Для этого серу вымывают из сорбента специальным растворителем. Далее промытый уголь очищают от растворителя, сушат. При этом возникает проблема рекуперации растворителя, а также проблема очистки газовых выбросов от паров растворителя. Процесс поглощения сероводорода активированным углем не находит широкого применения еще и потому, что в аппаратах очистки возможно протекание сильно экзотермичной реакции окисления сероводорода до серной кислоты, что может быть причиной возгорания угля.
Поглощение и химическое превращение сероводорода в элементарную серу используется в процессах очистки промышленных газов от органических сернистых соединений.
2.4.3. Очистка газов от оксида серы (IΥ)
Сернистый газ – одно из основных загрязнений атмосферного воздуха, оказывающее сильное негативное воздействие на живые организмы. В обычных условиях это бесцветный газ с резким характерным запахом. В атмосфере он постепенно окисляется до серного ангидрида, а последний при взаимодействии с водой образует серную кислоту. Из атмосферы сернистый газ и продукты его химических превращений вымываются с осадками, поступая в водоемы, почву. Время пребывания сернистого газа в атмосфере зависит от многих факторов
и составляет от нескольких часов до 4÷5 суток. Предельно допустимая концентрация этого вещества в воздухе (среднесуточная) составляет 0,005 мг/м3.
Сернистый газ – кислотный оксид, способы улавливания SO2 из загрязненных промышленных газов основаны на способности его взаимодействовать с водой, основными оксидами, некоторыми солями (табл. 2.5).
Таблица 2.5
Методы очистки газов от SO2
метод |
основные процессы метода |
|
Известковый метод очист- |
SO2 |
+ CaCO3 = CaSO3 + CO2 |
ки газов от SO2 |
SO2 + CaO = CaSO3 |
|
|
SO2 |
+ Ca(OH)2 = CaSO3 + H2O |
|
2CaSO3 + O2 = 2 CaSO4 |
|
Аммиачный метод очистки |
SO2 |
+ (NH4)2SO3 + H2O = 2 NH4HSO3 |
138

газов от SO2 |
|
Поглощение SO2 углерод- |
(SO2 + H2O + О2) → уголь |
ными пористыми сорбен- |
SO2 + H2O = H2 SO3 |
тами |
H2 SO3 + ½ O2 = H2 SO4 |
Известковый метод очистки газов от SO2. Это один из наиболее простых в техническом отношении методов. Однако в процессе очистки образуются твердые отходы, которые не находят практического применения, сбрасываются в отвалы. Поэтому метод применим только при небольших содержаниях SO2 в очищаемом газе. Метод основан на необратимом химическом взаимодействии сернистого газа с известняком (известью или мелом), в результате чего образуется сульфит кальция, который на воздухе окисляется до сульфата кальция.
Аммиачный метод очистки газов от SO2 имеет несколько вариантов, отличающихся условиями проведения процесса. Однако во всех вариантах этого метода первая стадия одинакова - это поглощение сернистого газа водным раствором сульфита аммония с образованием гидросульфита аммония. Далее варианты метода отличатся по направлениям переработки гидросульфита аммония. Наибольший интерес с точки зрения эколога представляют те методы, в которых происходит превращение SO2 в какой-либо продукт, используемый в других производствах или в сфере потребления. При таком подходе более интересен аммиачноавтоклавный метод. Здесь на второй стадии процесса гидросульфит амония разлагается в автоклаве при повышенных температурах и давлениях с получением в качестве товарных продуктов серы и сульфата аммония: 2 NH4HSO3 + (NH4)2SO3 = 2(NH4)2SO4 + S + H2O
Поглощение SO2 углеродными пористыми сорбентами является одним из наиболее перспективных методов. При контакте содержащего SO2 газа с пористым сорбентом вначале происходит сорбция SO2 и других компонент загрязненного газа на активной поверхности сорбента. Далее в результате взаимодействия сорбированных веществ между собой образуются вещества, представляющие собой товарные продукты. Так образование серной кислоты может быть представлено следующей схемой:
SO2 H2O О2 |
SO2 + H2O = H2 SO3 |
|
|
|
H2 SO3 + ½ O2 = H2 SO4 |
|
|
|
2.4.4. Очистка газов от оксидов азота
Оксиды азота, как и сернистый газ, являются одним из основных загрязнений атмосферы. Наиболее устойчив в атмосфере оксид азота (IY). Предельно допустимая концентрация установлена для всех оксидов азота в пересчете на NO2 и составляет 0,085 мг/м3 в воздухе населенных пунктов. Источниками загрязнения атмосферы оксидами азота являются процессы сжигания топлива, а также производства азотной кислоты, минеральных удобрений.
Наиболее экологичным способом очистки промышленных газовых выбросов от оксидов азота является каталитическое восстановление их до молекулярного азота.
При этом в качестве восстановителей могут использоваться СО, Н2, СН4, NН3, различные газовые смеси. Катализаторы – металлы подгруппы платины на различных носителях.
В различных процессах могут образоваться выхлопные газы с различным содержанием оксидов азота. Если содержание их мало, то применяются относительно простые системы очистки. Например, в производстве разбавленной азотной кислоты образуются выхлопные
газы с содержанием оксидов азота 0,2÷0,25%, кислорода - до 3 %, паров воды - до2,0%. Ос-
новной компонент таких газов – азот. Для восстановления оксидов азота используется
аммиак при температуре 120ОС и давлении 0,3 МПа:
6 NO + 4 NH3(избыток) = 5 N2 + 6H2O
6 NO2 + 8 NH3 (избыток) = 7 N2 + 12H2O
139
Оставшийся аммиак окисляется кислородом воздуха:
4 NH3 + 3О2 = 2 N2 + 6H2O
Очищенный от оксидов азота газ выбрасывается в атмосферу. Поскольку все используемые в схеме очистки химические процессы проводятся при повышенных температурах, то выбрасываемый после очистки газ является источником энергетического загрязнения атмосферы. Если содержание оксидов азота в выхлопных газах повышено, то применяют многоступенчатые системы очистки, которые также основаны на каталитическом восстановлении оксидов азота до молекулярного азота.
2.4.5. Очистка газов от аммиака
Аммиак - токсичный газ, исходное сырье в производстве азотной кислоты. ПДК аммиака в воздухе населенных пунктов 0,2 мг/м3. Промышленные газы могут содержать аммиак в широком интервале концентраций. Очистка газов от аммиака основана на его хорошей растворимости в воде и щелочных свойствах.
Амиак легко удаляется из загрязненных газов промывкой водой, иногда добавляют дополнительную ступень доочистки раствором серной или фосфорной кислоты:
NH3 + H2O = NH4OH
2NH3 + Н2SO4 = (NH4)2 SO4
3NH3 + Н3РО4 = (NH4)3РО4
Адсорбцию аммиака водой проводят в системе, состоящей из последовательно включенных насадочных и тарельчатых колонн при давлении 1,6 МПа и температуре 60ОС с получением товарного продукта – аммиачной воды.
Наиболее экологичным является метод каталитического разложения аммиака при повышенных температурах:
2 NH3 = N2 + 3 Н2
Образующийся при этом газ содержит такое количество водорода, что может сгорать с выделением большого количества теплоты.
Очистку газов от аммиака при небольшом содержании этого компонента в газовых смесях можно проводить, используя активированные угли или крупнопористые иониты. На активированных углях имеет место процесс адсорбции аммиака. На ионитах – процесс ионообменной адсорбции, в котором участвует гидроксид аммония, образующийся в присутствии
влаги в очищаемом газе:
NH4OH = NH4+ + ОН-
HR + NH4OH = (NH4) R + H2O HR – катионит в Н-форме.
Катионит регенерируют, промывая водой или слабым раствором кислоты.
2.3. Рассеивание в атмосфере выбросов промышленных предприятий 2.3.1. Контроль качества атмосферного воздуха в зоне влияния выбросов про-
мышленных предприятий. ПДВ
Аэродисперсные системы, газы, пары, образующиеся в технологическом процессе предприятия в виде отходов, как правило, содержат компоненты, способные оказывать негативное воздействие на биоту и человека в определенных концентрациях. При существующих технологиях получения целевых продуктов и существующих способах очистки выбросов уменьшение концентраций опасных загрязнений в окружающей среде обеспечивают пу-
тем рассеивания загрязненных газов через высокие трубы на больших расстояниях от источников выброса. При этом предполагают, что достигается только такой уровень аэротехногенного загрязнения окружающей среды, при котором еще возможно естественное самоочищение всех природообразующих сфер (воды, воздуха, почвы). В качестве критерия качества атмосферного воздуха устанавливаются ПДК – максимальная концентрация при-
140

месей в атмосферном воздухе, отнесенная к определенному времени осреднения, которая при периодическом воздействии или на протяжении всей жизни человека не оказывает на него вредного влияния, включая отдаленные последствия.
Максимальная разовая ПДК устанавливается для кратковременного воздействия вредных веществ на человека (до 30 мин). ПДК среднесуточная устанавливается для предупреждения прямого или косвенного влияния на организм человека при неопределенно длительном воздействии вредного вещества (рис. 2.8).
ПДК максимальная разовая
ПДК загрязняющих веществ в воздухе населенных мест
ПДК среднесуточная
ВИДЫ ПДК
ПДК загрязняющих веществ  в воздухе рабочей зоны
в воздухе рабочей зоны
Рис. 2.8. Схема определения ПДК
Наибольшая концентрация каждого вредного вещества См (мг/м3) в приземном слое атмосферы не должна превышать максимальной разовой предельно допустимой концентрации ПДКМР:
CM ≤ ПДКМР .
Если в состав выброса входят несколько вредных веществ, то должно выполняться неравенство:
ПДКC1 1 + ПДКС2 2 +... + ПДКСn n ≤1
C1 +C2 ПДК1 +... +Сn ПДК1 ≤ ПДК1 , ПДК2 ПДКn
где С1 - Сn – концентрации вредных веществ в атмосферном воздухе в одной и той же точке местности, мг/м3; ПДК - предельно допустимые концентрации загрязняющих веществ (МР).
Наибольшая концентрация каждого вредного вещества См не должна превышать 0,8 ПДК для атмосферного воздуха населенных пунктов, на территориях санитарных охранных зон курортов, в местах размещения крупных санаториев и домов отдыха, в зонах отдыха городов с населением более 200 тыс. чел.
В целях ограничения загрязнения атмосферного воздуха для предприятий устанавли-
вается ПДВ (предельно допустимый выброс) − максимальный выброс загрязняющих веществ для конкретного источника, устанавливаемый из условия, что выбросы от данного источника и всей совокупности источников выбросов данной территории (города, др. населенного пункта) с учетом их рассеивания и превращения в атмосфере, а также перспектив развития региона, не создадут в приземном слое атмосферы концентраций загрязнений, превышающих нормативы ПДКМР. Если по каким-либо причинам на некотором этапе невозможно выполнить норматив ПДВ, то по согласованию с Комитетом по природным ресурсам и охране ОС может быть установлен ВДВ-временно согласованный выброс. Норматив ПДВ пересматривается не реже, чем раз в 5 лет.
2.3.2. Способы выброса загрязненных промышленных газов в атмосферу.
141

Рассеивание выбросов в атмосфере
Загрязнение окружающей среды при рассеивании выбросов предприятий через высокие трубы зависит от многих факторов: высоты трубы, скорости выбрасываемого газового потока, расстояния от источника выброса, наличия нескольких близко расположенных источников выбросов, метеорологических условий и др. (рис. 2.9).
Высота выброса и скорость газового потока
С увеличением высоты трубы и скорости выбрасываемого газового потока эффективность рассеивания загрязнений увеличивается, т.е. рассевание выбросов происходит в большем объеме атмосферного воздуха, над большей площадью поверхности земли.
Ветер |
График зависимости С(загр)= f (расстояния от источника) |
||
|
Приземный слой атмосферы |
|
|
|
Зона переброса факела |
зона задымления |
зона постепенного |
|
|
(наибольшего загрязнения) |
снижения уровня |
|
|
|
загрязнения |
Рис. 2.9. Схема рассеивания и распределения концентраций вредных веществ в приземном слое атмосферы под факелом высокого и мощного источника выбросов
Выбросы рекомендуется делать на эффективной высоте НЭ (рис. 2.10): НЭ = НТР + ∆Н
∆Н – высота подъема струи загрязненного газа над устьем трубы
НЭ |
НТР – высота трубы от поверхности земли
Рис. 2.10. Схема расчета эффективной высоты выбросов
Трубы строят как можно большей высоты (180÷250 м и более). Для повышения скорости истечения газов из устья трубы применяют факельный способ выброса, который предусматривает наличие на конце трубы специального устройства (конфузора с направляющими насадками). Эти устройства позволяют увеличить дальнобойность выходящей струи газа.
Значение величины ∆Н находят по формуле:
∆Η =1,24 w0 ∆Τ D2  (u3 Τa ),
(u3 Τa ),
142

где w0 − начальная скорость газовоздушной смеси в устье трубы; ∆Τ − разница температур газов и атмосферного воздуха; D − диаметр устья трубы, м; u − скорость ветра, м/с; Τa −
температура атмосферного воздуха, 0С.
Если выбросы холодные, т.е. ∆Τ=0, то величину ∆Н находят по формуле:
∆Η = 4,77 
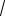 V w
V w (1+ 0,43 u
(1+ 0,43 u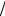 w),
w),
где V – количество газо-воздушной смеси, выбрасываемой в атмосферу, м3/с.
Если предприятие находится вблизи жилых домов (на расстоянии не более 5-кратной высоты зданий ), то рекомендуемая эффективная высота выброса должна быть не менее
2,5 h(здания):
∆ΗЭФ ≥ 2,5 h(здания).
Горизонтальное перемещение выбрасываемого газового потока определяется в основном скоростью ветра, а вертикальное – характером изменения температуры наружного воздуха в вертикальном направлении вблизи трубы.
Скорость ветра. Ветер – турбулентное движение воздуха над поверхностью земли. Направление и скорость ветра не остаются постоянными, скорость ветра возрастает при увеличении перепада атмосферного давления. Наибольшее загрязнение атмосферы возможно
при слабых ветрах 0÷5 м/с при рассеивании выбросов на малых высотах в приземном слое атмосферы. При выбросах из высоких источников наименьшее рассеивание загрязнений
имеет место при скоростях ветра 1÷7 м/с (в зависимости от скорости выхода струи газа из устья трубы).
Температурная стратификация. Способность поверхности земли поглощать или излучать тепло влияет на вертикальное распределение температуры в атмосфере. В обычных
условиях при подъеме вверх на 1 км температура уменьшается на ≈ 6,50: градиент температуры равен 6,50/км. В реальных условиях могут наблюдаться отклонения от равномерного уменьшения температуры с высотой – температурная инверсия. Различают приземные и приподнятые инверсии. Приземные характеризуются появлением более теплого слоя воздуха непосредственно у поверхности земли, приподнятые – появлением более теплого слоя воздуха(инверсионного слоя) на некоторой высоте. В инверсионных условиях ухудшается рассеивание загрязнений, они концентрируются в приземном слое атмосферы. При выбросе загрязненного газового потока из высокого источника наибольшее загрязнение воздуха возможно при приподнятой инверсии, нижняя граница которой находится над источником вы-
броса и наиболее опасной скорости ветра 1÷7 м/с. Для низких источников выбросов наиболее неблагоприятным является сочетание приземной инверсии со слабым ветром.
Рельеф местности. Даже при наличии сравнительно небольших возвышенностей существенно изменяется микроклимат в отдельных районах и характер рассеивания загрязнений. Так в пониженных местах образуются застойные, плохо проветриваемые зоны с повышенной концентрацией загрязнений. Если на пути загрязненного потока находятся здания, то над зданием скорость воздушного потока увеличивается, сразу за зданием – снижается, постепенно увеличиваясь по мере удаления, и на некотором расстоянии от здания скорость потока воздуха принимает первоначальное значение. Аэродинамическая тень – плохо проветриваемая зона, образующаяся при обтекании здания потоком воздуха. В зависимости от типа зданий и характера застройки образуются различные зоны с замкнутой циркуляцией воздуха, что может оказывать существенное влияние на распределение загрязнений (рис. 2.11, а, б, в).
143
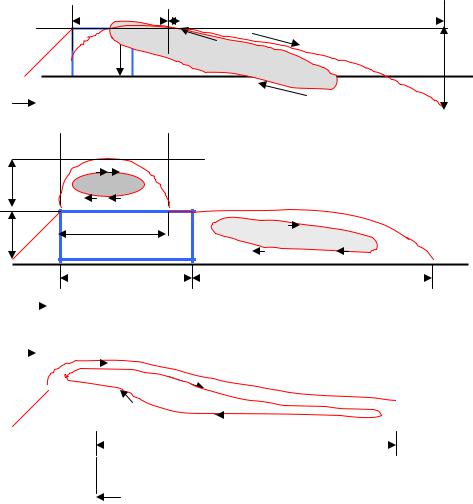
а)
2,5 НЗД |
|
|
|
10 НЗД |
Н |
Направление ветра |
б)
0,8НЗД
НЗД |
2,5 НЗД |
|
|
|
|
|
|
|
В > 2,5 НЗД |
|
|
|
4НЗД |
|
|||||
|
|
|
|
|
Направление ветра |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
в) |
|
|
|
|
|
|
|
||||||||||
|
|
Направление ветра |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
В < Х 10 НЗД
заветренная сторона здания Ширина межкорпусной циркулярной зоны равна 8НЗД, если первое здание широкое
Рис. 2.11. Схема формирования аэродинамическая тени при различной застройке:
а) – узкое отдельно стоящее здание; б) – широкое отдельно стоящее здание; в) – группа зданий: первое узкое
Только низкие источники выбросов, высота которых не превышает высоты крыши здания, загрязняют циркуляционные зоны зданий.
Высота источников выбросов НЗАГР, при которой они загрязняют циркуляционные зоны, определяется из формул:
для узкого отдельно стоящего здания НЗАГР = 0,36 ВЗ + 2,5 НЗД; для широкого отдельно стоящего здания НЗАГР = 0,36 ВЗ + 1,7 НЗД; для группы зданий НЗАГР = 0,36 (ВЗ + Х) + НЗД.
ВЗ – расстояние от источника выброса до заветренной стороны здания.
2.3.3. Санитарно-защитная зона предприятия. Формирование фитофильтра в санитарно-защитной зоне.
Методика расчета рассеивания в атмосфере вредных веществ, содержащихся в выбросах, основана на определении концентраций этих веществ (мг/м3) в приземном слое воздуха. Степень опасности загрязнения приземного слоя атмосферного воздуха выбросами вредных веществ определяется по наибольшему рассчитанному значению концентрации вредных ве-
144
ществ, которое может установиться на некотором расстоянии от источника выброса при наиболее неблагоприятных метеоусловиях (скорость ветра достигает опасного значения, наблюдается интенсивный турбулентный вертикальный обмен и др.). Расчет рассеивания выбросов проводится по ОНД-86. (ОНД – основной нормативный документ).
Предприятия, выбрасывающие в окружающую среду вредные вещества, должны быть отделены от жилой застройки санитарно-защитными зонами. Расстояние от предприятия до жилой застройки (размеры санитарно-защитной зоны) устанавливаются в зависимости от количества и вида выбрасываемых в окружающую среду загрязняющих веществ, мощности предприятия, особенностей технологического процесса.
Предприятие (класс) |
размеры санитарно-защитной зоны |
|
1 класс |
1000 |
м |
2 класс |
500 |
м |
3 класс |
300 |
м |
4 класс |
100 |
м |
5 класс |
50 |
м |
При определенных условиях границы санитарно-защитной зоны могут быть увеличены, но не более, чем в 3 раза.
Одна из функций санитарно-защитной зоны – биологическая очистка атмосферного воздуха средствами озеленения. Древесно-кустарниковые насаждения газопоглотительного назначения (фитофильтры) способны поглощать газообразные загрязняющие вещества. На-
пример, установлено, что луговая и древесная растительность может связывать 16÷90% сернистого газа. Роль отдельных компонентов биоценоза в связывании загрязнений зависит от периода вегетации и фотосинтетической активности, температуры, освещенности, влажности воздуха. Расчет поглотительной способности насаждений рассчитывается по формуле:
P = K U TU , TВ
где Р – поглотительная способность 1 га насаждений за вегетацию, кг/га; U – сухая фитомасса листьев и хвои, кг; К – коэффициент физиологически допустимого накопления серы (лиственные породы – 0,002; хвойные – 0,001); ТU – время удаления серы из листьев и хвои (10 дней); ТВ – длительность вегетации, дней.
Для насаждений с фитомассой листьев и хвои 5 т/га уровень накопления серы составляет (в кг на 1 га насаждений):
• физиологически допустимый – 150 кг (для лиственного леса), 36 кг (для хвойного
леса),
•при слабых повреждениях (до 20%) – 300 кг и 83 кг соответственно,
•при средних повреждениях (40%) – 412 кг и 145 кг соответственно,
•при сильных повреждениях – 720÷800 кг и 260 кг соответственно,
Для растительности определяют три уровня поглотительной способности:
1.физиологический (недопустимы некрозы и снижение фотосинтетической продук-
тивности),
2.биологический (допускается определенная степень повреждения листьев и хвои, снижение продуктивности и возможная гибель особо чувствительных видов),
3.максимальный (потенциальный) (возможна гибель растительности и засоление или отравление почв).
В соответствии с уровнями поглотительной способности коэффициент физиологически допустимого накопления серы К принимает следующие значения (табл. 2.6):
Таблица 2.6 Значения коэффициента физиологически допустимого накопления серы К
145

Уровень поглотительной спо- |
Лиственные |
по- |
Хвойные породы |
собности растительности |
роды |
|
|
физиологический |
0,002 |
|
0,001 |
биологический |
0,004; 0,006 |
|
0,002 |
максимальный |
0,01 |
|
0,004 |
Структура и функции зеленого фильтра приведены на рис. 2.12.
Структура и функции зеленого фильтра
Фронтальная часть |
средняя часть |
тыловая часть |
||||||
|
F |
|
F |
|
F |
|
|
|
|
|
|
|
|
|
|
|
|
Разрушение |
снижение |
полная очистка |
||||||
газовых |
концентраций |
газовых потоков |
||||||
|
потоков |
загрязнений |
от загрязнений |
|
||||
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
выполнение функций достигается подбором высокогазоустойчивых видов растений с максимально выраженной назопоглотительной способностью, обладающих значительной биомассой листьев и различными сроками облиствения
Рис. 2.12. Структура и функции зеленого фильтра
Фронтальная часть зеленого фильтра должна быть представлена групповыми и линейными посадками с коридорами, образующими организованную аэродинамическую систему. Средняя и тыловая части фильтра должны способствовать полному перехвату газообразных загрязнений. Для этой цели рекомендуются семирядные трехъярусные лесные полосы с возрастающей густотой зеленых насаждений. Площадь насаждений в санитарнозащитных зонах зависит от класса промышленного предприятия. Ассортимент растений подбирают в соответствии с климатическими и почвенными условиями, составом и количествами загрязнений, расстояниями от источников выбросов. Обычно вблизи промышленных предприятий по состоянию растительности выделяют несколько характерных зон. В радиусе
100÷500 м погибают многие древесные(в первую очередь хвойные) породы. В этой зоне следует высаживать наиболее устойчивые виды травянистых растений и некоторых кустарни-
ков. В радиусе 500÷1000 м возможно создание устойчивых газонов, защитных полос и дру-
гих форм насаждений из устойчивых кустарников и древесных пород. В радиусе 1÷2 км для озеленения используют среднеустойчивые и даже газочувствительные виды. Устойчивость фитофильтра в некоторых случаях можно повысить путем промывания лиственной массы (полив).
Некоторые виды растений, используемые для озеленения санитарно-защитных зон при различных загрязнениях приведены в табл. 2.7.
|
Таблица 2.7 |
Растения, применяемые для озеленения санитарно-защитных зон |
|
|
|
Загрязнение |
Ассортимент растений (примеры) |
Оксиды се- |
Айва японская; арония черноплодная; барбарис обыкновенный; |
ры |
береза повислая; груша обыкновенная; клен остролистный; липа; |
|
сирень обыкновенная; туя западная; черемуха обыновенная; чу- |
|
146 |
|
бушник; яблоня домашняя; ясень обыкновенный |
Фенолы, |
Арония черноплодная; береза плакучая; вишня обыкновенная; ель |
ксилол |
колючая серебристая; липа; роза (культурные сорта); сирень |
|
обыкновенная; туя западная |
Оксиды азо- |
Арония черноплодная; барбарис обыкновенный; береза повислая; |
та |
вишня обыкновенная; груша обыкновенная; ель колючая; ель ко- |
|
лючая серебристая; липа мелколистная; лиственница; сирень |
|
обыкновенная; тополь; туя западная; форзиция; чубушник |
147
