
- •Оглавление
- •Принятые сокращения
- •Введение
- •1. ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ ХИМИИ ВЫСОКОМОЛЕКУЛЯРНЫХ СОЕДИНЕНИЙ
- •1. 1. Классификация полимеров
- •1. 2. Номенклатура полимеров
- •1. 3. Особенности макросвойств полимеров
- •1. 4. Краткая характеристика реакций синтеза полимеров
- •Контрольные вопросы
- •2. ЦЕПНАЯ ПОЛИМЕРИЗАЦИЯ
- •2. 1. Термодинамика полимеризации
- •2. 2. Мономеры, используемые в реакциях полимеризации
- •2. 3. Радикальная полимеризация
- •2. 3. 1. Способы инициирования радикальной полимеризации
- •2. 3. 2. Стадии процесса радикальной полимеризации
- •2. 3. 3. Реакции свободных радикалов
- •2. 3. 4. Ингибирование и замедление радикальной полимеризации
- •2. 3. 5. Кинетика радикальной полимеризации
- •2. 3. 6. Влияние различных факторов на скорость полимеризации и молекулярную массу полимера
- •2. 4. Ионная (каталитическая) полимеризация
- •2. 4. 1. Катионная полимеризация
- •2. 4. 1. 1. Стадии процесса катионной полимеризации
- •2. 4. 1. 2. Кинетика катионной полимеризации
- •2. 4. 2. Анионная полимеризация
- •2. 4. 2. 1. Стадии процесса анионной полимеризации
- •2. 4. 2. 2. Кинетика анионной полимеризации
- •2. 4. 3. Полимеризация, протекающая без обрыва цепи
- •2. 4. 4. Ионно-координационная полимеризация
- •2. 5. Сополимеризация
- •2. 5. 1. Типы и номенклатура сополимеров
- •2. 5. 2. Уравнение состава сополимера
- •2. 5. 3. Анализ уравнения состава
- •2. 5. 4. Определение констант сополимеризации
- •2. 5. 4. 1. Экспериментальные методы
- •2. 5. 4. 2. Теоретический метод
- •2. 6. Способы проведения полимеризации
- •Контрольные вопросы
- •Список использованной литературы
- •Приложение

Такой теломер после аминирования Cl-группы и гидролиза CCl-группы превращается в аминокарбоновую кислоту, являющуюся ценным техническим мономером для получения поликонденсационного полиамида.
Cl CH2 CH2 nCCl3 + NH3
CH2 CH2 nCCl3 + NH3  H2N
H2N CH2 CH2 nCCl3 + HCl
CH2 CH2 nCCl3 + HCl
H N |
|
|
|
CH |
|
CH |
|
|
|
CCl |
+ 2 H O |
|
H2N |
|
|
CH2 |
|
|
|
|
COOH + 3 HCl |
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
2 |
|
|
|
2 |
2 |
n |
3 |
2 |
|
|
|
|
|
|
|
|
n |
|||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Схема 6
Все реакции передачи цепи приводят к уменьшению молекулярной массы полимера (кроме передачи цепи на полимер). В технологии они имеют значение как способ получения теломеров, а также при получении полимеров заданной молекулярной массы.
Рассмотрим, в какие реакции способны вступать свободные радикалы в процессе полимеризации.
|
|
|
|
|
|
|
|
2. 3. 3. Реакции свободных радикалов |
|
||||||||||||||||||||||||||||||||||
|
Свободные радикалы вступают в реакции пяти типов: |
|
|||||||||||||||||||||||||||||||||||||||||
1. |
Реакция рекомбинации, |
объединение двух радикалов с образованием |
|||||||||||||||||||||||||||||||||||||||||
|
новой связи |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
X + Y |
|
|
|
|
|
|
|
X |
|
|
|
Y |
(2.75) |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
CH3 + CH3 |
|
|
|
|
CH2 |
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
CH3 |
|
CH2 |
|
|
CH2 |
|
CH3 |
(2.76) |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
2. Реакция фрагментации, разделение на фрагменты |
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
X |
|
|
|
Y |
|
|
|
|
|
|
|
|
X + Y |
(2.77) |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
H3C |
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(2.78) |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
C |
|
O |
|
|
|
|
|
|
H3C + H3C |
|
C |
|
CH3 |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
||||||||||||||||||||||
3. |
Передача радикала |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
X + Y |
|
Z |
|
|
|
|
|
|
|
|
X |
|
Y + Z |
(2.79) |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
CF3 + CH4 |
|
|
|
|
|
|
|
CF3H + CH3 |
(2.80) |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
62 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
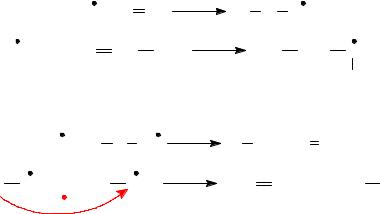
4. |
Реакция присоединения |
|
|
|
|
X + Y |
Z |
X Y Z |
(2.81) |
|
CH3 + CH2 CH |
CH3 |
CH3 CH2 CH |
(2.82) |
|
|
|
CH3 |
|
5. |
Реакция диспропорционирования |
|
||
|
X + Y Z W |
X Y + Z W |
(2.83) |
|
|
CH3 CH2 + CH3 CH2 |
CH2 CH2 + CH3 CH3 |
(2.84) |
|
|
H |
|
|
|
При реакциях 1 и 5 свободные радикалы исчезают, при остальных – происходит замена одних радикалов другими.
Рост кинетической цепи реакции 2 … 4.
Рост материальной цепи: присоединение к радикалу – реакция 4. Реакции 1 и 5 проходят на III стадии – стадии обрыва цепи. Истинный об-
рыв цепи приводит к обрыву материальной и кинетической цепи.
2. 3. 4. Ингибирование и замедление радикальной полимеризации
Ингибированием называются реакции передачи цепи в результате которых образуются неактивные радикалы, неспособные продолжать цепь. Иными словами, в присутствии некоторых веществ радикальная полимеризация приостанавливается.
По эффективности такие вещества делятся на ингибиторы и замедлители.
Ингибиторы (от лат. – останавливаю, сдерживаю) – вещества, уничтожающие все имеющиеся в системе радикалы, в их присутствии полимеризация не идет до полного исчерпания ингибитора, после чего начинается со скоростью, эквивалентной скорости процесса в отсутствие ингибитора.
Схематически реакцию ингибирования можно представить следующим образом:
R + HZ
+ HZ  RH + Z
RH + Z , (2.85)
, (2.85)
где HZ – ингибитор; Z∙ – неактивный образовавшийся радикал, то есть радикал, который не способен к реинициированию радикальной полимеризации.
63
Неактивные радикалы могут рекомбинировать (или диспропорциониро- |
|||||||||
авть) с активными радикалами или между собой: |
|
|
|||||||
|
|
|
Z + MyM |
Z MMy , |
|
(2.86) |
|||
|
|
|
|
Z |
+ Z |
Z |
Z . |
|
(2.87) |
Ингибиторы легко окисляются и поэтому разрушают пероксиды, обра- |
|||||||||
зующиеся при взаимодействии мономера или радикала с кислородом воздуха |
|||||||||
или специально введенные в систему. |
|
|
|
|
|||||
|
|
1 |
2 |
3 |
4 |
Результат |
действия |
ингибиторов |
|
|
100 |
показан на рис. 2.2. В присутствии инги- |
|||||||
|
|
|
|
|
|||||
Конверсия |
|
|
|
|
|||||
|
|
|
|
биторов реакция полимеризации начина- |
|||||
мономера, |
|
|
|
|
|||||
% |
|
|
|
|
|
ется не сразу, а лишь после израсходова- |
|||
|
|
|
|
|
|
||||
|
0 |
|
Время,ч |
ния ингибитора. |
Время до начала реак- |
||||
|
инд |
ции называется индукционным периодом |
|||||||
|
|
|
|
||||||
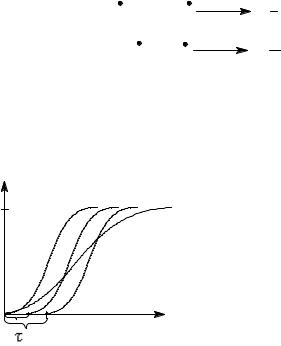
Рис. 2.2. Влияние различных ин- |
(τинд). Его величина зависит от концен- |
||||||||
гибиторов или различных концен- |
трации ингибитора; при этом, чем боль- |
||||||||
траций |
одного |
ингибитора, |
где |
ше концентрация ингибитора, тем боль- |
|||||
С3 > С2 (2, 3) и замедлителя (4) на |
|||||||||
кинетику полимеризации: (1) по- |
ше индукционный период (кривые 2, 3). |
||||||||
лимеризация без ингибитора и за- |
Количественно эффективность ин- |
||||||||
медлителя |
|
|
|
|
|||||
|
|
|
|
гибиторов (Э) характеризуют соотноше- |
|||||
|
|
|
|
|
|
||||
нием начальных скоростей полимеризации в отсутствие (V) и в присутствии |
|||||||||
(Vинг) ингибиторов (при одинаковых скоростях инициирования): |
|
||||||||
|
|
|
|
|
Э = V/Vинг. |
|
|
(2.88) |
|
Эффективность ингибиторов зависит как от их строения, так и от строе- |
|||||||||
ния мономеров. |
|
|
|
|
|
|
|
|
|
На рис. 2.2 показаны кинетические кривые полимеризации с использова- |
|||||||||
нием различных по эффективности ингибиторов (кривые 2, 3), которые совпа- |
|||||||||
дают с ходом кривых, взятых для различных концентраций одного и того же |
|||||||||
ингибитора. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
64 |
|
|
|
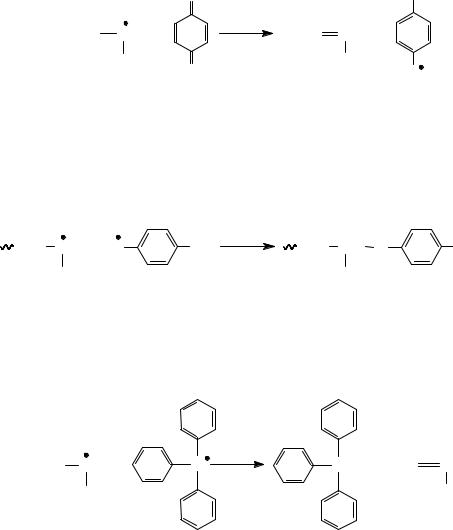
Ингибиторами являются хиноны (гидрохинон), ароматические амины, фенолы, а также стабильные свободные радикалы, не взаимодействующие друг с другом, но вступающие в реакции рекомбинации или диспропорционирования с активными радикалами.
Рассмотрим действие ингибиторов:
ØХиноны
Наибольшее распространение из них получил п-бензохинон.
|
O |
|
OH |
CH3 CH + |
|
CH2 CH + |
(2.89) |
X |
O |
X |
O . |
|
|
Полученный в результате реакции семихиноидный радикал из-за «втягивания» неспаренного электрона системой сопряжения обладает очень низкой активностью и участвует в реакции обрыва цепи, присоединяясь либо к первичному радикалу, либо к растущему макрорадикалу:
CH2 CH + O |
OH |
CH2 CH O |
OH (2.90) |
X |
|
X |
. |
Ø Стабильные свободные радикалы – не взаимодействуют друг с дру-
гом, но способны реагировать с активными радикалами. Например, трифенилметильный радикал реагирует по схеме:
H3C CH + |
C |
CH + CH2 CH |
(2.91) |
X |
|
X |
|
.
Ингибиторы применяют для предотвращения самопроизвольной преждевременной полимеризации при хранении или транспортировании мономеров и олигомеров в период между введением инициатора в реакционную среду и началом реакции.
65
