
- •Оглавление
- •Принятые сокращения
- •Введение
- •1. ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ ХИМИИ ВЫСОКОМОЛЕКУЛЯРНЫХ СОЕДИНЕНИЙ
- •1. 1. Классификация полимеров
- •1. 2. Номенклатура полимеров
- •1. 3. Особенности макросвойств полимеров
- •1. 4. Краткая характеристика реакций синтеза полимеров
- •Контрольные вопросы
- •2. ЦЕПНАЯ ПОЛИМЕРИЗАЦИЯ
- •2. 1. Термодинамика полимеризации
- •2. 2. Мономеры, используемые в реакциях полимеризации
- •2. 3. Радикальная полимеризация
- •2. 3. 1. Способы инициирования радикальной полимеризации
- •2. 3. 2. Стадии процесса радикальной полимеризации
- •2. 3. 3. Реакции свободных радикалов
- •2. 3. 4. Ингибирование и замедление радикальной полимеризации
- •2. 3. 5. Кинетика радикальной полимеризации
- •2. 3. 6. Влияние различных факторов на скорость полимеризации и молекулярную массу полимера
- •2. 4. Ионная (каталитическая) полимеризация
- •2. 4. 1. Катионная полимеризация
- •2. 4. 1. 1. Стадии процесса катионной полимеризации
- •2. 4. 1. 2. Кинетика катионной полимеризации
- •2. 4. 2. Анионная полимеризация
- •2. 4. 2. 1. Стадии процесса анионной полимеризации
- •2. 4. 2. 2. Кинетика анионной полимеризации
- •2. 4. 3. Полимеризация, протекающая без обрыва цепи
- •2. 4. 4. Ионно-координационная полимеризация
- •2. 5. Сополимеризация
- •2. 5. 1. Типы и номенклатура сополимеров
- •2. 5. 2. Уравнение состава сополимера
- •2. 5. 3. Анализ уравнения состава
- •2. 5. 4. Определение констант сополимеризации
- •2. 5. 4. 1. Экспериментальные методы
- •2. 5. 4. 2. Теоретический метод
- •2. 6. Способы проведения полимеризации
- •Контрольные вопросы
- •Список использованной литературы
- •Приложение
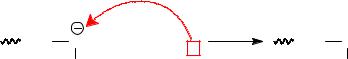
3) Передача цепи на растворитель. Отрыв протона растущей цепью от растворителя протекает при использовании растворителя, способного отдавать протон (жидкий аммиак, толуол):
H+ |
|
(2.155) |
CH2 CH Me+ + NH3 |
CH2 CH2 + NH2Me |
|
X |
X |
|
Передача цепи на полимер при анионной полимеризации практически не реализуется, поскольку образующиеся при этом анионы мало устойчивы; поэтому разветвленных полимеров при анионной полимеризации почти не получается.
В случае анионной полимеризации отсутствуют реакции, приводящие к обрыву кинетической цепи. Такой процесс анионной полимеризации протекает с образованием «живых» полимеров (см. раздел 2.4.3).
2. 4. 2. 2. Кинетика анионной полимеризации
Кинетика анионной полимеризации сложна и зависит от многих факторов, главным образом от типа катализатора, среды и активности мономеров, поэтому исследована только для простейших систем.
Для вывода кинетического уравнения анионной полимеризации рассмотрим полимеризацию стирола амидом калия в жидком аммиаке. Полимеризация проводится при температуре кипения аммиака (-33°С). Это полимеризация – один из небольшого числа примеров ионной полимеризации, когда инициирование осуществляется свободными ионами (ε↑), а не ионными парами. Причиной этого является высокая диэлектрическая проницаемость и большая сольватирующая способность жидкого аммиака.
I. Инициирование происходит путем диссоциации амида калия и присоединения образующегося амидного иона к мономеру:
98

|
|
|
|
|
|
k |
+ |
|
|
- |
|
|
|
|
|
(2.156) |
|
KNH2 ¬¾® K + H2N |
|
|
|
|
|
|
|||||||||
- |
|
|
|
|
|
kи |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H2N |
+ CH2 |
|
|
CH |
|
|
H N |
|
CH |
|
|
CH |
(2.157) |
|||
|
|
|
|
|||||||||||||
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
2 |
|
|
2 |
|
|
|
|
||
|
|
|
C6H5 |
|
|
|
|
|
|
C6H5 |
|
|||||
Скорость инициирования выражается уравнением:
V = k |
[H |
2 |
N − ] [M ] |
, |
(2.158) |
||
и и |
|
|
|
||||
из уравнения (2.156) находим значение константы k : |
|
||||||
k = |
[H2 N − ] [K + ] |
, |
|
(2.159) |
|||
|
[KNH2 ] |
|
|||||
|
|
|
|||||
решаем его относительно концентрации [H2 N − ] и подставляя в (2.158) полу-
чаем
Vи = |
k × k |
[KNH |
] [M ] |
|
|
||
и |
2 |
|
. |
|
(2.160) |
||
|
[K + ] |
|
|
||||
II. Рост цепи |
|
|
|
|
|
|
|
H2N-МnM |
- |
+ M |
k р |
|
|
- |
(2.161) |
|
¾¾® H2N-Mn+1M |
|
|||||
происходит со скоростью |
|
|
|
|
|
|
|
Vр = k p [R− ] [M ], |
|
(2.162) |
|||||
где [R− ] общая концентрация растущих анионных центров.
III. Обрыв цепи в этой системе не происходит путем перехода гидридного иона (Н-) к мономеру, о чем свидетельствует отсутствие ненасыщенности в по-
лимере. Не реализуется также маловероятная возможность комбинирования растущего иона с ионом калия, т.е. амид калия не расходуется в ходе полимеризации.
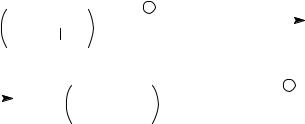
Обрыв цепи происходит в результате передачи цепи на растворитель с регенерацией инициирующего амидного иона.
99
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
kпер. S |
|
|
|||
|
H2N |
|
CH2 |
|
|
|
|
|
CH |
|
CH2 |
|
|
|
|
|
|
CH |
+ NH3 |
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
C H n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
C H |
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
6 |
5 |
|
|
|
|
|
6 |
5 |
|
|
|
|
|
|
|
|
|
|
(2.163) |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
H2N |
|
CH2 |
|
|
|
CH |
|
CH2 |
|
|
|
CH2 + H2N |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C H n |
|
|
C H |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6 |
5 |
6 |
5 |
|
|
|
|
|
|
|||||||||||||
или H2N-МnM |
- |
+ NH3 |
|
|
|
|
kпер.S |
|
|
|
|
|
|
|
|
|
|
- |
(2.164) |
|||||||||||||||||
|
¾¾¾® H2N-Mn+1Н + H2N |
|
||||||||||||||||||||||||||||||||||
Скорость обрыва дается уравнением
(2.165)
– скорость обрыва цепи происходящего в результате передачи цепи на рас-
творитель; – константа скорости передачи цепи на растворитель.
Лимитирующая стадия – рост кинетической цепи (2.162), чтобы убрать концентрацию растущих анионов [R− ], используем допущение квазистацио-
нарного состояния растущих частиц.
[R− ] = const, следовательно, Vи = Vпер ,
|
k × k |
[KNH |
] [M ] |
= kперS [R− ] [NH3 |
], |
|
|||
|
и |
2 |
|
|
(2.166) |
||||
|
|
[K + ] |
|
|
|||||
выражаем отсюда [R− ] и подставляем (2.162): |
|
|
|||||||
|
Vап = |
k kи k p [KNH 2 ] [M ] 2 |
|
|
|
||||
|
kперS [NH3 ] [K + ] , |
|
(2.167) |
||||||
|
|
|
|
||||||
где Vап – скорость анионной полимеризации.
Средняя степень полимеризации в этой системе определяется соотношением скорости роста и передачи цепи.
|
|
V |
k |
p |
[M ] |
|
|
|
|
||
n = |
p |
= |
|
|
|
|
|
. |
(2.168) |
||
V |
k |
перS |
[NH |
3 |
] |
||||||
|
|
пер |
|
|
|
|
|||||
Скорость полимеризации увеличивается с понижением температуры.
100
