
- •«Термодинаміка»
- •Основні поняття термодинаміки
- •Контрольні запитання
- •Суміші ідеальних газів
- •Контрольні запитання
- •3. Перший і другий закон термодинаміки
- •Контрольні запитання
- •Процеси зміни параметрів ідеального газу
- •Визначення основних характеристик термодинамічних процесів
- •Контрольні запитання
- •5. Рівняння стану реальних газів
- •Критичні параметри та параметри насичення [2]
- •6. Ізотерми газів
- •Контрольні запитання
- •Розв’язання
- •7. Перший закон термодинаміки для реальних газів
- •7.1. Ізохорний процес зміни стану газу
- •7.2. Ізобарний процес
- •7.3. Ізотермічний процес
- •7.4. Адіабатний процес
- •7.5. Стискування газів у компресорах
- •7.6. Процеси адіабатного руху газу в потоці і витікання газу
- •7.7. Дроселювання газів і пари
- •Контрольні запитання
7.7. Дроселювання газів і пари
Дроселюванням називається термодинамічний незворотний процес розширення газу чи пари при проходженні їх через місцеве звуження на трубопроводі (діафрагму, сідло клапана чи регулятора), що проходить без віддачі роботи у зовнішнє середовище.
Схема дроселя показана на рис. 13.
Процес дроселювання реальних газів і пари проходить за таких умов:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
i = const.
Із (39) випливає, що процес адіабатного дроселювання за відсутності роботи проходить при постійній ентальпії, i=const, (ізоінтальпний процес).
При проходженні
потоку газу через діафрагму (звуження)
внаслідок утрат енергії на подолання
місцевого опору тиск газу зменшується,
![]() ,
а питомий об’єм збільшується,
,
а питомий об’єм збільшується,![]() ,
тобто газ розширюється. Це явище і
називають дроселюванням, або зім’яттям.
,
тобто газ розширюється. Це явище і
називають дроселюванням, або зім’яттям.
 Рис.
13. Схема дроселя
Рис.
13. Схема дроселя
Величина
витрат тиску
![]() на подолання місцевого опору у вигляді
раптового звуження (діафрагми) може
досягти значних розмірів і залежить
від витрат газу V, швидкості – W газу,
співвідношення між площею потоку в
отворі діафрагми Fд
і в трубі F1
(коефіцієнта стиснення потоку).
на подолання місцевого опору у вигляді
раптового звуження (діафрагми) може
досягти значних розмірів і залежить
від витрат газу V, швидкості – W газу,
співвідношення між площею потоку в
отворі діафрагми Fд
і в трубі F1
(коефіцієнта стиснення потоку).
Визначення
![]() здійснюється за формулою Вейсбаха
здійснюється за формулою Вейсбаха
![]() ,
Па, (88)
,
Па, (88)
де
ζ – коефіцієнт місцевого опору діафрагми,
залежить від показника стиснення потоку
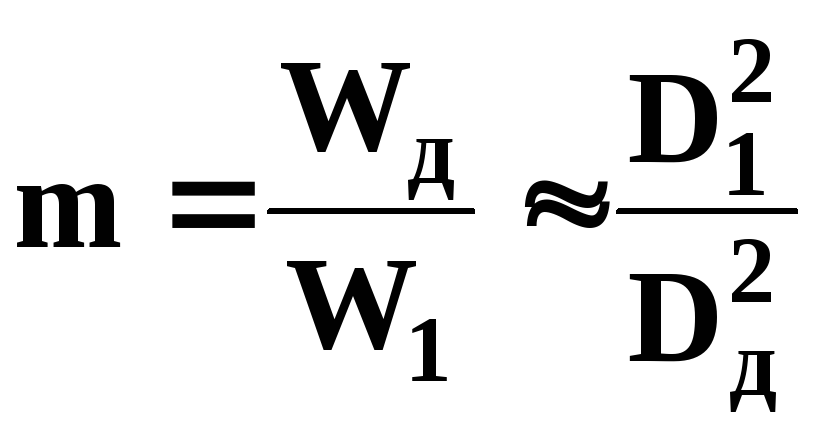 може прийматись за таблицею 9.
може прийматись за таблицею 9.
Таблиця 9
Значення коефіцієнта місцевого опору ζ для діафрагми
|
Показник стиснення Потоку m |
0,1 |
0,2 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
|
Коефіцієнт місцевого опору ζ |
0,4 |
0,39 |
0,34 |
0,3 |
0,27 |
0,2 |
0,16 |
Швидкість газу в трубопроводі до діафрагми W1 визначається за відомими годинними витратами газу V і площею перетину труби F1 згідно із залежністю
![]() ,
м/с, (89)
,
м/с, (89)
де V – годинні об’ємні витрати газу, м3/год;
F1 – площа перетину труби до діафрагми.
Діаметри труби D1 і D2 до й після діафрагми однакові. Значить, однаковими будуть швидкості потоку W1=W2 та його кінетична енергія до і після діафрагми.
У самому дроселі швидкість та кінетична енергія збільшуються, а ентальпія зменшується.
Зміна параметрів стану газу до і після дроселя визначається наступними залежностями:
– ентальпія
![]() ;
(90)
;
(90)
– внутрішня
енергія
![]() ;
(91)
;
(91)
– кількість теплоти q1,2 = 0;
– зміна
ентропії
 ;
(92)
;
(92)
– зміна
температури
![]() .
(93)
.
(93)
Величина α називається коефіцієнтом дроселювання, або диференційним дросель - ефектом, а ефект зміни температури при адіабатному дроселюванні – ефектом Джоуля – Томпсона.
Зміна температури газу в процесі адіабатного дроселювання при кінцевих значеннях p1 і p2 називається інтегральним дросель - ефектом
 ,
(94)
,
(94)
де T1 та T2 – температура газу відповідно до й після дроселя, 0К.
Для повітря диференціальний дросель-ефект дорівнює близько 0,25 град на 1 ат. Для метану в діапазоні від 200 до 100 ат диференціальний дросель-ефект становить 0,36 град на 1 ат. Таким чином, при зменшенні тиску метану на 100 ат температура після дроселя зменшиться на 25÷36 град.
Величину інтегрального дросель-ефекту можна визначити за діаграмами стану газу, побудувавши на них ізоентальпний процес дроселювання. Початкову точку процесу т.1 знаходять за відомими параметрами стану(p1 ,υ1 , T1, i1). Кінцева точка процесу знаходиться на перетині ізоентальпи, проведеної із т.1 та ізобари P2 після дроселя. За ізотермами, що проходять через т.1 і т.2, визначають інтегральний дросель-ефект ΔT = T2 – T1 ( рис. 14).
Ідеальний газ дроселюється без зміни температури. Це одна із характер-
них ознак ідеального газу. Адіабата дроселювання ідеального газу проходить
ізоентальпно i1 = i2 та ізотермічно T1 = T2. Тоді і величина αi = 0.
 Рис.14.
Процес дроселювання пари в І–S
- діаграмі
Рис.14.
Процес дроселювання пари в І–S
- діаграмі
1-2 - процес дроселювання при i1 = i2 = const;
1-3 - адіабатний процес розширення газу до дроселя від тиску p1 до p3;
2-3′ - адіабатний процес розширення газу після дроселя від тиску p2 до p3;
T2 – T1 = ΔT інтегральний дросель-ефект
Досліди показують, що для реальних газів знак αi може бути різним залежно від початкових параметрів стану газу. Стан газу, для якого αi = 0, називається точкою інверсії ефекту Джоуля–Томсона. Якщо початкова температура Т1 (до дроселя) дорівнює температурі інверсії Т1=Тінв, то при дроселюванні температура газу не змінюється і процес проходить ізотермічно:
п
 ри
Т1
<
Тінв αi
<
0
ри
Т1
<
Тінв αi
<
0
Т2 < Т1 газ охолоджується,
п
 ри
Т1
>
Тінв αi
>
0
ри
Т1
>
Тінв αi
>
0
Т2 > Т1 газ нагрівається.
Значення Тінв із достатньою точністю можна обчислити за формулою
Тінв ≈ 6,25 Ткр, 0К, (95)
де Ткр – критична температура газу. Для повітря Тінв=760 0К, для водяної пари Тінв=4370 0К, а для Н2, Тінв=216 0К. Тому, якщо до дроселя температура газу становить 200С (2930К), то після дроселя температури водяної пари і повітря будуть зменшуватись, а водню – збільшуватись.
Дроселювання супроводжується зменшенням роботоздатності газу, яке оцінюється розраховуваним перепадом ентальпій у процесі одержання роботи при розширенні газу від початкового стану до й після дроселя.
Зменшення роботоздатності при дроселюванні визначається залежністю:
Δl = l1-2 – l2-3 = (i1 – i3) – (i2 – i3′) = i3′ – i3 . (96)
Із рис. 14 видно, що в ході дроселювання вологий газ у т.1 до дроселя перетворюється в перегрітий газ у т.2 після дроселя за умови, що T2 < T1. Зміна стану газу за відсутності підведення теплоти і зменшенні температури газу пояснюється падінням тиску газу після дроселя та відповідним зниженням температури насичення. Процес дроселювання використовують для зниження температури РТ у холодильних машинах, для осушування газу, очищення його від компонентів із великою температурою конденсації (насичення) при низькотемпературній сепарації. Залежність (88) перепаду тиску на діафрагмі від швидкості і витрат газу, що протікає через неї, використовується у вузлах обліку газу чи пари. За показанням дифманометрів, які вимірюють перепад тиску на вимірювальних діафрагмах, визначають величину швидкості W і витрати газу V.
