
- •Конспект лекцій з фізики
- •Конспект лекцій з фізики
- •Частина 2
- •Кінетична теорія газів
- •Рівняння стану ідеального газу
- •Основне рівняння молекулярно-кінетичної теорії ідеального газу
- •Розподіл молекул за швидкостями
- •Барометрична формула. Розподіл Больцмана частинок у зовнішньому потенціальному полі
- •Фізичні основи термодинаміки
- •Внутрішня енергія системи
- •Робота при зміні об’єму
- •Ступені вільності
- •Принцип рівнорозподілу енергії за ступенями вільності
- •Теплоємність
- •Перший закон термодинаміки
- •Застосування першого закону термодинаміки до газових процесiв
- •Iзобаричний процес
- •Iзотермiчний процес
- •Iзохоричний процес
- •Адіабатний процес
- •Другий закон термодинаміки
- •Ентропія
- •Розрахунок зміни ентропії у процесах ідеального газу
- •Середня довжина вільного пробігу молекул газу
- •Явища переносу
- •Дифузія в газах
- •Внутрішнє тертя у газах
- •Теплопровідність газів
- •Реальні гази
- •Внутрішня енергія реального газу
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Завдання для самостійного контролю знань
- •1. 2. 3. 4.
- •1. Ізобаричного 2. Адіабатичного 3. Ізотермічного 4. Ізохоричного
- •1. Ізотермічного 2. Адіабатичного 3. Ізохоричного 4. Ізобаричного
- •1. Ізотермічного 2. Адіабатичного 3. Ізохоричного 4. Ізобаричного
- •1. Ізотермічного 2. Адіабатичного 3. Ізохоричного 4. Ізобаричного
- •Задачі для самостійного розв’язування
- •Рекомендована література
Розв’язання
Зміна ентропії
![]() S
=
S
=![]() ,
,
де
![]() Q
= РdV
при ізотермічному процесі. З рівняння
Менделєєва-Клапейрона
Q
= РdV
при ізотермічному процесі. З рівняння
Менделєєва-Клапейрона
РV
=
![]() тиск Р
=
тиск Р
=
![]() ,
,
тоді
![]() ,
,
а зміна ентропії
![]() .
.
Перевіримо
одиниці
виміру![]() S.
S.
![]()
Підставивши числові значення й обчислюючи, одержимо
![]()
Відповідь![]() S=2,85Дж/К.
S=2,85Дж/К.
Задача 16. Деякий газ (v=1кмоль) займає об’єм V1=1м3. При розширенні газу до об’єму V2=1,5м3 було виконано роботу А проти сил міжмолекулярного тя-жіння , що дорівнює 45,3кДж. Визначити поправку а, що входить у рівнян-ня Ван-дер-Ваальса.
Дано:v=1кмоль=103моль,V1=1м3, V2=1,5м3, А=45,ЗкДж=4,53.104Дж.
Визначити а.
Розв’язання
Робота, виконана проти сил міжмолекулярного тяжіння,

де![]() -
внутрішній
тиск,
зумовлений
силами
взаємодії
молекул.
Таким
чином,
-
внутрішній
тиск,
зумовлений
силами
взаємодії
молекул.
Таким
чином,

Звідси
![]()
Перевіримо одиниці виміру а.
![]()
Підставивши числові значення й обчислюючи, одержимо
![]() =0,136(Нм4/моль2)
=0,136(Нм4/моль2)
Відповідь a=0,136Нм4/моль2.
Завдання для самостійного контролю знань
1. По якій з формул можна підрахувати загальну кількість молекул газу в посудині?
1. 2. 3. 4.
2. Якими ефектами в газі потрібно знехтувати, щоб газ вважати ідеаль-ним?
1. Розмірами молекул.
2. Взаємодією молекул при зіткненні.
3. Взаємодією молекул на відстані.
4. Зіткненнями молекул.
3. Які величини є параметрами стану макросистеми?
1. Температура.
2. Тиск.
3. Число ступенів вільності молекули.
4. Ентропія.
4. Яка з приведених формул являє собою рівняння стану ідеального газу?
1.
![]() 2.
2.![]() 3.
3.![]() 4.
4.![]()
5. Яка з приведених формул виражає основне рівняння кінетичної теорії газів (рівняння Клаузіуса)?
1.
![]() 2.
2.![]() 3.
3.![]() 4.
4.![]()
6. Яка з приведених формул описує розподіл молекул газу за швид-костями?
1.
![]() 2.
2.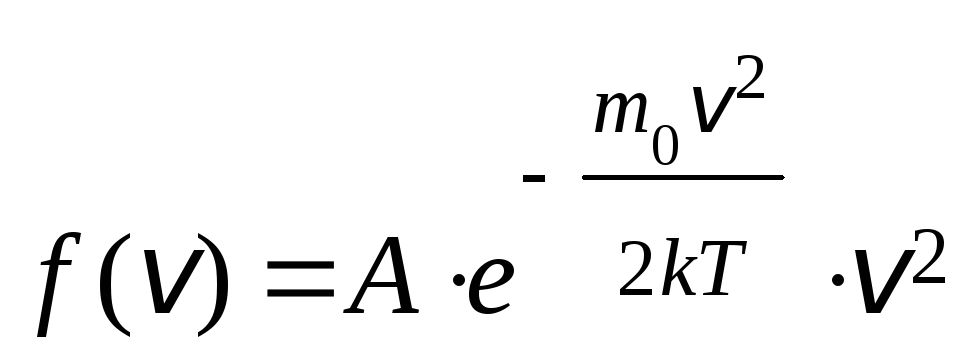 3.
3.![]() 4.
4.![]()
7. Яке співвідношення температур газу, графік розподілу молекул за швидкостями для якого має вид:
1. T1 < T2 < T3
2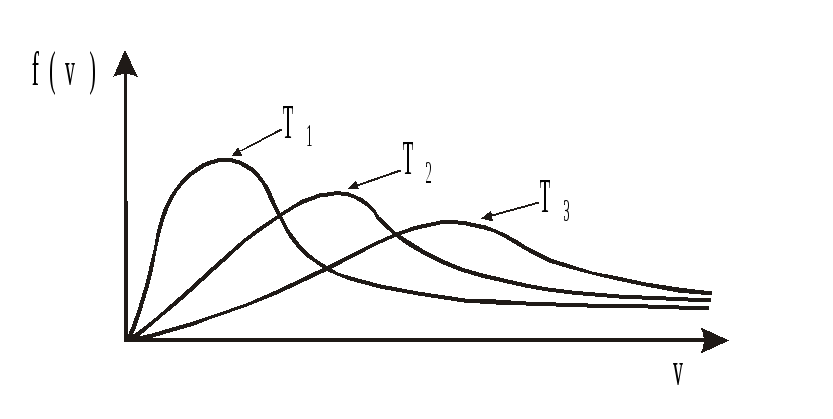 .T1
> T2
> T3
.T1
> T2
> T3
3. T1 > T3 > T2
4. T2 > T1 > T3
8. Які з формул виражають залежність тиску газу від висоти в полі тяжіння Землі?
(m
- маса молекули, M - молярна маса,
![]() -
густина газу)
-
густина газу)
1.
![]() 2.
2.![]() 3.
3.![]() 4.
4.![]()
9. Яка з приведених формул описує розподіл молекул газу по висоті в полі тяжіння Землі?
1.
![]() 2.
2.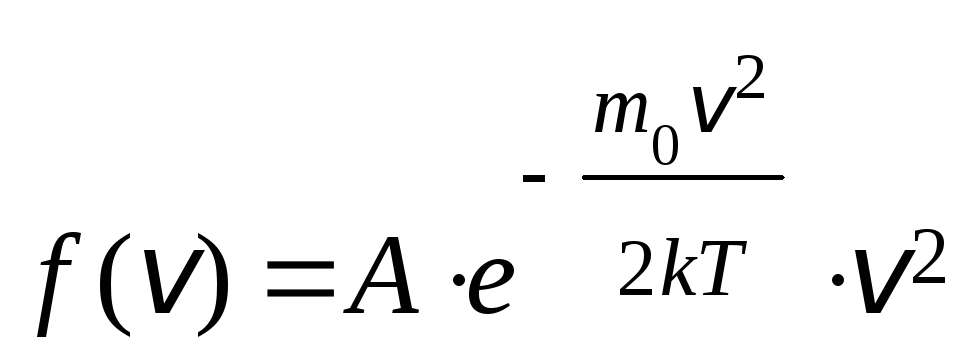 3.
3.
![]() 4.
4.
![]()
10. На рисунку приведені графіки залежності концентрації молекул газу в полі тяжіння від висоти при різних температурах. Яке співвідношення темпе-ратур газу?
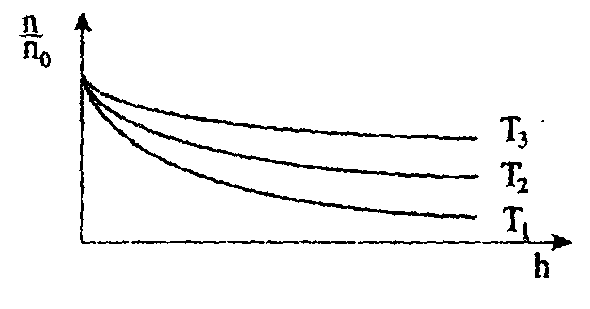
1. T3 < T2 < T1
2. T1 < T2 < T3
3. T3 > T1 > T2
4. T3 < T1 < T2
11. Які з перерахованих видів енергії входять до складу внутрішньої енергії системи?
1. Кінетична енергія руху системи як цілого.
2. Потенціальна енергія взаємодії молекул і атомів системи.
3. Потенціальна енергія системи в зовнішніх полях.
4. Кінетична енергія хаотичного руху молекул і атомів системи.
12. Як залежить внутрішня енергія ідеального газу від температури?
1. U~T
2.
![]() 3.
3.
![]() 4.
4.
![]()
13. Які з перерахованих величин є функцією стану системи?
1. Виконана робота.
2. Ентропія.
3. Внутрішня енергія.
4. Кількість тепла.
14. Що називається кількістю тепла?
1. Міра енергії, переданої тілу при теплопередачі.
2. Енергія тіла за винятком кінетичної енергії тіла як цілого і потен- ціальної енергії тіла в зовнішньому силовому полі.
3. Ступінь нагріву тіла.
4. Кількість енергії, передана одним тілом іншому.
15. Яка з формул є математичним виразом першого закону термодинаміки?
1.
![]() 2.
2.
![]() 3.
3.![]() 4.
4.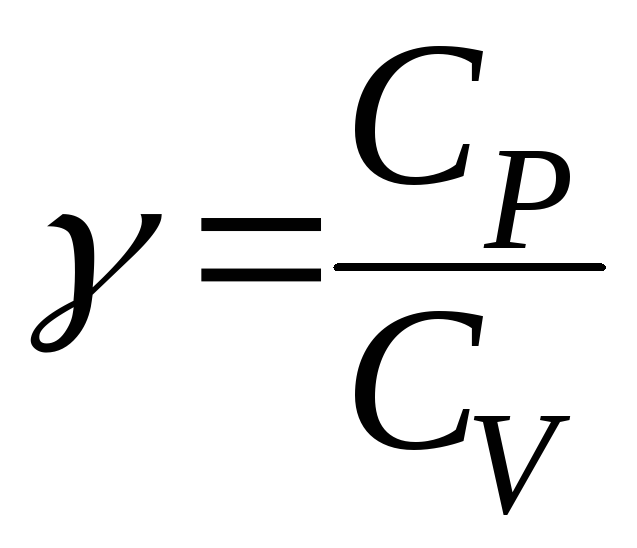
16. Чому дорівнює молярна теплоємність ідеального газу при сталому об'ємі ?
1.
![]() 2.
2.
![]() 3.
3.![]() 4.
4.![]()
17. Чому дорівнює молярна теплоємність ідеального газу при сталому тиску?
1.
![]() 2.
2.
![]() 3.
3.![]() 4.
4.![]()
18. Яке з приведених співвідношень називають рівнянням Роберта Майєра?
1.
![]() 2.
2.![]() 3.
3.![]() 4.
4.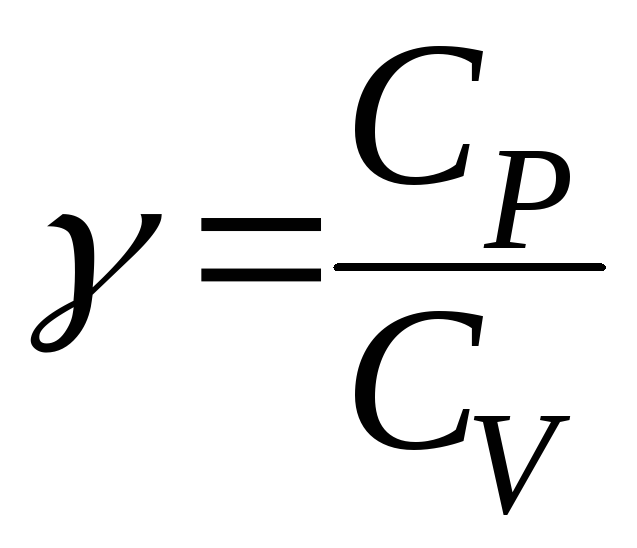
19.Яка з приведених формул зв'язує ентропію з термодинамічною ймо-вірністю?
1.
![]() 2.
2.![]() 3.
3.![]() 4.
4.![]()
20. Для
якого з процесів при m = const виконується
рівність
 ?
?
