
- •Конспект лекцій з фізики
- •Конспект лекцій з фізики
- •Частина 2
- •Кінетична теорія газів
- •Рівняння стану ідеального газу
- •Основне рівняння молекулярно-кінетичної теорії ідеального газу
- •Розподіл молекул за швидкостями
- •Барометрична формула. Розподіл Больцмана частинок у зовнішньому потенціальному полі
- •Фізичні основи термодинаміки
- •Внутрішня енергія системи
- •Робота при зміні об’єму
- •Ступені вільності
- •Принцип рівнорозподілу енергії за ступенями вільності
- •Теплоємність
- •Перший закон термодинаміки
- •Застосування першого закону термодинаміки до газових процесiв
- •Iзобаричний процес
- •Iзотермiчний процес
- •Iзохоричний процес
- •Адіабатний процес
- •Другий закон термодинаміки
- •Ентропія
- •Розрахунок зміни ентропії у процесах ідеального газу
- •Середня довжина вільного пробігу молекул газу
- •Явища переносу
- •Дифузія в газах
- •Внутрішнє тертя у газах
- •Теплопровідність газів
- •Реальні гази
- •Внутрішня енергія реального газу
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Розв’язання
- •Завдання для самостійного контролю знань
- •1. 2. 3. 4.
- •1. Ізобаричного 2. Адіабатичного 3. Ізотермічного 4. Ізохоричного
- •1. Ізотермічного 2. Адіабатичного 3. Ізохоричного 4. Ізобаричного
- •1. Ізотермічного 2. Адіабатичного 3. Ізохоричного 4. Ізобаричного
- •1. Ізотермічного 2. Адіабатичного 3. Ізохоричного 4. Ізобаричного
- •Задачі для самостійного розв’язування
- •Рекомендована література
Розв’язання
Енергія
поступального
руху
молекул
азоту
![]() відкіля
m=2,5г
.Відпо-відно
до
основного
рівняння
MKT
відкіля
m=2,5г
.Відпо-відно
до
основного
рівняння
MKT
![]() (1),
(1),
де
n-
число молекул в одиниці об'єму, m0-
маса однієї молекули. Очевидно, що
добуток nm0=
![]() -густина
азоту. Тоді V
пm0=V
-густина
азоту. Тоді V
пm0=V![]() =m-маса
всього азоту, що знаходиться в балоні.
Помноживши праву і ліву частини рівняння
(1) на V,
одержимо
=m-маса
всього азоту, що знаходиться в балоні.
Помноживши праву і ліву частини рівняння
(1) на V,
одержимо
РV
=
![]() .
.
але
![]() ,
отже
,
отже
m=
2W/![]() .
РV
=
.
РV
=![]() ,
,
відкіля
Р
=![]() .
.
Перевіримо одиниці виміру m і P.
![]()
![]()
Підставимо числові значення й обчислюючи, одержимо:
m=2,5*10-3(кг)
Р=1,67*105=167(кПа)
Відповідь: m=2,5*10-3кг; Р=167кПа.
Задача 6. Знайти питому теплоємність кисню для: а)V=соnst; б)Р=соnst.
Дано: М=32*10-3кг/моль, і=5, R=8,31Дж/мольК.
Визначити: сv і cp.
Розв’язання
Молярна
теплоємність
С
і питома
теплоємність
с зв'язані
співвідношенням
С=Mс.
Відкіля с=С/М.
а) При V=соnst
Сv
=![]() .Для
кисню і=5
, отже , Сv=
.Для
кисню і=5
, отже , Сv=
![]() . Тоді питома теплоємність кисню при
сталому об’ємі с v
=
. Тоді питома теплоємність кисню при
сталому об’ємі с v
=
![]() ;
б) При Р=соnst
Сp=Сv+R=7/2R.
Звідси с p
=
;
б) При Р=соnst
Сp=Сv+R=7/2R.
Звідси с p
=
![]() .
.
Перевіримо одиниці виміру с.
![]()
Підставивши числові значення й обчислюючи, одержимо
сv==650(Дж/кг.К); сp= 910 (Дж/кг.К).
Відповідь: сv=650Дж/кг.К ; сp=910Дж/кг.К.
Задача 7. Знайти питому теплоємність сp газової суміші, що складається з кількості v1=3кмоль аргона і кількості v2=3 кмоль азота.
Дано: v1=v2=3кмоль=3*103моль; М1=40*10-3кг/моль; М2=28*10-3кг/моль; R=8,31Дж/мольК . Визначити сp.
Розв’язання
Кількість
тепла, необхідна
для
нагрівання
суміші
газів
на
деяку
температуру![]() Т
Т
Q=сp(m1+m2)![]() T
T
або
Q=(cp1m1+сp2m2)![]() Т.
Т.
Тоді
сp(m1+m2)![]() Т=(сp1m1+cp2m2)
Т=(сp1m1+cp2m2)![]() T,
T,
звідси
![]() .
.
Оскільки аргон –газ одноатомний, число ступенів волі і=3, a азот-двохатомний ,тому і=5,
то
![]() і
і
![]() .
.
Тоді теплоємність суміші при Р=cоnst:
![]()
Перевіримо одиниці виміру сp.
![]()
Підставивши числові значення й обчислюючи, одержимо:
![]() =733(Дж/кг.К.)
=733(Дж/кг.К.)
Відповідь cp=733Дж/кг.К.
Задача 8. Яка частина молекул азоту при t=150С має швидкості від 300 до 325м/с?
Дано: t=150С, Т=423К; v1=300м/с; v2=325м/с; М=28*10-3кг/моль; R=8,31Дж/моль.К.
Визначити
![]() .
.
Розв’язання
З закону Максвелла маємо
![]() (1),
(1),
де
u = v 1/ v в - відносна швидкість (2)
![]() u=
u=
![]() (3).
(3).
Тут
v
в
=![]() (4)-найбільш
ймовірна швидкість молекул. Вирішуючи
спільно рівняння (1)-(4), одержимо
(4)-найбільш
ймовірна швидкість молекул. Вирішуючи
спільно рівняння (1)-(4), одержимо
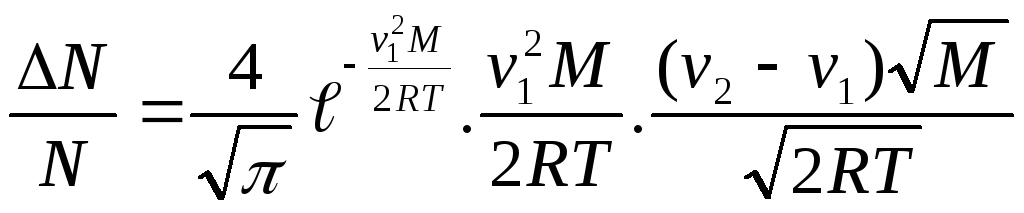
Підставивши числові значення й обчислюючи, одержимо
![]() =2,8%.
=2,8%.
Відповідь![]() =2,8%.
=2,8%.
Задача 9. Яку массу m вуглекислого газу можна нагріти при Р= соnst від температури t1=200 С до t2=100 0С кількістю теплоти Q=222Дж? На скільки при цьому зміниться кінетична енергія однієї молекули?
Дано: Р=соnst; t 1=200C, Т1=293К; t2=1000C, Т2=373К; Q=222Дж.
Визначити: m і W.
Розв’язання
Кількість
тепла
Q=cpm![]() Т.
Т.
Теплоємність при Р=соnst:
![]()
Молярна масса М= Мс+2Мо. Оскільки СО2 - газ трьохатомний, і= 6.
Тоді
![]()
Отже
![]()
виходить,
![]() .
.
Кінетична енергія поступального руху молекул
![]() ,
при
i=6:
W1=3kT1
; W2=3kT2.
,
при
i=6:
W1=3kT1
; W2=3kT2.
Тоді
![]() W=W2-W1=3k(T2-T1).
W=W2-W1=3k(T2-T1).
Перевіримо
одиниці виміру m
і
![]() W.
W.
![]() ;
;![]() .
.
Підставивши числові значення й обчислюючи, одержимо:
m
=![]() =3,67*10-3(кг)=3,67г;
=3,67*10-3(кг)=3,67г;
W=3*1,38*10-23(373-293)=3,31*10-21(Дж).
Відповідь: m=3,67г; W=3,31*10-21Дж.
Задача 10. На якій висоті h густина газу вдвічі менше його густини на рівні моря? Температуру газу вважати сталою і рівною t=0оС. Задачу вирішити для повітря.
Дано: t=00C, Т=273К; М=29*10-3кг/моль ; g=9,8м/с2; R=8,31Дж/моль.К.
Визначити h.
