
- •Міністерство освіти і науки україни
- •Частина і. Термодинаміка
- •1.1 Основи термодинаміки
- •1.1.1 Основні поняття технічної термодинаміки. Основні термодинамічні параметри. Рівняння стану.
- •1.1.2 Газові суміші
- •1.1.3 Калоричні параметри стану
- •1.1.4 Ентропія
- •1.1.4.1 Робота зміни об’єму
- •1.1.5 Робота і теплота
- •1.1.6 Перший закон термодинаміки
- •1.1.7 Теплоємність
- •1.1.8 Теплоємність металів і металовмісних сполук
- •1.1.9 Термодинамічні процеси ідеальних газів у закритих системах
- •Політропний процес
- •1.1.10 Другий закон термодинаміки
- •Цикл Карно
- •1.1.11 Формулювання другого закону термодинаміки
- •1.2 Основи хімічної кінетики
- •1.2.1 Швидкість хімічних реакцій
- •1.2.2 Вплив температури на швидкість хімічних реакцій
- •1.2.3 Хімічна рівновага
- •1.2.4 Константа рівноваги хімічної реакції залежить від температури.
- •1.3 Основи хімічної термодинаміки, поняття хімічної термодинаміки
- •1.3.1 Основи хімічної термодинаміки
- •1.3.2 Закон Гесса і його наслідки
- •1.3.3 Залежність теплового ефекту хімічної реакції від температури. Закон Кірхгофа
- •1.4 Деякі явища в рідних середовищах і на поверхні розподілу фаз
- •1.4.1 Розчинність газів
- •1.4.2 Розподіл компонента між двома рідинами
- •1.4.3 Поверхневий натяг
- •1.4.4 Адсорбція
- •1.4.5 Умова змочування і незмочування рідин
- •1.4.6 Дисоціація окисів
- •2 Теплообмін при зварюванні
- •2.1 Теплопровідність
- •2.1.1 Теплопровідність під час стаціонарного режиму і граничних умов 1 роду
- •2.1.2 Частинні випадки рівняння теплопровідності
- •Крайові умови
- •2.1.3 Теплопровідність за наявності внутрішніх джерел теплоти
- •Необмежена пластина
- •Циліндричний стержень
- •2.1.4 Необмежена плоска стінка
- •2.1.5 Циліндрична стінка
- •2.1.6 Теплопровідність під час стаціонарного режиму і граничних умовах III роду (теплопередача)
- •2.1.7 Теплопередача через плоску стінку
- •Розв'язання
- •2.2 Конвективний теплообмін
- •2.2.1 Основні поняття та визначення конвективного теплообміну
- •2.2.2 Узагальнюючі залежності (рівняння подібності) конвективного теплообміну
- •2.3 Теплообмін випроміненням
- •2.3.1 Основні поняття і визначення
- •2.3.3 Випромінення сірих тіл
- •2.3.4 Теплообмін випроміненням між твердими тілами
- •2.3.5 Теплові екрани
- •2.3.6 Випромінення газів
- •Перелік використаних і рекомендованих джерел
1.4.4 Адсорбція
Частини твердого тіла (атомів, іонів, молекули) утворюють кристалічну гратку. У середині об’єму їх взаємодія врівноважується. На поверхні їх взаємодія не зрівноважена і поверхня твердого тіла прилягає до молекули речовини із газової фази. Явище зростання концентрації речовини на границі розподілу фаз називається – адсорбцією. Поглинаюча речовина називається – адсорбентом, а поглинута речовина – адсорбатом.
Розрізняють адсорбцію фізичну і хімічну. Фізичною називається адсорбція, яка не супроводжується в поверхневому шарі хімічними реакціями. Якщо в результаті адсорбції утворюються хімічні сполуки, то така адсорбція називається хемосорбцією.
Для
того щоб молекула адсорбувалась, вона
повинна ударитись об поверхню і потрапити
на вільне місце. Внаслідок того, що число
ударів пропорційне концентрації С
у довкіллі, то і ймовірність їх потрапляння
на незаняте місце пропорційна цій
конструкції, тобто швидкість адсорбції
 ,
тут:
,
тут:
 -постійна;
-постійна;
 -доля
зайнятих місць на поверхні.
-доля
зайнятих місць на поверхні.
Молекула
може десорбуватись, якщо її енергія
буде достатньою, щоб відірватись від
поверхні. Число таких молекул пропорційне
загальному числу адсорбованих молекул
і швидкість їх з поверхні
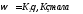 .
.
У
момент рівноваги

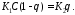
Розв’яжуючи
це рівняння відносно
 ,
отримаємо
,
отримаємо

де

Якщо
позначити кількість речовини, яка
адсорбується на частині поверхні
 черезГ,
то на всій поверхні буде адсорбовано
черезГ,
то на всій поверхні буде адсорбовано
 ,
звідки
,
звідки Підставивши в
Підставивши в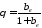 замість
замість його значення отримуємо рівняння
ізотерми Ленгмюра.
його значення отримуємо рівняння
ізотерми Ленгмюра.

З
цього рівняння випливає, що при
 адсорбція досягає насичення
адсорбція досягає насичення .
При
.
При
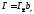 ,
тобто адсорбція описується рівнянням
Генрі.
,
тобто адсорбція описується рівнянням
Генрі.
1.4.5 Умова змочування і незмочування рідин
При
достатньому збільшенні молекул між
ними виникають сили зчеплення. Розрізняють
між молекулярні сили когезії і адгезії
. Когезією — називаються сили притягання
між однаковими молекулами. Під роботою
когезії розуміють роботу розриву
однофазної системи, наприклад,
стовпчика рідини з поперечним перерізом
1 см2
на дві частини. При цьому утворюється
нова поверхня величиною 1 см2,
а зміна вільної поверхні буде дорівнювати
 .
Величина енергії когезії рідин
приблизно дорівнює теплоті випаровування,
а твердих тіл - сублімації.
.
Величина енергії когезії рідин
приблизно дорівнює теплоті випаровування,
а твердих тіл - сублімації.
Сила притягання між різнорідними молекулами, які перебувають в різних фазах, називаються - адгезією. Робота адгезії характеризується роботою, яку необхідно виконати для відокремлення двох фаз з площею контакту 1 см2, при розділі фаз замість однієї границі і розділу між фазами виникали дві поверхні кожної фази. Різниця між сумою нових поверхневих енергій між фазною поверхневою енергією дорівнює роботі адгезії.
Розглянемо умови рівноваги рідини (рисунок 1.9), яка стискається з твердим тілом і газом на границі розділу всіх трьох фаз: рідина Р, газ Г і тверде тіло Т.
Умови розтікання або нерозтікання енергетичними співвідношеннями в системі, тобто величиною між фазної енергії, а також співвідношеннями між адгезією і когезією.
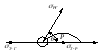

Рисунок 1.9
В точці А тангенціально до поверхні натягу діють такі сили:
 -
поверхневий натяг на границі рідини -
газ;
-
поверхневий натяг на границі рідини -
газ;
 -
поверхневий натяг на границі тверде
тіло - рідині;
-
поверхневий натяг на границі тверде
тіло - рідині;
 -
поверхневий натяг на границі тверде
тіло - газ.
-
поверхневий натяг на границі тверде
тіло - газ.
Сила
 намагається
розтягнути краплю вздовж границі
твердого тіла. В протилежному напрямі
діє сила
намагається
розтягнути краплю вздовж границі
твердого тіла. В протилежному напрямі
діє сила .
Сила, яка діє на границі розділу газ -
рідина, напрямлена по дотичній до
поверхні краплі. Ця дотична утворює з
поверхнею твердого тіла в точці зіткнення
трьох фаз. Кут
.
Сила, яка діє на границі розділу газ -
рідина, напрямлена по дотичній до
поверхні краплі. Ця дотична утворює з
поверхнею твердого тіла в точці зіткнення
трьох фаз. Кут - називається краєвим кутом, або кутом
змочування. Умова рівноваги краплі в
точці визначають рівнянням:
- називається краєвим кутом, або кутом
змочування. Умова рівноваги краплі в
точці визначають рівнянням:
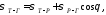
або

Це
рівняння є математичним виразом закону
Лапласа, який формується так: краєвий
кут змочування або
 залежить від молекулярної природи
поверхні розділу і не залежить від
розмірів краплі.
залежить від молекулярної природи
поверхні розділу і не залежить від
розмірів краплі.
Якщо вільна поверхнева енергія на границі тверде тіло-газ більша н ж на границі тверде тіло-рідина, то тверде тіло буде змочуватись рідиною.
Умову змочування можна записати:

У
цьому випадку
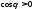 і краєвий кут гострий. При
і краєвий кут гострий. При ,
, ,
тобто відбувається повне змочування.
,
тобто відбувається повне змочування.
Якщо на границі тверде тіло-рідина вільна поверхнева енергія більша, ніж на границі тверде тіло-газ, то рідина розділятися не буде, це можна виразити нерівністю:

При
цьому
 і
краєвий кут тупий. Крапля не розділяється
і змочує поверхню твердого тіла. Повна
незмочуваність характеризується
і
краєвий кут тупий. Крапля не розділяється
і змочує поверхню твердого тіла. Повна
незмочуваність характеризується і
і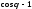 .
.
