
- •Основи молекулярної фізики і термодинаміки §28. Статистичний і термодинамічний методи дослідження. Термодинамічні параметри. Рівноважний стан і процеси
- •§29. Рівняння молекулярно-кінетичної теорії ідеального газу для тиску
- •§30. Середня кінетична енергія молекул. Молекулярно-кінетичне трактування абсолютної температури
- •§31. Розподіл Максвелла молекул ідеального газу за швидкостями теплового руху
- •§32. Барометрична формула. Розподіл Больцмана частинок у зовнішньому потенціальному полі
- •§33. Закон рівномірного розподілу енергії за ступенями вільності молекул
- •§34. Перший закон термодинаміки. Робота газу при зміні його об’єму
- •Пулюй іван
- •Шіллер микола миколайович
- •§35. Теплоємність. Класична молекулярно-кінетична теорія теплоємностей ідеального газу та її обмеженість
- •§36. Застосування першого закону термодинаміки до ізопроцесів
- •Ізохорний процес .
- •Ізобарний процес.
- •Ізотермічний процес.
- •§37. Адіабатний процес. Політропний процес
- •§38. Середнє число зіткнень і середня довжина вільного пробігу молекул
- •§39. Явища перенесення у термодинамічно нерівноважних системах
- •1. Дифузія у газах
- •2. Теплопровідність газів
- •3. Внутрішнє тертя у газах
- •Пулюй іван павлович
- •§40. Коловий процес. Теплові двигуни і холодильні машини. Оборотні I необоротні процеси
- •§41. Цикл Карно I його коефіцієнт корисної дії для ідеального газу
- •§42. Ентропія. Ентропія ідеального газу
- •§43. Ентропія і термодинамічна ймовірність
- •§44. Другий і третій закони термодинаміки
- •§45. Реальні гази. Рівняння Ван-дер-Ваальса
- •1. Врахування власного об’єму молекул
- •2. Врахування притягання молекул
- •§46. Порівняння ізотерм Ван-дер-Ваальса з експериментальними. Критичний стан
- •Авенаріус михайло петрович
- •Надєжкін олександр іванович
- •§47. Внутрішня енергія реального газу
§31. Розподіл Максвелла молекул ідеального газу за швидкостями теплового руху
Завдяки безладним рухам молекул і завдяки взаємним зіткненням молекул під час цього руху кожна молекула зокрема може змінювати свою швидкість як за величиною, так і за напрямком. Тому в газі будуть як швидкі, так і повільні молекули. Але, хоча швидкості окремих молекул змінюються, властивості газу у стані термодинамічної рівноваги загалом при цьому не змінюються: параметри системи залишаються сталими. Зумовлено це тим, що швидкості газових молекул підлягають певному законові, тобто, незважаючи на повну хаотичність молекулярних рухів, розподіл молекул за швидкостями виявляється не випадковим, а цілком визначеним. До того ж він є однозначним і єдино можливим.
Дж. Максвелл
теоретично розв’язав задачу про розподіл
молекул ідеального газу за швидкостями
поступального руху. Він встановив закон,
що дає змогу визначити, яка кількість
молекул dnіз загальної кількостіnмолекул ідеального газу в одиниці об’єму
мають при даній температурі швидкості,
які лежать в інтервалі від![]() до
до![]() .
Дж. Максвелл вважав,
що газ складається з великої кількостіnоднакових молекул, температура в
усіх частинах посудини з газом теж
однакова і відсутні зовнішні дії на
газ.
.
Дж. Максвелл вважав,
що газ складається з великої кількостіnоднакових молекул, температура в
усіх частинах посудини з газом теж
однакова і відсутні зовнішні дії на
газ.
Якщо
розбити діапазон швидкостей молекул
на нескінченно малі інтервали, які
дорівнюють
![]() ,
то на кожний інтервал швидкості
припадатиме деяка кількість молекул
,
то на кожний інтервал швидкості
припадатиме деяка кількість молекул![]() ,
що мають швидкість в інтервалі
,
що мають швидкість в інтервалі![]() .
.
Закон
Максвелла описується деякою функцією
![]() ,
що називається
функцією
розподілу молекул за швидкостями
руху.Ця функція визначає відносну
кількість молекул
,
що називається
функцією
розподілу молекул за швидкостями
руху.Ця функція визначає відносну
кількість молекул![]() ,
швидкості яких лежать в інтервалі від
,
швидкості яких лежать в інтервалі від![]() до
до![]() ,
тобто
,
тобто
![]() ,
звідси
,
звідси
![]() .
.
Добуток
![]() – це ймовірність того, що величина
швидкості окремої молекули знаходиться
між
– це ймовірність того, що величина
швидкості окремої молекули знаходиться
між![]() і
і![]() .
.
Застосовуючи
методи теорії ймовірності, Максвелл
знайшов функцію
![]() у такому вигляді:
у такому вигляді:
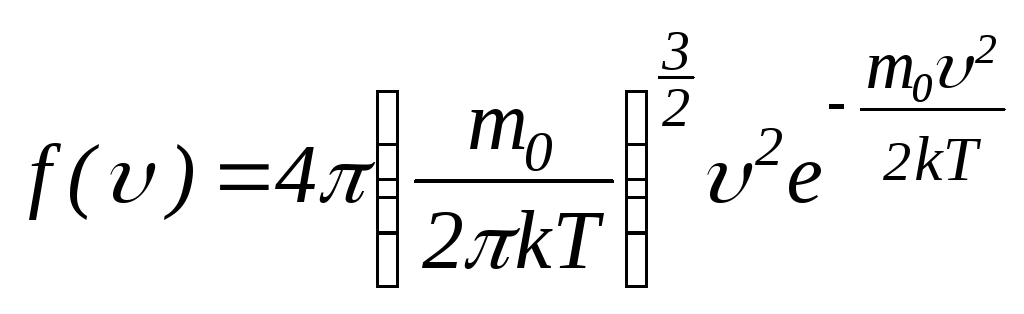 .
.
Конкретний
вигляд функції залежить від роду газу
![]() і від параметра стану
і від параметра стану![]() .
Графік функції
.
Графік функції![]() наведений на рис. 55.
Функція
наведений на рис. 55.
Функція![]() починається від нуля, досягає максимуму,
а потім асимптотично прямує до нуля.
Крива несиметрична відносно максимального
значення
починається від нуля, досягає максимуму,
а потім асимптотично прямує до нуля.
Крива несиметрична відносно максимального
значення![]() .
Відносна кількість молекул
.
Відносна кількість молекул![]() ,
швидкості яких лежать в інтервалі від
,
швидкості яких лежать в інтервалі від![]() до
до![]() ,
числово дорівнює площі заштрихованої
ділянки на рис. 55.
,
числово дорівнює площі заштрихованої
ділянки на рис. 55.

Вся площа, обмежена кривою розподілу і віссю абсцис, числово дорівнює числу молекул, швидкості яких мають різні значення від 0до ∞. Оскільки цю умову задовольняють всіnмолекул, то площа, що розглядається, дорівнює одиниці:
![]() .
.
Швидкість,
при якій
![]() максимальна,називається
найімовірнішою швидкістю
максимальна,називається
найімовірнішою швидкістю ![]() .
Для знаходження
.
Для знаходження![]() використаємо умову максимуму функції
використаємо умову максимуму функції![]() :
:
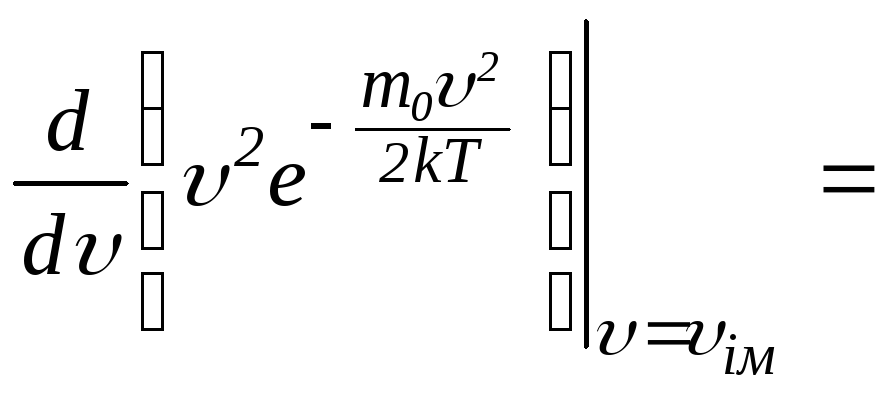
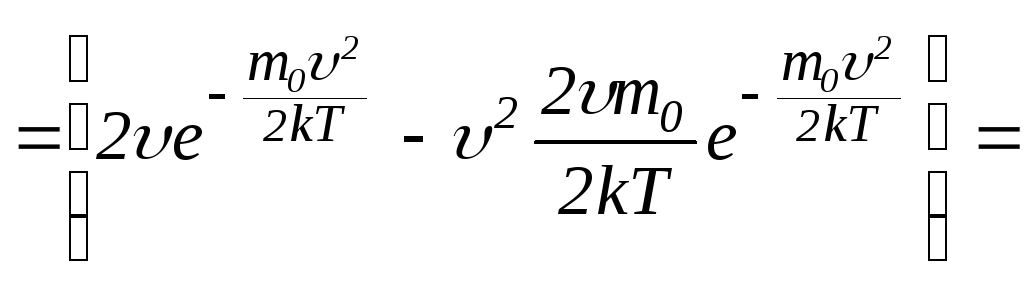
 .
.
Звідси,
![]() ,
,
оскільки
![]() ,
,
![]() .
.
Середня
арифметична швидкість молекул
![]() визначається за формулою
визначається за формулою
![]() .
.
Підставляючи
сюди
![]() й інтегруючи, отримаємо
й інтегруючи, отримаємо
![]() .
.
Отже, є три швидкості, які характеризують стан газу (рис. 55):
найімовірніша
![]() ;
;
середня арифметична
![]() ;
;
середня квадратична
![]() .
.
При
збільшенні температури (або зменшенні
маси молекул) максимум кривої
![]() зміщується у бік більших швидкостей, а
його абсолютна величина зменшується,
причому площа, яка охоплена кривою
зміщується у бік більших швидкостей, а
його абсолютна величина зменшується,
причому площа, яка охоплена кривою![]() і віссю
і віссю![]() ,
залишається незмінною (рис. 56).
,
залишається незмінною (рис. 56).

На
рис. 56 наведено дві
криві розподілу, які відповідають
температурам![]() і
і![]() для молекул одного газу або масам
для молекул одного газу або масам![]() і
і![]() молекул різних газів при однаковій
температурі.
молекул різних газів при однаковій
температурі.
Закон
Максвелла зручно формулювати, ввівши
відносну швидкість
![]() ,
де
,
де![]() – дана швидкість, а
– дана швидкість, а![]() – найімовірніша швидкість для молекул
даного газу при даній температурі.
– найімовірніша швидкість для молекул
даного газу при даній температурі.
Розподіл,
який визначає кількість молекул, відносні
швидкості яких лежать в межах від
![]() до
до![]() ,
має такий вигляд:
,
має такий вигляд:
![]() .
.
Знайдемо середню відносну швидкість молекул ідеального газу:
 ,
,
де
![]() – середня арифметична швидкість.
– середня арифметична швидкість.
Виходячи із розподілу молекул за швидкостями
 ,
,
можна
знайти розподіл молекул за значеннями
кінетичної енергії поступального руху.
Для цього перейдемо від змінної
![]() до змінної
до змінної![]() .
Звідси
.
Звідси
![]() і
і
![]() .
.
Підставимо
ці вирази у
![]() .
У результаті отримуємо співвідношення,
яке визначає кількість молекул, кінетична
енергія поступального руху яких має
значення, які лежать в межах від
.
У результаті отримуємо співвідношення,
яке визначає кількість молекул, кінетична
енергія поступального руху яких має
значення, які лежать в межах від![]() до
до![]() :
:
![]()
![]() .
.
