
02.Углеводороды
.pdf
Сульфирование. Замещение атома водорода в бензольном ядре на сульфогруппу – SO3H осуществляют действием на бензол и его гомологи концентрированной серной кислоты или дымящей серной кислоты (олеума). В результате реакции образуются аренсульфокислоты:
|
|
|
|
|
SO3H |
||
+ H2SO4 |
|
|
|
|
|
|
+ H2O |
|
|
|
|
|
|
||
|
|
||||||
|
|
|
|
|
|
||
|
|
|
|
бензолсульфокислота |
|||
2.6.4.2. РЕАКЦИИ ПРИСОЕДИНЕНИЯ
Для ароматических углеводородов реакции присоединения не являются характерными. Однако в жестких условиях они все же происходят.
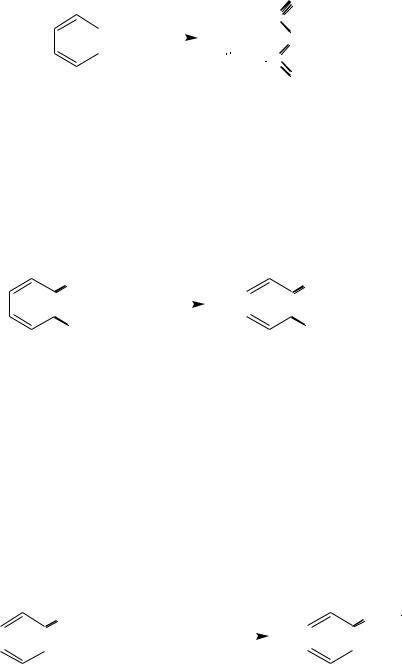
Гидрирование. При повышенных температуре и давлении, в присутствии катализаторов, из которых чаще применяют мелкопористый никель (никель Ренея), бензол и его гомологи присоединяют три молекулы водорода, образуя циклогексан и его производные:
Ni
+ 3H2
бензол |
циклогексан |
Хлорирование. При интенсивном солнечном освещении или под действием ультрафиолетового излучения бензол присоединяет хлор. Реакция протекает по радикальному механизму с образованием 1,2,3,4,5,6- гексахлорциклогексана (гексахлорана), который отщепляет хлористый водород, давая 1,3,5-трихлорбензол:
|
|
|
Cl |
|
|
Cl |
|
hv |
Cl |
Cl |
|
|
|
|
|
|
|
|
|
|
+ |
3Cl2 |
|
|
- 3HCl |
|
|
|
|
Cl |
Cl |
Cl |
Cl |
|
|
|
|
||||
|
|
|
Cl |
|
|
|
бензол |
1,2,3,4,5,6-гексахлорциклогексан |
1,3,5-трихлорбензол |
||||
2.6.4.3. РЕАКЦИИ ОКИСЛЕНИЯ
Окисление бензольного цикла. Бензольное кольцо очень устойчиво к действию окислителей. В обычных условиях такие сильные окислители, как перманганат калия, азотная кислота, оксид хрома (VI), пероксид водорода не окисляют бензол. Но в жестких условиях, например при действии кислорода воздуха в присутствии оксида ванадия (V) в качестве катализатора, при температуре 400 500 оС бензол окисляется, образуя малеиновый ангидрид:
68
|
|
|
|
|
|
|
|
O |
|
|
|
O2; V2O5 |
|
CH |
|
C |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
O + 2CO2 + H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
CH |
|
C O |
||
|
|
|
|
|
||||
бензол |
малеиновый ангидрид |
|||||||
Окисление гомологов бензола. Алкилбензолы, в отличие от незамещенного бензола, окисляются значительно легче. В этом случае при действии сильных окислителей (KMnO4, K2Cr2O7 и др.) подвергаются окислению боковые цепи. Продуктами окисления являются ароматические карбоновые кислоты. Причем каждый алкильный радикал в бензольном кольце, независимо от длинны углеродной цепи, окисляется в карбоксильную группу:
|
|
CH3 |
[ O ] |
|
|
|
COOH |
|
|
CH2CH3 |
|
|
|
|
+ H2O + CO2 |
|
|
|
|||||
|
|
|
|
|
|
COOH |
|
о-этилтолуол |
|
|
фталевая кислота |
||||
2.6.4.4.ГАЛОГЕНИРОВАНИЕ ГОМОЛОГОВ БЕНЗОЛА
СУЧАСТИЕМ БОКОВОЙ ЦЕПИ
Взаимодействие гомологов бензола с галогенами (хлор или бром) в условиях свободнорадикального замещения осуществляется с участием боковой цепи. При этом на атом галогена замещается, как правило, атом водорода при углероде, непосредственно связанном с бензольным кольцом:
|
|
|
|
|
|
|
|
Cl |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2CH3 |
|
hv |
|
|
|
CH |
|
CH3 |
|
|
|
|
|
|
|
|
|||||
|
|
+ |
Cl2 |
|
|
|
|
|
|
|
+ HCl |
|
|||||||||||
этилбензол |
|
|
|
1-хлорэтилбензол |
|||||||
2.6.5. НАПРАВЛЯЮЩЕЕ ДЕЙСТВИЕ ЗАМЕСТИТЕЛЕЙ В БЕНЗОЛЬНОМ КОЛЬЦЕ НА ПРОТЕКАНИЕ РЕАКЦИЙ
ЗАМЕЩЕНИЯ В ПРОИЗВОДНЫХ БЕНЗОЛА
2.6.5.1.ОРИЕНТАЦИЯ В МОНОЗАМЕЩЁННЫХ БЕНЗОЛАХ
Вмолекуле незамещенного бензола электронная плотность распределена равномерно, а поэтому входящий реагент может атаковать в равной степени любой из шести атомов углерода. Если в бензольном кольце содержится какой-
либо заместитель, то под его влиянием происходит перераспределение -
69
электронной плотности цикла и новая группа вступает уже в строго определенные положения по отношению к имеющемуся заместителю.
В зависимости от природы действующего реагента реакции замещения в бензольном кольце могут быть разделены на два типа:
1)реакции электрофильного замещения (алкилирование, галогенирование, нитрование и др.);
2)реакции нуклеофильного замещения (гидроксилирование (с NaOH),
аминирование (с NaNH2) и др.)
По влиянию на направление реакций замещения и реакционную способность производных бензола заместители, содержащиеся в бензольном кольце, также можно разделить на две группы:
1. Заместители I рода. По индуктивному эффекту, как правило, слабо
стягивают на себя электронную плотность с бензольного кольца ( I), по эффекту сопряжения нагнетают (+М), причем нагнетают значительно сильнее, чем стягивают. Результирующее действие нагнетание электронной плотности на бензольное кольцо. Такие заместители называются электронодонорными. К ним относятся:
O |
|
; |
|
NR ; |
|
NHR ; |
|
NH ; |
|
OH ; |
|
OR ; |
|
NHCOR ; |
|
OCOR ; |
|
R |
|
|
|
|
|
|
|
|
|||||||||||
|
2 |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
||||
|
:NH |
|
2 |
|
|
|
|
- I + M
Заместители I рода
-нагнетают электронную плотность в бензольное кольцо;
-облегчают (в сравнении с бензолом) реакции электрофильного замещения и направляют их в орто- и пара-положения:
|
NH2 |
|
|
NH2 |
NH2 |
|||||||||
2 |
|
|
|
+ 2X+ |
|
|
|
|
|
X + |
|
|
|
+ 2H+ ; |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
X
- затрудняют (в сравнении с бензолом) реакции нуклеофильного замещения
инаправляют их в мета-положения.
Кзаместителям (ориентантам) I рода относят также галогены:
F; Cl; Br; I.
70
Ориентирующая способность галогенов совпадает с ориентирующей способностью заместителей I рода, однако влияние галогенов на реакционную способность кольца противоположно влиянию заместителей I рода. Это объясняется наличием у атомов галогенов наряду с большим положительным мезомерным эффектом (+ М) большого отрицательного индуктивного эффекта ( I). Таким образом галогены затрудняют реакции электрофильного замещения, но направляют их в орто- и пара-положения, облегчают реакции нуклеофильного замещения, но направляют их в мета- положения.
2. Заместители II рода. И по индуктивному ( I), и по эффекту сопряжения ( М) стягивают электронную плотность с бензольного кольца. Такие заместители называются электроноакцепторными. К ним относятся:
+ |
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
O |
; |
|
NR3 ; |
|
NH3 ; |
|
|
NO2 ; |
|
|
SO3H ; |
|
C |
|
|
N ; |
|
C H ; |
|
C R |
||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
O |
|
|
|
O |
|
|
O |
|
|
|
|||||||||||
C OH ; |
|
|
C |
OR ; |
|
C |
NH2 . |
|
|
|
|||||||||||
|
|
|
|
|
|
||||||||||||||||
NО2 |
|
|
|
|
|
|
- I - M |
Заместители II рода
-стягивают электронную плотность с бензольного кольца;
-затрудняют (в сравнении с бензолом) реакции электрофильного замещения и направляют их в мета-положения:
NO2 |
NO2 |
+ X+ |
+ H+ ; |
|
X |
- облегчают (в сравнении с бензолом) реакции нуклеофильного замещения и направляют их в орто- и пара-положения.
Описанная выше ориентация замещения не является абсолютной, а указывает лишь на наиболее предпочтительное направление протекания реакции. Так, при нитровании нитробензола образуется 93% мета-, 6% орто- и 1% пара-динитробензола.
2.6.5.2. ОРИЕНТАЦИЯ В ДИЗАМЕЩЁННЫХ БЕНЗОЛАХ
При наличии в бензольном кольце двух заместителей их ориентирующее влияние осуществляется более сложно, но и в этом случае часто можно правильно предсказать предпочтительное место вхождения нового заместителя.
71

В зависимости от электронной природы заместителей и их взаимного расположения различают согласованную и несогласованную ориентацию.
При согласованной ориентации оба имеющихся заместителя направляют новую группу в одни и те же положения бензольного кольца.
Согласованная ориентация характерна для дизамещенных бензола, в которых соблюдается два условия:
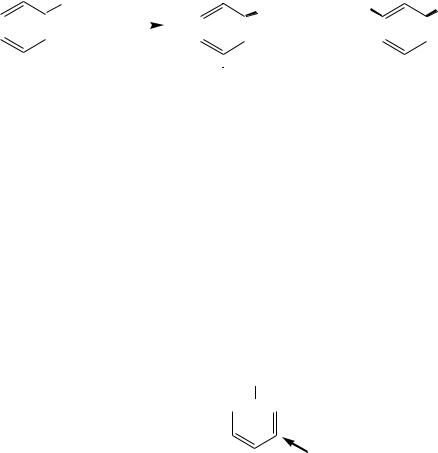
1. Заместители находятся в мета-положении относительно друг друга и принадлежат к ориентантам одного и того же рода (предпочтительные места вхождения нового заместителя указаны стрелками):
CH3 |
NO2 |
OH |
SO3H |
|
|
м-метилфенол |
м-нитробензолсульфокислота |
2. Заместители находятся в орто- или пара-положении по отношению друг к другу, но один из них является ориентантом I рода, а второй - ориентантом II рода
|
OH |
COOH |
|
OH |
|
|
NO2 |
о-гидроксибензойная кислота |
п-нитрофенол |
(салициловая кислота) |
|
При несогласованной ориентации один из заместителей направляет новую группу в одни, а другой – в иные положения бензольного кольца. В результате,
как правило, образуется несколько различных изомеров. Вместе с тем предпочтительное направление замещения можно определить, используя следующие правила.
1. Если один из заместителей является ориентантом I рода, преимущественное направление замещения определяет ориентант I рода:
OH |
OCH3 |
NO2 |
NO2 |
м-нитрофенол |
м-метоксинитробензол |
72
2. Если оба заместителя являются ориентантами I рода, преимущественное направление замещения определяется более сильным ориентантом. По силе ориентирующего влияния заместители I рода можно расположить в следующий ряд:
O‾ > NR2 > NHR > NH2 > OH > OR > NHCOR > OCOR > Alk > F > Cl > Br > I
Например, при нитровании 2-бромфенола образуется преимущественно 2-бром-4-нитрофенол и 2-бром-6-нитрофенол:
|
OH |
|
|
OH |
|
OH |
|||||||||
|
|
|
|
Br |
2 HNO3 |
|
|
|
|
Br |
O2N |
|
|
|
Br |
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
2 |
|
|
|
|
|
|
|
|
+ |
|
|
|
|
+ 2H2O |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NO2 |
|
|
|
|
|
|||
2-бромфенол |
|
2-бром-4-нитрофенол |
2-бром-6-нитрофенол |
||||||||||||
3. Если оба заместителя являются ориентантами II рода, электрофильное замещение осуществляется с большим трудом, а преимущественное место вхождения третьего заместителя определяется более сильным ориентантом. По силе ориентирующего влияния в реакциях SE заместители II рода можно расположить в следующий ряд:
COOH > SO3H > NO2 > CHO > COCH3 > CN
Например, в о-нитробензойной кислоте замещение идѐт преимущественно в мета-положение относительно карбоксильной группы:
COOH
O2N

о - нитробензойная кислота
Наряду с электронной природой заместителей на соотношение продуктов замещения оказывают существенное влияние пространственные факторы. При прочих равных условиях из-за стерических препятствий маловероятно вхождение третьей группы между двумя уже присутствующими заместителями.
73
