
02.Углеводороды
.pdf
Уникальность подобранного Лебедевым катализатора состоит в том, что он катализирует каждую стадию процесса: во-первых, способствует дегидрированию этанола с образованием этаналя, во-вторых, будучи щелочным, вызывает альдольную конденсацию образовавшегося этаналя, в- третьих, катализирует гидрирование альдегидной группы и, наконец, облегчает дегидратацию образовавшегося при этом диола. Таким образом, разностороннее действие катализатора Лебедева позволяет за один проход паров этанола над катализатором превратить этанол в дивинил.
Из муравьиного альдегида и ацетилена (способ Реппе). Метод включает конденсацию двух молекул муравьиного альдегида с ацетиленом, гидрирование образовавшегося бутиндиола до бутандиола и отщепление двух молекул воды от последнего:
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
OH |
|
|
|
|
|
|
|
|
|
|
OH |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
C |
|
|
O + H |
|
|
C |
|
C |
|
|
H + O |
|
|
C |
|
|
|
|
CH2 |
|
|
C |
|
|
|
|
C |
|
CH2 |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
H |
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
муравьиный |
ацетилен |
|
|
|
|
|
|
|
|
|
|
|
|
|
бутин-2-диол-1,4 |
||||||||||||||||||||||||||||
|
|
альдегид |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
2 H2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2SO4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
CH2 |
|
|
CH2 |
|
|
CH2 |
|
CH2 |
CH2 |
|
|
|
CH |
|
|
|
CH |
|
CH2 |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
Ni |
|
|
|
|
|
- 2 H2O |
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
бутандиол-1,4 |
|
|
|
|
|
|
|
|
|
|
|
|
бутадиен-1,3 |
||||||||||||||||||||
Из ацетилена через винилацетилен. Метод заключается в избирательном гидрировании винилацетилена, образующегося при димеризации ацетилена:
|
|
|
Cu Cl |
|
|
|
|
|
|
|
H2 |
|
|
|
|
|
|
|
|
|
|||
2 HC |
|
CH |
2 |
2 |
CH2 |
|
CH |
|
C |
|
CH |
|
|
CH2 |
|
|
CH |
|
CH |
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
Ni Ренея |
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
ацетилен |
|
|
|
|
винилацетилен |
|
|
|
|
|
бутадиен-1,3 |
||||||||||||
2.4.2.2. ПОЛУЧЕНИЕ 2-МЕТИЛБУТАДИЕНА-1,3 (ИЗОПРЕНА)
Каталитическое дегидрирование изопентан-изопентеновой фракции нефти. Реакция протекает в присутствии смешанного алюмохромового катализатора Cr2O3 / Al2O3 при температуре 550 оС:
CH3 |
|
|
CH |
|
|
CH2 |
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
CH3 |
|
|
|
|
|
t, кат. |
2 CH2 |
|
C |
|
CH |
|
|
CH2 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
2-метилбутан (изопентан) |
|
|
|
|
|
||||||||||||||||||||
- 3 H2 |
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
CH |
|
|
CH |
|
|
CH2 |
|
|
|
|
|
CH3 |
|
|
|
||||||
|
|
|
|
|
|
|
2-метилбутадиен-1,3 (изопрен) |
||||||||||||||||||
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
3-метилбутен-1(изопентен) |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
48

Из ацетона и ацетилена (метод А.Е. Фаворского):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
KOH |
|
|
|
OH |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
CH3 |
|
C |
|
O |
+ H |
|
C |
|
|
|
|
C |
|
H |
|
|
|
|
|
CH3 |
|
C |
|
C |
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||||||||||||||||||||||
|
|
ацетон |
|
|
|
|
|
ацетилен |
|
|
|
|
|
2-метилбутин-3-ол-2 |
|||||||||||||||||||||||||||||||||||||
|
|
|
H2 |
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
CH3 |
|
|
|
C |
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
C |
|
CH |
|
|
CH2 |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
(электро-химическое |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- H2O |
|
|
||||||||||||||||||||||||||||||
|
гидрирование) |
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
2-метилбутен-3-ол-2 |
|
|
|
|
|
|
2-метилбутадиен-1,3 |
|||||||||||||||||||||||||||||||||
2.4.2.3. ПОЛУЧЕНИЕ 2-ХЛОРБУТАДИЕНА-1,3 (ХЛОРОПРЕНА)
Хлоропрен получают гидрохлорированием винилацетилена,
образующегося при димеризации ацетилена:
|
|
|
Cu2Cl2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
HCl |
|
|
|
|
|
|
|
|
|
CH2 |
||
2 HC |
|
CH |
|
|
CH2 |
|
CH |
|
C |
|
|
|
CH |
|
CH2 |
|
|
CH |
|
C |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
ацетилен |
|
|
|
винилацетилен |
|
|
|
|
хлоропрен |
|||||||||||||||
2.4.3. ХИМИЧЕСКИЕ СВОЙСТВА АЛКАДИЕНОВ С СОПРЯЖЕННЫМИ ДВОЙНЫМИ СВЯЗЯМИ
Для алкадиенов с сопряженными двойными связями характерны реакции присоединения и полимеризации, свойственные алкенам. Однако наряду с этим в химическом поведении алкадиенов-1,3 имеются некоторые особенности. Вопервых, по сравнению с алкенами алкадиены с сопряженными двойными связями проявляют более высокую реакционную способность. Во-вторых, в реакциях электрофильного присоединения чаще всего образуется два продукта, из которых один является результатом присоединения по месту двойной связи (1,2-присоединение), а второй – по концам сопряженной системы (1,4- присоединение). Соотношение этих продуктов зависит от условий проведения реакции (температура, растворитель), а также от природы электрофильного реагента.
Гидрирование. В присутствии катализаторов (Ni, Pt) алкадиены-1,3 присоединяют водород в 1,2- и 1,4-положения с образованием соответствующих алкенов, которые подвергаются дальнейшему гидрированию до алканов:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
CH |
|
|
CH2 |
|
|
CH3 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2 |
|
|
|
|
|
|
|
|
|
||||||||||
2 CH2 |
|
|
CH |
|
CH |
|
|
|
CH2 |
|
|
|
|
|
|
|
бутен-1 |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
кат. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
бутадиен-1,3 |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
CH |
|
|
CH |
|
|
|
CH3 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
бутен-2 |
|
|
|
|||||
|
H2 |
|
|
2 CH3 |
|
|
|
CH2 |
|
|
CH2 |
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
кат. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
бутан
49

Присоединение галогенов. Присоединение галогенов к алкадиенам с сопряженными двойными связями приводит к образованию смеси продуктов 1,2- и 1,4-присоединения, состав которой зависит от природы галогена, структуры диенового углеводорода и условий проведения реакции. Как правило, при повышении температуры и переходе от хлора к йоду возрастает выход продукта 1,4-присоединения. Например, в процессе бромирования бутадиена-1,3 при температуре –80 °С образуется преимущественно продукт 1,2-присоединения (3,4-дибромбутен-1), а при 40 °С образуется преимущественно продукт 1,4-присоединения (1,4- дибромбутен-2):
|
|
|
|
|
|
|
|
Br Br |
Br |
|
|
|
|
|
|
Br |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 CH2 |
|
CH |
|
CH |
|
CH2 + 2 Br2 |
|
CH2 |
|
CH |
|
CH |
|
|
CH2 |
+ CH2 |
|
CH |
|
|
CH |
|
CH2 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
бутадиен-1,3 |
|
|
3,4-дибромбутен-1 |
|
|
1,4-дибромбутен-2 |
|||||||||||||||||||
Аналогично алкенам присоединение галогенов к алкадиенам с сопряженными двойными связями происходит по ионному электрофильному механизму. Особенность механизма состоит в том, что электрофильная
частица всегда атакует концевой атом углерода сопряженной системы,
поскольку при этом образуется мезомерно стабилизированный карбкатион, строение которого можно представить граничными структурами I и II:
CH2 |
|
CH |
|
CH |
|
CH2 + Br2 |
|
|
CH2 |
|
|
CH |
|
|
CH |
|
|
|
CH2 |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
- Br |
- |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
|
|
Br |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- комплекс |
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
CH2 |
|
|
CH |
|
CH |
|
CH2 |
|
|
|
|
|
|
CH2 |
|
|
CH |
|
|
CH |
|
CH2 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
Br |
|
|
I |
|
|
|
|
|
Br |
|
|
|
II |
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Последующая атака карбкатиона бромидионом приводит к образованию продуктов 1,2- (III) и 1,4-присоединения (IV):
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
CH |
|
|
CH |
|
|
CH2 |
|
Br- |
|
CH2 |
|
|
|
|
CH |
|
|
CH |
|
|
CH2 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Br |
|
|
|
I |
+ |
|
|
|
|
Br |
Br |
III |
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
CH |
|
|
CH |
|
|
CH2 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
CH2 |
|
CH |
|
|
CH |
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
Br |
|
|
|
II |
|
|
|
|
|
|
|
|
Br |
|
|
|
|
|
IV |
|
Br |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Присоединение галогеноводородов. Как и в случае галогенирования,
присоединение к сопряженным диенам галогеноводородов происходит с образованием продуктов 1,2- и 1,4-присоединения:
50
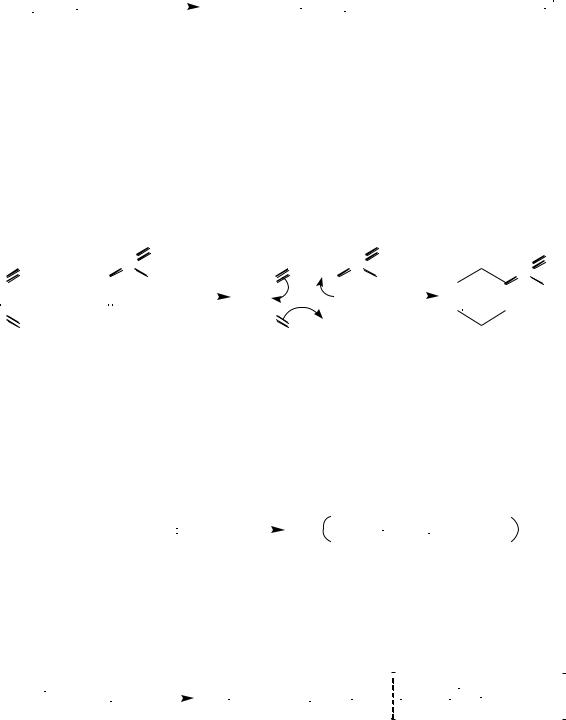
|
|
|
|
|
|
|
2 HCl |
|
|
Cl |
|
|
|
|
|
|
Cl |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
2 CH2 |
|
CH |
|
CH |
|
CH2 |
CH3 |
|
CH |
|
CH |
|
CH2 + CH3 |
|
CH |
|
CH |
|
CH2 |
||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
3-хлорбутен-1 |
|
|
1-хлорбутен-2 |
||||||||||
Реакция Дильса–Альдера (диеновый синтез). Сопряженные диены взаимодействуют с веществами, имеющими в своем составе активированную двойную или тройную углерод-углеродную связь (диенофилами). Кратная связь называется активированной, когда она находится в сопряжении с электроноакцепторной или электронодонороной группой (CN, NO2, CHO, COR, COOH, COOR, галогены, OR и др.). В процессе реакции сопряженные диены присоединяют диенофилы в положения 1,4 с образованием циклических структур:
|
|
|
|
|
|
|
C |
O |
|
|
|
|
|
|
|
C |
O |
|
|
|
|
|
O |
|
|
CH |
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
C |
|||
|
|
2 |
|
|
|
H |
|
|
|
2 |
|
|
H |
|
|
|
|
|
|||||
HC |
|
CH |
t |
HC |
CH |
|
|
|
|
H |
|||||||||||||
|
|
+ |
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HC |
CH2 |
|
CH2 |
|
|
HC |
CH2 |
CH2 |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
тетрагидробензойный |
||||||||||||||||||
|
|
|
акролеин |
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
бутадиен-1,3 |
|
(диенофил) |
|
|
|
|
|
|
|
|
|
|
|
|
альдегид |
|
|||||||
Полимеризация. Важным свойством алкадиенов с сопряженными двойными связями является их склонность к полимеризации. В качестве инициаторов полимеризации применяют органические и неорганические пероксиды, металлоорганические соединения, щелочные металлы. Образование полимера происходит преимущественно по типу 1,4-присоединения:
n . CH |
|
CH |
|
CH |
|
CH |
2 |
|
|
|
CH |
2 |
|
CH |
|
CH |
|
CH |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
бутадиен-1,3 |
|
|
|
|
|
|
1,4-полибутадиен |
|
|
|
|||||||||
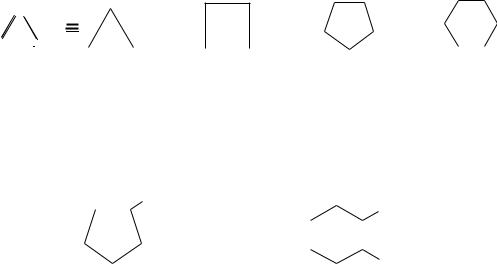
При полимеризации замещенных диенов 1,4-присоединение осуществляется по принципу " голова к хвосту ", например:
n . CH2 |
|
|
CH |
3 |
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
CH3 |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
C |
|
|
CH |
|
CH2 |
|
|
|
CH2 |
|
C |
|
CH |
|
CH2 |
|
|
CH2 |
|
C |
|
CH |
|
CH2 |
|
|
n |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
изопрен |
|
|
|
|
|
|
|
|
|
|
|
полиизопрен |
|
|||||||||||||||||
Реакции полимеризации сопряженных диенов широко используются в производстве синтетического каучука. Применение в качестве инициаторов полимеризации катализаторов Циглера-Натта позволяет получать стереорегулярные каучуки, которые по своим физико-механическим свойствам превосходят натуральный каучук.
51
=============================================================
2.5. ЦИКЛОАЛКАНЫ
=============================================================
Циклоалканы – это алициклические углеводороды, в молекулах которых все углеродные атомы, образующие цикл, соединены лишь связями.
Их еще называют цикланами, циклопарафинами, полиметиленовыми углеводородами, а также нафтенами.
Циклоалканы подразделяются:
1)по числу атомов углерода в кольце на циклопропановые (с трехчленными циклом), циклобутановые (с четырехчленным циклом), циклопентановые (с пятичленным циклом) и т. д;
2)по числу колец в молекуле на моноциклические (одноядерные), бициклические, трициклические, полициклические (многоядерные);
3)по взаимному расположению колец на спираны (два кольца имеют один общий атом углерода), конденсированные (два кольца имеют два общих соседних атома углерода) и мостиковые (два кольца имеют три и более общих атомов углерода ).
2.5.1.НОМЕНКЛАТУРА И ИЗОМЕРИЯ МОНОЦИКЛИЧЕСКИХ ЦИКЛОАЛКАНОВ
В соответствии с правилами ИЮПАК названия моноциклических циклоалканов образуют от названий алканов с соответствующим количеством атомов углерода, прибавляя префикс цикло-. Структурные формулы их записывают в упрощенном виде, изображая только геометрическую форму цикла. Каждая точка соединения линий означает углеродный атом; подразумевается, что при каждом из них имеется нормальное число атомов водорода.
CH2
H2C |
|
CH2 |
|
|
|
|
циклопентан |
|
|
|
|
|
циклобутан |
циклогексан |
|||||||
|
циклопропан |
|||||||||
Положение заместителей в кольце обозначают цифрами. Нумерацию углеродных атомов цикла начинают с атома, имеющего заместитель, и проводят таким образом, чтобы остальные заместители получили возможно меньшие номера:
|
|
|
|
C2H5 |
|
|
3 |
|
CH3 |
4 |
3 |
|
|
4 |
2 |
||||
|
|
|
|
|
|
|
|
||
5 |
2 |
|
5 |
|
1 |
|
|||
|
|
1 |
|
|
6 |
CH3 |
|||
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
||
1-метил-3-этилциклопентан |
1,2-диметилциклогексан |
||||||||
52
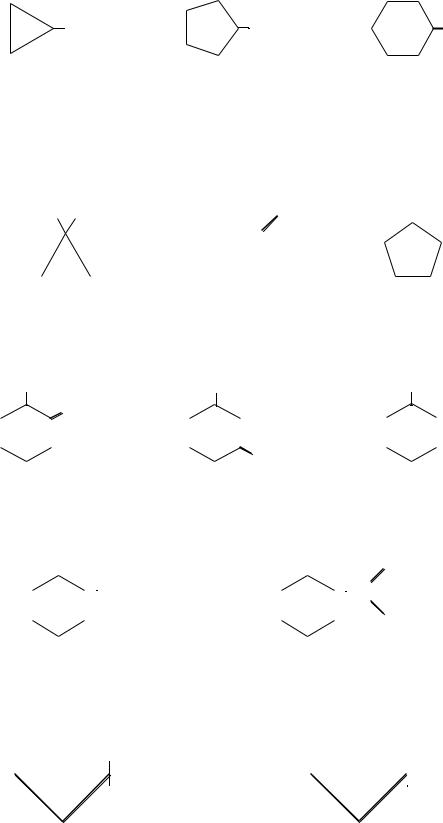
Названия одновалентных радикалов, образованных из циклоалканов, получают путем замены в названии соответствующего углеводорода суффикса
-ан на -ил:
циклопропил |
циклопентил |
циклогексил |
Для циклоалканов характерна структурная и пространственная (геометрическая и оптическая) изомерия.
С т р у к т у р н а я и з о м е р и я может быть обусловлена: а) разным размером цикла:
H |
C CH |
3 |
|
CH3 |
||
3 |
|
|
|
|
||
|
|
|
|
|
|
|
1,1-диметилциклопропан |
метилциклобутан |
циклопентан |
б) разным положением заместителей в цикле:
|
|
CH3 |
|
CH3 |
|
CH3 |
||||||
|
|
|
|
|
|
|
||||||
|
|
|
|
CH3 |
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
1,2-диметилциклогексан |
|
|
|
|
|
CH3 |
||||||
1,3-диметилциклогексан |
1,4-диметилциклогексан |
|||||||||||
в) разной структурой боковых цепей:
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
CH2CH2CH3 |
|
|
|
|
CH |
|||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
||||
|
пропилциклогексан |
изопропилциклогексан |
|||||||||||
Г е о м е т р и ч е с к а я |
и з о м е р и я циклоалканов связана с |
||||||||||||
различным расположением заместителей относительно плоскости цикла: |
|||||||||||||
|
CH3 |
|
CH3 |
|
H |
|
|
|
CH3 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H H |
|
H |
|
H3C |
|
H H |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
H |
|||
цис-1,2-диметилциклопропан |
транс-1,2-диметилциклопропан |
||||||||||||
53

2.5.2. ТЕОРИЯ НАПРЯЖЕНИЯ ЦИКЛОВ
После того, как было доказано существование циклов с разным числом атомов углерода в кольце, возник вопрос об их относительной устойчивости. Была установлена непрочность трехчленных и четырехчленных циклов, а шестичленному циклу долгое время приписывали исключительно большую устойчивость по сравнению с другими.
Однако, постепенно выяснилось, что все циклы, начиная с пятичленного, довольно близки по устойчивости.
Первые общие теоретические представления относительно устойчивости циклов, были высказаны в 1885г. А. Байером в его "Теории напряжения циклов". Байер предположил, что всякое отклонение валентностей от их нормальной тетраэдрической ориентации требует определенных усилий. Как следствие в молекуле возникает "напряжение". Молекула приобретает повышенную энергию то есть становится менее устойчивой. Угол отклонения
(α) в расчете на одну связь для трехчленного кольца:
|
|
109 |
0 28' 60 |
0 |
240 44' |
|
|
|
|
|
|
||
109o28' |
|
|
2 |
|
|
|
60o |
|
|
|
|
|
|
|
|
|
|
|
|
|
То же для четырехчленного кольца:
90o |
|
|
|
|
|
|
|
109o28' |
|
109 |
0 |
28' 90 |
0 |
90 44' |
|
|
|
|
|
2 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Для пятичленного кольца Для шестичленного кольца Для семичленного кольца
………+ 0о44'
………- 5о16'
………- 9о33'
Мера напряженности цикла обусловливает легкость образования цикла и его относительную устойчивость. Таким образом, по Байеру, наиболее устойчивым должен быть циклопентан, а затем - циклогексан. А циклобутан и циклогептан должны обладать меньшей и почти одинаковой устойчивостью. Высшие циклы должны быть всѐ менее и менее устойчивыми.
Но уже для шестичленного цикла экспериментальные данные вступили в противоречие с теорией Байера. Шестичленные циклы (внутренний угол 120о), имеющие значительное отклонение валентных углов от угла тетраэдра, оказались устойчивее пятичленных, в которых внутренние углы наиболее близки к тетраэдрическим.
54

Причиной несоответствия теории Байера экспериментальным данным явилось ошибочное представление автора о плоском строении циклов. В действительности единственным циклом, имеющим плоское строение, является трехчленный. Все остальные алициклы, начиная с четырехчленного, имеют неплоское строение: циклобутан форму квадрата, несколько изогнутого по диагонали; циклопентан форму конверта. Циклогексан без углового напряжения существует в двух формах (конформациях) «кресло» и «ванна»:
" кресло " |
" ванна " |
Наиболее устойчивая форма " кресло".
Конформации - это энергетически неравноценные формы молекул, переходящие друг в друга только за счет свободного вращения или изгиба связей.
Современная наука также признает, что отклонение валентностей от их нормального положения невыгодно: создает «напряжение» в молекуле, т. е. увеличивает запас энергии в ней и тем самым снижает устойчивость. Однако «угловое» (байеровское) напряжение сегодня считают лишь одной из ряда причин повышения внутренней энергии молекул.
2.5.3. СПОСОБЫ ПОЛУЧЕНИЯ ЦИКЛОАЛКАНОВ
Циклоалканы встречаются в природе. Так, циклопентан, циклогексан, а также их гомологи входят в состав некоторых видов нефти, из которых могут быть выделены в чистом виде. Существует также ряд синтетических методов получения циклоалканов.
Дегалогенирование α,ω-дигалогеналканов (внутримолекулярная реакция Вюрца). Дигалогеналканы, содержащие атомы галогенов у первого и последнего атомов углерода углеродной цепи, под действием металлического натрия, калия, магния или цинка превращаются в соответствующие циклоалканы. Так получают трех-, четырех-, и пятичленные циклоалканы:
CH2 |
|
|
|
CH2 |
|
|
Br |
|
CH2 |
|
|
CH2 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
+ Zn |
|
|
|
|
|
|
|
|
+ |
ZnBr 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
CH2 |
|
|
CH2 |
|
|
Br |
|
CH2 |
|
|
|
CH2 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||||||||
1,4-дибромбутан |
|
|
циклобутан |
|
|
||||||||||||||
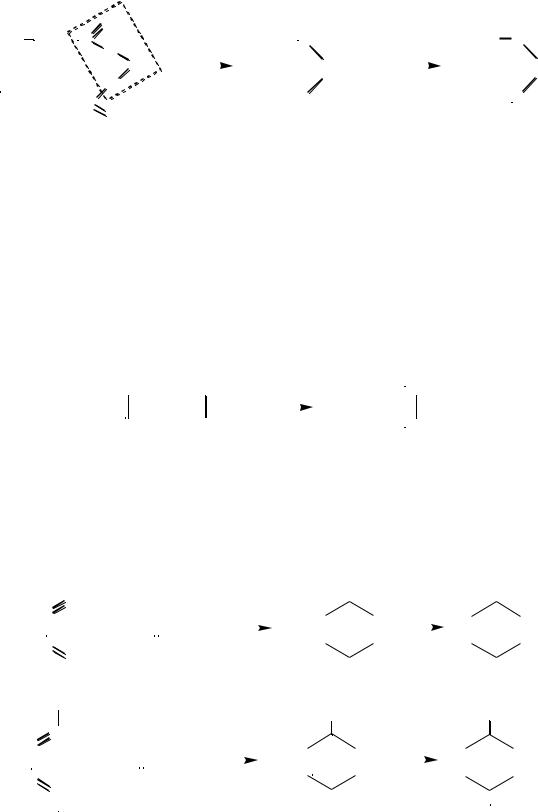
Пиролиз кальциевых, бариевых или ториевых солей дикарбоновых кислот приводит к образованию циклических кетонов, которые затем восстанавливают до соответствующих циклоалканов:
55
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
CH2 |
|
|
C |
O Ca |
|
|
CH2 |
|
|
CH2 |
4 |
[ H ] |
CH2 |
CH2 |
|||||||||||
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C O |
|
|
|
CH2 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
- CaCO3 |
|
|
|
|
|
|
|
- Н2O |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
CH2 |
|
|
CH2 |
|
|
C |
O |
|
|
|
CH2 |
|
|
CH2 |
|
|
|
CH2 |
|
CH2 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кальция адипинат |
|
|
|
циклопентанон |
|
|
|
|
циклопентан |
||||||||||||||||
Кальциевые и бариевые соли дикарбоновых кислот образуют с хорошими выходами только пяти- и шестичленные циклы. Для получения больших циклов используют соли тория.
Реакции циклоприсоединения. Циклоприсоединением называют процесс соединения двух или более ненасыщенных молекул с образованием продукта циклического строения.
Д и м е р и з а ц и я а л к е н о в. Циклоприсоединение двух молекул алкена происходит только под действием ультрафиолетового света (фотохимически) и приводит к образованию циклобутана и его производных:
|
CH2 |
|
CH2 |
h |
|
CH2 |
|
|
CH2 |
|
|
|
|||||||||
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH2 |
CH2 |
|
CH2 |
|
|
CH2 |
||||
|
|
|
||||||||
|
этилен |
|
|
|
|
циклобутан |
||||
Р е а к ц и я Д и л ь с а - А л ь д е р а (д и е н о в ы й с и н т е з). Эта реакция представляет собой присоединение алкена к сопряженному диену. Протекает легко при комнатной температуре или незначительном нагревании. Образующийся циклоалкен восстанавливают до циклоалкана:
HC |
|
CH2 |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
[ H ] |
|
|
|
|
|
|
|||||||
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HC |
|
CH2 |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
бутадиен-1,3 |
|
|
|
этилен |
|
|
|
|
циклогексен |
|
циклогексан |
||||||||||||||||||
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
CH3 |
|||||||||||
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|||
HC |
+ |
|
CH2 |
1 |
|
|
|
|
5 [ H ] |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
HC |
|
CH |
|
CH2 |
2 |
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
CH3 |
||||||||||
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
гексадиен-2,4 |
|
этилен |
|
3,6-диметилциклогексен-1 |
1,4-диметилциклогексан |
|||||||||||||||||||||||||
Гидрирование бензола и его производных. Этим методом могут быть получены циклогексан и его производные:
56

|
CH3 |
|
Ni |
|
CH3 |
|||||
|
|
|
+ |
3 H2 |
|
|
|
|
||
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
||
t, P |
|
|
|
|
||||||
метилбензол |
|
|
|
|
|
|||||
|
|
метилциклогексан |
||||||||
(толуол) |
|
|
|
|
|
|
|
|||
2.5.4. ХИМИЧЕСКИЕ СВОЙСТВА ЦИКЛОАЛКАНОВ
Циклоалканы сильно отличаются между собой по устойчивости цикла. Наименее устойчивы трехчленные, а наиболее устойчивы пяти- и шестичленные циклы. Поэтому химические свойства циклоалканов зависят от размера их циклов. Циклопропан и циклобутан по своей способности вступать в реакции присоединения напоминают непредельные углеводороды, а циклы с большим числом звеньев становятся похожими на предельные углеводороды, вступая преимущественно в реакции замещения.
Гидрирование. При каталитическом гидрировании трех-, четырех- и пятичленные циклы разрываются с образованием алканов. Особенно легко идет эта реакция в случае циклопропана. Пятичленный цикл разрывается только в процессе гидрирования при высоких температурах:
|
|
|
|
|
CH2 |
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
+ H2 |
Ni, 80-120 C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
H2C |
|
|
|
|
|
CH2 |
|
|
|
|
|
|
CH3 |
|
|
|
|
CH2 |
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
циклопропан |
|
|
|
|
|
|
|
|
|
|
|
пропан |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
H2C |
|
|
|
|
|
CH2 |
+ H2 |
Ni, 1800C |
|
CH3 |
|
|
|
|
CH2 |
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
CH3 |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
H2C |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
циклобутан |
|
|
|
|
|
|
|
|
|
|
|
|
|
бутан |
|
|
|
|
|
|
|
|||||||||||||||||||||||||
H2C |
|
|
|
|
|
|
CH2 |
+ H2 |
|
Ni, 3000C |
|
CH3 |
|
|
|
|
CH2 |
|
|
|
|
|
|
|
CH2 |
|
|
|
|
CH2 |
|
|
|
CH3 |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
H2C CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
циклопентан |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пентан |
|
|
|
|
|
|
|
||||||||||||||||
Галогенирование. Трехчленный цикл при действии галогенов легко |
||||||||||||||||||||||||||||||||||||||||||||||
размыкается: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
Cl2 |
|
|
CH2Cl |
|
|
CH2 |
|
|
CH2Cl |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
H2C |
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
циклопропан |
|
|
|
|
|
|
|
|
|
|
|
1,3-дихлорпропан |
|||||||||||||||||||||||||||||
Циклоалканы с пяти- и шестичленными циклами реагируют с галогенами как обычные алканы с замещением водорода галогеном:
57
