
05.Альдег.кет
.pdf
Глава 5. АЛЬДЕГИДЫ И КЕТОНЫ
=============================================================
Альдегиды и кетоны – это производные углеводородов, содержащие карбонильную группу (оксогруппу) >C=O. Поэтому их ещѐ называют карбонильными соединениями или оксосоединениями. В молекулах альдегидов по крайней мере одна из валентностей углерода карбонильной группы затрачивается на соединение с атомом водорода. В молекулах кетонов карбонильная группа связана с двумя углеводородными радикалами:
|
|
|
|
|
O |
|
|
|
O |
||||
|
|
|
|
|
|
|
|
|
|
|
|
R' |
|
R |
|
|
|
C |
H |
R |
|
|
C |
|
|||
|
|
|
|
|
|||||||||
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
альдегиды |
|
кетоны |
|||||||||||
В зависимости от строения углеводородного радикала альдегиды и кетоны подразделяют на алифатические, алициклические и ароматические.
|
C |
O |
Группа |
получила название альдегидной группы. Карбонильную |
 H
H
группу в кетонах часто называют кетогруппой.
=============================================================
5.1. АЛИФАТИЧЕСКИЕ АЛЬДЕГИДЫ И КЕТОНЫ
=============================================================
5.1.1 НОМЕНКЛАТУРА И ИЗОМЕРИЯ АЛИФАТИЧЕСКИХ АЛЬДЕГИДОВ И КЕТОНОВ
Для альдегидов и кетонов используют тривиальные названия и названия, соответствующие номенклатуре ИЮПАК. Т р и в и а л ь н ы е названия альдегидов производят от тривиальных названий кислот, в которые они превращаются при окислении, т. е. с тем же числом атомов углерода.
|
|
|
|
ФОРМУЛА |
|
ТРИВИАЛЬНАЯ |
ЗАМЕСТИТЕЛЬНАЯ |
|||||||||
|
|
|
АЛЬДЕГИДА |
|
НОМЕНКЛАТУРА |
НОМЕНКЛАТУРА |
||||||||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
муравьиный альдегид |
метаналь |
|
H |
|
|
C |
H |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
O |
|
|
|
|
|
|
уксусный альдегид |
этаналь |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH3 C |
H |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
O |
|
|
|
пропионовый альдегид |
пропаналь |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH3CH2 |
|
C |
|
H |
|
|
|
|||||||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
масляный альдегид |
бутаналь |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH3CH2CH2 |
|
C |
H |
|
||||||||||||
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
валериановый альдегид |
пентаналь |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH3CH2CH2CH2 |
|
C |
H |
|||||||||||||
|
|
|
||||||||||||||
120

По правилам з а м е с т и т е л ь н о й номенклатуры ИЮПAK названия альдегидов образуют от названия углеводорода с тем же числом атомов углерода (включая углерод альдегидной группы), прибавляя суффикс –аль. Нумерацию атомов углерода главной углеродной цепи начинают с атома углерода альдегидной группы. Поскольку карбонильная группа в альдегидах всегда находится на конце цепи, нет необходимости указывать еѐ положение. Углеродный атом карбонильной группы в альдегидах всегда получает номер один.
При составлении названия кетонов по з а м е с т и т е л ь н о й номенклатуре выбирают самую длинную углеродную цепь, в состав которой входит кетогруппа. Нумеруют углеродные атомы так, чтобы карбонильный углерод получил возможно меньший номер (с конца, ближайшего к карбонильной группе). Затем к названию предельного углеводорода, содержащего такое же количество атомов углерода, добавляют суффикс -он и цифру, указывающую положение углерода карбонильной группы.
Для названия кетонов по р а д и к а л о – ф у н к ц и о н а л ь н о й номенклатуре перечисляют в алфавитном порядке углеводородные радикалы при карбонильной группе и прибавляют –кетон :
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
C |
|
CH3 |
|
|
|
|
|
|
CH3 |
|
CH2 |
C |
|
CH3 |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
пропанон (зам.) |
|
|
|
|
|
|
|
|
|
бутанон (зам.) |
||||||||||||||||||||||||
|
|
|
|
|
|
диметилкетон (рад.-функ.) |
|
|
|
|
|
|
|
метилэтилкетон (рад.-функ.) |
|||||||||||||||||||||||||||
|
|
O |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
C |
|
CH2 |
CH2 |
|
|
|
CH3 CH3 |
|
CH2 |
|
C |
|
CH2 |
|
CH3 |
|
|
|
|
CH3 |
|
C |
|
|
CH |
|
CH3 |
||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||
|
|
пентанон-2 (зам.) |
|
|
|
|
|
|
пентанон-3 (зам.) |
|
|
|
|
|
3-метилбутанон-2 (зам.) |
||||||||||||||||||||||||||
метилпропилкетон (рад.-функ.) |
диэтилкетон (рад.-функ.) |
изопропилметилкетон (рад.-функ.) |
|||||||||||||||||||||||||||||||||||||||
Для некоторых кетонов сохранились т р и в и а л ь н ы е названия, например, диметилкетон чаще называют ацетоном.
Для карбонильных соединений характерна структурная изомерия. Она может быть связана с различной структурой углеродной цепи: пентанон-2 и 3- метилбутанон-2. Альдегиды и кетоны, содержащие одинаковое количество атомов углерода, являются структурными изомерами: пропаналь и пропанон, бутаналь и бутанон. Для кетонов характерна также структурная изомерия, обусловленная положением карбонильной группы: пентанон-2 и пентанон-3.
5.1.2. СПОСОБЫ ПОЛУЧЕНИЯ АЛИФАТИЧЕСКИХ АЛЬДЕГИДОВ И КЕТОНОВ
Из спиртов (окислением или каталитическим дегидрированием). Из первичных спиртов получают альдегиды:
121
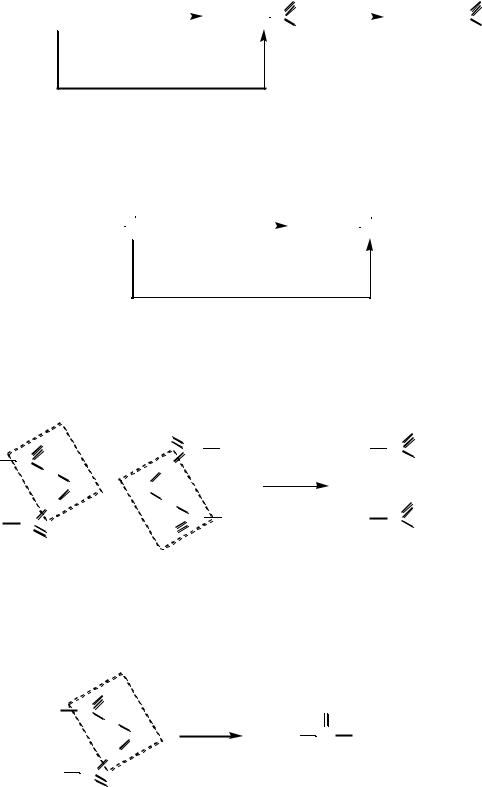
CH3 |
|
CH2 |
|
OH |
|
[ O ] |
CH3 |
|
C |
O |
[ O ] |
CH3 |
|
C |
O |
|
|
|
|
|
|
|
H |
|
|
OH |
|||||||
|
|
|
- H2O |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
окисление |
|
|
|
|
|
|
|
|
|
||
Pt, Cu, 300-4000C
- H2
каталитическое дегидрирование
Из вторичных спиртов получают кетоны:
|
|
OH |
|
|
|
|
|
O |
|||||||
|
|
|
|
|
|
|
[ O ] |
|
|
|
|
|
|
|
|
CH3 |
|
CH |
|
CH3 |
|
|
|
CH3 |
|
C |
|
CH3 |
|||
|
|
|
- H2O |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
окисление |
|
|
|
|
|
|
|
||
Pt, Cu, 300-4000C
- H2
каталитическое дегидрирование
Пиролиз кальциевых или бариевых солей карбоновых кислот.
Альдегиды получают из смеси солей двух различных кислот, одна из которых муравьиная:
|
O |
O |
C |
H |
|
CH3 |
C |
O |
|
|
|
|
|||||||
|
|
|
H |
||||||
CH3 |
C |
|
O |
|
|||||
|
|
|
o |
|
|
||||
|
|
O Ca + Ca |
|
|
300 C |
+ |
|
+ 2 CaCO3 |
|
|
|
O |
O C |
H |
|
|
|
O |
|
CH3 |
C |
|
CH3 |
C H |
|||||
O |
O |
|
|
|
|||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
ацетат кальция |
формиат кальция |
|
этаналь |
|
|||||
Кетоны |
|
получают из |
солей |
любых |
карбоновых кислот, кроме |
||||
муравьиной.
Симметричные кетоны получают пиролизом соли одной кислоты:
|
|
O |
|
|
|
O |
|
CH3 |
C |
|
|
|
|
|
|
O |
|
o |
|
|
|
||
|
|
Ca |
300 C |
CH3 |
C CH3 |
+ CaCO3 |
|
|
|
O |
|
||||
|
|
|
|
|
|
|
|
CH3 |
C |
O |
|
|
|
пропанон |
|
|
|
|
|
|
|
||
|
|
|
|
|
(диметилкетон, |
|
|
ацетат кальция |
|
|
ацетон) |
|
|||
Несимметричные кетоны получают пиролизом солей двух разных кислот в соотношении 1:1 :
122

|
|
|
O |
|
|
O |
|
|
|
|
O |
C CH2 CH3 |
CH3 |
C |
CH2 |
CH3 |
|
|
|
|
||||||
CH3 |
C |
|
O |
|||||
O Ca + |
|
o |
|
|
|
|||
|
|
Ca |
|
300 C |
O |
+ |
|
|
|
|
O |
O |
|
- 2CaCO3 |
|
|
|
CH3 |
C |
C CH2 CH3 |
CH3 |
C |
CH2 |
CH3 |
||
O |
O |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
ацетат кальция |
пропионат кальция |
бутанон (метилэтилкетон) |
||||||
Гидратация алкинов (реакция Кучерова). В присутствии солей ртути(ІІ)
алкины присоединяют воду. Присоединение происходит в соответствии с правилом Марковникова. При этом из а ц е т и л е н а получается у к с у с н ы й а л ь д е г и д :
H |
|
|
C |
|
|
C |
|
|
H + H2O |
|
HgSO4 |
|
|
|
|
|
O |
|
|
|
H |
|
|
|
|
|
|
|
|
|
O |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
C |
|
|
|
|
|
CH2 |
|
|
|
|
|
H |
|
|
C |
|
|
CH3 |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
этаналь |
|||||||||
|
|
|
ацетилен |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(уксусный альдегид) |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
Из г о м о л о г о в а ц е т и л е н а - к е т о н ы : |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
R |
|
|
C |
|
|
C |
|
|
H + H2O |
|
HgSO4 |
|
|
|
|
|
|
|
O |
|
|
H |
|
|
|
|
|
|
|
|
|
O |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
R |
|
C |
|
|
|
|
CH2 |
|
|
|
|
|
R |
|
C |
|
CH3 |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Оксосинтез. В промышленности альдегиды получают прямым присоединением CO и H2 к олефинам при 100 – 200 0С, под давлением 100 - 200 атм., в присутствии кобальтового или никелевого катализатора. При этом обычно образуется смесь альдегидов линейного и разветвлѐнного строения:
2 R |
|
|
|
|
t, p |
|
|
|
|
|
|
|
O |
O |
|||||
|
CH |
|
CH2 + 2CO + 2H2 |
|
R |
|
CH2 |
|
CH2 |
|
C |
H + R |
|
|
CH |
|
C |
|
|
|
|
кат. |
|
|
|
|
|
H |
|||||||||||
|
|
|
|
|
|||||||||||||||
CH3
Гидролиз геминальных дигалогеналканов. При гидролизе гем-
дигалогеналканов с атомами галогена у первичного атома углерода образуются альдегиды, а у вторичного – кетоны:
|
|
|
|
|
|
|
|
2 H2O |
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
CH3 |
|
|
CH2 |
|
CHCl 2 |
|
CH3 |
|
|
CH2 |
|
CH |
|
|
|
|
|
|
CH3 |
|
|
CH2 |
C |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|||||||||||||||||||||||
|
|
|
- 2 HCl |
|
|
|
- H2O |
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
1,1-дихлорпропан |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пропаналь |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
2 H2O |
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
CH3 |
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
CH3 |
|
|
CCl2 |
|
CH3 |
|
|
|
|
CH3 |
|
|
C |
|
|
|
|
|
|
|
C |
|
|
CH3 |
||||||||||||||||||
|
|
|
- 2 HCl |
|
|
|
|
|
|
|
|
- H2O |
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
2,2-дихлорпропан |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пропанон |
|
||||||||||||||
123

5.1.3. ХИМИЧЕСКИЕ СВОЙСТВА АЛИФАТИЧЕСКИХ АЛЬДЕГИДОВ И КЕТОНОВ
Химические свойства альдегидов и кетонов определяются наличием в их молекуле карбонильной группы. Атом кислорода как более электроотрицательный элемент притягивает к себе σ- и π-электроны, в результате чего двойная связь карбонильной группы сильно поляризована:
Благодаря такой поляризации альдегиды и кетоны способны
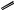 C
C O . вступать в реакции с нуклеофильными реагентами, которые атакуют атом углерода карбонильной группы.
O . вступать в реакции с нуклеофильными реагентами, которые атакуют атом углерода карбонильной группы.
Альдегиды, как правило, более реакционноспособны, чем кетоны. Это объясняется наличием в молекуле кетона двух алкильных радикалов, которые, нагнетая электронную плотность на углерод карбонильной группы, понижают на нѐм положительный заряд сильнее, чем в альдегидах, где с карбонилом соединена только одна алкильная группа. Кроме того, алкильные радикалы в молекуле кетона в большей степени затрудняют подход нуклеофила к углероду карбонильной группы.
Помимо реакций присоединения по карбонильной группе, для альдегидов и кетонов характерны также реакции по α-углеродным атомам, обусловленные влиянием на них карбонильной группы. Протекают также реакции окисления, восстановления, конденсации, полимеризации и др.
А. Р е а к ц и и п о к а р б о н и л ь н о й г р у п п е
Присоединение цианистоводородной (синильной) кислоты. Синильная кислота присоединяется к карбонильным соединениям, образуя циангидрины (α-оксинитрилы). Реакция протекает в присутствии основания, нуклеофилом является цианид-ион:
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
CH3 |
C H |
+ |
H C N |
|
|
|
CH C N |
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
этаналь |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
нитрил |
|
-оксипропановой |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислоты |
||||||||||||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||||||||||||
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
C |
|
CH3 + H |
|
|
C |
|
|
N |
|
|
|
CH3 |
|
C |
|
C |
|
|
|
N |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||||||||||
|
|
пропанон |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
нитрил |
-метил- -оксипропановой |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислоты |
||||||||||||||
Цианистый водород присоединяется очень медленно. Добавление капли цианистого калия вызывает сильное увеличение скорости реакции, в то время как добавление минеральной кислоты уменьшает скорость реакции практически до нуля. Это указывает на то, что присоединение цианистоводородной кислоты к альдегидам и кетонам начинается с атаки цианид-аниона, т. е. является реакцией нуклеофильного присоединения:
124

H C  N K C
N K C  N H2SO4
N H2SO4
R C
H + |
+ |
C |
|
|
|
|
|
|
|
N |
- |
|
|
||||||||||
|
|
|
- сильно увеличивает скорость реакции. |
||||||||
|
|
|
|
||||||||
K + |
+ |
C |
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|||||
H + |
+ |
HSO4- |
снижает скорость реакции практически до 0 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
O |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
OH |
||||||||||||
|
:N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ H + |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
R |
|
C |
|
|
C |
|
|
|
N |
|
|
|
|
|
||||||||||
H |
+ |
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
CH |
|
C |
|
N |
||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Присоединение гидросульфита (бисульфита) натрия. Альдегиды и метилкетоны (т.е. кетоны, содержащие группировку СН3СО) реагируют с гидросульфитом (бисульфитом) натрия, образуя «бисульфитные соединения». Кетоны более сложного строения этой реакции не дают. Реакция протекает без катализатора, так как гидросульфит-ион – достаточно сильный нуклеофил:
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
OH |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
R |
|
C |
+ |
NaHSO3 |
|
|
|
R CH SO3Na |
||||||||||||||
|
H |
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
C |
|
CH3 |
+ NaHSO3 |
|
|
|
R |
|
|
C |
|
|
SO3Na |
||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||||
Бисульфит натрия получается при растворении в воде метабисульфита натрия:
Na2S2O5 + H2O |
|
2 NaHSO3 |
|
||
метабисульфит |
|
бисульфит |
натрия |
|
натрия |
Бисульфитные соединения плохо растворимы в воде и выделяются в виде кристаллического осадка. При нагревании с раствором карбоната натрия они разлагаются с выделением свободного альдегида или кетона:
|
|
OH |
|
|
|
|
|
|
|
O |
|
|
|
|
|
2R |
|
|
|
|
SO Na |
+ Na CO |
t |
|
|
|
|
|
|
|
|
|
CH |
|
2R |
|
C |
+ 2 Na SO |
+ CO |
|
+ H O |
||||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
||||||||||
|
|
|
|
3 |
2 3 |
|
|
|
|
H |
2 3 |
|
2 |
2 |
|
Это даѐт возможность использовать реакции с бисульфитом натрия для качественного определения альдегидов и метилкетонов, а также для их
выделения и очистки.
Взаимодействие с магнийорганическими соединениями.
Присоединение алкил- и арилмагнийгалогенидов по карбонильной группе альдегидов и кетонов с последующим гидролизом образовавшихся продуктов – один из важнейших способов получения спиртов. При этом из формальдегида получаются первичные спирты, все остальные альдегиды дают вторичные спирты, а кетоны – третичные:
125

|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HCl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
H |
|
|
|
|
C |
H + R |
|
MgBr |
|
|
|
|
|
R |
|
CH2 |
|
|
|
|
O |
|
MgBr |
|
|
|
|
R |
|
CH2 |
|
|
|
OH |
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- MgBrCl |
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
первичные спирты |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
C |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
MgBr |
|
|
HCl |
|
|
|
|
|
|
|
|
|
OH |
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
CH3 |
|
|
|
|
H + R |
|
|
MgBr |
|
|
|
|
CH3 |
|
|
|
|
CH |
|
|
|
|
|
|
R |
|
|
|
|
CH3 |
|
|
|
|
CH |
|
|
|
R |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- MgBrCl |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
вторичные спирты |
|||||||||||||||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
MgBr |
|
|
HCl |
|
|
|
|
|
|
|
OH |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
CH3 |
|
|
|
C |
|
|
CH3 + R |
|
MgBr |
|
|
|
CH3 |
|
|
|
|
C |
|
|
|
|
|
CH3 |
|
|
CH3 |
|
|
|
|
C |
|
|
|
|
CH3 |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- MgBrCl |
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
третичные спирты |
|||||||||||||||||||||
Присоединение воды. Растворение альдегидов в воде сопровождается образованием гидратов (продуктов присоединения молекулы воды по карбонильной группе). Как правило, они неустойчивы, существуют только в водном растворе, находясь в динамическом равновесии с альдегидом:
|
|
|
O |
|
|
|
|
|
|
|
OH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
R |
|
C |
|
OH |
|
|
|
|
|
|
|
|
|
|
||||||
R C |
H |
H2O |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
H |
|||
|
|
|
|
|
|
|
|
|
гидрат альдегида |
|||||
Устойчивость гидрата определяется строением карбонильных соединений. Формальдегид в воде практически полностью гидратирован, ацетальдегид – наполовину, а ацетон почти не взаимодействует с водой. Если в молекуле альдегида (или кетона) карбонильная группа связана с сильным электроноакцепторным заместителем, то, как правило, гидрат такого альдегида (или кетона) может быть выделен в свободном виде. Например:
|
|
O |
|
|
|
|
|
OH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
CCl3 C H |
+ |
H2O |
|
CCl3 C OH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|||
хлораль |
|
|
|
хлоральгидрат |
|||||||
Хлоральгидрат – устойчивое кристаллическое вещество. Отнять воду от него удаѐтся только при действии сильных водоотнимающих средств. Хлоральгидрат применяется в медицинской практике как успокаивающее и противосудорожное средство.
Присоединение спиртов. При взаимодействии альдегидов со спиртами образуются полуацетали, а в присутствии следов минеральных кислот – ацетали:
126

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
.. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
:OH |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
O |
|
|
|
H |
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
R |
|
|
|
C H + |
R' |
|
|
|
|
O |
|
H |
|
|
|
|
|
|
|
|
|
|
|
R |
|
C |
|
|
|
|
H |
|
|
|
|
|
|
R |
|
|
C |
|
|
|
H |
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R' |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R' |
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
полуацетали |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
R' |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
.. |
|
|
|
|
|
|
|
|
|
|
O |
|
|
R' |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
- H O |
|
|
|
|
|
|
|
|
|
|
|
|
+ R' |
|
O |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
2 |
|
|
+ |
|
|
|
|
|
|
.. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
C |
|
|
|
H |
|
|||||||||||||||
|
|
|
|
|
|
R |
|
C |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
C |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
O |
|
|
R' |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
R' |
|
|
|
|
|
|
|
|
O |
|
|
|
R' |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ацетали |
|
|||||
Полуацетали, как правило, малоустойчивы. Ацетали устойчивы в щелочной среде, но легко гидролизуются до свободного альдегида в разбавленных кислотах. Такое свойство ацеталей используется в органическом синтезе для защиты альдегидной группы.
Ацетали кетонов получаются более сложно – действием на кетоны этиловых эфиров ортомуравьиной HC(OC2H5)3 или ортокремниевой Si(OC2H5)4 кислот.
Взаимодействие с хлоридом фосфора(V). Под действием карбонильный кислород в альдегидах и кетонах замещается двумя атомами хлора с образованием геминальных дихлоралканов:
|
|
|
C |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
R |
|
|
H |
+ |
PCl5 |
|
|
|
R |
|
|
CHCl 2 + |
POCl3 |
|||||||||
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
||||||||||||||||||
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
C |
|
R |
+ |
PCl |
|
|
|
R |
|
|
CCl |
|
|
R + |
POCl |
|
|||
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
2 |
|
|
3 |
|
Взаимодействие с аммиаком. Альдегиды, присоединяя молекулу аммиака, превращаются в неустойчивые аминоспирты, от которых внутримолекулярно отщепляется вода с образованием альдиминов:
|
|
|
O |
|
|
|
|
|
|
|
OH H |
|
|
|
|
|
|
N |
|
H |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
R |
|
C |
+ NH |
|
|
|
|
R |
|
CH |
|
NH |
|
|
R |
|
C |
|
+ H O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
H |
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
аминоспирты |
|
|
альдимины |
|
|||||||||||
Альдимины сразу же тримеризуются в гетероциклические соединения альдегидаммиаки:
127

|
|
|
NH |
|
|
|
|
|
NH |
||||||||
R |
|
HC |
|
CH |
|
R |
|
R |
|
HC |
|
CH |
|
R |
|||
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HN |
|
|
NH |
|
|
HN |
|
NH |
||||||||
|
|
|
CH |
|
|
|
|
|
CH |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
R |
||||||||
При R=CH3 получается "вулкацит", соединение, которое применяется в качестве ускорителя при вулканизации каучуков.
Своеобразно протекает реакция формальдегида с аммиаком. При комнатной температуре в водном растворе количественно получается гексаметилентетрамин, называемый также уротропин (А. М. Бутлеров):
|
|
|
|
|
|
|
|
N |
|
|
|
|
6 CH2 |
|
|
O + |
4 NH3 |
|
|
|
|
|
|
+ |
6 H2O |
|
|
|
|
|
|
|
|
|||||
|
|
|
N |
|
N |
|||||||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
гексаметилентетрамин |
|
|
||||
|
|
|
|
|
|
(уротропин) |
|
|
|
|
||
Уротропин применяется в производстве фенолформальдегидных смол, взрывчатых веществ (гексоген получают нитрованием уротропина). В медицине уротропин используется как антисептик при воспалительных заболеваниях. Комплекс уротропина с CaCl2 (кальцекс) обладает жаропонижающим действием.
Кетоны реагируют с аммиаком очень медленно, в более жестких условиях, чем альдегиды. Присоединяя молекулу аммиака, кетоны превращаются в неустойчивые аминоспирты, от которых межмолекулярно отщепляется вода с образованием кетоаминов:
|
|
|
O |
|
|
|
|
|
|
OH |
|
H |
|
O |
|
|
NH2 |
|
|
O |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
C |
|
CH3 CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH |
|
|
C |
|
CH |
|
+ NH |
|
CH |
|
|
C |
|
NH |
|
|
|
|
|
C |
|
CH |
|
|
C |
|
CH |
3 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
3 |
|
|
|
|
|
3 |
3 |
|
|
3 |
|
|
|
|
|
2 |
|
- H2O |
3 |
|
|
|
|
2 |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кетоамин |
|
|||||||
Таким образом реакция с аммиаком позволяет различать альдегиды и кетоны.
Взаимодействие с гидроксиламином. Продукты конденсации альдегидов и кетонов с гидроксиламином называют альдоксимами и кетоксимами соответственно. Они представляют собой кристаллические вещества с чѐткой температурой плавления. В кислой среде легко гидролизуются с образованием исходных веществ. Поэтому реакцию образования оксимов используют для выделения и идентификации альдегидов и кетонов.
128

|
|
|
|
|
|
|
O |
|
|
|
R |
|
|
CН N |
|
OH + H2O |
|||||||||||
R |
|
|
C H + H2N |
|
|
OH |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
альдоксим |
||||||||||
|
|
|
|
|
|
|
|
гидроксиламин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
O |
|
|
|
|
|
|
|
N |
|
|
OH |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
C |
|
R' + H2N |
|
OH |
|
|
|
|
R |
|
C |
|
|
R' + H2O |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кетоксим |
||||||||
Взаимодействие с гидразином и его производными. Альдегиды и кетоны реагируют с гидразином и его производными с образованием гидразонов, которые, подобно оксимам, хорошо кристаллизуются и используются для открытия карбонильных соединений и выделения их из смесей.
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
N |
|
NH2 |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
R |
|
C |
H + H2N |
|
|
NH2 |
|
|
|
R |
|
|
C H |
|
+ |
H2O |
||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
гидразин |
|
|
|
гидразоны |
|
|
|
||||||||||||||
|
|
|
O |
|
|
|
|
|
|
|
N |
|
NH2 |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
R |
|
|
C |
|
R' + H2N |
|
NH2 |
|
|
|
R |
|
C |
|
|
R' |
|
+ H2O |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ H2O |
||||||
R |
|
C H + H2N |
|
NH |
|
|
|
|
|
|
|
R |
|
CH |
|
N |
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
фенилгидразин |
|
|
|
|
фенилгидразон |
|
|
|
|
|||||||||||||
Реакции восстановления. Альдегиды восстанавливаются до первичных, а кетоны до вторичных спиртов:
|
|
|
|
C |
O |
|
|
|
Pt |
|
|
|
|
|
|
|
|
|
|
|
|||
R |
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
H |
H2 |
|
|
R |
|
|
CH2 |
OH |
|||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
первичные спирты |
|||||||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
OH |
|
||||||
|
|
|
|
|
|
|
|
|
+ H2 |
Pt |
|
|
|
|
|
|
|
|
|
|
|||
R |
|
|
|
C |
|
R' |
R |
|
|
CH |
|
|
R' |
||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||
вторичные спирты
Реакции окисления. Окисление альдегидов идет значительно легче, чем окисление кетонов. Альдегиды окисляются без изменения углеродного скелета и числа углеродных атомов до соответствующих карбоновых кислот:
|
|
O |
[ O ] |
|
|
C |
O |
R |
|
C H |
|
R |
|
OH |
|
|
|
|
Альдегиды, в отличие от кетонов, окисляются как сильными (H2Cr2O7, KMnO4), так и слабыми окислителями (Ag(NH3)2+, Cu2+). При использовании в качестве окислителя аммиачного раствора оксида серебра (реактива Толленса) протекает реакция «серебряного зеркала» (качественная реакция на альдегидную группу):
129
