
- •Федеральное агентство по образованию
- •Пояснительная записка
- •Лабораторная работа № 1 Техника безопасности в химических лабораториях
- •Общие правила по технике безопасности
- •Правила работы с кислотами и щелочами
- •Основные принципы безопасной работы с кислотами и щелочами
- •Первая помощь при ожогах
- •Лабораторная работа № 2 Химическая посуда
- •Посуда общего назначения
- •Посуда специального назначения
- •Мерная посуда
- •Фарфоровая посуда
- •Мытье химической посуды
- •Лабораторная работа № 3 Весы. Взвешивание.
- •Правила взвешивания
- •Лабораторная работа № 4 Основные приемы работы в лаборатории
- •Нагревание
- •Выпаривание
- •Высушивание
- •Прокаливание
- •Фильтрование
- •Лабораторная работа № 5 Способы очистки веществ
- •Дистилляция
- •Перегонка под обыкновенным давлением
- •Сублимация (возгонка)
- •Экстракция
- •Кристаллизация
- •Проведение кристаллизации
- •Охлаждение
- •Лабораторная работа № 6 Приготовление растворов заданной концентрации
- •Методика приготовления растворов
- •Измерение плотности растворов
- •Расчеты по приготовлению растворов
- •Ход работы
- •Лабораторная работа № 7 Скорость химических реакций и химическое равновесие
- •Лабораторная работа № 8 Электролитическая диссоциация
- •Лабораторная работа № 9 Произведение растворимости
- •Лабораторная работа № 10 Водородный показатель. Буферные растворы
- •Лабораторная работа № 11 Гидролиз солей
- •Лабораторная работа № 12 Приготовление растворов и определение их концентрации титрованием
- •Лабораторная работа № 13 Окислительно-восстановительные реакции
- •Лабораторная работа № 14 Комплексные соединения
- •Список литературы
- •Содержание
- •Сокульская Наталья Николаевна
Сублимация (возгонка)
Некоторые твердые неорганические и органические вещества обладают способностью при нагревании испаряться, не плавясь. При охлаждении паров таких веществ они переходят из газообразного в твердое состояние, минуя жидкую фазу. Этим свойством пользуются для очистки веществ. Сама операция называется возгонкой, или сублимацией.
Сублимацию, как и перегонку, можно проводить при обычном давлении или при уменьшении давления (вакуум-сублимация). Ниже рассматриваются случаи сублимации только при обычном давлении.
Из веществ, которые можно очистить сублимацией, следует назвать: иод, серу, оксиды мышьяка, хлорид аммония и др.
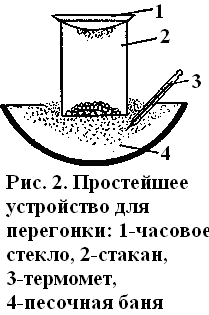
B лабораториях чаще всего приходится возгонять, иод. Устройство для возгонки небольших количеств вещества очень простое. Это — тонкостенный стакан, поставленный на песочную баню так, чтобы дно его было погружено в песок на 1–2 см. Стакан сверху накрывают часовым стеклом, причем выпуклая сторона его должна быть обращена внутрь стакана (рис. 2). При осторожном нагревании иод возгоняется и на часовом стекле собираются игольчатые кристаллы.
Технический иод перед возгонкой следует смешать с KI и CaO.
Иногда, для улучшения охлаждения, на часовое стекло наливают холодную воду или кладут небольшие кусочки льда.
Значительно удобнее работать с аппаратом, устроенным по типу холодильников, т.е. с постоянным током холодной воды. Один из аппаратов такого типа изображен на рис. 3.
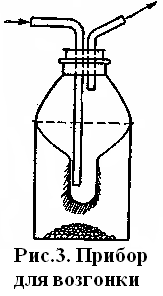
Одну трубку прибора присоединяют к водопроводному крану, а другая трубка служит для отвода воды; на нее следует надеть резиновую трубку и отвести ее к раковине или водосливу. Ток воды устанавливают не очень сильный.
Обычно иод для надежности возгоняют дважды. После вторичной возгонки препарат получается очень чистым, если его не загрязнить при снимании кристаллов со стекла. Кристаллы иода снимать при помощи металлического шпателя или ножа нельзя, так как иод взаимодействует с большинством металлов. Возогнанный иод с часового стекла или с аппарата для возгонки следует счищать стеклянной лопаточкой.
Аналогичным образом можно возогнать и другие вещества, упомянутые выше.
Экстракция
Экстракцией называют метод извлечения растворителями из смеси каких-либо веществ того или другого компонента.
В основе этого метода лежат закон распределения вещества, между двумя несмешивающимися жидкостями (если экстрагируют вещество из раствора в какой-нибудь жидкости) и различная растворимость отдельных веществ в данном растворителе (если вещество извлекают из смеси с другими веществами).
Большинство веществ (как жидких, так и твердых) растворяется в нескольких растворителях. Если данное вещество растворено в каком-либо растворителе и к этому раствору прибавить другой растворитель, не смешивающийся с первым, то часть вещества перейдет в этот растворитель, образуя два слоя несмешивающихся жидкостей, в которых будет содержаться данное вещество. При этом распределение вещества между двумя растворителями будет вполне определенным для каждого отдельного случая.
Например, уксусная кислота очень хорошо, растворяется в воде и в бензоле. Бензол же в воде практически нерастворим. Поэтому, если к водному раствору уксусной кислоты добавить бензол, то уксусная кислота распределится между водой и бензолом. Повторяя операцию несколько раз, можно извлечь из воды почти всю уксусную кислоту.
Отношение концентраций растворенного вещества в обеих жидких фазах называется коэффициентом распределения.
Если же взять такой случай, когда растворители смешиваются между собой, а данное вещество растворяется только в одном из них, то при добавлении в раствор другого растворителя вещество выпадает.
Например, скипидар растворяется в спирте; если же в спиртовой раствор его добавить воду, то он выпадет в виде тонкой эмульсии. Другой пример: воск хорошо растворяется на холоду в хлороформе, но плохо в холодном этиловом спирте. Поэтому, если к хлороформному раствору воска добавить некоторое количество спирта, то воск выделится из раствора в виде хлопьев.
Если же имеется смесь двух или нескольких веществ и нужно выделить одно из них, то почти всегда можно подобрать такой растворитель, который растворяет только нужное вещество и почти не растворяет других.
Одним из важнейших растворителей является вода, в которой растворяется очень большое число различных неорганических и органических веществ.
Экстракция органическими растворителями применяется не только для извлечения органических веществ. Очень многие неорганические соли, главным образом галогениды и нитраты, также растворяются в органических растворителях и при определенных условиях могут быть извлечены из водных растворов. На этом, в частности, основаны некоторые способы очистки различных неорганических солей с целью получения чистых металлов.
При экстрагировании большое значение имеет температура, особенно в тех случаях, когда экстрагируют водой.
В некоторых случаях приходится проводить так называемую реэкстракцию. Например, органическим растворителем можно извлечь из смеси какое-либо вещество, хорошо растворяющееся в воде. Вместо отгонки органического растворителя полученный экстракт можно обработать водой и все извлеченное вещество перейдет в водный раствор, очищенный же от примеси органический растворитель может быть снова использован для экстракции.
В зависимости от того, в каком виде находится экстрагируемое вещество, приемы экстракции и конструкция применяемых для этой цели приборов несколько изменяются.
Для удобства рассмотрения процесса экстракции можно наметить два случая: экстрагирование твердых веществ (система «твердое – жидкость») и экстрагирование жидкостей (система «жидкость – жидкость»).
Кроме того, в зависимости от применяемых растворителей различают экстракцию:
а) водой или водными растворами;
б) органическими растворителями;
в) расплавами.
