
Лекции / organic_2011_6
.pdf
21
«Секстетные» перегруппировки
|
|
|
O |
|
|
|
|
|
|
|
X |
|
N C O |
|
|
|
|
R |
N |
- X- |
|
|
|
|
|
R |
|
|
|||
|
|
|
|
|
изоцианат |
|
|
|
|
|
X- - Хорошая уходящая группа |
|
|
||
|
O |
|
Br2 |
|
O |
|
|
|
|
|
|
Br |
Гофман |
|
|
|
R |
NH2 |
HO- |
R |
|
||
|
N |
|
|
||||
|
|
|
|
|
O |
|
O |
|
|
|
NaN3 |
|
N |
HNO2 |
|
|
|
|
|
N |
|
||
|
|
RCOCl |
R |
R |
NHNH2 |
||
|
|
|
|
N |
|||
|
|
|
|
Курциус |
|
|
|
|
O |
1. Ac2O/NEt3 |
|
O |
Лоссен |
|
|
R |
NHOH |
2. HO- |
R |
OCOCH3 |
|
||
|
|
N |
|
|
|||

Галогенангидриды |
|
|
|
22 |
|||
|
|
O |
|
||||
|
|
R'COCl |
|
|
|
||
|
|
RCO2H |
|
F- |
|
||
|
RCOCl |
|
RCOF |
||||
|
R |
X |
|||||
|
|
- R'CO2H |
|
|
|||
|
|
SOCl2, PCl3, PCl5, PBr3 X = Cl, Br |
|
||||
Ангидриды карбоновых кислот |
|
|
|
||||
|
|
RCOCl |
O |
P2O5 |
|
|
|
RCO2Na |
R |
RCO2H не всегда возможно |
|||||
|
|
||||||
|
SOCl2 (0.5 моль) |
O |
PCl5 |
|
|
||
RCO2H |
R |
RCO2Na |
|
||||
|
|
|
|
||||
|
|
|
O |
|
|
|
|
Другие производные карбоновых кислот |
|
NH |
|
||||
|
|
CN- |
|
|
R |
Cl |
|
|
RX |
|
HCl |
имидоилхлорид |
|||
|
SN2 |
|
|
|
|||
|
|
R C |
N |
|
|
||
|
|
SOCl2 |
|
|
|||
RCONH2 |
|
R'OH/H+ |
|
||||
|
|
(R'O-) |
NH |
|
|||
|
|
|
|
|
|
||
|
|
|
|
|
R |
OR' |
|
иминоэфир
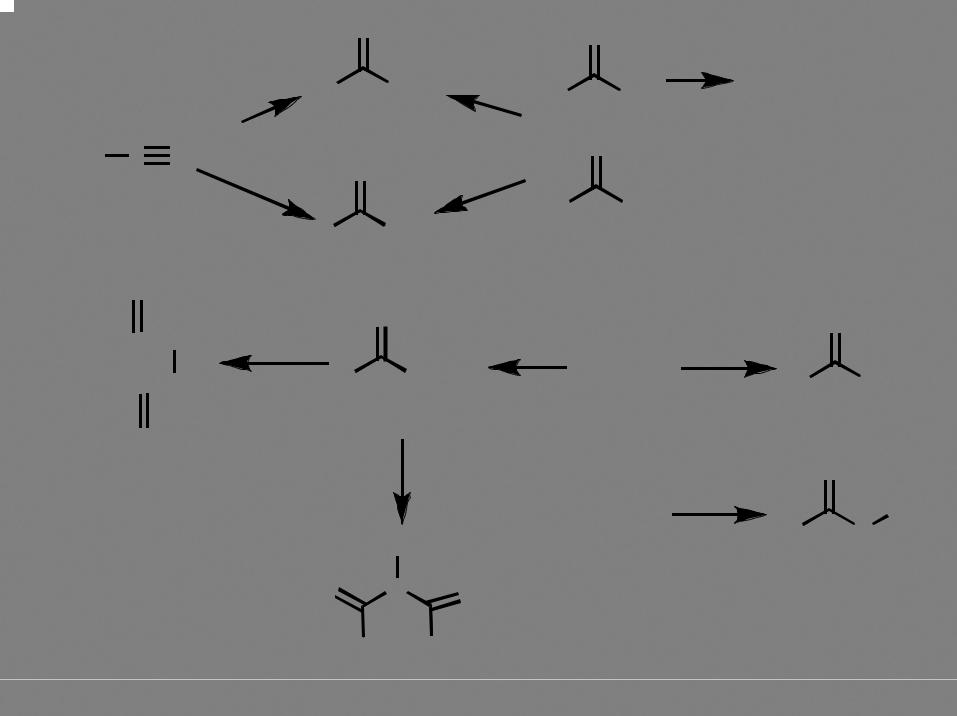
|
|
|
NH |
|
|
|
NH4Cl |
R |
NH2 |
NH3 |
R |
|
|
||||
|
|
амидин |
|
|
|
R C N |
|
. |
NOH NH2OH |
|
|
|
NH2OH HCl |
|
|||
|
|
R |
NH2 |
|
R |
|
|
|
|
||
амидоксим
O
R NH
NH
R NH
NH
O
N,N'-диацилгидразид
O |
|
RCO2Et |
N2H4 |
(RCOCl) R |
NHNH2 |
ацилгидразид |
|
1. NaH |
2. R'COCl |
NH2
O N  O
O
R R'
23
NH
H3O+ RCO2R'
OR'
NH
Cl
|
NH2OH |
O |
|
RCO2Et |
|
||
R |
NHOH |
||
|
|||
|
гидроксамовая |
||
|
|
кислота |
|
|
NH2OH |
O |
|
RCOCl |
NH2 |
||
R |
|||
|
O |
||
N,N-диацилгидразид

24
Свойства карбоновых кислот и их производных Пиролиз солей
CO2- |
Ca2+ |
t |
CO2- |
O |
|
|
|
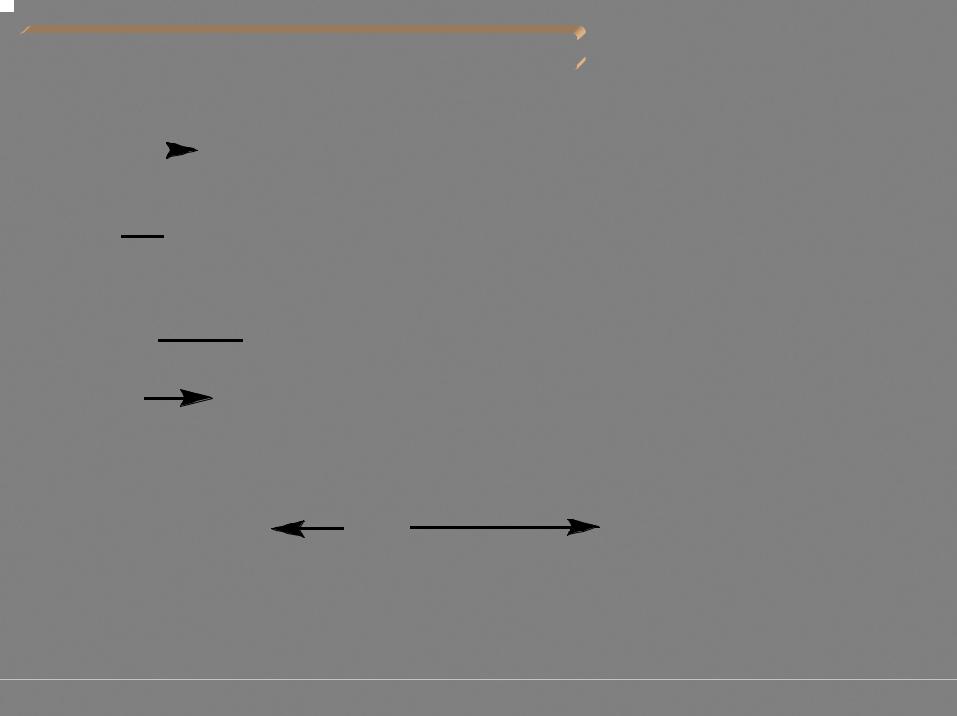
Электрохимическое окисление (синтез_Кольбе)
+ e
R R
Реакция Бородина-Хунсдиккера |
|
|
|
|
|
|
RCO2Ag |
Br2 |
RBr |
|
|
|
|
|
|||
Pb(OAc)4 |
|
|
|
R+ |
|
RCO2H |
(RCO2)Pb(OAc)3 |
|
R |
+ Pb(OAc)3 |
|
|
|
- CO2 |
- PbOAc2 |
|
|
|
|
|
|
- AcO- |
|
Например: |
|
|
|
O |
|
CO2H |
Cl |
|
|
|
|
|
|
Pb(OAc)2 |
|
||
|
Pb(OAc)2 |
|
|
|
|
|
LiCl |
|
|
O |
|
|
|
|
пиридин |
|
|
O
25
Восстановление производных карбоновых кислот 
RCO H |
[H] |
RCH2OH |
[H] = LiAlH4, B2H6, H2/катализатор - в жестких условиях |
|
|||
2 |
|
|
NaBH4 - нет |
|
|
|
RCO2R' [H] RCH2OH + R'OH [H] = LiAlH4, Na/EtOH
RCH2OH + R'OH [H] = LiAlH4, Na/EtOH
H2/катализатор - в жестких условиях
NaBH4 - нет
RCONH2 LiAlH4  RCH2NH2
RCH2NH2
RCOCl |
[H] |
[H] = LiAlH(OR')3, H2 / Pd/BaSO4 |
RCHO |
[H]1. LiAlH4 (1 экв.)
RCH2NH2 |
RCN |
RCHO |
|
|
2. H2O |
[H] = LiAlH4, H2/cat, B2H6, NaBH4/Ni

26
Взаимодействие производных карбоновых кислот с нуклеофильными реагентами
? |
Nu- |
O |
Nu- |
O |
O- |
|
O |
|
R |
Nu- |
R |
Nu |
R |
||||
|
R |
|||||||
|
O- |
- NuH |
X |
X |
-X- |
Nu |
||
|
|
|
(X = OH) |
|
|
|
|
Реакция происходит тем легче, чем лучше уходящая группа (вторая стадия - лимитирующая. Ряд активности производных карбоновых кислот:
галогенангидриды (X = I, Br, Cl) > ангидриды (X = OCOR) > эфиры (X = OR') >> амиды (X = RNHR') >> кислоты (X = OH, депротонирование!)
Взаимодействие производных карбоновых кислот с металлоорганическими соединениями
|
|
|
|
|
R'MgX |
|
|
|
|
|
|
1. R'MgX |
|
|
O |
|
|
|
|
||||
RCO H |
RCO |
- |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
2 |
-R'H |
2 |
|
2. H3O+ |
R |
|
|
R' |
|
|
|
|
||||||||
|
|
|
|
1. R'MgX |
|
O |
|
|
|
|
|
|
|
|
R'MgX |
|
|
|
R'MgX |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
|||||||
RCN |
|
|
|
|
|
|
|
|
|
|
RCONH2 |
|
|
|
|
|
RCONH |
|
|||||
|
2. H O+ |
R |
|
R' |
|
|
-R'H |
|
|
|
|||||||||||||
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|||||||
O |
|
|
|
1. R'2CuLi |
|
|
|
1. R'MgX /Cd2+ |
|
O |
|
||||||||||||
|
|
|
RCOCl |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
2. H3O+ |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
2. H3O+ |
|
|
|
R |
|
|
R' |
|
|||||||||
R |
|
R' |
|
|
|
|
|
|
|
||||||||||||||
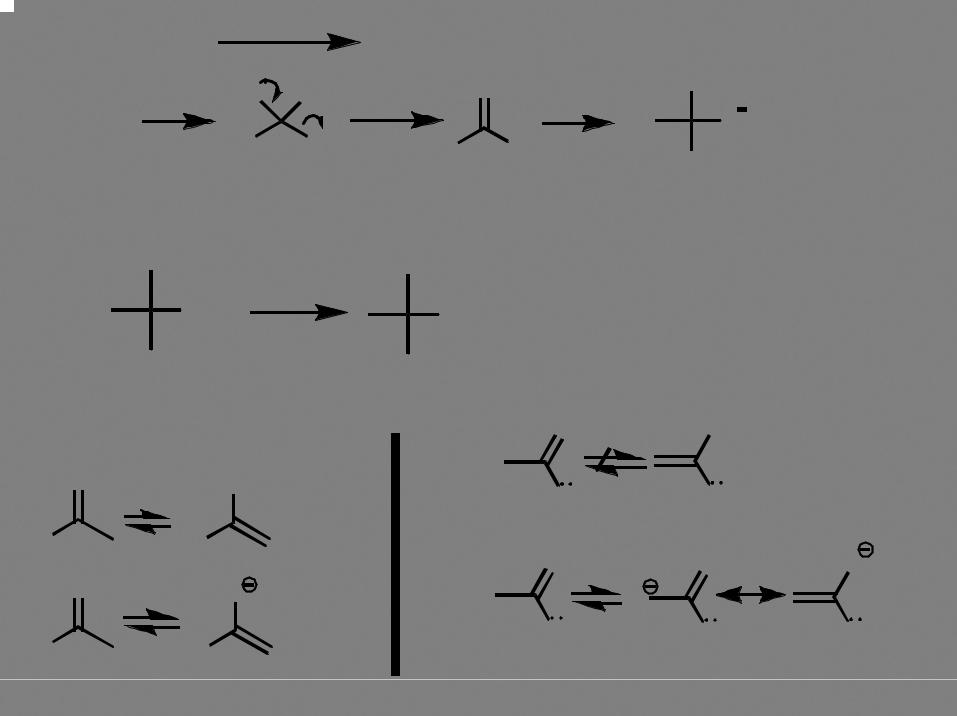
RCOCl |
R'MgX/FeCl3 |
|
|
|
27 |
|
|
RCOR' |
«обратный порядок прибавления» |
||||
|
-78o |
|
O |
|
R |
|
R'MgX |
-O |
R' |
|
R'MgX |
||
|
O |
|||||
RCO2R" |
R |
OR"- R"O- |
|
|
R' |
|
|
R |
|
R' |
R' |
||
|
|
|
|
|
|
|
реакцию практически невозможно остановить на стадии образования кетона - более активного, чем сложный эфир, нуклеофила (алкоксигруппа - донор по мезомерному эффекту, снижающий частичный положительный заряд на атоме углерода)
HCO2Et
MgCl
- 20o
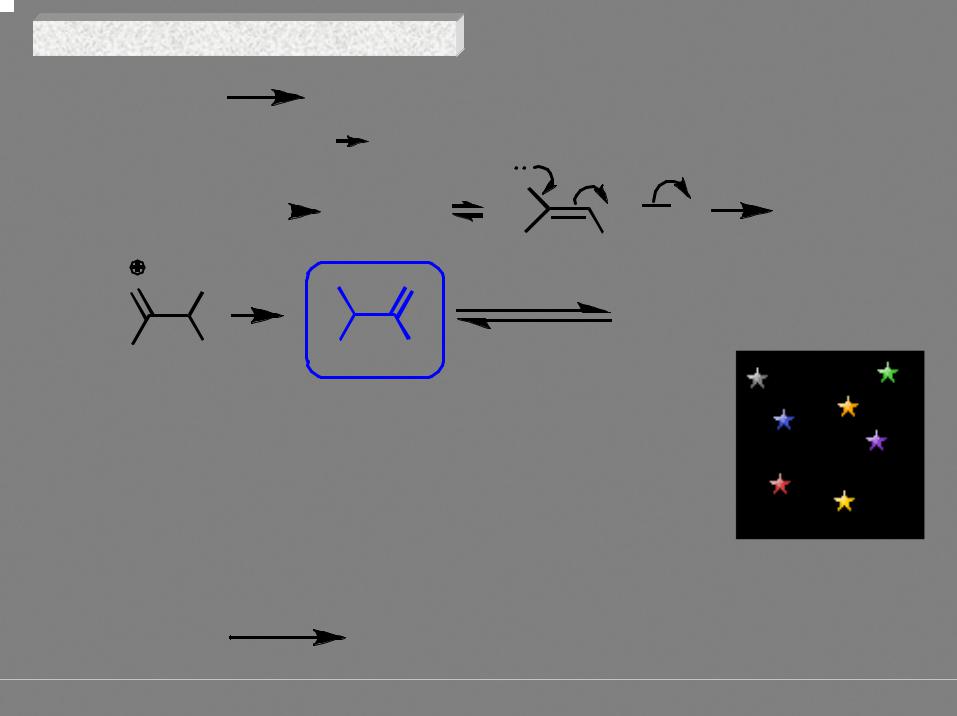
Реакции по α-углеродному атому
Карбонильные
соединения
O H+ OH
R R
O HO- O
R R
CHO |
«обратный порядок прибавления» |
Производные карбоновых кислот
O H+ OH
X X
нехарактерно, кроме Х = галоген
O |
B- |
O |
O |
X |
-H+ |
X |
X |
резонансная стабилизация малозначима (мезомерное влияние гетероатома)
28
Реакция Геля-Фольгарда-Зелинского
RCH2CO2H |
Br2 |
RCHBrCOBr или RCHBrCO H |
|||||
|
|
P |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
Br2 + P |
PBr3 |
|
|
|
|
RCH2CO2H |
PBr3 |
RCH2COBr |
HO |
|
Br Br |
||
|
|
||||||
-P(OH)3 |
|
|
|||||
|
|
|
|
Br |
R |
-Br- |
|
|
|
|
|
|
|
||
HO |
Br |
|
Br |
O |
RCH2CO2H |
|
RCHBrCO2H |
|
|
|
|
|
|
||
|
|
-H+ |
|
|
-RCH2COBr |
|
|
Br |
R |
R |
Br |
|
|
||
При использовании 1/3 моля красного фосфора продуктом реакции является галогензамещенный галогенангидрид, в случае каталитических количеств фосфора – галогензамещённая кислота. Для получения бромангидрида монобромзамещенной кислоты необходимо 2 моля брома.
Другие способы галогенирования:
RCH CO H |
SO2Cl2 |
RCHXCO2H |
X = Cl, Br |
|
2 |
2 |
|
|
|
(Br2/пиридин, Br2/RCOBr, CuBr2)

29
Конденсация Кляйзена
Более низкая СН-кислотность сложных эфиров по сравнению с карбонильными соединениями требует применения более сильного основания - EtO- (NaNH2, NaH, Na)
|
O |
|
O |
|
O O |
OEt |
|
RCH2CO2Et |
EtO- |
|
|
|
|||
EtO |
R |
EtO |
EtO |
|
|
-EtO- |
|
|
|
|
|||||
|
метиленовая |
|
R |
R |
R |
|
|
|
карбонильная |
|
|
|
|||
|
компонента |
компонента |
|
|
|
||
O |
O |
|
O |
O |
O |
O |
|
EtO |
EtO- |
EtO |
|
EtO |
|
|
|
-EtOH |
|
|
|
||||
|
|
|
|
|
R |
R |
|
R |
R |
|
R |
R |
|
||
все стадии процесса обратимы, равновесие сдвигается в сторону образования продукта за счёт солеобразования на последней стадии

Перекрестная конденсация |
30 |
|
эфир + эфир = β-кетоэфир
RCO Et + R'CH CO Et EtO- |
O |
|
возможно при отсутствии в молекуле |
||||||||
|
CO Et |
||||||||||
|
карбонильной компоненты атомов |
||||||||||
2 |
2 |
2 |
|
R |
|
2 |
водорода у |
α |
-углеродного атома в составе R |
||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
R' |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
HCO2Et, (CH3)3CCO2Et, CF3CO2Et, |
|||
|
|
|
|
EtO- |
|
CO2Et |
|||||
ArCO2Et |
+ CH3CO2Et |
Ar |
(EtO)2CO, (CO2Et)2 |
|
|||||||
|
|
|
|
||||||||
Эфир + карбонат = малоновый эфир |
|
|
|
|
|
||||||
|
O |
|
|
|
|
O |
|
CO2Et |
CO Et |
||
|
+ |
|
CH3CO2Et |
NaH |
|
|
|
|
|
2 |
|
|
|
EtO |
|
OEt |
|
- EtO- |
|
||||
EtO |
OEt |
|
|
|
|
|
|
CO2Et |
|||
малоновый
эфир
