
Лекции / organic_2011_6
.pdf
Эфир + формиат = β-альдегидоэфир |
31 |
||||||||||||
|
|
|
|
||||||||||
|
|
|
R'CH2CO2Et |
+ HCO Et |
NaH |
O |
CO2Et |
||||||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R' |
|
б) эфир + кетон = β-дикетон |
|
|
|
|
|||||||||
O |
|
|
|
|
O |
|
O |
||||||
|
|
+ |
R'CH CO Et |
EtO- |
|
|
|
|
|
R' |
|||
|
|
|
|
|
|
|
|||||||
R |
2 |
2 |
R |
|
|
|
|
||||||
|
|
|
|
|
|
||||||||
метиленовая |
карбонильная |
|
|
|
|
||||||||
компонента |
компонента |
|
|
|
|
|
|
|
|
|
|||
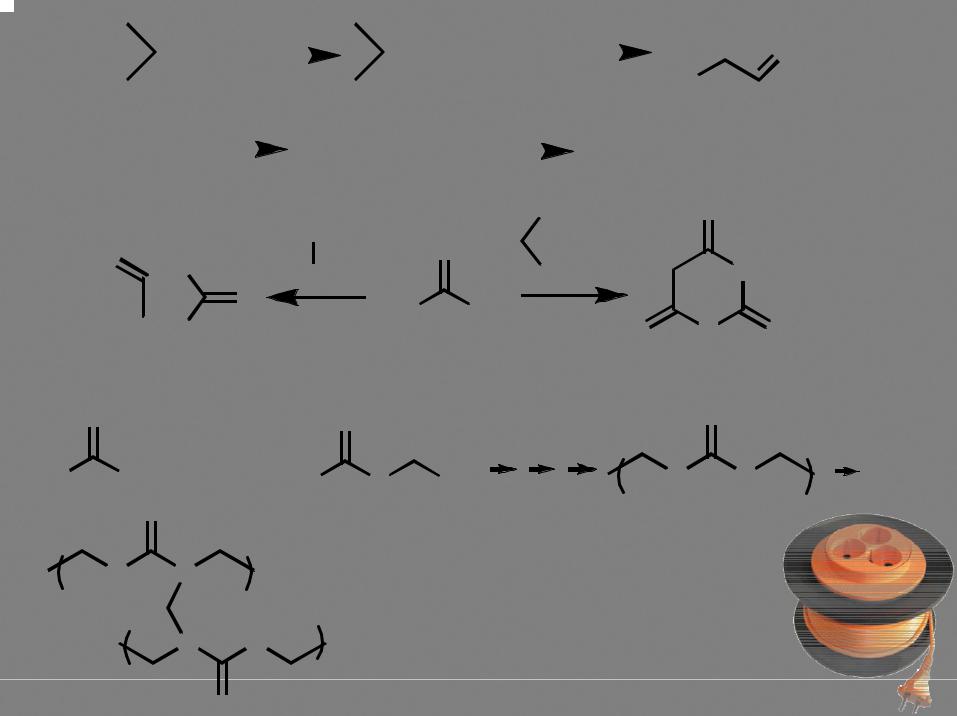
СН-кислотность кетона заметно выше, чем у сложного эфира (резонансная  стабилизация). Поэтому, применение достаточно сильного основания позволяет проводить реакцию таким образом, чтобы кетон преимущественно выступал в качестве метиленовой компоненты.
стабилизация). Поэтому, применение достаточно сильного основания позволяет проводить реакцию таким образом, чтобы кетон преимущественно выступал в качестве метиленовой компоненты.
в) эфир + альдегид
Такую перекрестную конденсацию осуществить, как правило, не удается – альдегид и более сильная СН-кислота, и значительно более активная карбонильная компонента, чем сложный эфир. Будет происходить конденсация альдегида самого с собой. 

а если у альдегида нет протонов у α-углеродного атома? |
32 |
||
EtO- |
|||
PhCO2Et + PhCH2OH |
EtO- |
||
PhCHO + CH3CO2Et |
конденсация |
||
Канницаро а если сложный эфир сильная СН-кислота?
CO2Et |
NEt3 |
CO2Et |
RCHO + |
|
Кневенагель |
CO2Et |
R |
CO Et |
|
2 |
|
CH3CO2Et 1. LDA |
|
CO2Et |
2. PhCHO Ph |
|
|
такая конденсация в принципе возможна, поскольку альдегид не может быть метиленовой компонентой, а очень сильное основание (и очень слабый нуклеофил!) может создать большую концентрацию аниона из сложного эфира.
CH CO Et + CH3CH2O |
CH CO Et + |
CH |
CHO |
самоконденсация |
||
2 |
2 |
3 |
2 |
2 |
|
альдегида |
|
|
|
|
|
|
|
При наличие протона у α-углеродного атома альдегида реакция сильно затрудняется
(осуществима с трудом) вследствие переноса этого протона на анион сложного эфира)
Конденсация Перкина
RCHO |
Ac2O |
R |
CO2H |
R не должен содержать протонов |
|
AcONa |
|
у α-углеродного атома |
|
|
t |
|
|
|
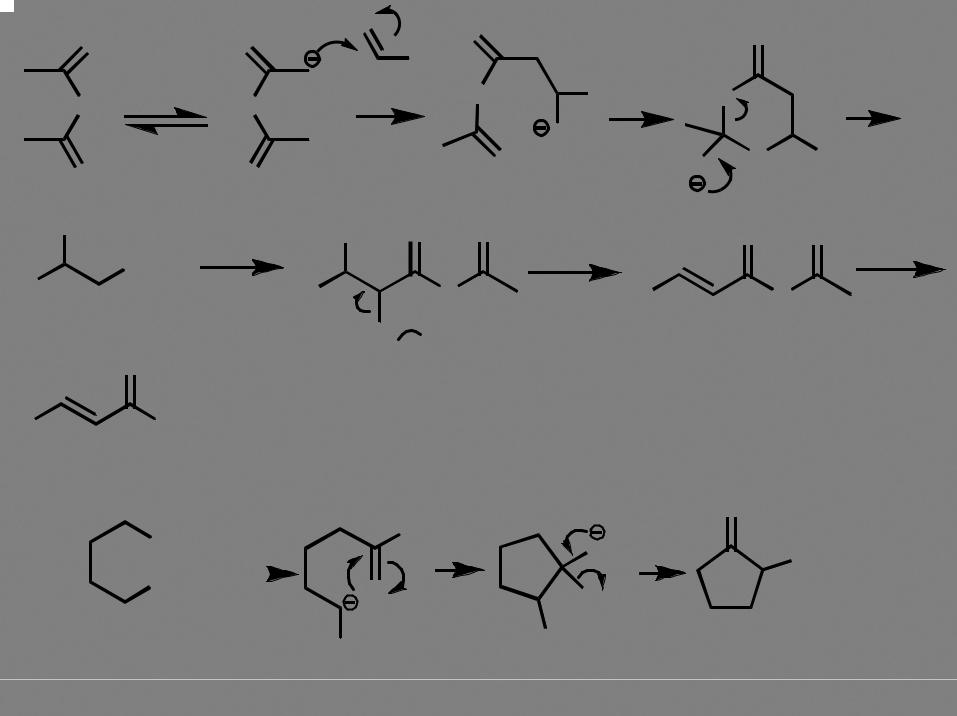
O
O
O
OAc
R
O
AcONa O
- AcOH
O
CO2- Ac2O
- AcO-
O
O
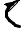 OAc
OAc
R
H
|
O |
|
O |
|
33 |
R |
|
|
|
||
|
|
|
|
|
|
|
O |
R |
O |
|
|
|
|
O |
O O |
R |
|
|
|
O |
|
||
O |
O |
E2 |
O |
O |
H3O+ |
|
|
||||
|
O |
- AcOH R |
|
O |
|
|
|
- AcO- |
|
|
|
 -OAc
-OAc
R |
OH R = Ph - коричная кислота |
Конденсация Дикмана - разновидность конденсации Кляйзена, приводящая к
образованию циклических продуктов
O
CO2Et EtO- |
OEt |
|
|
O |
CO Et |
||
CO2Et |
O |
|
2 |
OEt |
|
||
|
CO2Et |
CO2Et |
|
|
реакция подходит для синтеза 5- и 6-членных циклов |
|
|

межмолекулярная конденсация Дикмана |
|
34 |
||
|
|
|||
|
|
O |
|
|
CO2Et |
EtO2C |
|
EtO C |
O |
|
EtO- |
OEt |
2 |
|
2 |
|
OEt |
||
|
|
|
||
CO2Et |
EtO2C |
CO Et |
EtO2C |
|
|
|
2 |
|
CO2Et |
|
|
|
|
|
EtO2C |
O |
O |
|
|
OEt |
EtO2C |
|
O |
OEt |
||
|
|||
CO2Et |
O |
||
|
|||
EtO |
CO2Et |
||
|
|||
|
|
EtO |
Реакции дианионов
|
|
NaNH2 |
|
CO2 |
|
R |
CO2H |
R |
CO2- |
||
(LDA) |
|||||
|
|
|
R'X |
||
|
|
|
|
SN2 |
EtO2C
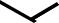 O
O
O
 CO2Et
CO2Et
CO2-
RCO2-
-78 oC
R CO2-

Ацилоиновая конденсация |
|
|
35 |
||
|
|
|
|||
|
|
O |
|
O |
|
CO2Et |
Na |
|
OEt |
OEt |
|
n(H2C) |
эфир |
n(H C) |
|
n(H2C) |
-2OEt- |
CO2Et |
2 |
OEt |
OEt |
||
O |
O |
|
O |
|
O |
|
|
OH |
n(H C) |
Na |
n(H2C) |
H2O |
n(H2C) |
|
2 |
|
|
|
|
|
O |
|
O |
|
ацилоин |
O |
|
|
|
|
|
реакция пригодна для получения макроциклов
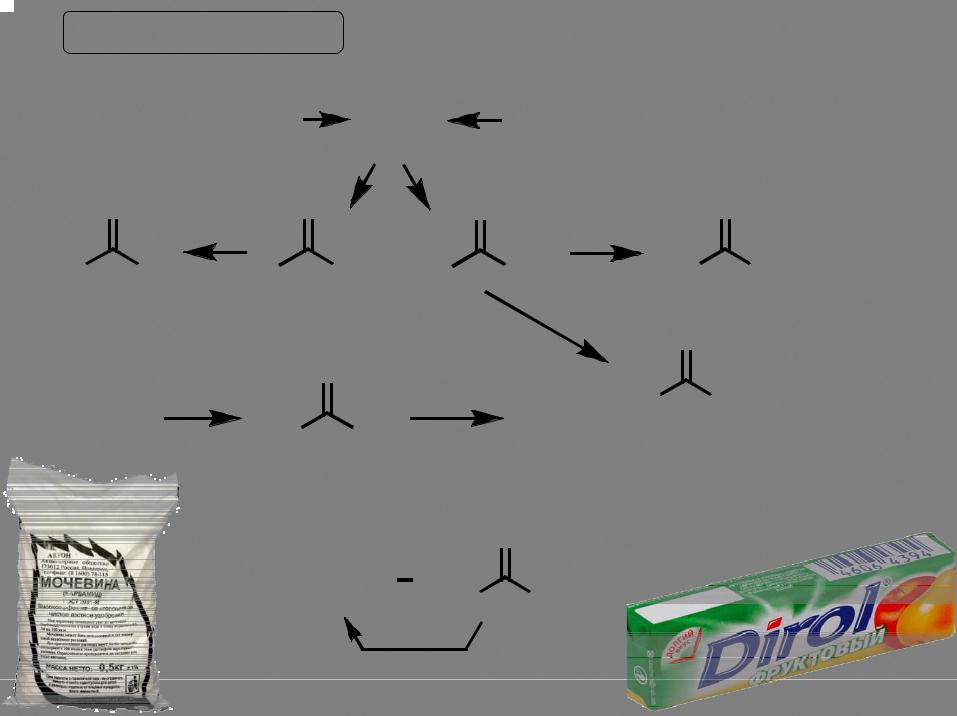
Дикарбоновые кислоты |
|
|
|
|
|
36 |
|||
|
|
|
|
|
|
||||
Производные угольной кислоты |
|
|
|
|
|||||
|
CO + Cl2 |
C |
COCl2 |
CCl4 |
+ SO3 |
|
|||
|
t |
|
|||||||
|
|
|
|
фосген |
|
|
|
|
|
|
|
|
ROH |
|
RNH2 |
|
|
|
|
|
O |
O |
|
O |
|
RNH2 |
|
O |
|
|
ROH |
|
|
|
|
|
|
|
|
RO |
OR |
Cl |
OR |
|
Cl |
NHR |
|
RHN |
NHR |
карбонат |
хлорформиат |
|
ROH |
мочевина |
|||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
O |
|
|
CO2 |
|
O |
|
H3O+ |
|
|
RO |
NHR уретан |
|
|
|
|
ROH |
|||||
|
RONa |
NaO |
OR |
|
|
|
|||
|
t |
- CO2 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
Мочевина (карбамид)
O
CO2 + NH3 t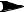
P H2N NH2
H2O
(медленно)
37
|
|
N2 |
|
|
H O |
|
O |
|
t |
|
|
||
|
|
|
CN2Ca |
|
|
|
NH4CNO |
||||||
NH CNS |
CaC |
|
|
2 |
|
|
|
|
|
||||
2 |
|
|
|
|
|
|
H2N |
NH2 |
|
|
|
||
|
4 |
t |
|
|
|
|
|
|
Велер |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||
|
t |
CO2 |
|
NH3 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
NH |
|
|
|
O |
O |
||||
|
S |
|
H2O |
|
|
t |
|
||||||
|
|
H2S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
N |
NH2 |
|
H2 |
NH2 |
H NCN |
|
H N |
|
NH |
|
|
|||||
2 |
|
|
2 |
|
|
H |
|
||||||
|
|
|
2 |
|
|
|
|
|
|
||||
N |
|
|
|
|
гуанидин |
|
|
|
биурет |
||||
|
|
|
|
|
|
|
|
||||||
Свойства мочевины |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
O |
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- H+ |
H2N |
|
NH2 |
|
H2N |
NH2 |
|
|
|||
|
H2N |
NH |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
сравнительно высокая |
|
низкая основность и нуклеофильность |
|
|
||||||||
|
кислотность |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HNO2 |
O |
NH |
CH |
3 |
Cl- |
HO |
NHCH3 |
|
|
O |
|
N2 + CO2 + H2O |
|
|
|
3 |
|
|
|
|
|
|
|
||
H O H2N |
|
NH2 |
|
t |
|
|
H2N |
NH3 |
|
H2N |
N |
||
|
|
|
|
|
|
|
|||||||
|
|
2 |
|
|
|
|
|
|
|
|
- NH3 |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
||
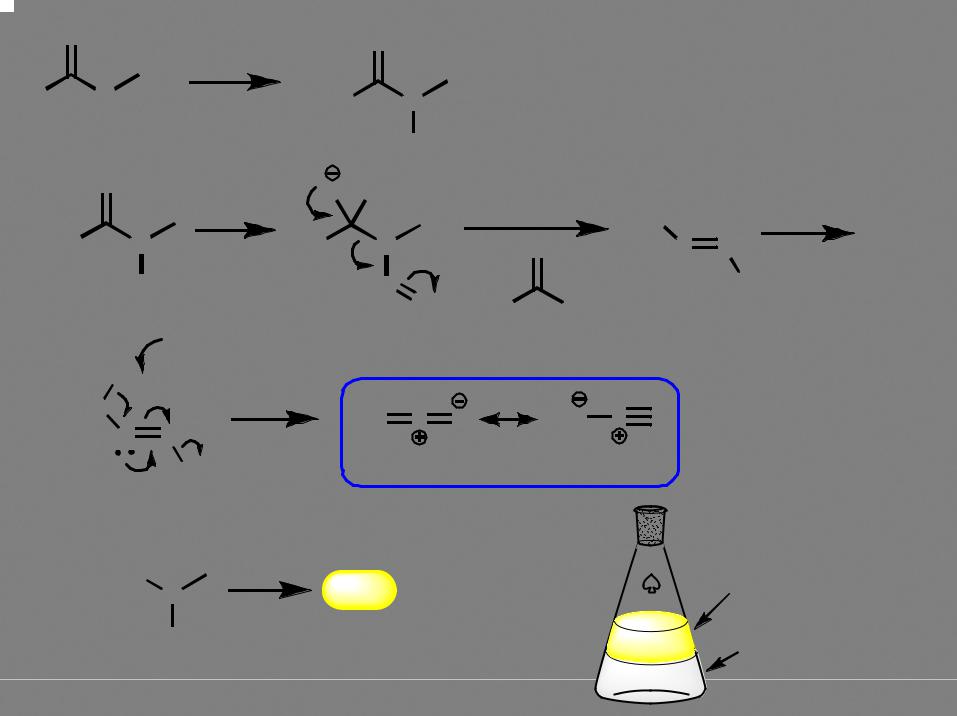
O |
|
|
|
O |
|
|
|
38 |
|
NaNO2 |
|
|
нитрозометилмочевина - канцероген. |
||||
|
|
|
|
|
||||
H N |
N |
|
|
|
|
Реакция происходит по этому атому азота |
||
H3O+ |
H2N |
N |
вследствие донорного влияния метильной группы |
|||||
2 |
H |
|
|
|
||||
|
|
|
|
|
NO |
|
|
|
|
O |
HO- |
O |
OH |
|
|
H3C |
H O |
|
|
|
|
|
|
|||
H2N |
N |
|
H2N |
N |
|
|
2 |
|
|
|
O |
N N |
- HO- |
||||
|
NO |
|
|
N |
|
_ |
|
O- |
|
|
|
O H2N |
O- |
||||
|
|
|
|
|
||||
|
-OH |
|
|
|
|
|
|
|
|
H |
- H2O |
|
|
|
|
|
|
H2C |
H C N N |
H2C N N |
|
|||||
|
|
|
||||||
|
N N |
- HO- |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
OH |
|
|
|
диазометан |
|
|
ArO2S |
HO- |
раствор |
N |
CH2N2 |
диазометана в эфире |
NO |
|
концентрированный |
|
|
водный раствор KOH |
|
|
|
|
|
HgO |
|
|
|
|
|
2CH2N2 |
O |
39 |
||||||
|
|
NNH |
N |
RCOCl |
|
|
|
N2 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
2 |
|
|
|
|
|
2 |
|
|
|
|
- CH3Cl R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
CH2N2 |
|
|
|
|
|
CH |
N |
- N2 |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
RCO2H |
|
|
|
RCO2CH3 |
ROH |
|
2 |
|
2 |
ROCH3 |
|
|
|
|
|||||
|
|
|
|
BF3 |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
O H
 N
N
O
O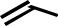 N H
N H
парабановая
кислота
O
CH2O H2N NH2 
|
O |
|
N |
N |
n |
H |
|
|
|
N |
H |
|
N |
|
|
|
O |
CO2H |
|
|
CO2H |
|
O |
|
|
|
O |
|
|
|
|
|
|
CO2H |
|
CO2H |
|
|
NH |
|
|
|
|
|
|
|
|||
t |
H2N |
NH2 |
t |
O |
N |
O |
|
|
|
|
|
|
H |
|
|
|
|
|
|
барбитуровая |
|
||
|
|
|
|
|
кислота |
|
|
O |
|
|
|
|
O |
|
|
H2N |
N |
OH |
|
|
N |
N |
n |
|
H |
|
|
|
H |
H |
|
мочевино-формальдегидные смолы
 n
n
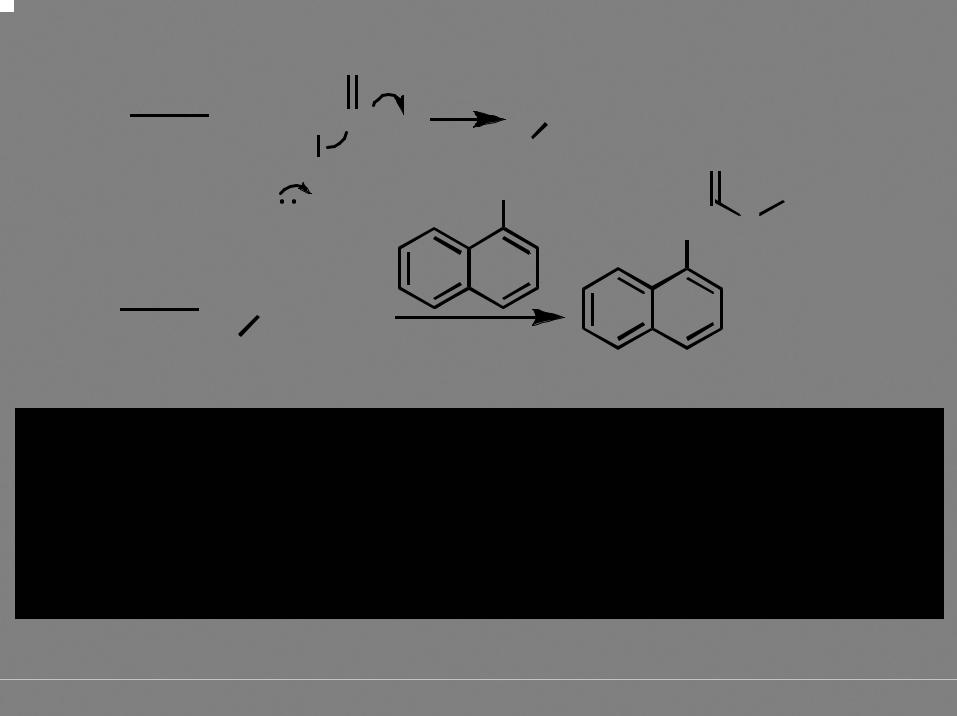
Изоцианаты, изотиоцианаты Синтез O
COCl2
ArNH2 t  Ar
Ar N
N Cl
Cl
H
ArNH
COCl2
CH3NH2 t  N
N C
C O
O
40
N C
C O
O
Ar
O
OH
O N
N
H
"севин" - гербицид
Бхопальская катастрофа — последствия аварии на химическом заводе Union Carbide в индийском городе Бхопал (штат Мадхья-Прадеш) ранним утром 3 декабря 1984 года, повлёкшей смерть, по крайней мере, 18 тысяч человек, из них 3 тысячи человек погибли непосредственно в день трагедии, и 15 тысяч — в последующие годы. По различным данным, общее количество пострадавших оценивается в 150—600 тысяч человек. Эти цифры дают основание считать бхопальскую трагедию крупнейшей в мире техногенной катастрофой по числу жертв
