
Лекции / organic_2011_6
.pdf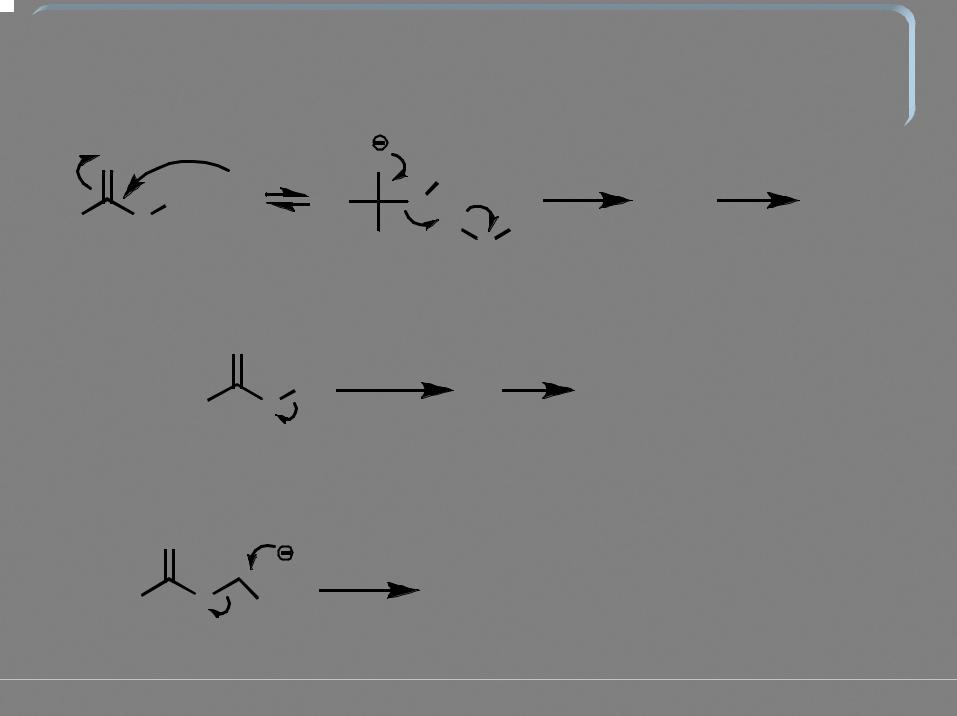
Образование эфиров при взаимодействии карбоновых кислот со спиртами в |
11 |
||||||||||
условиях щелочного катализа невозможно вследствие того, что первая стадия |
|
||||||||||
процесса – депротонирование карбоксильной группы, а образующийся |
|
|
|||||||||
карбоксилат-анион является очень слабым электрофилом. |
|
|
|
||||||||
|
O |
HO- |
O |
|
R' |
|
- HO- |
|
HO- |
|
|
R |
R' |
R |
O |
|
RCO2H |
RCO2- |
|
||||
O |
|
OH |
|
H |
H - R'OH |
|
-H2O |
|
|
||
|
|
|
|
O |
|
|
|
|
|
|
|
|
реакция необратима |
|
|
|
|
|
|
|
|
||
Другие механизмы гидролиза |
|
|
|
|
|
|
|
|
|||
|
|
O |
|
|
|
H2O |
|
|
|
|
|
|
SN1 |
|
R |
|
R+ |
|
|
|
|
||
|
O |
|
- H+ |
ROH |
|
|
|
|
|||
|
R' |
- R'CO2- |
|
|
|
|
|
|
|||
возможно только в случае образования устойчивых катионов - аллильного, бензильного, трет-бутильного!
скорость реакции не зависит от рН среды
|
O |
I |
|
|
|
|
SN2 |
|
LiI |
R'CO - |
+ |
RCH I |
|
R' |
O |
R |
DMSO |
2 |
2 |
|
|
|
|
||||
|
|
|
|
|
реакция очень чувствительна к характеру заместителя и позволяет гидролизовать метиловые эфиры (R =H) в присутствие этиловых (R = CH3)
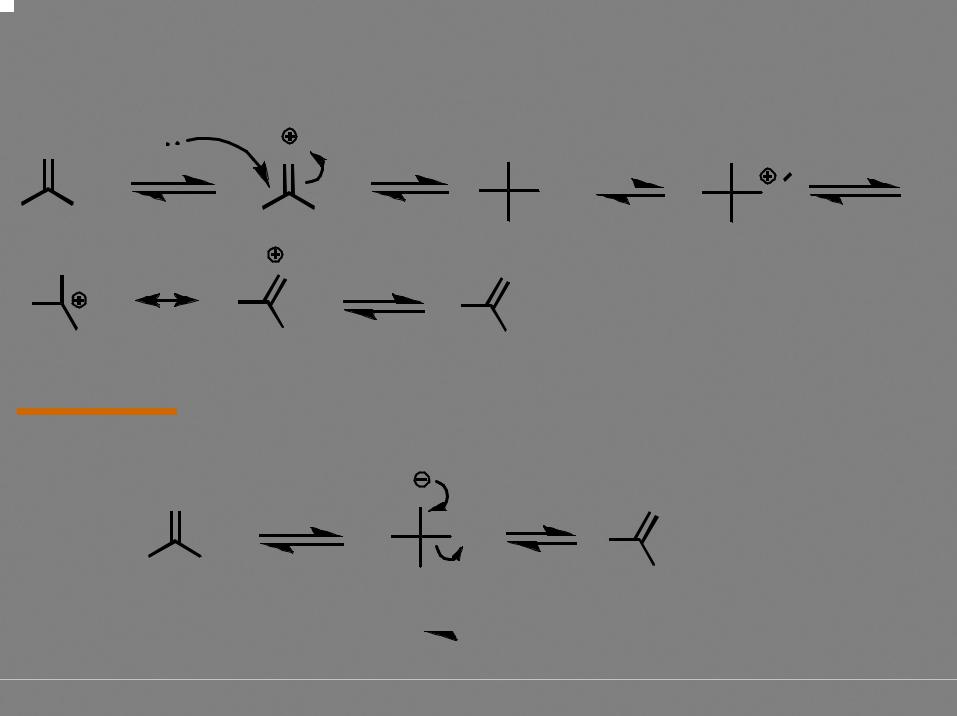
Другие способы получения сложных эфиров |
12 |
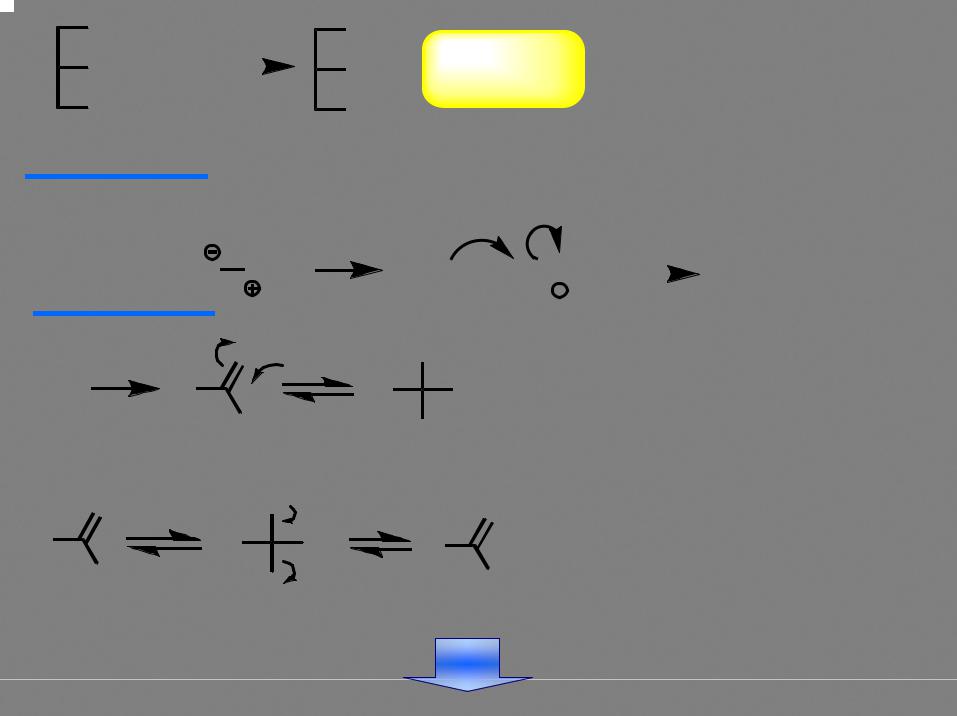
Переэтерификация в кислой среде
|
O |
R"OH |
|
HO |
|
|
OH |
+ H |
+ |
OH |
R' |
|
|
|
|
|
|
|
|
||||||||
R |
OR' |
|
H+ |
R |
OR' |
|
R |
OR' |
|
R |
OH |
- R'OH |
|
|
- H+ |
OR" |
|
|
OR" |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
OH |
|
|
|
OH |
_ |
|
O |
|
|
|
|
|
R |
|
R |
|
|
+ H+ |
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
OR" |
|
|
|
OR" |
|
|
OR" |
|
|
|
|
|
|
Все стадии реакции обратимы. Положение равновесия определяется избытком спирта |
||||||||||||
|
|
основный катализ |
|
|
|
|
|
|
|
|
|||
|
|
|
O |
|
R"OH |
|
O |
|
|
|
O |
|
|
|
|
R |
OR' |
|
R"O- |
R |
OR' |
- R'O- |
R |
|
|
|
|
|
|
|
|
OR" |
|
|
OR" |
|
|
||||
R'O- + R"OH 
 R"O- + R'OH
R"O- + R'OH
Положение равновесия определяется избытком спирта
OCOR1 |
|
|
|
OH |
|
|
13 |
EtOH |
|
|
ΣRiCO2Et |
|
|
||
OCOR2 |
|
OH + |
|
|
|||
H+(EtO-) |
|
|
|
||||
|
|
||||||
|
|
|
|||||
OCOR3 |
|
|
|
OH |
|
|
|
|
|
1. "биодизель" |
|
||||
|
|
|
|
||||
|
|
|
|
|
|
||
2. анализ растительных жиров в виде эфиров
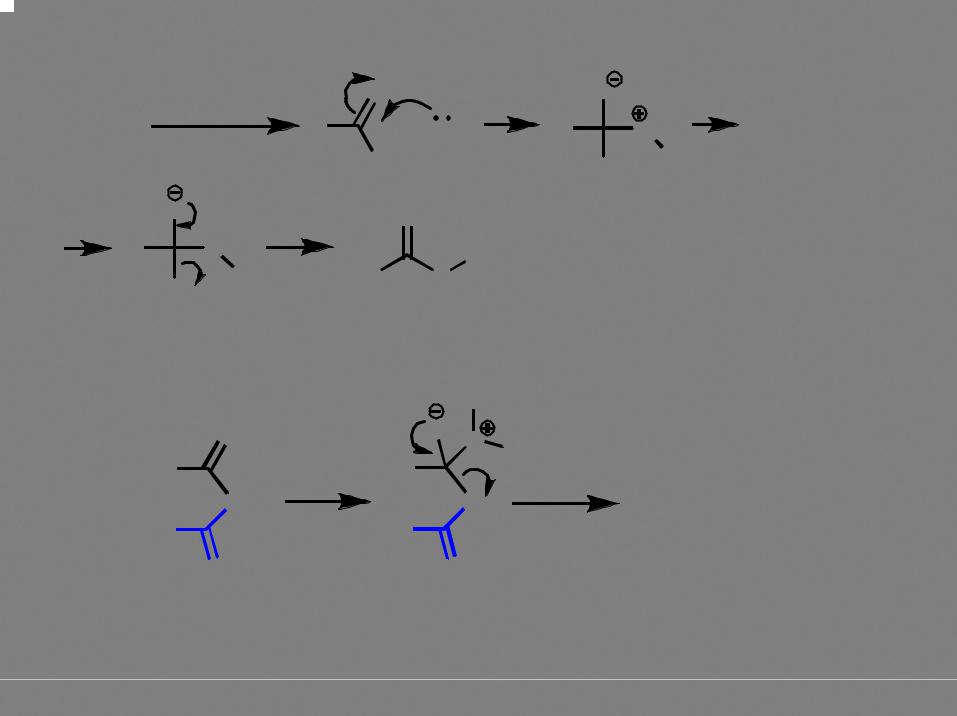
Взаимодействие с диазометаном
RCO2H + H2C N N
N
RCO2H |
Nu- |
O |
Nu- |
R |
|
||
- NuH |
|
||
|
O- |
|
|
|
|
|
|
|
|
слабый |
|
|
|
электрофил |
|
|
RCO2- + |
H3C |
|
N |
|
N |
SN2 |
RCO2CH3 |
|||
|
|
|
|||||||||
|
|
|
- N2 |
||||||||
|
|
|
|||||||||
|
O- |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|||||
|
нет приемлемой уходящей группы кроме |
||||||||||
R |
|
|
Nu |
Nu- - карбоновые кислоты и их соли очень |
|||||||
|
|
||||||||||
|
|
|
|
малореакционноспособны по отношению к |
|||||||
|
O- |
нуклеофилам! |
|
||||||||
O |
Nu- |
|
O- |
O |
R |
- X- |
|||
R |
|
Nu |
R |
|
X |
|
|
X |
Nu |
если группа Х не способна к депротони-
рованию и является хорошей уходящей, то реакции с нуклеофилами происходят легко!
Синтез эфиров из хлорангидридов
|
SOCl2 |
|
|
O |
|
||
RCO2H |
|
R |
|
R'OH |
|||
(PCl5, PCl3) |
Cl |
||||||
|
|
|
|||||
|
|
|
|
|
|
||
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
||
R |
|
O |
-Cl- |
|
R |
R' |
|
|
|
R' |
|
||||
|
Cl |
|
|
O |
|||
|
|
|
|
|
|
||
14
|
O |
|
|
R |
|
OH |
-H+ |
|
Cl |
R' |
|
|
|
|
Cl- - хорошая уходящай группа!
Синтез эфиров из ангидридов |
|
|
|
|
|
|
|
O |
R' |
|
|
|
O |
O |
H |
|
|
R |
|
R |
|
||
R'OH |
|
- RCO2- |
|
||
|
|
O |
RCO2R' |
||
R |
O |
R |
- H+ |
||
|
|
|
|||
|
O |
|
O |
|
|
|
RCO2- - хорошая уходящая группа! |
||||
15
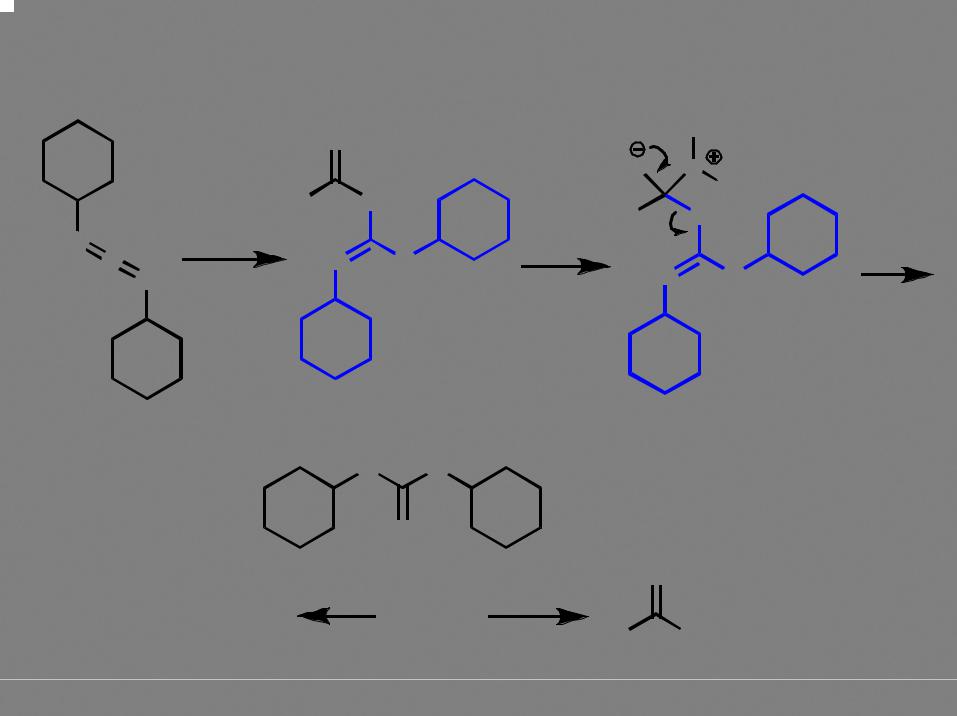
Активация карбоксильной группы при этерификации (конденсация в присутствие дициклогексилкарбодиимида – ДЦК)
|
|
O |
|
|
|
|
H |
|
|
|
|
O |
|
O |
|
|
|
|
|
|
|
||
|
R |
|
O |
|
|
|
R' |
N δ+ |
|
|
R |
|
O |
||
RCO2H |
|
|
|
|
|||
N |
|
N |
R'OH |
|
|
||
C |
|
|
|
N |
N |
||
N |
|
|
|
H |
|
||
|
|
|
|
|
|
|
H |
хорошая уходящая группа |
|
|
|
ДЦК |
H |
|
|
H |
|
|
|
N |
N |
|
|
RCO2R' + |
O |
|
|
|
|
|
|
ДЦК |
R'NH2 |
|
O |
|
|
||
(RCO)2O |
RCO2H |
R |
NHR' |
|
ДЦК |
||
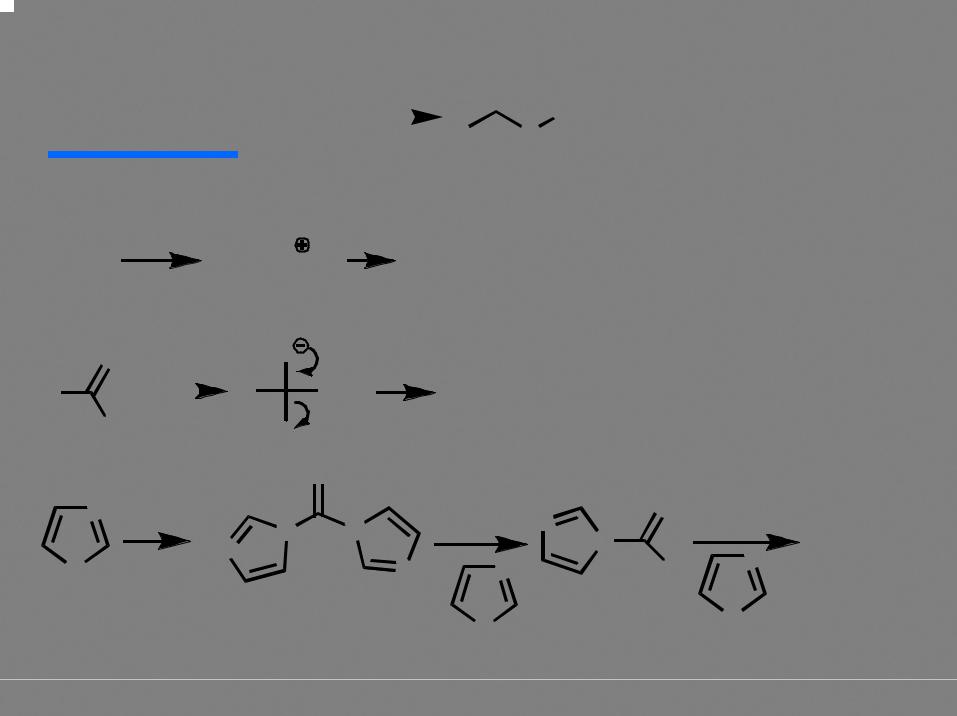
Синтез эфиров из солей карбоновых кислот |
16 |
||||
|
|||||
RCO - R'X |
O |
|
|||
|
|
|
R' |
||
|
|
|
|||
2 |
SN2 R |
|
|
O |
|
|
|
|
|
||
Амиды карбоновых кислот
R'NH2 |
RCO2- R'NH3 |
t |
RCO2H |
RCONHR' |
аммонийная
соль
реакция происходит в жестких условиях - нет хорошей уходящей группы!
O |
R'NH2 |
O |
|
|
если Х- - хорошая уходящая |
||
R |
NHR' |
RCONHR' |
группа (галогенид-, карбоксилат-, |
||||
R |
-H+ |
в некоторой степени |
|
||||
X |
X |
-X- |
|
OR), реакция происходит легко |
|||
|
|
|
|||||
|
|
|
O |
|
|
|
|
N |
COCl |
|
|
RCO2H N |
O |
R'NH |
|
|
2 |
N |
N |
N |
2 |
RCONHR' |
|
|
|
N |
|
N |
N |
||
N |
|
|
N |
R |
|
||
|
|
- |
|
||||
H |
|
|
|
- |
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
H |
|
|
|
|
17 |
|
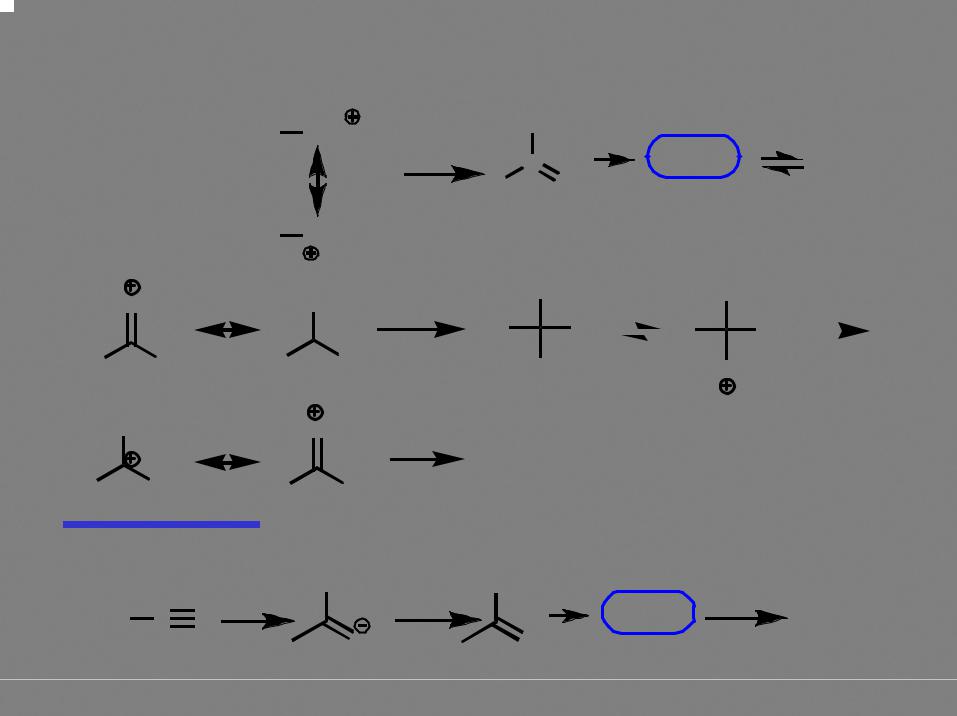
Гидролиз нитрилов |
||
|
||
|
|
в кислой среде
H3O+ RCN 
OH
R NH2
OH
R OH
R C NH
NH
R C NH
NH
OH
R  NH2
NH2
OH
R OH
H2O
-H+
H2O
-H+
-H+
OH |
H+ |
|
C |
||
RCONH2 |
||
R |
NH |
|
OH |
H+ |
OH |
|
|
|
||||||
R |
|
|
OH |
|
|
|
|
|
||||
|
|
|
|
|
R |
|
|
OH |
|
|
||
|
|
|
|
|
|
|
- NH |
|||||
|
|
|
|
|
|
|
||||||
|
NH2 |
|
|
|
|
NH |
3 |
|||||
|
|
|
|
|
|
|
|
3 |
|
|
||
RCO2H
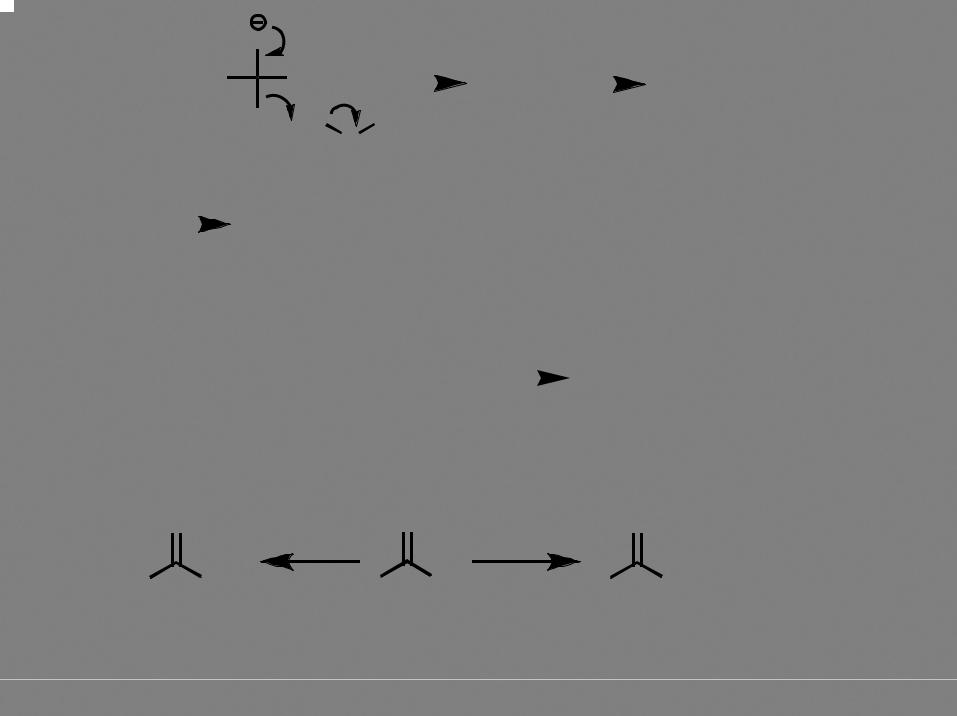
в щелочной среде |
OH |
OH |
|
||
δ+ |
|
HO- |
HO- |
||
|
H2O |
|
|||
R C |
N |
H2O |
N -HO- |
NH |
RCONH2 |
18
|
|
|
O |
|
|
|
|
|
|
|
|
|
|||
|
|
R |
|
|
OH |
|
|
|
RCO H |
HO- |
|
RCO2- |
|||
|
|
|
|
||||||||||||
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
- NH |
2 |
|
H2O |
|
||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
NH2 H |
H |
|
3 |
|
|
|
|
|
||||
|
|
|
-HO- |
|
|
|
|
|
|||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
H2O2 |
|
|
|
селективныйгидролиз нитрилов вамиды |
||||||||||
RCN |
RCONH2 |
(происходит вболее мягких условиях, поскольку |
|||||||||||||
|
|
вкачестве нуклеофила выступает более сильный, |
|||||||||||||
HO- |
|||||||||||||||
|
|
|
|
чем гидроксид-анион - супероксид анион НО2- |
|||||||||||
|
|
|
|
|
|
||||||||||
Обратная реакция (дегидратация амидов) |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
RCONH2 |
|
SOCl2 |
|
|
RCN |
|
|||
|
|
|
|
|
|
|
или P O |
5 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
t |
|
|
|
|
|
|
Амиды могут быть получены из кетонов (оксимов) перегруппировкой Курциуса (Бекмана)
O |
N - |
O |
1. NH OH |
|
O |
|
3 |
|
2 |
|
|
R |
NHR H2SO4 R |
R |
2. H+ |
R |
NHR |
|
Курциус |
|
|
Бекман |
|
19
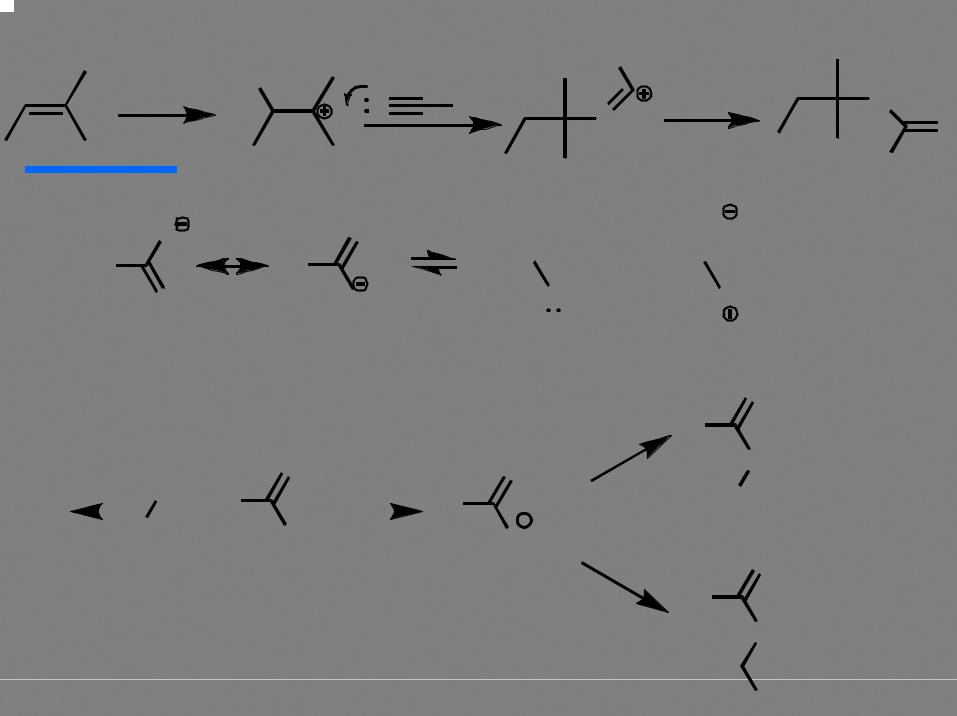
Риттер |
|
|
R |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
RCN |
N |
R |
N |
+ H2O |
NH |
H2SO4 |
|
|
- H+ |
O |
|
|
|
|
|||
Некоторые свойства амидов |
|
|
|
|
R |
|
|
|
|
|
O |
O |
R |
R |
NH |
NH |
±
H+
O O R 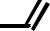
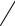

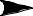 R
R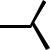
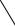
NH2 NH2
повышенная NH-кислотность
(струтура изоэлектронна карбоксилат-аниону) |
|
пониженная основность |
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
R'X (SN2) |
R |
|
|
|
|
|
N |
|
|
R |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
R'X (SN2) |
|
O |
|
|
O |
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
NaH |
|
|
|
|
|
|
|
|
|
|
R' |
|
|
||||||||
|
|
R |
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
R'COCl |
HN |
|
R |
- H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
N |
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R'COCl |
|
|
|
|
|
|
O |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
N |
|
|
R |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R' |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
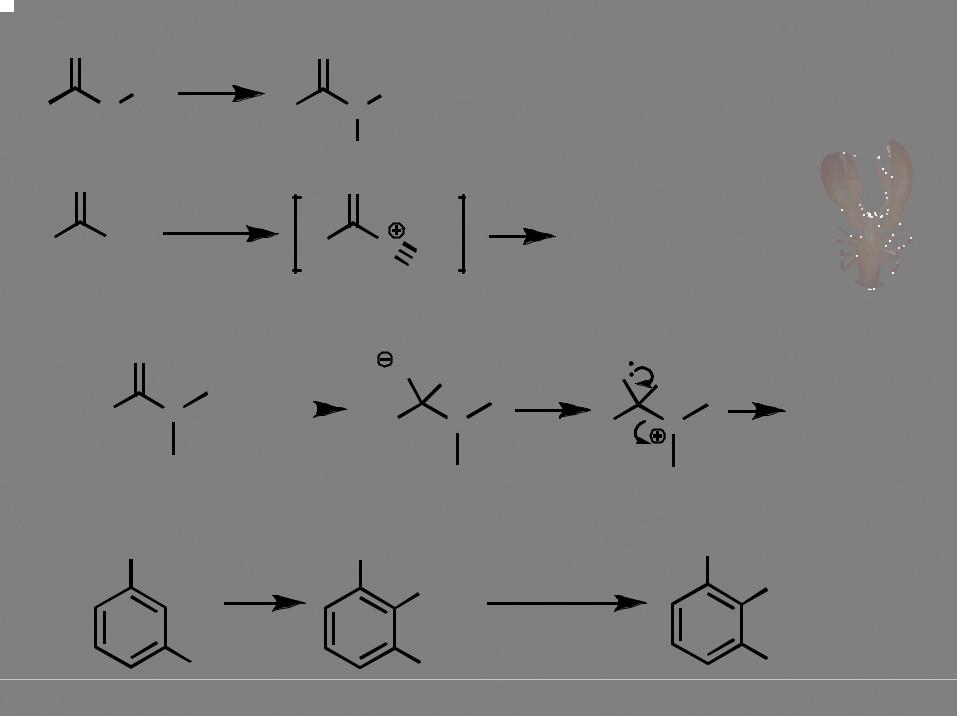
нитрозирование |
|
|
|
|
|
|
|||
|
O |
|
O |
|
|
|
|
|
|
|
R' |
NaNO2 |
R' |
N-нитрозоамиды - канцерогены |
|||||
R |
+ |
R |
|||||||
N |
N |
|
|
|
|
||||
|
H |
H3O |
|
NO |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
O |
NaNO2 |
|
O |
|
|
|
|
|
|
|
|
|
|
H2O |
|
|
||
R |
NH2 |
H3O+ |
R |
N |
|
RCO2H |
|
||
|
+ |
|
|
||||||
|
|
|
|
N |
|
-N2, -H |
|
|
|
|
|
|
очень хорошая уходящая группа - |
|
|||||
|
|
|
легко протекающий гидролиз |
|
|
||||
|
O |
|
|
O |
R |
H3O+ |
O |
R |
|
|
|
|
RMgX |
||||||
|
H |
N |
|
|
|||||
|
|
H |
N |
|
H |
H |
|||
|
|
|
|
|
N |
||||
нет хорошей уходящей группы
Например:
OCH |
OCH |
OCH3 |
3 |
3 |
1. HCON(CH3)2 |
BuLi |
Li |
|
|
|
2. H O+ |
|
|
3 |
20
RCHO
CHO
OCH |
OCH |
OCH3 |
3 |
3 |
|
