
8bb268da_lektsii__po_onkologiii
.pdf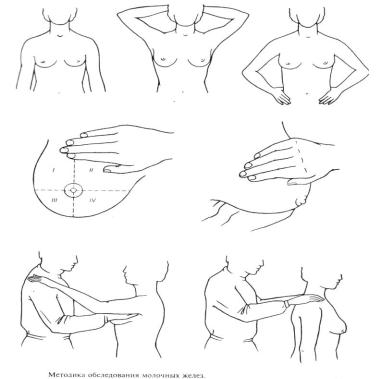
направлению к наружному ее краю по радиусу кверху, затем кнаружи, вниз. При ощупывании внутренней половины правой молочной железы правую руку кладут под голову, а обследование выполняют левой рукой в такой же последовательности — от центра к внутреннему краю молочной железы по радиусу кверху, затем кнутри, вниз. Все эти приемы повторяют при обследовании левой молочной железы.
Рис.3. Методика осмотра молочных желез.
Специальные методы исследования
Маммография — рентгенологическое исследование молочных желез без применения
контрастного вещества. На специальном аппарате выполняют рентгенограммы молочных желез в двух проекциях. При необходимости делают прицельные рентгенограммы с увеличением. Метод позволяет установить изменения структуры ткани молочной железы, выявить опухоль диаметром менее 10 мм, т. е. опухоль такою размера, которую врач, как правило, не может определить при пальпации (непальпируемые опухоли), особенно если она расположена в глубоких отделах молочной железы большого размера. Маммография остается наиболее чувствительным методом обнаружения рака молочной железы, хотя специфичность метода недостаточно велика. Некоторые изменения на маммограммах и пальпаторные данные не всегда являются точными: маммограмма дает одинаковое изображение злокачественного и доброкачественного узла и даже вариации нормальной архитектуры железы. Поэтому исследование целесообразно сочетать с ультразвуковым, позволяющим отличить кистозный узел от солидного, и другими методами.
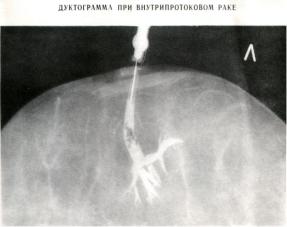
Дуктография молочной железы (рис.4) — рентгенографическое исследование протоков молочной железы после введения в них контрастного вещества с последующим проведением маммографии. Дуктография помогает проводить дифференциальную диагностику между доброкачественными новообразованиями и раком молочной железы. Показанием являются выделения из сосков. Область ареолы и соска обрабатывают спиртом. По капле секрета отыскивают наружное отверстие сецернирующего млечного протока. В него на глубину 5 — 8 мм. вводят тонкую иглу с тупым концом. Через иглу под небольшим давлением в проток вводят 0,3—1 мл. 60% раствора верографина или урографина до появления чувства небольшого распирания или легкой болезненности. Анализ снимков позволяет сулить о форме, очертаниях, дефектах наполнения протоков.
71
Ультразвуковое (эхографическое) исследование в настоящее время является одним из основных методов инструментального исследования молочных желез. УЗИ дает возможность определить изменения структуры молочной железы, выявить узелки опухоли, провести дифференциальный диагноз между раком и доброкачественными опухолями молочной железы, выявить образования небольших размеров (кисты выявляются от 0,2 см. в диаметре). Непосредственно перед операцией УЗИ позволяет точно указать локализацию
Рис.4 Дуктография, внутрипротоковый рак.
опухоли и более приемлемый доступ к ней. В связи с отсутствием лучевой нагрузки УЗИ можно использовать многократно в любой возрастной группе.
Магнитно-резонансная томография (МР-томография) позволяет не только визуализировать патологический очаг в молочной железе, но и дать характеристику его (киста, опухоль, содержащая мало жидкости), а также изменениям в окружающей ткани. Этот дорогостоящий метод следует применять по специальным показаниям.
Морфологической исследование является основным методом дифференциальной диагностики. Для этой цели используют тонкоигольную биопсию опухоли под контролем УЗИ. Полученный материал, так же как выделения из соска, подлежит цитологическому исследованию. Отрицательный ответ не исключает наличия злокачественной опухоли. Только обнаружение опухолевых клеток дает уверенность в диагнозе и позволяет наметить план лечения больной до операции. Окончательный ответ в сомнительных случаях может быть получен только после гистологического исследования удаленного сектора, содержащего опухоль. Биопсию следует производить только в тех лечебных учреждениях, где возможно затем выполнить срочную радикальную операцию.
Скрининг на рак молочной железы — массовое периодическое обследование здорового населения с целью выявления скрыто протекающего онкологического заболевания. Как показывает опыт, методика массовых профилактических осмотров врачами общей лечебной сети себя не оправдала из-за низкой эффективности. Поэтому широкое распространение получила концепция вторичной профилактики рака молочной железы, в частности скрининга. Подобные мероприятия приняты во многих странах в виде национальных программ — программ предупреждения рака молочной железы. По данным В. Ф. Семиглазова и соавт. (2001), скрининг предусматривает применение методики выявления скрытой патологии у большой группы практически здоровых лиц и поэтому должен отвечать следующим требованиям: высокая чувствительность метода или теста (благодаря чему обнаруживается большинство злокачественных опухолей в обследуемой группе при минимальном числе ложноотрицательных заключений); высокая специфичность метода позволяет исключить большинство здоровых женщин, у которых нет рака молочной железы, и свести к минимуму число ложноотрицательных заключений); приемлемая средняя стоимость одного выявленного случая рака; минимальный вред для здоровья обследуемой; простота эксплуатации и содержания оборудования.
Эффект массового скрининга может быть оценен тремя основными путями: оценкой воздействия на здоровье населения, определением показателей выявляемости рака молочной железы и характеристикой скринингового теста. Скрининг предусматривает применение таких инструментально-диагностических средств, которые обнаруживали бы проявление значительно более ранних форм опухолей, излечимых существующими методами (хирургическими, химиогормональными или лучевыми). Современный скрининг включает
72
высокочувствительную маммографию, квалифицированное ежегодное физикальное обследование молочных желез и методически правильное ежемесячное самообследование. Наиболее рациональна организация системы маммологической помощи с целью ранней диагностики рака молочной железы и оказания консультативной помощи при неопухолевых заболеваниях. Маммологическая служба состоит из следующих функционально взаимосвязанных звеньев: автоматизированный анамнестический скрининг на этапе доврачебного приема — смотровые (женские) кабинеты поликлиник маммологические кабинеты общей лечебной сети — онкологи поликлиник — онкологические поликлиники и диспансеры.
Дифференциальный диагноз
При дифференциальной диагностике рака молочной железы от других заболеваний определяющее значение играет цитологическое исследование пунктата из уплотнения и выделений из соска. Рак молочной железы необходимо дифференцировать от доброкачественных новообразований молочной железы (различных узловых форм мастопатии, фиброаденом, липом, лимфогранулем, галактоцеле, ангиоматозных опухолей, сарком). Необходимо проводить комплексное обследование и на основе данных клиники, маммографии, ультразвуковой диагностики, цитологии дифференцировать эти заболевания. Необходимо дифференцировать маститоподобные формы рака, отечно-инфильтративную форму раки молочной железы и острый мастит. Мастит имеет острое и короткое начало, сопровождается болями и поддастся противовоспалительному лечению; чаще встречается у молодых женщин и бывает связан с лактацией.
Хирургическое лечение
Хирургическое вмешательство до настоящего времени занимает доминирующее положение в лечении РМЖ.
. В зависимости от объема удаляемых тканей различают следующие варианты операций.
1.Стандартная радикальная мастэктомия /Halsted W., 1889; Meyer W., 1894/ заключается в одноблочном удалении молочной железы вместе с большой и малой грудной мышцами и их фасциями, подключичной подмышечной и подлопаточной клетчаткой с лимфатическими узлами в пределах анатомических футляров. Следует подчеркнуть особенность абластического выполнения операции, которая заключается в аккуратности и последовательности выполнения ее этапов, в частности, выделение подключичноподмышечной клетчатки, начиная с грудинно-ключичного сочленения и дальнейшего перехода в подмышечно-подлопаточную область. Показанием к выполнению мастэктомии по Холстеду в недавнее время был рак молочной железы всех стадий, но в последние годы к ней прибегают только при диффузных отечно-инфильтративных формах рака IIIб стадии и при опухолевой инфильтрации большой грудной мышцы,
2.Модифицированная радикальная мастэктомия отличается от мастэктомии Холстеда сохранением большой грудной мышцы /Patey D.,, Dyson W., 1948/ или обеих грудных мышц /Auchincloss H., 1956; Madden J.,1965/. Обоснованием для оставления грудных мышц явилась редкость наблюдений прорастания их опухолью. При оставлении мышц мастэктомия выполняется менее травматично и с меньшей кровопотерей, послеоперационная рана лучше заживает. Сохранение мышц приводит к лучшему косметическому результату и функции верхней конечности. Поэтому такие операции получили название функциональнощадящих. Показанием для них являются не только начальные, но и местно-распространенные стадии заболевания при условии отсутствия инфильтрации опухолью грудных мышц, особенно у лиц пожилого возраста, при тяжелых сопутствующих заболеваниях при двухстороннем синхронном раке молочных желез, когда необходимо выполнить одномоментную двухстороннюю радикальную мастэктомию, стремясь к меньшей травматизации больной.
73
В настоящее время модифицированная радикальная мастэктомия – основной вид оперативного вмешательства. Включает удаление молочной железы Подкожная клетчатка отсепаровывается до грудины, ключицы, реберной дуги, щирочайшей мышцы спины. Удаляются лимфатические узлы между большой и малой грудной мышцей (Роттера). Проводится подмышечная, подключичная, подлопаточная лимфаденэктомия. Активное дренирование раны. Ушивание раны стандартное .
3.Расширенная подмышечно-грудинная радикальная мастэктомия, сверхрадикальная расширенная мастэктомия /Margottini M. А., Bucalossi P., 1949; Urban J., 1951; Veroseni U., 1952, Wangensteen O., 1952 Холдин С.А., Дымарский Л.Ю., 1975/ предусматривает одноблочное удаление молочной железы с грудными мышцами, подключично-подмышечной и подлопаточной клетчаткой, а также с участком грудной стенки с парастернальными лимфатическими узлами и внутренними грудными сосудами. В настоящее время операция имеет лишь историческое значение . В некоторых клиниках внедряются методики парастернальной лимфаденэктомии торакоскопическим способом.
4.Простая мастэктомия — удаление молочной железы с фасцией большой грудной мышцы с онкологических позиций не может бытъ отнесена к радикальному онкологическому вмешательству. Показанием к такой операции является распадающаяся опухоль, преклонный возраст больных, тяжелые сопутствующие заболевания.
5.Радикальная секторальная резекция молочной железы является органосохраняющей операцией и предусматривает удаление сектора молочной железы вместе с опухолью, части подлежащей фасции большой грудной мышцы, иссечение малой грудной мышцы или только ее фасции, а также подключичной, подмышечной, подлопаточной клетчатки с лимфатическими узлами в одном блоке. В 1927 г. работами J/Hirsh положено начало консервативному хирургическому лечению РМЖ ( секторальная резекция , туморэктомия, квадрантэктомия в сочетании с аксилярной диссекцией). При локализации опухоли в медиальных отделах молочной железы операция может быть выполнена из двух разрезов кожи — на молочной железе и в подмышечной области. Для выполнения подобных операций важно соблюдать критерии отбора больных. Основными критериями являются: начальная I и IIа стадии заболевания (Т1-2N0М0), размер опухоли не более 3-3,5 см в диаметре, медленный темп и моноцентричный характер роста узла опухоли, отсутствие лимфо-гематогенных метастазов и желание больной сохранить молочную железу. Лечение может быть дополнено проведением послеоперационной лучевой на оставшуюся часть молочной железы.
6.Секторальная резекция молочной железы как самостоятельный метод лечения при раке не имеет обоснования к выполнению. Она возможна при одиночных очагах неинвазивного рака in situ. При множественных очагах показана подкожная мастэктомия. Иногда в удаленном секторе устанавливают рак in situ, а в дальнейшем появляются мультицентричные очаги рака или метастазы в регионарных лимфатических узлах. Поэтому секторальную резекцию при раке, не считая как диагностическую, следует применять в исключительно редких случаях и дополнять лучевой терапией.
7.Кожсберегающая мастэктомия.
Понимание принципов прогрессии опухоли онкологами позволило широко применять не только органосберегающие операции, но и в случае имеющихся противопоказаний к ним, модифицировать классическую мастэктомию. Значимым событием в области реконструкции молочной железы, явилась разработка в начале 90-х годов кожсберегающей мастэктомии. При этом удаляется железистая ткань, и сохраняется большая часть кожи молочной железы.
В 1991 г. B.Тorth et P.Lappert опубликовали принципы мастэктомии и планирования реконструкции молочной железы с использованием данной техники.
74
Это побудило их широко использовать технику КСМ при выполнении одномоментных реконструктивнопластических операций. С накоплением клинического опыта многие исследователи приходят к выводу, что сохранение кожи молочной железы не увеличивает риск возникновения местных рецидивов.
Пластика молочной железы.
Пластика молочной железы не ухудшает онкологический результат лечения. После проведения реконструктивной операции возможно проведение адьювантной химиотерапии и лучевой терапии .Потребность в пластике молочной железы испытывают 7% женщин пожилого и 38% молодого возраста. Современные подходы к реабилитации больных состоят в том, чтобы устранить соматические проявления постмастэктомического синдрома, помочь женщине справиться с психосоциальными последствиями радикального лечения
.Реконструкция молочной железы может выполняться как отсрочено после окончания радикального лечения РМЖ, так и одномоментно после окончания мастэктомии.
Виды лоскутов, применяемых при реконструкции молочной железы.
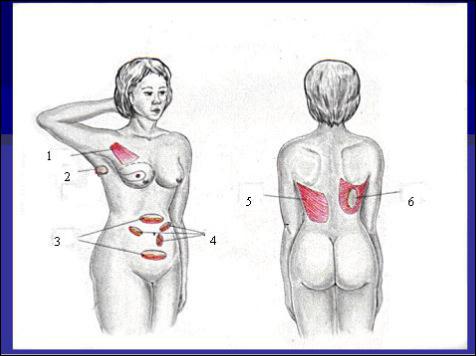
Существует три основных вида реконструкции молочной железы.1 Восстановление молочной железы при помощи силиконовых имплантов, и эспандеров. 2. Сочетание имплантов и эспандеров с мышечными лоскутами. 3 Лоскутные методики (пластика лоскутом передней брюшной стенки на основе прямой мышцы живота, торакодорзальный лоскут, расширенный торакодорзальный лоскут, боковые лоскуты с грудной стенки, лоскут Рубенса-кожножировой лоскут подвздошной области с частью крыла подвздошной кости с питанием из глубоких нижних подвздошных сосудов, верхний и нижний ягодичные
лоскуты)(рис.5).
Рис.5. Виды лоскутов. 1.Пекторальный
мышечный лоскут. 2.Кожный
подмышечный лоскут 3. верхний и нижний Трам лоскут на прямой мышце живота 4. Эпигастральные кожные лоскуты.
5. Торакодорзальный лоскут 6. Расширенный
торакодорзальный лоскут.
Лучевая терапия рака молочной железы
Лучевую терапию применяют в предоперационном и послеоперационном периоде. В задачи предоперационной лучевой терапии входит снижение степени злокачественности опухоли за счет девитализации наиболее анаплазированных клеток, инактивации радиорезистентных опухолевых клеток, повреждение до полной регрессии микродиссеминантов и микрометастазов в зонах возможного субклинического распространения. Для достижения этих задач достаточными являются дозы 40-45 Грей, проведенных за 4-5 недель. Возможно
75
проведение лучевой терапии средними и крупными фракциями за 3-4 сеанса. Предоперационная терапия применяется только у больных с 3а-3б стадией при неэффективности предоперационной химиотерапии . Надключичную и парастернальную зоны облучают через 10-14 дней после операции в классическом режиме — по 2 Грея ежедневно на каждую зону до суммарной дозы 44 Грея. При отечно-инфильтративных формах рака применяют классический режим фракционирования дозы на молочную железу и все зоны регионарного лимфоотока в предоперационном плане.
Химиотерапия рака молочной железы
Химиотерапия в отличие от лучевой терапии обладает не только местным, но и общим противоопухолевым цитостатическим действием на раковые клетки, распространяющиеся гематогенно по всему организму больной. Каждый химиопрепарат действует только на те клетки, которые находятся в определенной фазе клеточного цикла. Поэтому монохимиотерапия менее эффективна, чем полихимиотерапии в виде сочетания нескольких препаратов с различной фазовоспецифичностью и механизмом действия. Химиотерапия может быть предоперационной (неоадьювантной при 2б-3б стадиях), профилактической (адьювантной) и лечебной – при метастатическом раке молочной железы. Клинический опыт показал, что при раке молочной железы, наиболее эффективными дополнительными /адьювантными/ к операции являются химиопрепараты — циклофосфан, фторурацил, метотрексат, адриамицин /доксорубицин/,таксол, таксотер, гемзар, карбоплатина, кселода и некоторые другие, противоопухолевое действие которых потенцеируется при различном их сочетании. Различные схемы химиотерапии применяют при распространенном раковом процессе. Химиотерапию проводят под тщательном контролем гемопоэза.
Гормонотерапия рака молочной железы
Более чем 100 лет назад Джордж Бетсон впервые сообщил о ремиссии, достигнутой у 3 больных распространенным раком молочной железы после выполнения овариоэктомии (1). С тех пор для лечения больных распространенным раком молочной железы были предложены различные гормональные методики лечения. Тамоксифен был предложен для лечения больных раком молочной железы в 1971 г. и до настоящего времени остается наиболее популярным препаратом как для проведения адъювантной терапии, так и при лечении больных с диссеминированным РМЖ.
Сегодня для лечения метастатического РМЖ используется поочередное применение различных гормональных препаратов.
Выключение функции яичников хирургическим или лучевым методом в пременопаузесейчас применяется реже в связи с широким внедрением в практику препаратовингибиторов лютеинизирующегорилизинг факторов гозерелина( золадекса), бузерелина и лейкопролида. Данные препараты применяются ежемесячно в течении 2-х лет.
Ингибиторы ароматазы (анастрозол, летрозол, экземестан) применяются для блокады фермента ароматазы, препятствуя тем самым синтезу эстрогенов из андрогенов в мышечной и жировой ткани у женщин в менопаузе. Прерывая синтез эстрогенов, как факторов роста РМЖ, ингибиторы ароматазы, тем самым, реализуют цитостатический эффект
Таргентная терапия
76
Сегодня можно с уверенностью сказать, что терапия злокачественных новообразований переживает свое второе рождение. Стремительное развитие фундаментальной науки, более глубокое понимание механизмов внутриклеточной передачи сигнала и регуляция клеточного цикла привело к созданию и внедрению в клиническую практику препаратов целенаправленного действия - «таргентных» препаратов. На сегодня идентифицировано много новых факторов прогноза течения РМЖ. Одним из них является уровень экспрессии в ткани злокачественной опухоли рецептора НЕR2\neu. Установлено, что у женщин, страдающих раком молочной железы, происходит активация гена НЕR2\neu, в результате чего на поверхности опухолевых клеток располагается большое число человеческих эпидермальных факторов роста 2 типа (сокращенно рецепторов НЕR2).Рецепторы НЕR2 на мембране нарушают нормальный клеточный цикл и вынуждают клетки бесконтрольно делиться. Исследованиями установлено, что примерно у 30% больных раком молочной железы имеется гиперэкспрессия НЕR2 на поверхности опухолевых клеток. Показано также, что больные с гиперэкспрессией НЕR2имеют менее благоприятный прогноз. Рецепторы НЕR2представляют собой новую мишень для терапевтического воздействия. Гуманизированное моноклональное антитело к НЕR2 трастузумаб (герцептин) первый лекарственный препарат, действие которого направлено непосредственно на рецепторы НЕR2. После того как герцептин заблокировал НЕR2рецепторы на поверхности раковой клетки, её дальнейший рост прекращается и в ряде случаев наблюдается уменьшение опухоли.
Предпосылкой для успешного лечения Герцептином является точное и надежное выявление гиперэкспрессия НЕR2. С этой целью в нашей стране чаще используют иммуногистохимический метод.
Комбинированное и комплексное лечение
При начальных формах рака молочной железы неинвазивной карциноме in situ, I /Т1N0М0/ и IIa /Т2N0М0/ стадии может быть применено одно хирургическое лечение — секторальная резекция или подкожная мастэктомия при карциноме in situ и модифицированная мастэктомия у больных с I и IIа cтадией. Если же выполняется радикальная резекция при I и IIa cтадии рака, то она должна быть дополнена послеоперационной лучевой терапией на оставшуюся часть молочной железы при выявлении в удаленном секторе неблагоприятных факторов, повышающих риск рецидива, таких как дольковый или внутрипротоковый рак в первичной опухоли, очаги рака in situ в окружающих тканях и дисплазия эпителия III степени.
Больным с IIб /Т1,2N1М0/ и III /T3N0М0/ стадией рака проводят комплексное лечение: 4 курса предоперационной химиотерапии затем выполняют мастэктомию или радикальную резекцию молочной железы. Хирургический этап одномоментно можно дополнить реконструкцией молочной железы, или коррекцией её формы.
Больным с IIIа стадией рака /Т3N1М0; Т1,2,3N2М0/ показано комплексное лечение с применением лучевой и химиогормональной терапии и модифицированной радикальной мастэктомии.
Больным с отечно-инфильтративной формой рака IIIб стадии /Т4в 1,2М0/ комплексное лечение целесообразно начинать с общего воздействия гормонотерапии в виде двусторонней овариэктомии и приема тамоксифена. При этом имеется возможность исключить распространенность процесса в брюшную полость и оценить влияние гормонотерапии в виде удаления яичников на степень регрессии первичной опухоли. В следующем этапе проводят химиотерапию по схеме ЦАФ в виде двух курсов, лучевую терапию на молочную железу и
77
все зоны регионарного лимфоотока, затем мастэктомию и курсы профилактической ( адьювантной ) полихимиотерапии.
Результаты лечения
Результаты лечения принято оценивать по пятилетней выживаемости больных. Выживаемость больных во многом зависит от стадии заболевания, при которой начато лечение. Современные методы лечения позволяют получить 5-летнюю выживаемость при I стадии рака 90-96%, IIa — 90%, IIб — у 80%, IIIа — у 87%, IIIб — у 67% больных. При возникновении отдаленных метастазов проводится лечебная химиотерапия с применением циклофосфана, 5-фторурацила, метотрексата, адриамицина /доксорубицин/,таксола, таксотера, гемзара, карбоплатины, кселоды.
Профилактика Профилактика рака молочной железы подразделяется на первичную и вторичную. Нормализация семейной жизни, осуществление своевременной детородной функции, грудное вскармливание младенца, исключение браков при обоюдной онкологической отягощенности, следует относить к первичной профилактике. Вторичная профилактика заключается в выявлении и лечении предопухолевых заболеваний молочных желез — различных форм мастопатии, фиброаденом, других нераковых заболеваний, а также нарушений эндокринной системы, заболеваний женских половых органов, нарушений функции печени, Если первичная профилактика рака молочной железы в большой степени относится к трудно корректируемой социальной сфере, то вторичная профилактика является важнейшей задачей лечебной медицинской практики.
Лекция 7
РАК ЛЕГКИХ А.А. Менг
Вбольшинстве стран Европы рак легких находится на 1 месте среди злокачественных новообразований. В настоящее время в России рак легких также является самой распространенной опухолью. 200 лет назад это заболевание встречалось крайне редко. В мировой литературе упоминалось лишь несколько случаев. С развитием промышленности заболевание стало встречаться чаще. Врачи в Германии рак легких в основном наблюдали у рабочих шахт, в связи с чем долго называли заболевание «болезнь рудокопов». В конце позапрошлого, начале прошлого века появились серьезные научные работы, описывающие характер поражения легких, гистологические признаки болезни, эпидемиологию, особенности канцерогенеза, а также разрабатывались подходы к лечению. Во второй половине 20 века заболеваемость резко возросла. Наряду с этим выработаны варианты и обобщен опыт комбинированного и комплексного лечения.
Вмире ежегодно выявляется около 1 млн. случаев рака легких. В России каждый год заболевают 55 тыс. человек. Заболеваемость в нашей стране постоянно увеличивалась. Начиная с 80 -х годов прошлого века в структуре онкозаболеваемости занимает 1 место и составляет 13%. В структуре смертности онкопатология легких давно и прочно лидирует и составляет 20%. Мужчины составляют 85% от числа всех заболевших. В популяции самая высокая заболеваемость наблюдается среди мужчин старше 70 лет и составляет примерно
500 на 100000 человек.
Вгеографических зонах с холодным климатом отмечается большая заболеваемость. В нашей стране основная часть заболевших проживают в Северо-Западном, Уральском,
78
Восточно-Сибирском и Дальневосточном административных округах. В Иркутской области в 2004 году заболело 949 человек. Заболеваемость у нас составляет 38 на 100000 чел.
Факторы риска
Выделяют генетические и модифицирующие факторы риска развития рака легких. Из генетических значимы первичная множественность опухолей и наличие трех и более случаев рака легкого у ближайших родственников. Из модифицирующих экзогенные – химические и физические канцерогены и эндогенные – возраст более 45 лет и хронические легочные заболевания воспалительной природы. Основную роль в появлении рака легких играют химические канцерогены, особенно полициклические ароматические углеводороды. Соли некоторых металлов также способствуют развитию опухолей, особенно хром, никель, кобальт. Мощным канцерогенным фактором является асбестоз легких, развивающийся в результате систематического вдыхания асбестовой пыли. Табакокурение является разновидностью химического канцерогенеза и по распространению среди мужчин и женщин намного превосходит промышленные факторы. Эта привычка вредит как самим курящим, так и их ближайшему окружению. Давно доказана пагубность никотина табачного дыма при пассивном курении. Для жителей крупных городов все большее значение приобретают выбросы автотранспорта. Подсчитано, что в России суммарный вес микрочастиц в выхлопных газах составляет около 15 млн. тонн.
Ионизирующее излучение обладает мощным канцерогенным потенциалом. Зависимость степени относительного риска от дозы облучения доказана в исследованиях, проведенных среди пациентов, переживших атомные бомбардировки. Причем, у них чаще имеет место мелкоклеточный рак легкого. Радиоиндуцированная иммуносупрессия является также серьезным канцерогенным фактором.
Злокачественные новообразования легких чаще диагностируют у больных, имеющих в анамнезе неопухолевые заболевания легких, такие как силикоз, хронический бронхит, частые пневмонии, туберкулез, эмфизема легких, бронхиальная астма. Исследованиями доказано, что до 50% лиц с туберкулезом в анамнезе заболевают раком легкого, причем чаще железистой его формой.
Имеющаяся информация о причинах развития опухолей легких, позволяет выделить группы риска. Это длительно курящие мужчины, старше 45 лет, работающие на пылевом производстве, либо находящиеся в частом контакте с горюче-смазочными материалами и часто болеющие простудными заболеваниями дыхательной системы. Именно эта группа нуждается в регулярных осмотрах и рентгенологическом контроле. Появление легочной симптоматики должно заставить врача провести комплекс исследований, направленных, в первую очередь, на поиск опухолей в легких.
Классификация рака легких
В отечественной литературе принята клинико-анатомическая классификация, предложенная А.И.Савицким (1957):
1.Центральный рак легкого (ЦРЛ):
эндобронхиальный
перибронхиальный узловой
перибронхиальный разветвленный
2.Периферический рак легкого (ПРЛ):
круглая опухоль или «шаровидный» рак
пневмониеподобный рак
рак верхушки легкого (Пенкоста)
3.Атипичные формы:
79
медиастинальная
костная
мозговая
печеночная
милиарный карциноз и т.д.
Гистологически выделяют немелкоклеточный рак и мелкоклеточный рак легкого. Далее представлены наиболее частые варианты:
1.Плоскоклеточный рак (40-45%)
2.Мелкоклеточный рак (20-25%)
3.Аденокарцинома (30-35%)
4.Крупноклеточный рак (5-7%)
5.Железисто-плоскоклеточный рак (1,5%)
6.Карциноидная опухоль (1-2%)
7.Рак бронхиальных желез (0,5%)
8.Другие (карциносаркома, меланома, лимфома)
Отечественная классификация рака легких по стадиям (1956г.)
I стадия – опухоль до 3 см в наибольшем измерении, расположенная в одном сегменте (ПРЛ) или в пределах сегментарного бронха (ЦРЛ) без признаков метастазирования.
II стадия – опухоль до 6 см, расположенная в пределах одной доли (ПРЛ) или долевого бронха (ЦРЛ). В пульмональных и бронхопульмональных лимфатических узлах единичные метастазы.
III стадия – опухоль больше 6 см, переходит на соседнюю долю (доли) (ПРЛ) или с переходом с одного долевого бронха на другой или главный бронх (ЦРЛ). Метастазы в бифуркационных, трахеобронхиальных, паратрахеальных лимфатических узлах.
IV стадия – как при центральной, так и при периферической формах опухоль вышла за пределы легкого, распространяется на соседние органы (грудную стенку, диафрагму, средостение, перикард) с обширными регионарными и отдаленными метастазами. Раковый плеврит.
Международная классификация по системе ТNM (1998)(табл.1)
Т- первичная опухоль Тх – недостаточно данных для оценки первичной опухоли или опухоль доказана только
наличием опухолевых клеток в мокроте или промывных водах бронхов, но не выявляется методами визуализации или при бронхоскопии.
Т0 – первичная опухоль не определяется Тis – преинвазивная карцинома
Т1 – опухоль не более 3 см. в наибольшем измерении, окруженная легочной тканью или висцеральной плеврой, без видимой инвазии проксимальнее долевого бронха при бронхоскопии (без поражения главного бронха).
Т2 – опухоль более 3 см. в диаметре в наибольшем измерении или опухоль любого размера, прорастающая висцеральную плевру, или сопровождающаяся ателектазом, или обструктивной пневмонией, распространяющаяся на корень легкого, но не захватывающая все легкое. По данным бронхоскопии проксимальный край опухоли располагается не менее 2 см. от карины.
Т3 – опухоль любого размера, непосредственно переходящая на: грудную стенку (включая опухоль верхней борозды), диафрагму, медиастинальную плевру, перикард или опухоль, не доходящая до карины менее чем на 2 см., но без вовлечения карины, или опухоль с сопутствующим ателектазом или обструктивной пневмонией всего легкого.
Т4 – опухоль любого размера непосредственно переходящая на средостение, сердце, крупные сосуды, трахею, пищевод, тела позвонков, карину.
80
