
8bb268da_lektsii__po_onkologiii
.pdfпревышает 80% -При II стадии (степень распространения опухоли соответствует ТЗ-4 N0M0) пятилетняя выживаемость при хирургическом лечении составляет 40-50%, при комбинированном — 60-70%. Пятилетняя выживаемость больных раком прямой кишки III стадии (соответствует степени распространения опухоли Т1-4N1-3М0) составляет при хирургическом лечении 30-40%, при комбинированном — 40-50%. . Больным раком прямой кишки после радикальных операций с наложением колостомы (экстирпация прямой кишки и резекция по Хартманну) противопоказаны напряжённый физический и умственный труд в организованных коллективах, так как ограничения участия в трудовой деятельности носят значительный характер. У данной категории больных имеет место резкое нарушение самообслуживания, значительное ограничение передвижения и общения. После проведения больным раком прямой кишки радикальных сфинктеросохряняющих операций (чрезбрюшная и брюшно-анальная резекции прямой кишки) и при отсутствии у них отдалённых осложнений ограничения участия в трудовой деятельности носят умеренный характер. Физический груд и умственная работа не противопоказаны. Ограничения самообслуживания умеренные, ограничения передвижения незначительные.
Таким образом, больным раком прямой кишки после ее экстирпации независимо от стадии заболевания должна устанавливаться II группа инвалидности без срока переосвидетельствования по анатомическому дефекту. После резекции прямой кишки по Хартманну больные также должны признаваться инвалидами II группы, однако в дальнейшем необходимо переосвидетельствование, так как у части из них возможны повторные операции по восстановлению непрерывности толстой кишки.
Больные раком прямой кишки I-III стадий после чрезбрюшной резекции при отсутствии у них отдалённых послеоперационных осложнений могут вернуться к умственному и умеренному физическому труду через 4-6 мес. без установления группы инвалидности, либо им устанавливается III группа инвалидности с последующим переосвидетельствованием. При наличии отдалённых осложнений у данной группы больных необходимо устанавливать II группу инвалидности с обязательным направлением для реабилитации и последующим переосвидетельствованием.
После проведения больным раком прямой кишки I-III стадий брюшно-анальной резекции прямой кишки должна устанавливаться III группа инвалидности, а при наличии отдалённых осложнений — II группа инвалидности с направлением для реабилитации и последующим переосвидетельствованием.
Всем больным раком прямой кишки после радикальных расширенных и комбинированных операций, а также независимо от степени распространения опухоли и вида операции работникам тяжёлого физического труда необходимо устанавливать II группу инвалидности.
После паллиативного лечения, как правило, должна устанавливаться I группа инвалидности без срока переосвидетельствования.
Медицинская реабилитация больных
Медицинская реабилитация как неотъемлемая часть саногенеза является процессом, направленным на компенсацию или устранение с помощью медицинских средств последствий суммарного влияния болезни и врачебных воздействий, в результате которого больной достигает ранее (до болезни) приобретенного социального статуса.
Больные после экстирпации прямой кишки с постоянной концевой одноствольной колостомой нуждаются в обучении ирригации ободочной кишки, применению калоприёмников и пневмообтураторов, советах по правильному питанию и психокоррекционной помощи, направленной на создание уверенности в их излеченности и ценности для семьи и общества. При выпадении престомального участка ободочной кишки и рубцовых стриктурах колостомы проводятся повторные хирургические вмешательства. После сфинктеросохраняющих операций (чрезбрюшная и брюшно-анальная резекции прямой кишки) реабилитационные мероприятия сводятся в основном к улучшению функции низведенной кишки, лечению недостаточности анального сфинктера и рубцовых стриктур анастомоза.
111
Больные после резекции прямой кишки по Хартманну должны направляться в специализированные стационары для выполнения восстановительных операций. Высокоэффективная медицинская реабилитация больных раком прямой кишки возможна только в условиях специализированных (проктологических) отделений или реабилитационных центров.
Профессиональная реабилитация
Профессиональная реабилитация проводится с целью обучения лиц, утративших трудоспособность, новым профессиям, доступным им по состоянию здоровья. Началом профессиональной реабилитации является определение индивидуальных для каждого больного возможностей общественно полезной деятельности. При трудоустройстве необходимо учитывать такие факторы, как степень утраты трудоспособности, форму и степень ограничения жизнедеятельности и социальной недостаточности, вид проведенной операции, профессия, уровень образования, особенности личности больного.
Как правило, прекращают трудовую деятельность или переходят на работу при облегчённых условиях лица, профессия которых была связана со значительным или умеренным физическим напряжением (грузчики, каменщики, бетонщики, слесари и др.).
Большинство больных, занятых до лечения на работах с незначительным физическим напряжением (лаборанты, сторожа и т.п.) или работах умственного характера (экономисты, бухгалтеры, учителя и т.п.), возвращаются к прежней профессии. Таким больным необходимы соответствующие производственные и санитарно-гигиенические условия: дополнительные перерывы, возможность на непродолжительное время отлучаться с рабочего места, достаточная обеспеченность туалетами и т.д. Они нуждаются в освобождении от командировок.
Принципиальное значение в возможности трудоустройства лиц после операций на прямой кишке по поводу рака имеет наличие или отсутствие колостомы.
Независимо от сроков давности после лечения противопоказаны виды труда, связанные с общей вибрацией, инфракрасным и лазерным излучением, токсическими и радиоактивными веществами, высокой общей физической нагрузки и высоким уровнем нервной напряжённости.
Профессиональная реабилитация предусматривает возможность возвращения больного на прежнее рабочее место, приспособление к новой работе или переквалификации. Обучение инвалидов осуществляется индивидуально, непосредственно на рабочем месте и в системе производственно-технического обучения.
112
Лекция 12
РАК ПЕЧЕНИ
С.В.Соколова, К.А.Корнеев
Рак печени входит в десятку наиболее распространенных злокачественных опухолей человека. С клинической точки зрения различают первичный и вторичный (метастатический) рак печени, причем частота метастатических опухолей в 30 раз превышает частоту первичных.
Первичный рак печени среди всех злокачественных опухолей человека занимает 7 место по частоте. Наиболее высокий уровень заболеваемости (более 30,0 на 100 тыс. населения) зарегистрирован на юге Африки: в Мозамбике, Мали, Южно-Африканской республике, где рак печени является самой частой злокачественной опухолью. Другой зоной высокой заболеваемости является Юго - Восточная Азия: Гонконг, Япония, Сингапур, Новая Зеландия в которой рак печени занимает 3 место по частоте после рака желудка и рака легкого.
В России первичный рак печени составляет 3 – 5 % в общей структуре злокачественных новообразований. Наибольшие показатели заболеваемости отмечаются в Республике Саха (Якутия) – 17,2 на 100 тыс. населения. Мужчины заболевают примерно в 2 раза чаще, чем женщины.
Этиология и факторы риска
Цирроз независимо от природы может рассматриваться как предраковое состояние. Узловая гиперплазия при этом прогрессирует в рак. Дисплазия гепатоцитов, которая проявляется увеличением их размеров, ядерным полиморфизмом и наличием многоядерных клеток, поражает группы клеток или целые узлы и может представлять собой промежуточную стадию развития опухоли. При циррозе с высокой пролиферативной активностью гепатоцитов отмечается более высокий риск развития рака печени. Кроме того, канцерогенез может быть связан с генетическим дефектом определенного клона клеток.
113
При вирусном поражении печени рак печени развивается на фоне хронического гепатита и цирроза. Некроз и усиленная митотическая активность гепатоцитов способствует развитию узлов регенерации, что при определенных условиях приводит к развитию рака. Канцерогенез в данном случае многостадийный, в нем играет роль как вирус, так и организм хозяина. При гепатите В вирус интегрируется в хромосомную ДНК хозяина, однако молекулярный механизм канцерогенного эффекта HBV остается неясным. Интеграция сопровождается хромосомными делениями и транслокациями, которые влияют на рост и дифференцировку клеток.
Риск развития рака печени в 4 раза выше среди больных алкоголизмом, особенно в пожилом возрасте. Алкоголь сам по себе не является печеночным канцерогеном, однако у больных алкоголизмом всегда обнаруживаются признаки цирроза печени. Алкоголь может быть коканцерогеном HBV. Стимулируемая алкоголем индукция ферментов может усиливать превращение коканцерогенов в канцерогены. Алкоголь так же может стимулировать канцерогенез вследствие угнетения иммунитета.
Описторхозная инвазия. Возбудителем описторхоза является двуустка кошачья или двуустка сибирская, относящаяся к классу трематод типа плоских червей. Характеризуется очаговостью распространения в речных бассейнах Днепра, Камы, Волги, Дона, Северной Двины, Печоры, Невы, Оби, Иртыша. Заражение происходит при употреблении в пищу сырой рыбы. Хроническая описторхозная инвазия приводит к механическому повреждению эпителия присосками гельминтов, усилению пролиферации эпителия протоков и появлению аденоматозных разрастаний. Нарушаются структура и функция клеточных мембран, обменные процессы в клетках, накапливаются продукты перекисного окисления липидов. Снижается активность факторов, регулирующих пролиферацию и дифференцировку клеток. Из-за скопления в протоках гельминтов, слизи и слущенного эпителия наблюдается желчестаз и длительный контакт вторичных желчных кислот с клетками-мишенями, что создает условия для реализации их канцерогенного эффекта.
Высокий уровень заболеваемости в странах Южной Африки и Юго-Восточной Азии связан с употреблением в пищу сельскохозяйственных культур, зараженных грибком Aspergellus flavus, продуцирующим афлотоксин В.
К другим факторам риска относят: гемохроматоз, воздействие канцерогенов (полихлорированные дифенилы, хлорированные углеводородные растворители, например, тетрахлористый углерод, нитрозамины, органические хлорсодержащие пестициды), курение (риск увеличивается при одновременном употреблении алкоголя), длительное применение анаболических стероидов.
Патологоанатомическая характеристика
Локализация. Опухоль чаще располагается в правой доле печени или поражает обе доли. В левой доле основной массив опухоли локализуется примерно у 10% больных.
Макроскопические формы. Узловая форма – наиболее часто встречающаяся, составляет 60 – 85% среди всех остальных форм рака. Почти всегда сопровождается циррозом. Увеличенная в размерах печень содержит в своей толще многочисленные опухолевые очаги различного размера – от микроскопических до нескольких сантиметров в диаметре.
Массивная форма – встречается почти в 25% всех случаев первичного рака печени. Подразделяется на массивную в виде одиночного узла, полостную и массивную с сателлитами. Массивная форма в виде одиночного узла представляет собой бугристую опухоль значительных размеров, занимающую целый сегмент, долю или даже половину печени. На разрезе массивный рак имеет вид серо-желтого плотного образования с довольно четкими границами. Нередко в окружности массивного узла располагаются множественные небольшие опухоли. Такая форма получила название массивной с сателлитами. Полостная форма массивного рака представляет собой большую опухоль с обширной полостью и толстыми стенками, наполненную распадающимися опухолевыми массами и жидкостью грязно-коричневого цвета.
114
Диффузная форма – при ней большая часть паренхимы печени замещена сливающимися друг с другом опухолевыми узлами различных размеров. Разновидностью диффузной формы является цирроз-рак печени.
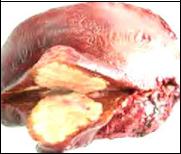
Гистологическое строение. Обычно опухоль белого цвета, иногда окрашена желчью и может содержать очаги кровоизлияния и некроза (рис. 1). Крупные внутрипеченочные ветви воротной и печеночной вен часто тромбированы и содержат опухолевые массы. Чаще всего (65 – 80%) первичный рак печени развивается из печеночных клеток
Рис.1 Гепатоцеллюлярная карцинома
(гепатоцеллюлярный рак). Микроскопически клетки напоминают нормальные гепатоциты и располагаются в виде компактных пальцевидных отростков или солидных трабекул. Сходство опухоли с нормальной печеночной тканью может быть выражено в разной степени. Клетки опухоли иногда секретируют желчь и содержат
гликоген. Межклеточная строма отсутствует. Клетки опухоли обычно меньшего размера, чем нормальные гепатоциты; имеют полигональную форму и зернистую цитоплазму. Иногда обнаруживаются атипичные гигантские клетки. В центре опухоли часто отмечаются очаги некроза. Ранним признаком является инфильтрация перипортальных лимфатических сосудов опухолевыми клетками.
Примерно у 15 – 25% больных опухоль возникает из эпителия внутрипеченочных желчных протоков (холангиоцеллюлярный рак). Изредка в строении опухоли имеются клетки, характерные для того и другого вида опухоли (смешанный рак). В отдельных случаях клетки мало дифференцированы, поэтому решить вопрос о генезе опухоли не удается (недифференцированный рак.)
Метастазирование. Первичный рак печени характеризуется высоким уровнем метастазирования. При аутопсии метастазы в лимфатические узлы встречаются у 50 – 60% умерших. Наиболее часто поражаются печеночные лимфатические узлы, расположенные в печеночно-двенадцатиперстной связке. Метастазы в легкие обнаруживаются на поздних стадиях примерно в 10% случаев. В настоящее время установлено, что одним из ранних проявлений первичного рака печени в 1.5 – 5.0% случаев являются гематогенные метастазы в ребра и позвоночник. Иногда метастазами поражаются надпочечники, поджелудочная железа, почки. Может быть внутриорганное метастазирование с поражением одной доли или всей печени Значительно чаще происходит внепеченочное распространение опухоли в близлежащие органы: диафрагму, желудок, двенадцатиперстную кишку.
Клиническая классификация TNM (2003) критерий Т:
Тх - недостаточно клинических данных для оценки первичной опухоли; T0 – первичная опухоль не определяется;
Т1 - солитарная опухоль до 2 см в наибольшем измерении без инвазии сосудов Т2 - солитарная опухоль до 2 см в наибольшем измерении с инвазией в сосуды или множественные опухоли до 5 см.в наибольшем измерении;
Т3 - множественные опухоли более 5см или опухоль, вовлекающая большую ветвь воротной
115
вены или печеночной вены; Т4 – опухоль с прямым распространением на прилежащие органы, исключая желчный
пузырь, или с перфорацией всицеральной брюшины. Прорастание висцеральной брюшины;
критерий N:
N0 - лимфоузлы ворот печени и гепатодуоденальной связки не поражены;
N1 – имеется поражение метастазами лимфоузлов ворот печени или гепатодуоденальной связки;
критерий M:
М0 |
– нет данных за наличие отдаленных метастазов; |
|
М1 |
- наличие отдаленных метастазов. |
|
|
Группировка по стадиям развития опухоли |
|
I стадия |
T1 N0 M0 |
|
II стадия |
T2 N0 M0 |
|
IIIа стадия |
T3 N0 M0; |
|
Шb стадия |
Т1-3 N1 M0 |
|
IVa стадия |
T4 N0-1 M0 |
|
IVb стадия |
T1-4 N0-1 M1 |
|
Клиника
Особенностями клинической картины первичного рака печени являются неспецифичность субъективных симптомов, быстрое течение болезни, в результате чего диагноз почти всегда устанавливается в запущенной стадии заболевания.
Больные обращаются к врачу впервые спустя в среднем 3 месяца с момента появления первых симптомов заболевания. Примерно 75% больных жалуются на похудание, отсутствие аппетита, боли в животе. Более половины больных сами обнаруживают у себя опухоль в области печени. Из предъявляемых больными жалоб следует выделить выраженную общую слабость, вялость, быструю утомляемость, увеличение размеров живота, желтуху, повышение температуры тела, понос, тошноту, рвоту, появление отеков, носовые кровотечения.
Гепатомегалия – основной объективный симптом, наблюдается у 90% больных первичным раком печени. Увеличение печени сопровождается ощущением распирания в правом подреберье и эпигастрии. При пальпации печень очень плотная, каменистой консистенции. Боль часто наблюдается у больных раком печени, однако лишь в редких случаях она бывает интенсивной. Обычно это тупая постоянная боль в эпигастрии, правом подреберье. Интенсивная боль свидетельствует о перигепатите или поражении диафрагмы. Нарушение функции желудочно-кишечного тракта при раке печени встречается часто. Проявляется отсутствием аппетита, метеоризмом и запорами. Может быть диарея, которая обусловлена холестазом или выработкой опухолью активных веществ. Одышка – поздний симптом, вызванный большими размерами опухоли, которая давит на диафрагму или прорастает в нее, либо метастазами в легкие. Желтуха – редко бывает интенсивной и не зависит от размеров опухоли. Причиной ее возникновения является сдавление или прорастание опухолью внутрипеченочных желчных протоков. Повышение температуры тела
– наблюдается у большинства больных. Носит субфебрильный характер, обусловлено раковой интоксикацией. Иногда лихорадка наблюдается при распаде опухоли или холангите. Асцит – обнаруживается у половины больных, соответствует синдрому портальной гипертензии. Часто асцит носит геморрагический характер. Асцитическая жидкость обычно не содержит опухолевых клеток. Кровотечение из варикозно расширенных вен пищевода – частое и, как правило, смертельное осложнение.
По преобладанию одного или группы симптомов описаны различные клинические формы первичного рака печени. В.С,Шапкин выделил следующие формы:
Типичный рак: для него характерны общие симптомы, как слабость, снижение веса и аппетита. Затем вследствие увеличения размеров печени может появиться боль в правом подреберье. Со временем наступает печеночная недостаточность, портальная гипертензия.
116
Цирроз-рак. Эта форма развивается на фоне имеющегося цирроза печени. Клиника та же, что и при циррозе.
Осложненный рак. Здесь на фоне благополучия по клинической картине проявляются осложнения опухоли. Например, кровотечение, механическая желтуха и т.д.
Маскированный рак. Проявляется признаками вторичных поражений, обусловленными метастазами в другие органы (легочная форма, костная и т.п.).
Бессимптомный рак.
Фиброламелярный рак. Развивается в молодом возрасте, морфологически характеризуется преобладанием стромы, накоплением медьсодержащих белков и В12связывающих белков.
Диагностика
Распознавание рака печени в начальных стадиях довольно трудно, так как нет специфических симптомов заболевания. Поэтому рак печени часто диагностируют уже в далеко зашедших стадиях. Определенное значение имеют данные анамнеза (лихорадка, боли
вправой половине живота, увеличение печени), клинического обследования (увеличение или деформация живота, выраженная подкожная сосудистая сеть в верхней половине живота, изменение формы и размеров печени). В основе диагностического алгоритма лежат инструментальные, преимущественно лучевые методы диагностики.
Лабораторные исследования обнаруживают гипохромную анемию, лейкоцитоз, ускорение СОЭ, увеличение активности трансаминаз и щелочной фосфатазы. Проба Абелева-Татаринова предполагает обнаружение повышенного содержания альфафетопротеина в сыворотке больных (в норме 20нг/л).
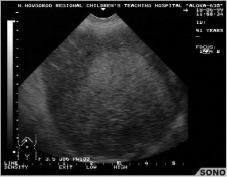
УЗИ - метод позволяет дифференцировать солидные образования и кисты, гемангиомы и злокачественные опухоли. Метод высоко информативен в определении пораженной доли и сегментов печени, позволяет судить о состоянии ворот, инвазии опухоли
вприлежащие к печени органы, выявляет увеличенные лимфоузлы ворот печени, гепатодуоденальной связки, панкреатодуоденальной и парааортальной групп, асцит. Информативность метода в отношении сосудов печени еще более возрастает если применяется ультразвуковое доплеровское сканирование.
Рис.2 УЗС печени. Узловая форма рака печени
Рентгеновская компьютерная томография или магнитно-резонансная томография.
Позволяет дифференцировать первичный рак печени от гемангиом, узлов регенераторной гиперплазии, метастазов опухолей внепеченочных локализаций. Метод информативен в топической диагностике.
Тонкоигольная пункционная биопсия метод морфологической диагностики опухолей печени осуществляется под контролем УЗИ, КТ, лапароскопии, при пальпируемых опухолях «в слепую». Может выполняться неоднократно в амбулаторных условиях. Осложнениями практически не сопровождается. Используются иглы длиной 10 – 15 см с наружным диаметром иглы 0.5 – 1.2 мм.
Ангиография высоко информативна в установлении природы, характера опухоли печени, в распространении процесса внутри и вне печени. Четкая визуализация печеночных артерий во время целиакографии, воротной вены и ее ветвей при возвратной
117
спленопортографии, нижней полой вены при нижней каваграфии – дает незаменимую информацию о сосудистой анатомии печени и ее воротах. Метод позволяет достоверно судить о резектабельности процесса в печени.
Оценка функционального состояния печени. Проводится при помощи бромсульфалеинового, антипиринового тестов. Клиренс индоцианида-зеленого для больных которым планируются обширные резекции печени должен быть не менее 1.0 мг/кг/мин.
Радиоизотопное исследование. Позволяет обнаружить «холодные очаги» в печени, соответствующие локализации опухоли, а так же исследовать поглотительновыделительную функцию печени.
Пока результаты диагностики рака печени нельзя признать обнадеживающими. Как правило, опухоль диаметром более 6 см, дающая общеклиническую симптоматику оказывается неоперабельной.
Дифференциальная диагностика рака печени
Проводится с метастатическими карциномами печени, доброкачественными опухолями, алкогольными гепатопатиями и другими неопухолевыми заболеваниями печени. Диагностика вторичной опухоли становится очевидной, если выявлен первичный очаг. При циррозе печени – реакция на АФП отрицательная. Кисты печени непаразитарной природы имеют округлую форму, эластичную консистенцию, четкую рентгенологическую картину и характерные проявления при радиоизотопном сканировании. В дифференциальной диагностике эхинококкоза печени имеют значение анамнестические данные, эозинофилия, положительные иммунологические реакции. Инода схожую картину может давать абсцесс печени.
Лечение рака печени
Хирургическое лечение. Во всех случаях, когда это, возможно, производится хирургическое удаление опухоли. Различают обширные резекции печени (право- и левосторонняя гемигепатэктомия), сегментарные резекции печени (чаще всего 4 сегмент, 2 и 3 сегменты, 8 сегмент, 6-7 сегменты, редко 1 сегмент) и атипичные резекции печени (любое сочетание сегментов, краевые резекции). Летальность после операций на печени составляет 6.1%. Причинами послеоперационной летальности являются: интраоперационное кровотечение, ДВС-синдром, гнойно-септические осложнения, печеночная недостаточность, острая сердечная недостаточность, ТЭЛА. 5 –летняя выживаемость радикально оперированных больных колеблется от 10.3 до 77.9 %. Вероятность рецидива опухоли в оставшейся ткани печени в течение 2 лет составляет 57%. К факторам, определяющим успех резекции печени при ГЦК относят: размер опухоли менее 5 см., поражение одной доли, наличие капсулы, отсутствие прорастания в сосуды, начальные стадии цирроза, относительно молодой возраст больных.
У сравнительно небольшой части больных осуществляется пересадка печени. Она выполняется у лиц моложе 60 лет, при отсутствии метастазов и тяжелых внепеченочных заболеваний.
Химиотерапия. При невозможности хирургического лечения у части больных проводится химиотерапия (схемы приведены ниже). Эффективность ее невысока, ремиссии удается достичь у 27.3 % подвергшихся лечению.
Липиодолизация – селективная региональная химиотерапия опухоли, включающая введение вместе с противоопухолевым препаратом (адриабластин, 5-фторурацил) йодолипола. Таким образом, в участке опухоли создаются масляные депо противоопухолевого средства. Препараты можно вводить повторно через 3 – 6 мес.
Артериальная эмболизация. Катетеризация печеночной артерии через бедренную артерию и чревный ствол позволяет эмболизировать питающие опухоль сосуды, метод недостаточно эффективен из-за развития артериальных коллатералей. Эмболизацию используют при нерезектабельных опухолях, рецидивах опухоли. Этот метод можно использовать в качестве экстренного мероприятия при внутрибрюшном кровотечении, вызванном разрывом опухоли. Процедуру эмболизации выполняют под местной или общей
118
анестезией и под «прикрытием» антибактериальной терапии. Воротная вена должна быть проходимой. Ветвь печеночной артерии, питающую опухоль, эмболизируют желатиновой пеной. Опухоль подвергается полному или частичному некрозу. К побочным эффектам эмболизации печеночной артерии относятся: боль, лихорадка, тошнота, асцит, значительное повышение активности сывороточных трансаминаз. Из других осложнений следует назвать формирование абсцесса и эмболизацию артерий, питающих здоровую ткань.
Внутриопухолевые инъекции этилового спирта. Небольшие (не более 5 см.) инкапсулированные опухолевые узлы, если их не более 3-х можно разрушатьчрезкожным введением в них 95% этилового спирта. Препарат вводят 2 раза в неделю по 2-12 мл. Курс лечения включает от 3 до 15 процедур. Спирт вызывает тромбоз артерий, питающих опухоль, ее ишемию и коагуляционный некроз опухолевой ткани. Однако при далеко зашедшем циррозе такое лечение не рекомендуется.
В настоящее время разрабатывается и применяется как самостоятельно, так и в сочетании с другими методами радиочастотная термоблация опухолей печени. Суть метода состоит в введении электродов в очаг (под контролем УЗИ или КТ). По ним подается переменный ток, происходит повышение температуры внутри опухолевого узла и вызывается коагуляционный некроз. Здесь имеются ограничения по размеру очагов, их количеству, также противопоказанием является близость к очагу магистрального сосуда.
Лучевая терапия как правило неэффективна и может выполняться лишь в послеоперационном периоде.
Метастазы в печень
Печень – наиболее частая локализация гематогенных метастазов опухолей независимо от того, дренируется ли первичная опухоль системой воротной вены или другими венами большого круга кровообращения. Метастазы в печень выявляются примерно у трети больных раком, причем при раке желудка, молочной железы, легких и толстой кишки они наблюдаются у половины больных. Следующими по частоте метастазирования в печень являются рак пищевода, поджелудочной железы и меланома. Метастазы в печень рака предстательной железы и яичника наблюдаются чрезвычайно редко.
Патогенез. Инвазия печени путем прорастания в нее злокачественных опухолей соседних органов, ретроградного метастазирования по лимфатическим путям и распространения по ходу кровеносных сосудов относительно редка.
Портальные эмболы попадают в печень из злокачественных опухолей органов бассейна воротной вены. Метастатическое обсеменение через печеночную артерию трудно установить гистологически, так как картина при этом такая же, как при внутрипеченочном метастазировании.
Макроскопическая картина. Степень поражения печени может быть различной. Возможно выявление только микроскопически 1 – 2 узлов или значительно увеличенной печени, «нафаршированной» метастазами. Метастазы обычно имеют белый цвет и четкие границы. Консистенция опухоли зависит от соотношения объема опухолевых клеток и фиброзной стромы. Центральный некроз метастатических узлов – следствие недостаточного кровоснабжения; он приводит к появлению втяжений на поверхности печени. Часто наблюдается инвазия в воротную вену. Клетки опухоли быстро метастазируют с вовлечением обширных участков печени как по околососудистым лимфатическим путям, так и вдоль ветвей воротной вены.
Гистологическое исследование. Метастазы в печень могут иметь такое же гистологическое строение, как и первичная опухоль. Однако это не является правилом; нередко первичный очаг представляет собой высокодифференцированную опухоль, в то время как ее метастазы в печень могут быть настолько слабо дифференцированными, что с помощью гистологического исследования невозможно установить их происхождение.
Клиника и диагностика. Клиническая картина складывается из симптомов метастазов в печень и симптомов первичной опухоли. В диагностике метастатических опухолей печени используют УЗИ, КТ, лапароскопию с взятием биопсии.
119
Лечение. Результаты лечения остаются неудовлетворительными. При одиночном метастазе печени основным методом лечения является хирургический. В остальных случаях проводится химиотерапия или эмболизация питающих опухолевые узлы ветвей печеночной артерии.
Также применяются различные методики локального воздействия на очаги. Их можно подразделить на химические и термические. К химическим относят введение различных химических агентов в очаг под УЗИ или КТ-наведением (уксусная кислота, этанол). В термических методиках используют влияние низких температур (криодеструкцию очагов жидким азотом) и высоких температур. К последним относят радиочастотную аблацию, воздействие лазерным излучением. Также применяется метод электрохимической аблации (комбинация термического действия с влиянием кислот и щелочей, образующихся вокруг электродов вследствие электрохимического лизиса тканей). Позиционирование электродов выполняется под УЗИ-контролем или КТ, МРТ («золотой стандарт»). Данные методики пока еще не получили широкого распространения, но активно исследуются в ведущих хирургических клиниках.
Прогноз и диспансерное наблюдение
Прогноз при раке печени неблагоприятный. Послеоперационная летальность составляет 6.1%; 5-летняя выживаемость – 10.3 – 30.9%; рецидив рака печени в течение 2 лет отмечается в 57% случаев.
Диспансерное наблюдение за больными, излеченными от рака печени, осуществляется по общим правилам. Учитывая возможность ранних рецидивов, промежутки между осмотрами должны быть сокращены. Во время каждого контрольного осмотра больным проводится ультразвуковое исследование печени, а лицам, излеченным от гепатоцеллюлярного рака, ставят реакцию на альфа-фетопротеин. Установлено, что синтез его возобновляется при рецидивах опухоли задолго до появления клинических симптомов.
Лекция 13
РАК ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ С.В. Соколова, К.А.Корнеев
«Распознавание рака поджелудочной железы и тем более излечение от этого недуга представляет собой одну из наиболее трудных задач клинической медицины». В.Х.Василенко
В последние десятилетия среди онкологических заболеваний рак поджелудочной железы по частоте приобретает лидирующее положение у населения большинства индустриально развитых стран. Наиболее высокий уровень смертности от этого заболевания отмечен в США, а наиболее низкий в Японии и Италии. В России по структуре заболеваемости рак поджелудочной железы занимает 7-8 место среди всех злокачественных опухолей, 4 место среди опухолей желудочно-кишечного тракта и составляет 70% среди опухолей панкреатодуоденальной зоны. Заболеваемость раком поджелудочной железы в России увеличивается в среднем на 1.2% в год. Среди городского населения рак поджелудочной железы встречается чаще, чем среди жителей сельской местности, у мужчин - в 2 раза чаще, чем у женщин. В структуре смертности от злокачественных новообразований в России удельный вес рака поджелудочной железы составляет около 5%.
Этиология, факторы риска
Экспериментально установлено, что важную роль в возникновении рака поджелудочной железы играют присутствующие в табаке компоненты нитрозамина, избыточное потребление животного протеина и углеводов. Наблюдается связь развития рака поджелудочной железы с работой в некоторых областях химической промышленности.
120
