
Акушерство_Савельева Г.М._2000
.pdfкомпенсаторных реакций организма происходит активация функций боль шинства систем, В дальнейшем наступает их угнетение, и в конечном итоге кислородная недостаточность вызывает деструктивные процессы в жизнен но важных органах. Наиболее значительными считаются изменения макро-
имикрогемодинамики, метаболизма.
Вначальных стадиях гипоксии плода наблюдается универсальная ком пенсаторно-защитная реакция, направленная на сохранение функции жиз ненно важных органов и систем. Под влиянием дефицита кислорода про исходят активация функции мозгового и коркового слоев надпочечников, выработка большого количества катехоламинов и других вазоактивных ве ществ, которые вызывают тахикардию и повышение тонуса периферических
сосудов в органах, не имеющих жизненно важного значения. Вследствие тахикардии, централизации и перераспределения кровотока увеличиваются минутный объем сердца, кровообращение в мозге, сердце, надпочечниках, плаценте и уменьшается — в легких, почках, кишечнике, селезенке, коже, в результате чего развивается ишемия этих органов. На фоне ишемии возмож ны раскрытие анального сфинктера и выход мекония в околоплодные воды.
Длительная или тяжелая гипоксия, наоборот, приводит к резкому угне тению функции надпочечников, сопровождающемуся снижением уровня кортизола и катехоламинов в крови. Угнетение гормональной регуляции сопровождается угнетением жизненно важных центров, уменьшением час тоты сердечных сокращений, снижением артериального давления, венозным застоем, скоплением крови в системе воротной вены.
Одновременно с изменениями макрогемодинамики происходят выра женные нарушения в системе микроциркуляции. Расстройства микрогемо динамики при кислородной недостаточности происходят по трем направле ниям: снижение тонуса резистивных сосудов, повышение проницаемости стенок сосудов, изменение агрегатного состояния крови с нарушением ее текучих свойств. Снижение тонуса артериол и прекапилляров вызывает расширение сосудов и увеличение объема сосудистого русла, что в сочетании с уменьшением минутного объема сердца приводит к замедлению кровотока вплоть до стаза. В условиях ацидоза и снижения скорости кровотока повы шаются вязкость крови, агрегационная активность клеток крови и коагуляционный потенциал с развитием синдрома диссеминированного внутрисосудистого свертывания крови и сладж-синдрома со снижением газообмена в эритроцитах, уменьшением адекватного газообмена в тканях. Нарушение трофики сосудистой стенки приводит к повышению ее проницаемости и выходу первоначально жидкой части крови, а затем и форменных элементов крови из сосудистого русла. Результатом этих изменений являются гипово лемия, гемоконцентрация, отек тканей, диапедезные кровоизлияния в жиз ненно важные органы.
Под влиянием кислородной недостаточности происходят значительные изменения параметров метаболизма: повышается активность ферментов, Участвующих в окислительно-восстановительных процессах, что приводит к Усилению тканевого дыхания и энергообразования в печени плода. Основ ной компенсаторно-приспособительной реакцией организма плода, способ ствующей меньшему повреждению его тканей при недостатке кислорода, является усиление процессов анаэробного гликолиза. В результате этого происходят уменьшение количества гликогена и накопление кислых про дуктов обмена (молочная кислота, кетоновые тела, лактат) в печени, сердце,
451
мозге, мышцах и крови плода, что приводит к метаболическому или ресли- раторно-метаболическому ацидозу. Одновременно происходит активация перекисного окисления липидов с высвобождением токсичных радикалов которые наряду с недоокисленными продуктами обмена при прогрессировании гипоксии угнетают ферментативные реакции, снижают активность дыхательных ферментов, нарушают структурно-функциональные свойства клеточных мембран с повышением их проницаемости для ионов. Наиболее значительны изменения баланса ионов калия, которые выходят из клеточного пространства, и уровень их в плазме крови плода повышается. Аналогичные изменения происходят в отношении ионов магния и кальция. Клиническое значение этих нарушений велико. Гиперкалиемия наряду с гипоксией и ацидозом играет важную роль в перевозбуждении парасимпатической нерв ной системы и развитии брадикардии. Следствием повышенной проницае мости клеточных мембран являются энергетический голод и гибель клеток.
Вследствие выраженных изменений макро- и микрогемодинамики, ме таболизма в тканях жизненно важных органов могут развиваться ишемия и некрозы, приводящие к необратимым деструктивным нарушениям. Эти патологические изменения не исчезают после рождения плода, а сохраня ются тем дольше, чем более тяжелую гипоксию перенес плод, определяя развитие ребенка в дальнейшем. Последствия гипоксии прежде всего про являются в головном мозге, в котором отек и микрокровоизлияния вызы вают нарушение функций центров регуляции, в первую очередь дыхатель ного и сердечно-сосудистого. При повышении внутричерепного давления даже при физиологических родах указанные изменения могут быть фоном для кровоизлияний, в том числе массивных, что в последующем может привести к развитию церебральных параличей.
К л и н и ч е с к а я к а р т и н а и д и а г н о с т и к а . Клинические про явления гипоксии плода во время беременности скудны. К ним относят изменения двигательной активности плода, ощущаемые беременной. В на чальной стадии внутриутробной гипоксии беременная отмечает беспокойное поведение плода, которое выражается в учащении и усилении его двигатель ной активности. При про фесе ирующей или длительной гипоксии происхо дит ослабление движений плода, вплоть до их прекращения. Уменьшение числа движений плода до 3 в течение 1 ч и менее является признаком внутриутробного страдания плода и служит показанием к проведению сроч ного дополнительного исследования.
Д и а г н о с т и к а г и п о к с и и п л о д а в о время б е р е м е н н о с т и состоит в непосредственной оценке его состояния и анализе результатов применения косвенных методов, позволяющих определить функциональное состояние фето плацентарной системы (кард иото ко граф ия, эхография, допплерометрия кровотока в системе мать—плацента—плод, определение био физического профиля плода, Р0 и Р с о , уровня лактата и показателей КОС в крови матери, околоплодных водах и крови плода, уровня хорионического гонадотропина, плацентарного лактогена, эсгриола).
Наиболее информативными и точными методами оценки состояния плода во время беременности (в последнем триместре) являются кардиомониторный контроль и ультразвуковое сканирование. К начальным признакам гипоксии плода при кардиотокографии относятся тахикардия (до 170 уд/MHHj или умеренная брадикардия (до 100 уд/мин), понижение вариабельности сердечного ритма, кратковременная (до 50 % записи) монотонность ритма»
452

Рис. 16.3. Выраженные признаки гипоксии плода: монотонность (а), парадоксальная реакция на функциональные пробы (б), синусоидальный ритм (в).
ослабление реакции на функциональные пробы. Кардиограмма при этом оце нивается в 5—7 баллов. При выраженном страдании плода наблюдаются зна чительная брадикардия (ниже 100 уд/мин) или тахикардия (более 170 уд/мин),
монотонность ритма (свыше 50 % записи), парадоксальная реакция на функ циональные пробы (поздние децелерации в ответ на шевеление плода при нестрессовом тесте) или ее отсутствие (рис. 16.3). О выраженной гипоксии плода свидетельствует оценка кардиотокограммы в 4 балла и менее.
Дополнительным критерием оценки состояния плода во время беремен ности является его биофизический профиль (БФП). При гипоксии проис
ходит прогрессивное угнетение биофизических функций плода. Параметры БФП при гипоксии плода делят на "острые", или быстрореагирующие (нестрессовый тест, дыхательные движения, двигательная активность и Тонус плода), и "хронические" показатели длительности страдания плода, Которые возникают в результате повторяющейся или прогрессирующей ги
поксии (маловодие и преждевременное созревание плаценты). В начальной стадии развития гипоксии в первую очередь осуществляют постановку неРеактивного нестрессового теста (НСТ), при котором с целью оценки сте-
453
пени тяжести гипоксии проводят ультразвуковое исследование и определе ние остальных биофизических параметров. При этом определение БФП заменяет проведение стрессового теста. Вслед за НСТ происходит снижение дыхательной активности плода вплоть до исчезновения его дыхательных дви жений, при прогрессирующей гипоксии исчезают движения и тонус плода Изменения биофизической активности в процессе нарастания гипоксии плода происходят в обратной последовательности от сроков созревания в эмбрио- и фетогенезе регулирующих центров ЦНС. Суммарная оценка БФП 6—7 баллов указывает на сомнительное состояние плода, в связи с чем требуется проведе ние повторного исследования, а оценка 4—5 баллов и менее свидетельствует
оналичии выраженной внутриутробной гипоксии плода.
Вдиагностике гипоксии плода важное значение придают допплерометрической оценке кровообращения в аорте и сосудах головного мозга плода. Допплерометрия позволяет несколько раньше, чем кардиотокография, диа гностировать внутриутробную гипоксию, что способствует выявлению груп пы беременных, подлежащих тщательному наблюдению и лечению. Гемодинамические нарушения в аорте и сосудах головного мозга плода вторичны
исвидетельствуют о нарушении центральной гемодинамики плода в ответ на уменьшение плацентарной перфузии. Увеличение диастолической ско рости кровотока в головном мозге плода при гипоксии указывает на сохра нение церебрального кровотока плода в этих условиях за счет вазодилатацци. Компенсаторный механизм поддержания нормального кровоснабжения го ловного мозга при сниженной плацентарной перфузии носит название "ох ранный круг кровообращения". Существует коррелятивная связь между средней скоростью кровотока в аорте и средней мозговой артерии плода,
рН, Р с 0 и Ро в его крови. При тяжелой гипоксии уменьшение ПИ в средней мозговой артерии достигает максимума, что отражает максимальную дилатацию этого сосуда. Крайне неблагоприятный прогностический при знак для плода — появление нулевых или отрицательных значений диасто лического компонента кровотока в аорте, что свидетельствует о декомпен сации фетоплацентарной системы. Как правило, эти изменения сочетаются с патологическим кровотоком в артерии пуповины, однако показатели пуповинного кровотока могут быть и нормальными. В более поздних стадиях по мере прогрессирования гипоксии возникают нарушения венозного кро вотока (венозный проток, печеночные вены).
С целью диагностики кислородной недостаточности у плода проводят осмотр и биохимическое исследование околоплодных вод. В случае гипок сии плода при амниоскопии обнаруживают окрашивание околоплодных вод меконием. Наиболее информативными тестами при исследовании около плодных вод, получаемых при амниоцентезе, являются рН ниже 7,02; Рсо2 выше 55 мм рт.ст., Р0^ ниже 80 мм рт.ст., концентрация калия выше
6,5 ммоль/л. О кислородной недостаточности плода, кроме того, свидетель ствуют повышение активности щелочной фосфатазы в околоплодных водах более чем в 2 раза. Определение концентрации плацентарных гормонов в сыворотке крови и моче беременных позволяет диагностировать плацентар ную недостаточность, приводящую к гипоксии плода. Уровень плацентар ного лактогена в сыворотке крови беременных при гипоксии плода снижа ется в 3 раза (норма 10 мкг/мл). Из фракций эстрогенов наиболее инфор мативен показатель экскреции эстриола: экскреция гормона менее 12 мг/сут (в околоплодных водах менее 50 мг/100 мл) свидетельствует о плацентарной
454
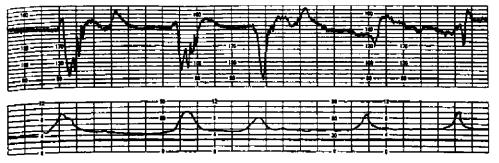
Рис. 16.4. Признаки гипоксии плода в родах (V- и W-образные децелерации).
недостаточности. Заслуживает внимания используемый в настоящее время новый метод диагностики гипоксии плода на основании результатов изуче ния различных параметров его крови (КОС, уровень гемоглобина и др.), полученной с помощью кордоцентеза.
Д и а г н о с т и к а г и п о к с и и п л о д а в р о д а х основывается на выявлении нарушений его сердечной деятельности. Помимо аускультации, наиболее доступным методом выявления гипоксии плода в родах является кардиотокография (рис. 16.4). При кардиомониторном наблюдении к на чальным признакам гипоксии плода в первом периоде родов относятся брадикардия до 100 уд/мин как при головном, так и тазовом предлежании плода, периодическая монотонность сердечного ритма. Реакция на схватку прояв ляется кратковременными поздними децелерациями до 70 уд/мин. Во вто ром периоде родов начальными признаками гипоксии служат браликардия до 90 уд/мин или тахикардия до 200 уд/мин, регистрируется периодическая монотонность ритма. В ответ на потугу возникают поздние децелерации до 60 уд/мин. К выраженным признакам гипоксии плода в первом периоде родов относятся брадикардия до 80 уд/мин при головном предлежании, брадикардия ниже 80 уд/мин или тахикардия до 200 уд/мин при тазовом предлежании плода. Независимо от предлежания плода регистрируются стойкая монотонность ритма и аритмия. Реакциями на схватку являются возникновение длительных поздних W-образных децелерации при головном предлежании и комбинация акцелераций с децелерациями до 80 уд/мин при тазовом предлежании плода.
В периоде изгнания к выраженным признакам гипоксии относится появление на кард иото ко грамме выраженной брадикардии до 80 уд/мин или тахикардии более 190 уд/мин; регистрируется стойкая монотонность ритма 11 аритмия, в ответ на потугу отмечаются длительные поздние децелерации До 50 уд/мин как при головном, так и тазовом предлежании плода. При головном предлежании вне схватки регистрируются W-образные децелера ции до 50 уд/мин.
В процессе родов в отличие от антенатального периода прогностически неблагоприятным фактором в отношении гипоксии следует расценивать Появление дыхательной или двигательной активности плода. Регулярная вЫраженная дыхательная активность плода как в первом, так и во втором Периодах родов представляет собой большую угрозу для новорожденного, являясь причиной развития у него аспирационного синдрома.
455
Большое значение в выявлении гипоксии плода имеет исследование КОС крови, полученной из предлежащей части. В первом периоде родов рН ниже 7,2 свидетельствует о гипоксии, а от 7,20 до 7,24 — о преацидозе в связи с чем требуется повторное исследование. Нижняя граница нормы рН во втором периоде родов 7,14.
Выделение мекония в процессе родов не столько характеризует состоя ние плода, сколько заставляет обратить внимание на угрожающую ситуацию и имеет значение лишь при головном предлежании. В зависимости от длительности и глубины гипоксии примесь мекония в водах имеет разный характер: от взвешенных кусочков в начальной стадии гипоксии до образо вания грязной эмульсии при тяжелой гипоксии. Наличие мекония в около плодных водах может указывать не только на острую, но и кратковременную или длительную гипоксию плода, возникшую до родов, и плод в отсутствие новых эпизодов гипоксии может родиться без асфиксии.
Л е ч е н и е , Во время беременности лечение хронической гипоксии плода должно быть комплексным. Кроме лечения основного заболевания, беременной необходимо проводить терапию, направленную на нормализа цию плацентарного кровообращения, улучшение снабжения плода кислоро дом и энергетическими веществами, повышение адаптационных возможнос тей в системе мать—плод и устойчивости плода к гипоксии, создание усло
вий, благоприятствующих течению обменных процессов. Для решения этих задач в первую очередь следует воздействовать на кислородотранспортную функцию плаценты путем: 1) расширения маточно-плацентарных сосудов; 2) расслабления мускулатуры матки; 3) нормализации реокоагуляционных свойств крови; 4) активации метаболизма миометрия и плаценты.
Прежде всего беременным необходимо обеспечить покой. Постельный режим, при котором улучшается кровоснабжение матки, показан при выяв лении гипоксии плода и отставании его в развитии, особенно при недоно шенной беременности.
Снабжение организма матери кислородом улучшается в результате ин галяции его с помощью маски. При этом оптимальным вариантом является вдыхание беременной 40—60 % кислородно-воздушной смеси в количестве 4—5 л/мин в течение 30—60 мин 1—2 раза в день. Выраженный эффект дает применение кислородного коктейля или кислородной пены. Кислородный коктейль всасывается медленно; его принимают по 150—200 мл в течение 5—10 мин и более за 1,5 ч до или через 2 ч после еды. Для профилактики и лечения гипоксии у матери и плода при сердечно-сосудистых заболеваниях
суспехом применяют гипербарическую оксигенацию.
Сцелью улучшения маточно-плацентарного кровообращения в состав комплексной терапии включают эстрогены, которые влияют на обменные процессы в эндометрии, повышают проницаемость плаценты, увеличивают переход глюкозы и питательных веществ к плоду. Одним из препаратов, оказывающих слабое эстрогенное действие и улучшающих маточно-плацен- тарный кровоток, является сигетин, который вводят в виде 1—2 % раствора по 2—4 мл в 20 мл 40 % раствора глюкозы. Его целесообразно применять на фоне введения сосудорасширяющих средств (2,4 % раствор эуфиллина внутривенно струйно или капельно в дозе 5—10 мл, компламин по 0,15 г 3 раза в день во время еды или по 2 мл 15 % раствора 1—2 раза в день, курантил по 0,5 мл/кг внутривенно капельно в течение 2—5 ч или перорально по 0,025 г 2—3 раза в день после инфузии).
456
Для нормализации маточно-плацентарного кровотока и активации ме таболизма в плаценте применяют токолитики (р-адреномиметики) нового поколения — бриканил, гинипрал в виде внутривенных инфузии (на раство ре глюкозы) по 0,5 мг, длительно.
С целью нормализации реокоагуляционных свойств крови используют дезагреганты (трентал, низко молекулярные декстраны) и антикоагулянты (гепарин по 20 ООО ЕД/сут в виде подкожных инъекций или внутривенных инфузии).
К препаратам, влияющим непосредственно на метаболические процес сы, относятся АТФ, кокарбоксилаза, фолиевая кислота, концентрированные растворы глюкозы, метионин, ударные дозы витамина В12, галаскорбин.
При лечении хронической гипоксии плода обязательно применяют мембраностабилизаторы (эссенциале-форте или липостабил по 2 капсулы 3 раза в день либо внутривенно по 5 мл) и антиоксиданты (витамин Е по 600 мг/сут, аскорбиновая кислота по 600 мг/сут, глутаминовая кислота по 0,3 г/сут).
Коррекцию баланса кислот и щелочей у беременных следует проводить под контролем параметров КОС крови, поскольку патологические состоя ния у них не всегда сопровождаются ацидозом. Лечение ацидоза должно быть направлено на коррекцию баланса кислот, щелочей и улучшение периферической циркуляции. Введение таких лекарственных препаратов, как глюкоза, витамин С, кокарбоксилаза, АТФ, приводит к нормализации КОС крови, поэтому проведение инфузионной терапии само по себе кор ригирует нарушения кислотно-основного обмена, а иногда может наблю даться тенденция к алкалозу.
Хороший эффект дают вещества, повышающие устойчивость ткани мозга к недостатку кислорода (седуксен, оксибутират натрия). Наряду с улучшением энергетического обеспечения мозга они обеспечивают сниже ние потребления кислорода ЦНС без существенного подавления функций ее жизненно важных центров. В условиях гипоксии выраженное защитное действие ГОМК оказывает также на клетки миокарда, печени, почек.
Особенно важны терапия и подготовка к родоразрешению при прежде временных родах, когда гипоксия плода усугубляется незрелостью легочной ткани. Для ускорения созревания легочной ткани показаны глюкокортикоиды: дексаметазон 4 раза в день в течение 2—3 сут, разовая доза 2 мг, суточная — 8 мг, курсовая — 16—24 мг.
При отсутствии эффекта от комплексной терапии хронической гипок сии плода при сроках гестации 28—32 нед и более выраженные изменения кардиото ко граммы и биофизического профиля плода, обнаружение мекония а околоплодных водах, маловодие, острая гипоксия плода являются показа ниями к экстренному родоразрешению независимо от срока гестации. При этом предпочтение следует отдавать кесареву сечению.
В родах терапию изменяют в зависимости от акушерской ситуации, выбирая быстродействующие эффективные препараты (глюкоза, увлажнен ный кислород, эуфиллин, кокарбоксилаза, сигетин, аскорбиновая кислота), введение которых предшествует оперативному родоразрешению (кесарево сечение, акушерские щипцы, извлечение плода за тазовый конец, вакуумэкстракция, перинеоили эпизиотомия).
Профилактика гипоксии плода и асфиксии новорожденного должна основываться на ранней дородовой диагностике и состоять из следующих компонентов:
457
•своевременной госпитализации беременной из группы риска развития гипоксии плода;
•проведения интенсивной терапии акушерской и экстрагенитальной патологии беременных;
•выбора адекватных методов родоразрешения;
•комплексной терапии гипоксии плода, включающей коррекцию рас стройств гемодинамики, микроциркуляции, нарушений метаболизма функции фетоплацентарного комплекса;
•досрочного родоразрешения при отсутствии эффекта от проводимой терапии.
В процессе родов лечение и профилактика гипоксии плода, асфиксии новорожденного обязательны в следующих случаях:
•слабость родовой деятельности и длительный безводный промежуток при несвоевременном излитии вод;
•перенашивание беременности;
•гестозы (длительно текущие или тяжелые формы);
•тазовое предлежание плода;
•изосерологическая несовместимость крови матери и плода;
•сахарный диабет, сердечно-сосудистые заболевания и другие состоя ния, влияющие на плод.
16.4.ВНУТРИУТРОБНАЯ ИНФЕКЦИЯ
Внутриутробная инфекция (ВУИ) занимает одно из ведущих мест в струк туре причин перинатальной заболеваемости и смертности.
Различают внутриутробную инфекцию и инфицирование. При внутри утробных инфекциях и инфицировании плода и новорожденного заражение происходит в перинатальном периоде или в родах и источником его является мать.
Внутриутробная инфекция — заболевание, клинически проявляющееся в виде пиодермии, гепатита, гастроэнтерита, пневмонии, отита и другой патологии вплоть до сепсиса.
Инфицирование плода выражается лишь в проникновении в его орга низм возбудителя и не сопровождается клиническими проявлениями, что, возможно, объясняется мобилизацией иммунитета и защитных механизмов
всистеме мать—плацента—плод.
Взарубежной литературе для обозначения группы инфекций со сход ными клиническими проявлениями, вызывающих в последующем стойкие структурные изменения органов и систем у детей, используют аббревиатуру TORCH: Т — токсоплазмоз, О — другие (other) инфекции (сифилис, хла мидиоз, энтеровирусные инфекции, гепатиты А и В , гонорея, листериоз), R — краснуха (rubeola), С — цитомегаловирусная инфекция (cytomegaHa), Н — герпесвирусная инфекция (herpes). Среди многообразных возбудителей ВУИ значительную роль играют грамотрицательные аэробные бактерии, неспорообразующие анаэробы, микоплазмы, стрептококки группы В, дрожжеподобные грибы.
Внашей стране принята классификация ВУИ, в которой в I группу
458
объединены все вирусные заболевания эмбриона и плода, а во 2-ю — забо левания плода, вызванные бактериальной флорой.
Клинические проявления и тяжесть течения ВУИ зависят от вида воз будителя, его вирулентности, массивности обсеменения, уровня иммунной реактивности организма и стадии инфекционного процесса у беременной, срока гестации в момент инфицирования, путей проникновения возбудителя в организм беременной.
При ВУИ, возникших в первые 3 мес беременности, соответствующие периодам органогенеза и плацентации, возникают инфекционные эмбриопатии, для которых характерны истинные пороки развития, первичная пла центарная недостаточность, неразвивающаяся беременность, самопроиз вольные выкидыши. Ведущую роль в возникновении эмбриопатий играют микроорганизмы с внутриклеточным циклом развития (в частности, виру сы), обладающие высоким тропизмом к эмбриональным тканям.
В случае возникновения ВУИ после 3 мес гестации развиваются инфек ционные фетопатии, которые сопровождаются внутриутробной задержкой роста плода, формированием вторичной плацентарной недостаточности, возникновением дизэмбриогенетических стигм, собственно инфекционным поражением плода. В раннем фетальном периоде еще не происходит лока лизации воспалительного процесса, поэтому ВУИ, как правило, протекает генерализованно, сопровождается нарушением маточно-плацентарного кро вообращения, дистрофическими, некробиотическими реакциями, наруше нием формообразовательных процессов с избыточным разрастанием соеди нительной ткани (глиоз мозга, эндокардиальный фиброэластоз). Воспали тельные изменения пролиферативного характера могут вызвать сужение или обтурацию существующих анатомических каналов и отверстий с последую щим развитием аномалии уже сформированного органа (гидроцефалия, гид ронефроз). Во второй половине фетального периода (с 6—7-го месяца) благодаря становлению клеточного и гуморального иммунитета плод при обретает способность специфически реагировать на внедрение возбудителей инфекции.
Наиболее характерными клиническими симптомами ВУИ являются многоводие, стойкая тахикардия у плода, задержка роста плода, реже встре чается маловодие.
В диагностике внутриутробного инфицирования основными являются бактериологические и иммунологические методы. К ним относятся обнару жение в посевах этиологически значимых микроорганизмов в количестве, превышающем 5-102 КОЕ/мл, и более современный и специфичный метод молекулярной гибридизации, суть которого заключается в идентификации определенных фрагментов ДНК или РНК клеток возбудителя. Посевы и соскобы (для выявления внутриклеточного расположения возбудителей) берут у беременных из влагалища и канала шейки матки.
Наиболее чувствительным и специфичным методом диагностики внут риутробного инфицирования является ELISA-метод, в основу которого по ложено определение моноклональных антител в жидкостях и средах орга низма с помощью тест-системы. Высокий титр антител в сочетании с выделенным антигеном (возбудителем) свидетельствует об инфицированНости плода и элементов плодного яйца.
Кроме специфических серологических и иммунологических тестов, по зволяющих уточнить характер возбудителя инфекции, стадию процесса и
459
риск инфицирования плода, немаловажное значение имеют следующие ла бораторные тесты: дизиммуноглобулинемия (снижение уровня IgG до 7,9 г/л и ниже в сочетании с повышением уровня IgM до 2 г/л), увеличение содер жания циркулирующих иммунных комплексов до 7,6—8,8 ед., лимфопения снижение фагоцитарной активности лейкоцитов до 60—62 %, повышение уровня средне молекулярных пептидов до 0,30 у.е., нарушения в интерфероновом статусе.
Наиболее характерными признаками ВУИ при УЗИ считают плацентит утолщение плаценты, несвоевременное созревание плода и плаценты, уве личение размеров живота плода, гепатомегалию, пиелоэктазии у плода многоводие, наличие газа в желчном пузыре.
Общи е принцип ы профилактик и и лечени я ВУИ . 1. Этиотропная противомикробная терапия с учетом стадии, общих и локальных симптомов, длительности течения инфекционного воспалительного заболе вания, наличия смешанной инфекции, срока гестации, клинико-лаборатор- ных данных.
2.Профилактика (лечение) нарушений функций фетоплацентарного комплекса в 10—12, 20—22 и 28—30 нед беременности (метаболическая терапия, вазоактивные препараты и антиагреганты).
3.Коррекция и профилактика нарушений микробиоценозов организма беременной: бифидумбактерин, лактобактерин (не менее 15 доз в сутки), флоррадофилус (1 капсула 2 раза в сутки) внутрь в течение 10—14 дней, ацилакт или лактобактерин вагинально. Курсы проводят в критические сроки беременности или сочетают с курсами антибактериальной терапии.
4.Лечение половых партнеров.
16.4.1. Вирусные заболевания эмбриона и плода
Краснуха. Наибольшую опасность для эмбриона с точки зрения тератоген ного действия представляет вирус краснухи. При беременности риск зара жения краснухой существует в случае отсутствия в крови матери антител к антигену вируса краснухи. Если женщина заболевает краснухой в первые 2 мес беременности, то вероятность инфицирования эмбриона достигает 80 %, а возникновения уродства — 25 %. Поражение эмбриона вирусом краснухи может закончиться его гибелью (эмбриотоксический эффект) или возникновением врожденных пороков сердца, глухоты, катаракты, микро офтальмии, хориоретинита и микроцефалии. Инфицирование плода в более поздние сроки может сопровождаться появлением у новорожденного типич ных кожных высыпаний, которые вскоре исчезают.
Принимая во внимание высокий риск возникновения эмбриопатий в случае развития заболевания в первые 3 мес беременности, необходимо ее прерывать. Введение глобулина беременным, больным краснухой, приводит к незначительному снижению частоты аномалий развития плода.
Ребенок, родившийся у женщины, перенесшей во время беременности краснуху, является носителем вируса, поэтому необходима его изоляцияПри подозрении на контакт беременной с больным краснухой, в случае, если она не болела ею в детстве или более позднем возрасте, необходима вакцинация, но не ранее 8—10 нед гестации, так как с этой целью исполь зуют живую ослабленную вакцину и возможен тератогенный эффект. По рекомендации ВОЗ женщинам детородного возраста вне беременности про-
460
