
65bbb357_pedfak_kpf
.pdf
3.Лактоза способствует лучшему усвоению кальция, магния и марганца, препятствуя развитию рахита и анемии.
Непереносимость сахарозы (сахарозно-изомальтазная недостаточность)
При врожденном недостатке мальтазы симптоматика проявляется при переходе на искусственное вскармливание, т. е. с введением в организм сахара и крахмала. Нелеченные синдромы мальабсорбции осложняются хроническим дисбактериозом.
Клиническая картина напоминает симптоматику непереносимости лактозы, однако, обусловлена введением в рацион питания ребенка сахарозы (сахара), содержащейся в частично адаптированных молочных смесях, фруктовом соке, фруктовом пюре, овощных блюдах, выпечке. Как правило, возникает типичная осмотическая диарея и любые варианты дисфункции кишечника (тошнота, рвота, вздутие живота, понос, боль в эпигастральной области).
Лечение. Диетотерапия — исключение из рациона питания продуктов, содержащих сахар и крахмал.
12.1.3. Нарушения первичного преобразования углеводов
Эти нарушения встречаются относительно нечасто, но представляют серьезную опасность в связи с токсическим действием некоторых промежуточных продуктов обмена углеводов, которые при этом накапливаются.
В кишечнике всасывается глюкоза, галактоза, фруктоза, но использует организм только глюкозу, а галактоза и фруктоза подвергаются унификации, превращению в глюкозу.
Галактоземия
Галактоземия связана с нарушением унификации галактозы в глюкозу. Процесс унификации представлен на рис 2.
|
|
|
|
Галактоза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
галактитол |
|
АТФ |
галактокиназа |
|
Галактоновая кислота + ксилулоза + |
|
||
|
|
|
|
|
СО2 |
|
|||
|
|
|
|
|
|
|
|
|
|
Проявления: |
|
|
1 |
|
|
|
|
||
|
|
|
|
|
|
||||
катаракта |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
||
|
|
|
|
Галактозо-1-фосфат |
|
|
|
||
|
|
|
|
|
|
|
|
||
|
|
|
УДФ-глюкоза |
Галактозо-1-фосфат-уридил трансфераза |
51 |
||||
|
|
|
|
|
|
|
|
|
|
Проявления: |
|
|
2 |
|
|
|
|
||
катаракта, |
|
|
|
|
|
|
|||
умственная |
|
|
|
|
|
|
|
||
Рис. 2. Пути обмена галактозы и его расстройства. Штриховыми линиями показаны альтернативные пути метаболизма
Галактоземия возникает при нарушении обмена галактозы, обусловленном наследственным дефектом любого из трёх ферментов, включающих галактозу в метаболизм глюкозы. Наследуется аутосомно-рециссивно.
Формы галактоземии
1)В организме больного с дефицитом галактокиназы накапливаются нерасщепленная галактоза и ее побочные метаболиты (рис. 2). При патологии избыток галактозы превращается в спирт галактитол (дульцитол), оказывающий токсическое влияние на хрусталик, где дульцитол накапливается и осмотически привлекает воду. Изменяется солевой состав хрусталика и его белки денатурируются, вследствие чего возникает катаракта в молодом возрасте. Катаракта возможна даже у плодов матерей с галактоземией, употреблявших молоко во время беременности.
2)Галактоземия, вызванная недостаточностью галактозо-1-фосфатуридилтрансферазы, наиболее хорошо изучена (рис. 2). Недостаточность этогофермента приводит к накоплению в тканях галактозо-1-фосфата и галактозы. Кроме поражения хрусталика при этой форме патологии галактозо-1-фосфат оказывает токсическое влияние на нейроны, гепатоциты и нефроциты; угнетает активность ряда ферментов печени, почек и других органов, в том числе активность фосфоглюкомутазы и глюкоза-6-фосфат-дегидрогеназы. Как результат поражения нейронов возможно возникновение задержки психомоторного развития. Для понимания патогенеза поражений ЦНС следует помнить, что галактоза — важный компонент
гликолипидов мозга. У больного имеется тенденция к гипогликемии, истощаются запасы гликогена в гепатоцитах, происходит компенсаторная мобилизация жиров, развивается стеатоз, а также некроз гепатоцитов и цирроз печени. В почках и кишечнике избыток галактозы и ее метаболитов ингибирует транспорт аминокислот.
52
Помимо токсического действия на ценральную нервную систему, галактоземия вызывает отек мозга вследствие повышения концентрации галактозы в спинномозговой жидкости и желудочках мозга. Поражение клеток печени приводит к гипопротромбинемии, гипопротеинемии, повышению уровня неконъюгированного билирубина в крови. Аминоацидурия, наблюдаемая при галактоземии, связана с тем, что галактозо-1- фосфатуридилтрансфераза инактивирует реабсорбцию аминокислот в почечных канальцах и повреждает капилляры клубочков. Эритроциты больного поглощают кислород на 25-30% меньше, чем в норме, что ведет к уменьшению продолжительности их жизни и гемолизу. В связи
сэтим часто развивается анемия.
Свозрастом, как правило, активность отсутствующей у младенцев УДФ-галак- топирофосфорилазы возрастает.
Ранние симптомы дефекта галактозо-1-фосфатуридилтрансферазы: рвота, диарея, дегидратация, уменьшение массы тела, желтуха. Они появляются вскоре после рождения, как только ребёнок начинает получать молоко. В крови, моче и тканях повышается концентрация галактозы и галактозо-1-фосфата.
3) Для галактоземии, вызванной дефектом фермента уридилфосфат-4-эпимераза характерны галактоземия и галактозурия (рис. 2). Тяжёлых клинических проявлений нет. Описаны единичные случаи заболевания.
Лечение галактоземии: устранение из рациона питания молочных продуктов.
Фруктозурия.
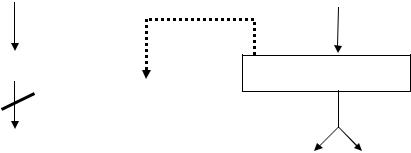
Фруктозурия связана с нарушением унификации фруктозы в глюкозу. Процесс унификации представлен на рис 3.
гликоген |
|
фруктоза |
|
|
|
|
|
|
|
|
|
|
блокада |
||
|
|
фруктокиназа |
|
Глюкозо-1-фосфат |
Фруктоза-1-фосфат |
|
фосфоглюкомутаза
 Фруктозо-1-фосфат-альдолаза
Фруктозо-1-фосфат-альдолаза
Глюкозо-6-фосфат
глицеральдегид фосфодиксинацетон
Рис. 3. Пути обмена фруктозы. Штриховой линией показано влияние на процесс
53
гликогенолиза
Фруктоземия — наследственное заболевание, передающееся по аутосомно-рецессивному типу, связано с резко пониженной активностью фермента фруктозо-1-фосфатальдолазы. При недостаточной активности этого фермента ассимиляция фруктозы задерживается до фруктозо-1- фосфата, который тормозит активность фосфоглюкомутазы (рис. 3). Последняя превращает глюкозо-1-фосфат в глюкозо-6-фосфат и обеспечивает конверсию продукта реакции, катализируемой фосфорилазой, в глюкозо-б-фосфат. Поэтому при фруктоземии происходит торможение распада гликогена на этапе глюкозо-1-фосфата и последующее развитие гипогликемии, усиление мобилизации липидов, формирование стеатоза печени и гиперурикемии.
Поступление фруктозы приводит к увеличению концентрации лактата, ингибирующего почечно-канальцевую секрецию уратов, что приводит к гиперурикемии, усугубляемой истощением внутрипечёноч-ного фосфата и ускоренной деградацией адениновых нуклеотидов.
Клинические проявления возникают при переводе детей на смешанное или искусственное вскармливание. После приема фруктового сока или фруктов возникают слабость, дрожь, судороги, потливость, рвота, нарушение сознания. Могут отмечаться транзиторная желтуха, протеинурия. Возможны гепатоспленомегалия и цирроз печени. Из-за ускоренного распада АТФ и понижения экскреции уратов в условиях метаболического ацидоза характерна гиперурикемия, в молодом возрасте формируется подагра.
Лечение фруктоземии заключается в исключении из рациона соков, ягод, фруктов и овощей. При своевременном выключении фруктозы ребенок развивается нормально и проявления заболевания приобретают обратное развитие.
12.1.4. Гипокликемия новорожденных
Выделяют патологическую и физиологичекую гипогликемию новорожденных.
Физиологическая гипогликемия новорожденных
Причины:
-повышенное потребление сахара организмом ребенка в период адаптации к постнатальной жизни;
-высокий тонус скелетной мускулатуры;
-повышенная выработка инсулина;
-незрелость гликогенолитической функции печени.
Патологическая гипогликемия новорожденных
Причины:
54

-внутриутробная гипотрофия, плацентарная недостаточность, приводящие к недостаточному поступлению питательных веществ;
-гипоксия, гипертермия, переохлаждение, инфекции, полицитемия, приводящие к интенсивному поглощение углеводов;
-наследственные аномалии обмена углеводов (галактоземия, непереносимость фруктозы);
-гилеринсулинизм новорожденных, рожденных от матерей с СД;
-недостаточность коры надпочечников.
Частота гипогликемии возрастает при низкой массе тела. Классические симптомы гипогликемии проявляются при содержании глюкозы <2, 8 ммоль/л.
12.1.5. Нарушение синтеза и распада гликогена в тканях. Гликогеновые болезни
В последние 2-3 месяца беременности синтез гликогена идет очень активно, данный гликоген используется организмом ребенка в первые дни его жизни. Самостоятельно же синтез гликогена начинается лишь на 2-3 месяце жизни.
Нарушение синтеза и распада гликогена, главным образом, проявляются в виде гликогеновых болезней. Гликогеновые болезни — группа наследственных нарушений, в основе которых лежит снижение или отсутствие активности ферментов, катализирующих реакции синтеза или распада гликогена, либо нарушение регуляции этих ферментов. Подразделяются на агликгенозы и гликогенозы.
Агликогеноз
Очень редкое заболевание обусловленое отсутствием активности гликогенсинтетазы в печени. Наследуется аутосомно-рецессивно. У больных содержание гликогена в печени через 4-6 ч после еды в 10 раз ниже, чем у здоровых людей. Из-за нарушения синтеза гликогена основное количество глюкозы превращается в ходе гликолиза в лактат. Глюкагон стимулирует глюконеогенез и приводит к превращению лактата в глюкозу.
Характерно своеобразное нарушение метаболизма — тяжелая гипогликемия с кетоацидозом утром натощак и гипергликемия с лактацидозом днем после еды. В результате гипогликемии наблюдается задержка психомоторного развития, умственная отсталость. Болезнь совместима с жизнью, хотя пораженные дети нуждаются в частом кормлении.
Глюкоза
гексокиназа
Глюкозо-6-Фосфат
фосфоглюкомутаза
Глюкозо-1-фосфат
55
УДФ
гл-1-ф-уридилтрансфераза
Рис. 4. Наследственные нарушения синтеза и распада гликогена
Гликогенозы
Гликогенозы — заболевания, обусловленные дефектом ферментов, участвующих в распаде гликогена (рис. 4). Они проявляются или необычной структурой гликогена, или его избыточным накоплением в печени, сердечной или скелетных мышцах, почках, лёгких и других органах.
По клиническим признакам различают три основные формы заболевания:
1)печеночную;
2)мышечную;
3)генерализованную.
Печеночная форма. Признаки появляются на первом году жизни, начиная с 8-9 месяца, когда отмечаются редкие приступы гипогликемии. Они характеризуются временной потерей
56
сознания, клоническими судорогами конечностей. Припадки начинаются до еды или утром, их появление можно предотвратить приемом сладкой воды. Характерный внешний вид детей: маленький рост, большой живот, худые конечности, "кукольное лицо". Отмечается увеличение печени. Самый опасный возраст — первые 4-5 лет. Инфекционные заболевания осложняют течение патологического процесса. С возрастом состояние больного улучшается благодаря развитию компенсаторных механизмов обмена. Интеллект, как правило, не нарушен. При гистохимическом исследовании печени обнаруживают сильное разрастание коллагеновой соединительной ткани, печеночные клетки которые богаты гликогеном, содержат много липидов. Основные биохимические формы: Болезнь Гирке, Болезнь Форбса-Кори (лимито-декстриноз), Болезнь Андерсена, Болезнь Херса.
Мышечная форма. Симптомы заболевания появляются с 7-10 лет. Больные становятся малоподвижными, быстро устают при физической нагрузке. Мышечная слабость прогрессирует, появляются боли в работающих мышцах, усиленное сердцебиение, одышка. Все эти симптомы развиваются до 25-35 лет. Внешний вид больных не меняется. Симптомов изменения печени и почек нет. При осмотре — выраженная атрофия мышц и их гипотония. При гистохимическом исследовании видно мышечные волокна с дегенерацией, вплоть до некроза. Они содержат вакуоли, наполненные гликогеном. Прогноз заболевания благоприятный, но известны летальные исходы в 20-30 лет. Основная биохимическая форма — Болезнь МакАрдля.
Генерализованная форма. При этой форме заболевания практически во всех органах и тканях накапливается большое количество гликогена. Клиника ее не похожа на клинику печеночной и мышечной форм, она многообразна, имеет прогрессирующее течение. Основная биохимическая форма — Болезнь Помпе.
Биохимические формы гликогенозов
I тип — болезнь Гирке. Развивается при отсутстви активности специфической глюкозо- 6-фосфатазы в печени и слизистой кишечника. Наследуется по аутосомно-рецессивному типу.
Неспособность организма больного превратить глюкозо-6-фосфат в глюкозу ведет к недостатку глюкозы в крови и накоплению гликогена в гепатоцитах и нефроцитах. Это приводит к гипоинсулинемии. В результате, активируется липолиз, формируется гиперлипопротеинемия, ацетонемия, метаболический ацидоз и ацетонурия.
С течением времени прогрессируют гепатомегалия и нефромегалия за счет гликогенной инфильтрации. Характерны отставание в росте, диспропорция тела (большая голова, короткие шея и ноги), кукольное лицо, гипотония мышц. В связи с резкой гипогликемией больные вынуждены почти постоянно принимать пищу. Часто присоединяющиеся вторичные инфекции приводят к значительному усилению кетоацидоза и гипогликемии и нередко являются причиной смерти. Нервно-психическое развитие удовлетворительное.
Биохимические нарушения: гипогликемия, кетоз, гиперлактацидемия, гиперлипемия,
57
повышение в крови уровня неэтерифицированных жирных кислот, гликогена, холестерина, мочевой кислоты, нарушение почечного клиренса для ряда веществ. В молодом возрасте формируется подагра и уролитиаз. Даже относительно непродолжительное голодание ведет к гипогликемии. Больным рекомендуют избегать употребления продуктов, содержащих сахарозу и лактозу.
II тип — болезнь Помпе. Наследуется по аутосомно-рецессивному типу. Болезнь имеет наиболее неблагоприятное течение, при этом во всех органах отсутствует лизосомная α-1,4- глюкозидаза, что приводит к накоплению гликогена во всех тканях и прежде интенсивно работающих мышцах и сердце.
Ведущий признак заболевания - увеличение сердца, что приводит к развитию тяжелой сердечной недостаточности. До некоторой степени поражается и печень, но главные события развиваются в мышечной ткани: нарастает слабость скелетных мышц (как следствие значительного накопления неутилизируемого гликогена в скелетной мускулатуре), формируется расширение сердца и наступает смерть в раннем возрасте, в результате сердечной недостаточности. Одним из внешних проявлений является увеличение языка. Сниженная активность фермента обнаруживается и в лейкоцитах, что обусловливает умеренный иммунодефицит.
Прогноз неблагоприятный: больные умирают в грудном возрасте. Эффективного лечения не существует. Возможна пренатальная диагностика этого заболевания методом амниоцентеза.
III тип — болезнь болезнь Кори (болезнь Форбса, лимитдекстриноз). Это аутосомно-
рецессивный дефект фермента, катализирующего гидролиз α-1,6-связей в молекуле гликогена. В клинической картине наиболее характерна гепатомегалия, как следствие накопления гликогена. С первых месяцев жизни наблюдаются гепатомегалия, мышечная гипотония, гипертрофия отдельных мышечных групп. Прогноз, как правило, благоприятный. Заболевание наиболее опасно в 4-5 лет, когда происходят частые приступы гипогликемии. В более зрелом возрасте симптомы заболевания сглаживаются. Лечение дает хорошие результаты при применении богатой белками диеты с частыми приемами пищи, для того, чтобы образование глюкозы шло обходным путем с помощью трансаминирования аминокислот.
IV тип — болезнь Андерсена (амилопектиноз). Это аутосомно-рецессивное заболевание, характеризующееся дефектом ветвящего фермента гликогена. Болезнь проявляется с первых месяцев жизни и характеризуется гепатосплено-мегалией, развитием цирроза печени, желтухой, гипогликемией. Дефицит ветвящего фермента также обнаруживается в лейкоцитах, мышцах и фибробластах. В связи с малым возрастом больных мышечные симптомы (гипотония, слабость) затушеваны печеночными. Данный тип гликогеноза не поддается лечению. Больные обычно погибают на первом году жизни.
V тип — болезнь Мак-Ардля. Заболевание характеризуется дефицитом фосфорилазы
58
только в мышцах. Наследуется по аутосомно-рецессивному типу. Клиника типична для мышечной формы гликогеноза. При этой патологии поражаются только скелетные мышцы. При тяжелой физической нагрузке могут возникнуть судороги, миоглобинурия, повышение уровня сывороточной креатинфосфатазы. В связи с гликогенной инфильтрацией скелетные мышцы увеличиваются в объеме, становятся очень плотными. Заболевание проявляется в первые десять лет жизни: при физической нагрузке появляются мышечная слабость, мышечные спазмы, тахикардия.
VI тип — болезнь Херса. Заболевание характеризуется отсутствием или недостаточной акивностью гепатоцитарной фосфорилазы. Наследуется по аутосомно-рецессивному типу. Проявляется обычно на первом году жизни. Клиника сходна с течением гликогеноза I типа, но симптоматика выражена в меньшей степени. Характерны значительное увеличение печени в результате гликогенной инфильтрации гепатоцитов, задержка роста, кукольное лицо, гиперлипемия. Больные подвержены гипогликемии, умеренному ацидозу.
12.1.6Особенности развития сахарного диабета у детей
Впопуляции больных СД 6-8 % составляют дети в возрасте до 14 лет. Ежегодный прирост числа детей, больных ИЗСД, составляет до 6 %. До 13 % больных сахарным диабетом детей — младше 5 лет. Наиболее часто в дестоком возрасте развивается ИЗСД.
Вотличие от взрослых сахарный диабет у детей протекает тяжело. Эти особенности обусловлены интенсивностью тех обменных процессов, которые свойственны детству. Потребность в гормонах, обладающих анаболическим действием, у детей очень велика. Инсулину присуще анаболическое действие, значит, и потребность детей в инсулине большая, чем у взрослых.
При назначении инсулина необходимо учитывть, что чувствительность к инсулину у детей выше, чем у взрослых. Кроме этого, у детей содержание большинства из контринсулярных гормонов значительно выше, чем у взрослых. Особенно высоко содержание соматотропного гормона в период физиологического ускоренного роста ребенка: 3-4 года, 7-8 лет и весь пубертатный период. В эти возрастные промежутки и развивается сахарный диабет у детей. Детскому организму свойственна повышенная лабильность нервной системы, особенно симпатической ее части, что приводит к избыточному образованию адреналина, а адреналин, в свою очередь, является причиной бурного распада гликогена в печени и мышцах, что способствует повышению содержания сахара в крови. Избыток контринсулярных гормонов может в значительной мере отягощать уже существующий диагноз сахарного диабета.
Сахарный диабет у детей развивается очень быстро, имеет прогрессирующий характер, который связан с общим развитием и ростом ребенка. В этом состоит его отличие от взрослого диабета. Прогрессирование сахарного диабета заключается в том, что существует большая
вероятность развития лабильного диабета с резкими колебаниями сахара в крови и плохо
59
поддающегося инсулинотерапии. Кроме того, лабильный диабет провоцирует развитие кетоацидоза и приступов гипогликемии. Течение сахарного диабета осложняется еще тем, что дети часто болеют инфекционными заболеваниями, которые способствуют декомпенсации диабета. Чем младше ребенок, заболевший диабетом, тем тяжелее протекает заболевание и тем больше угроза различных осложнений.
Самыми характерными признаками сахарного диабета являются быстрое похудание ребенка, неукротимая жажда и обильное мочеиспускание
12.2. Белковый обмен
Особенностью обменных процессов в детском организме является преобладание анаболических процессов над катаболическими. Растущему организму требуются повышенные нормы поступления питательных веществ, особенно белков. Для детей характерен положительный азотистый баланс. Белки, получаемые за сутки, должны покрывать от 10 до 15% общего калоража пищи; количество их составляет в среднем при грудном вскармливании около 2 г на 1 кг веса в сутки, при искусственном вскармливании 3,5— 5,4 г. Дети дошкольного и школьного возраста должны получать 2,5—3,5 г белков на 1 кг веса.
Увзрослых незаменимыми являются 8 аминокислот, у детей незаменимой аминокислотой до 3 мес. является цистеин, а до 5 лет — и гистидин.
Удетей иное соотношение компонентов остаточного азота, чем у взрослых. Первые 3 мес.
жизни характеризуются наименьшим содержанием в моче мочевины (в 2—3 раза меньше, чем у взрослых) и наибольшей экскрецией мочевой кислоты. Количество мочевины в моче нарастает у детей в возрасте от 3 до 6 месяцев, а содержание мочевой кислоты в это время снижается.
Содержание аммиака в моче детей в первые дни жизни невелико, но затем резко возрастает и держится на высоком уровне на протяжении всего 1-го года жизни.
Белково-калорийная недостаточность у детей протекает значительно тяжелее, чем у взрослых, что связано с большей и постоянно растущей потребностью в белках.
Дети более чувствительны к голоданию, чем взрослые, дефицит питания приводит к частым инфекциям. Длительная недостаточность белка в рационе питания детей первых 3 лет жизни может вызвать необратимые изменения, сохраняющиеся пожизненно.
Квашиоркор
Квашиоркор — заболевание, характеризующееся несбалансированной алиментарной белково-энергетической недостаточностью. Вызывается рационом с избытком калорийных небелковых продуктов (крахмала, сахара), при недостатке белка и незаменимых аминокислот.
Болезнь обычно возникает у детей 1-4 лет.
60
