
3. Поверхностная энергия металлов и соединений
При
достаточно высокой температуре, при
которой
![]() не
является функцией величины поверхности
раздела А, поверхностное натяжение, как
уже упоминалось выше, численно равно
свободной энергии поверхностей
не
является функцией величины поверхности
раздела А, поверхностное натяжение, как
уже упоминалось выше, численно равно
свободной энергии поверхностей
![]() (для
поверхности раздела
твердое — пар).
Так как для твердых тел
(для
поверхности раздела
твердое — пар).
Так как для твердых тел![]() =
=![]() и
при этом
и
при этом![]() и
и![]() практически
не зависят от температуры, то
практически
не зависят от температуры, то![]() и
и![]() можно
определить, измеряя
можно
определить, измеряя![]() как
функцию температуры. При температуре
абсолютного нуля
как
функцию температуры. При температуре
абсолютного нуля![]() ,
так как
,
так как![]()
Поверхностное
натяжение при нескольких температурах
было определено для меди, золота и
серебра. Из этих измерений можно получить![]() и
__
и
__![]() по тангенсу угла наклона прямой линии
и отрезку координаты при температуре
по тангенсу угла наклона прямой линии
и отрезку координаты при температуре![]() Величины
свободной энергии, энтальпии и энтропии
для поверхности
раздела твердое — газ приведены ниже.
Величины
свободной энергии, энтальпии и энтропии
для поверхности
раздела твердое — газ приведены ниже.
Эти
термодинамические величины — средние,
без учета зависимости
![]() от
кристаллографических направлений.
от
кристаллографических направлений.

Можно
попытаться подсчитать![]() ,
используя квазихимическую
теорию. Такое допущение приемлемо, так
как межатомные силы действуют на коротком
расстоянии и можно предположить, что
энергия натяжения поверхности раздела
возникает благодаря тому, что атомы на
поверхности не связаны с таким большим
числом соседних атомов, как атомы внутри
тела.
,
используя квазихимическую
теорию. Такое допущение приемлемо, так
как межатомные силы действуют на коротком
расстоянии и можно предположить, что
энергия натяжения поверхности раздела
возникает благодаря тому, что атомы на
поверхности не связаны с таким большим
числом соседних атомов, как атомы внутри
тела.
Согласно
Херрингу [36], рассмотрим кристалл с
координационным числом Z.
Количество связей в кристалле, содержащем
![]() атомов,
равно
атомов,
равно![]() .
Энергия связи е равна теплоте сублимации
.
Энергия связи е равна теплоте сублимации![]() ,
разделенной на общее количество связей
,
разделенной на общее количество связей
![]() (11.32)
(11.32)
Рассмотрим
кристаллы с решеткой гранецентрированного
куба. Пусть поверхность скола кристалла
образует плоскость (111). Каждый атом на
плоскости (111) связан с шестью соседними
атомами на этой плоскости, тремя атомами
нижней плоскости и с тремя атомами на
верхней плоскости. Поэтому при образовании
поверхности разрываются по три связи
у каждого атома. Однако при раскалывании
образуются две поверхности, так что
число разорванных связей на каждый атом
равно![]() .
Таким образом, энтальпия образования
поверхности на каждый атом равна
.
Таким образом, энтальпия образования
поверхности на каждый атом равна
![]() (11.33)
(11.33)
Если
на плоскости (111) имеется![]() атомов
на
атомов
на![]() ,
то энтальпия образования поверхности
на единицу площади равна
,
то энтальпия образования поверхности
на единицу площади равна
![]() (11.34)
(11.34)
Для
типичных атомов с диаметром около![]() равно
около
равно
около![]() на
на
![]() .
Отсюда величины
.
Отсюда величины![]() для
серебра, золота и меди равны соответственно
[37] 1,14; 1,55 и 1,38
для
серебра, золота и меди равны соответственно
[37] 1,14; 1,55 и 1,38![]()
(1140,
1550 и 1380![]() ).
Эти цифры очень хорошо соответствуют
экспериментальным данным, приведенным
ранее ("стр. 180). Для плоскости (100)
поверхностная энтальпия равна
).
Эти цифры очень хорошо соответствуют
экспериментальным данным, приведенным
ранее ("стр. 180). Для плоскости (100)
поверхностная энтальпия равна
![]() (11.35)
(11.35)
Из этих рассуждений, следует, что величина поверхностной энтальпии для вещества должна быть прямо пропорциональна теплоте сублимации.
Были
определены величины
![]() для
кремния [плоскость(111)], цинка [плоскость
(0001)] и железа, содержащего 3% кремния
[плоскость (100)]. Они равны 1,24; 10,5 и 1,36
для
кремния [плоскость(111)], цинка [плоскость
(0001)] и железа, содержащего 3% кремния
[плоскость (100)]. Они равны 1,24; 10,5 и 1,36![]() (1240, 105 и 1360
(1240, 105 и 1360
![]() )
соответственно. Эксперименты, в результате
которых были получены эти величины,
проводились при низкой температуре.
Так как при этих условиях
)
соответственно. Эксперименты, в результате
которых были получены эти величины,
проводились при низкой температуре.
Так как при этих условиях![]() —небольшая
величина, то величины
—небольшая
величина, то величины![]() близки
близки
![]() .
В соответствии с обсуждавшейся выше
квазихимической теорией у кремния будет
разорвана одна связь, у цинка —три и у
железа— четыре. Подсчитанные отсюда
величины
.
В соответствии с обсуждавшейся выше
квазихимической теорией у кремния будет
разорвана одна связь, у цинка —три и у
железа— четыре. Подсчитанные отсюда
величины
![]() для кремния и цинка составляют 1,31 и 5,1
для кремния и цинка составляют 1,31 и 5,1
![]() (1310
и 510
(1310
и 510
![]() )
соответственно. Расчеты, проведенные
на этой же основе для кристалла железа
с решеткой объемноцентрированного
куба, неверны, так как связи между
ближайшими атомами со второй плоскости
прочны, и, таким образом, рассмотрения
связей только с соседними атомами
недостаточно.
)
соответственно. Расчеты, проведенные
на этой же основе для кристалла железа
с решеткой объемноцентрированного
куба, неверны, так как связи между
ближайшими атомами со второй плоскости
прочны, и, таким образом, рассмотрения
связей только с соседними атомами
недостаточно.
Таблица 14
|
Величины поверхностной свободной энергии для некоторых соединений |
||||
|
|
Плоскость |
|
Литературный источник источник |
|
|
Соединение |
|
|
|
источник |
|
|
|
дж/м2 |
эрг/см2 |
|
|
NaCl |
(100) |
0,3 |
300 |
[38[ |
|
LiF |
(100) |
0,34 |
340 |
[37] |
|
MgO |
(100) |
1,2 |
1200 |
[37] |
|
CaF2 |
(111) |
0,45 |
450 |
[38] |
|
BaF2 |
(111) |
0,28 |
280 |
[37] |
|
СаСОз |
(1010) |
0,23 |
230 |
[37] |
|
|
||||
Величины
поверхностной свободной энергии
известны для очень многих соединений,
некоторые из этих величин приведены в
табл. 14. Эти величины были определены
при низких температурах, и так как
величина
![]() при
этих условиях мала, полученные
значения
при
этих условиях мала, полученные
значения![]() практически
равны
практически
равны![]()
Для кристаллов с ионной связью нельзя говорить о химических связях между атомами, так как силы, удерживающие атомы один около другого, по своей природе являются главным образом кулоновскими. Поэтому удобно придерживаться более общих положений можно было бы, которые, однако, применить и для металлов, и для кристаллов с ковалентной связью.
Рассмотрим
плоскость кристалла, сколотого таким
образом, что образовались две поверхности
раздела. До скалывания энергия
взаимодействия между атомами на плоскости
как функция межатомного расстояния
может быть представлена, как показано
на рис. 88,![]() .
Состояние равновесия соответствует
положению
.
Состояние равновесия соответствует
положению
![]() .
Поверхностная энергия может быть
представлена как работа, необходимая
для того, чтобы удалить атомы на плоскости
один от другого на неопределенное
расстояние. Сила взаимодействия ионов
(рис. 88,
.
Поверхностная энергия может быть
представлена как работа, необходимая
для того, чтобы удалить атомы на плоскости
один от другого на неопределенное
расстояние. Сила взаимодействия ионов
(рис. 88,![]() )
получена путем дифференцирования
данных, приведенных на рис. 88,
)
получена путем дифференцирования
данных, приведенных на рис. 88,![]() [взята
производная
[взята
производная
![]() ].
работа, а, следовательно, и поверхностная
энергия, необходимая для того, чтобы
удалить атомы, находящиеся один от
другого на расстоянии,
].
работа, а, следовательно, и поверхностная
энергия, необходимая для того, чтобы
удалить атомы, находящиеся один от
другого на расстоянии,
 соответствующем
положению равновесия
соответствующем
положению равновесия![]() ,
на неопределенно большое расстояние
,
на неопределенно большое расстояние![]() ,
равна площади, заключенной под кривой,
или
,
равна площади, заключенной под кривой,
или
![]() (11.36)
(11.36)
Для
выполнения интегрирования должно быть
известно уравнение зависимости![]() от
от
![]() .
Для упрощения интегрирования основную
часть кривой можно принять за синусоиду
(пунктирная линия на рис. 88,6). При этом
допущении не учитывается только небольшая
часть площади (от
.
Для упрощения интегрирования основную
часть кривой можно принять за синусоиду
(пунктирная линия на рис. 88,6). При этом
допущении не учитывается только небольшая
часть площади (от![]() до
до
![]() ).
Таким образом, функция зависимости
).
Таким образом, функция зависимости![]() приближенно
выражается уравнением
приближенно
выражается уравнением
![]() (11.37)
Работа
на единицу площади скалывания кристалла
равна
(11.37)
Работа
на единицу площади скалывания кристалла
равна
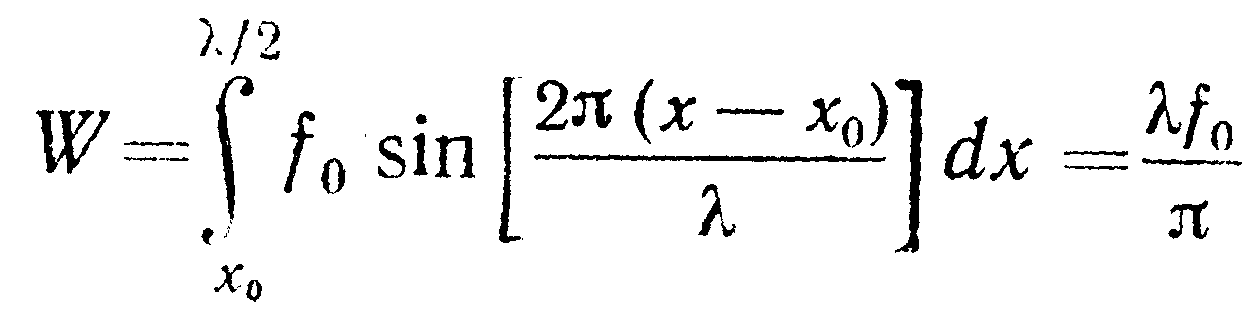 ; (11.38)
; (11.38)
следовательно, для двух поверхностей, которые образуются, работа на единицу площади равна
![]() (11.39)
(11.39)
Для
того чтобы выполнить расчеты, полученное
уравнение необходимо преобразовать,
так как силу
![]() трудно определить прямым измерением.
Вблизи положения х0
действует
закон Гука, согласно которому
трудно определить прямым измерением.
Вблизи положения х0
действует
закон Гука, согласно которому
![]() ,
(11.40)
,
(11.40)
где![]() —
модуль Юнга.
—
модуль Юнга.
Таким-образом, при небольшом скалывающем усилии
![]() (11.41)
(11.41)
Дифференцирование уравнения (11.37) дает
![]() (11.42)
(11.42)
Приравняв уравнения (11.42) и (11.41), получим
 (11.-43)
(11.-43)
В
условиях, для которых выводилось
уравнение для![]() ,
т. е. когда скалывающее усилие небольшое,
,
т. е. когда скалывающее усилие небольшое,
![]() и,
таким образом.
и,
таким образом.
Поэтому![]()
![]() (11.44)
(11.44)
Подставив уравнение (11.44) в уравнение (11.39), получим
![]() (11.45)
(11.45)
Модуль
Юнга для большинства веществ известен,
и поэтому
![]() легко
подсчитать, если значение
легко
подсчитать, если значение![]() может
быть определено. Кроме того, для твердых
тел величина
может
быть определено. Кроме того, для твердых
тел величина
![]() мала,
и отсюда
мала,
и отсюда
![]() ,
а при сравнительно низких температурах
,
а при сравнительно низких температурах![]()
![]()
Так
как экспоненциальный характер атомных
сил проявляется только на коротком
расстоянии,![]() является небольшой величиной и для
расчетов можно принять, что
является небольшой величиной и для
расчетов можно принять, что![]() .
Если ионы удалены
один от другого на такое расстояние, то
силы взаимодействия невелики. Величины
поверхностной энергии веществ,
рассчитанные этим способом, а также
экспериментальные данные представлены
в табл. 15. Экспериментальные данные
хорошо согласуются с теоретическими.
.
Если ионы удалены
один от другого на такое расстояние, то
силы взаимодействия невелики. Величины
поверхностной энергии веществ,
рассчитанные этим способом, а также
экспериментальные данные представлены
в табл. 15. Экспериментальные данные
хорошо согласуются с теоретическими.
Таблица 15
Экспериментальные
и расчетные величины поверхностной
энергии![]() [37]
[37]
|
Кристалл
|
Экспериментальные данные |
Расчетные данные |
||
|
|
|
|
|
|
|
|
дж/м2 |
эрг/смг |
дж/м2 |
эрг/см* |
|
NaCl |
0,3 |
300 |
0,31 |
310 |
|
LiF |
0,34 |
340 |
0,37 |
370 |
|
MgO |
1,2 |
1200 |
1,3 |
1300 |
|
CaF2 |
0,45 |
450 |
0,54 |
540 |
|
BaF2 |
0,28 |
280 |
0,35 |
350 |
|
СаСОз |
0,23 |
230 |
0,38 |
380 |
|
Si |
1,24 |
1240 |
0,89 |
890 |
|
Zn |
0,105 |
105 |
0,185 |
185 |
|
Fe(3%Si) |
1,36 |
1360 |
1,4 |
1400 |
