
2013.Термодинамика / Ферми.ВопросОтвет
.doc1.Что считал Ферми основным содержанием термодинамики?

2.На основе, каких представлений Карно установил ограничения, которые имеют место при превращении теплоты в работу?
Теплота особый вид жидкости, которая переходя от одного тела к другому всегда сохраняется
3.Кто и когда установил эквивалентность теплоты и работы.
Майер открыл эквивалентность теплоты и работы и сформулировал первый закон термодинамики в 1842 году.
4.Какой раздел механики объясняет законы термодинамики?
Статистическая механика.


5.Чем определяется состояние системыв термодинамике?
6.Когда нужно рассматривать поверхность в термодинамике?
Если отношения числа атомов на поверхности к числу атомов в объеме велико.
7. Какие независимые величины связывает между собой уравнение состояния?
![]()
8. Что соответстввует в термодинамике точке на плоскости (P,V)?
(состояние системы)
9.Какие независимые переменные определяею состояние однородного твердого тела.
Пара величин из(объем,температура,тензор напряжения), а при всестороннем сжатии (P,V,T)
10.Какие независимые переменные определяею состояние системы состояжие из химически разных веществ
(P,V,T, {Ci})
11. Как определить состояние гетерогенныъ систем?

12. Нужно ли при задании состояния системы задавать скорости различных частей системы?
13. Как определяет термодинапическое состояние Ферми?

14.Какие состояния являются наиболее важными в термодинамике и каким свойством они обладают?

15. Всегда ли преобразование однородной системы от начального к конечному состоянию может быть изображено на плоскости (P,V)?
Только для квазиравновесного процесса.
16.Дать определения обратимого процесса. Какие начальные и конечные состояния могут связывать обратимые процессы?
Только равновесные состояния.

17. Как осуществить обратимый процесс на практике?

18. Чему равна работа системы при переходе из состояния А в В? Когда возможно геометрическое толкование работы в этом переходе.
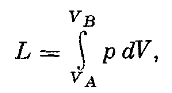
19. Какие процессы наиболее важны?
Циклические процессы.

20. Чему равна работа за цикл, если он может быть изображен на диаграмме (P,V)?
![]()
21. Какой процесс называется изохорным?
![]()

22.Дать определение изобарного и изотермического процесса?
23.Дать определение эмпирической и газовой шкалы температур. В чем преимущество газовой шкалы температур?


24. Выбор единиц абсолютной температуры?
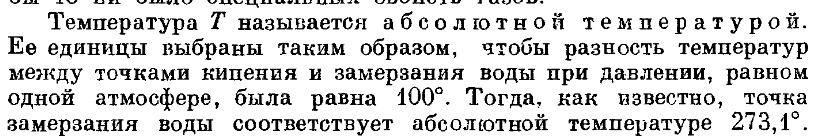
25.Уравнение состояния идеального газа?

26.Какие реальные газы подчиняются уравнению состояния идеального газа?
Никакие.
27. Выразить плотность газа через давление и температуру.
![]()
28. Как выглядит изотермическое превращения идеального газа на диаграмме (P,V)
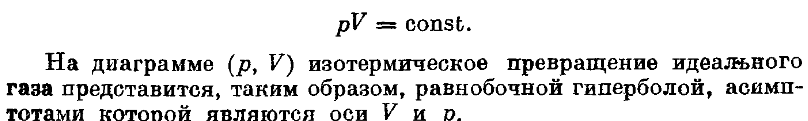
29. Вычислить работу, совершаемую газом при изотермическом расширении ои объема V1 до V2.
![]()
30.Дать определения парциального давления компоненты смеси газов.

31. Сформулировать закон Дальтона.
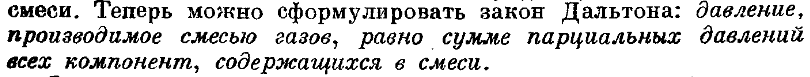
32.Решить задачи

33. Определить стандартное состояние простой системы?
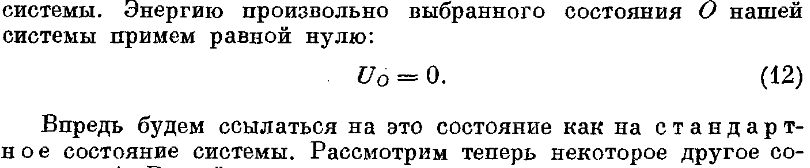
34. Сформулировать эмпирическое определение энергии и записать первый закон термодинамики.
![]() Для
теплоизолированной системы (адиабатической)
Для
теплоизолированной системы (адиабатической)
![]()
ΔU=Q Для изохорной системы
35. Чему равна работа во время циклического процесса?
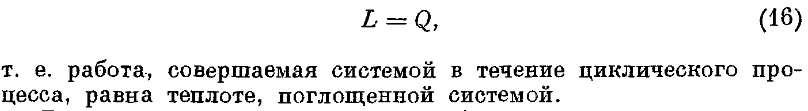

36. Расказать об эксперименте, приводящем к заключению об эквиваленьности теплоты и работы и также об экфивалентности энергии электромагнитного поля и теплоты.
37.Калориметрическаая единица теплоты

38. Соотношение между эргами и калориями
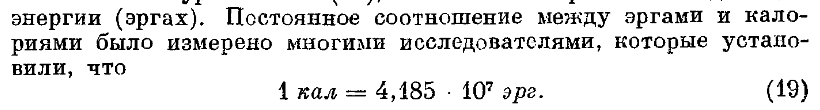
39.Отличаются ли значения
производных
![]() ,
,![]() ?
?
40. Записать первый закон термодинамики в дифференциальной форме, для случаев: a) независимые переменные (V,T) b) независимые переменные (P,T)
![]()
![]()
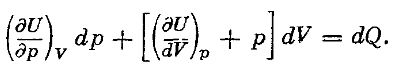
41. Дать определение теплоемкости тела.

42. Одинаковы ли
теплоемкости
![]() .
.
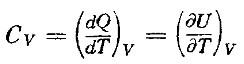 .
.
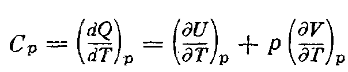
43. Молярные и удельные теплоемкости

44. Функцией каких переменных является внутренняя энергия идеального газа. Экспериментальное доказательство этого поллоожения.
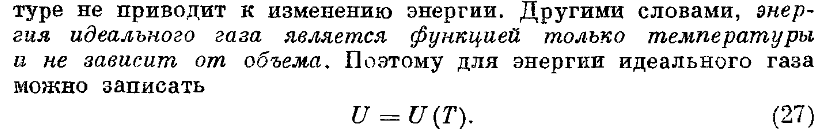
45. Определить вид зависимости внутрееней энергии идеального газа от темпратурры.

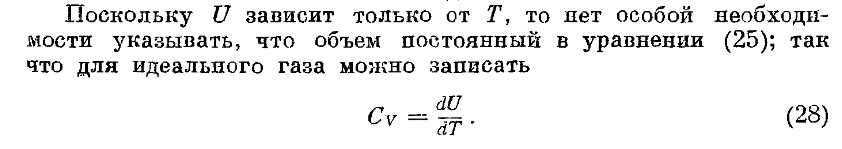
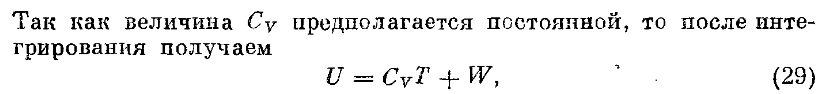
46.Записать первый закон термодинамики в дифференциальной форме в применении к идеальному газу
dU=CVdT=-PdV+δQ
47. Получить соотношение между теплоемкостями для идеального газа
![]() Дифференцируя уравнение
состояния для одного моля получаем
Дифференцируя уравнение
состояния для одного моля получаем
VdP+pdV=RdT
Подставляя его в первый закон термодинамики
![]() получаем
получаем
![]() Поделив на dT
при постоянном давлении получим
Поделив на dT
при постоянном давлении получим
![]()
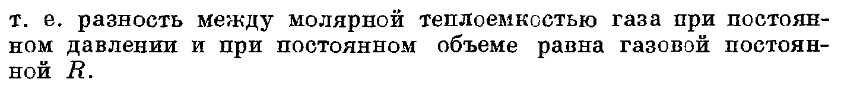
48.Чему равна теплоемкость одноатомного и двухатомных газов из молекулярно кинетической теории

49. Дать определение адиабатического равновесного процесса

50. Получить соотношение между температурой и объемом при адиабатическом прооцессе.
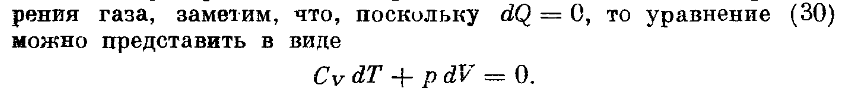
(это первый закон термодинамики) Воспользуемся уравненнием состояния для одного моля
![]()
![]()
![]()
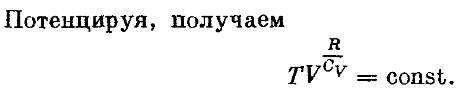
51. Сравнить адиабаты и изотермы на диаграмме (P,V)

52. Накладывает ли первый закон термодинамики какие-либо ограничения на превращения энергии?
Нет.
53. Какую машину назувают вечным двигателем второго рода?
54. Дать определение «источника теплоты».

55. Сформулировать постулат Кельвина

56.Сформулировать постулат Клаузиса
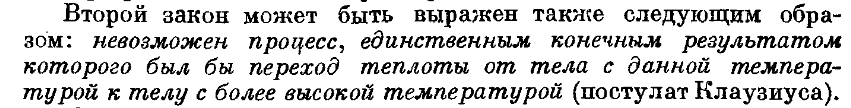

57.Определить цикл Карно

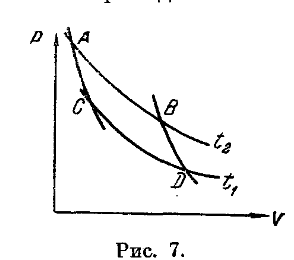
58. Дать определение коэффициента полезного действия
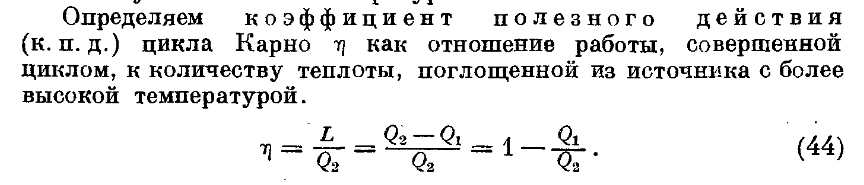
59. Записать коэффициент полезногодействия для обратимых
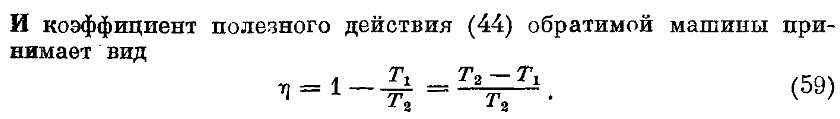
60. Чему равен
циклический интеграл
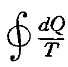 для
обратимого и необратимого циклов
для
обратимого и необратимого циклов
61. Как соотносятся интегралы от точки А до точки В для двух обратимых процессов
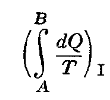 и
и
![]()

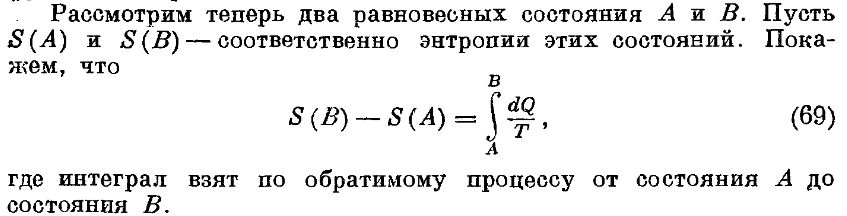


62. С какой точностью определяется энтропии

63. Чему равна энтропия системы,состоящей из отдельных частей

64.
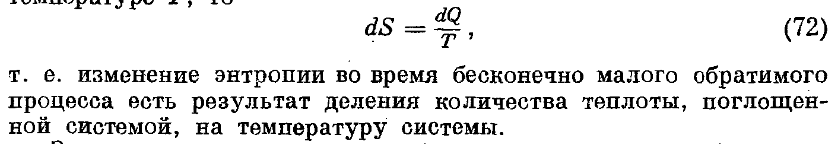
65.Существует ли фунуциональная зависимость между вероятностями состояний и энтропией
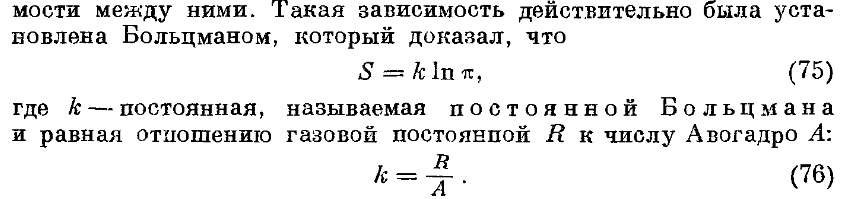
66. Показать на примере идеального газа, что dS является полным дифференциалом
(Ферми стр 59)
67.Показать![]()
![]()
![]()
68.Что называется критической точкой системы (жидкость-пар)
69.Какие области
диаграммы соответствуют жидкости,
насыщенному пару, жидкости– насыщенный
пар, Газ.
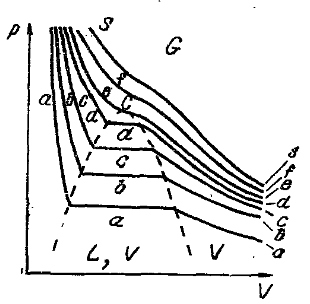
70. Записать уравнений Ван-дер-Ваальса.
71.
![]()
72.Физичесий смысл
выражения![]()

73. Если система динамически изолирована может ли быть увеличина свободная энергия Гельмгольца в результате какого-либо процесса?


73. Записать изохору Вант Гоффа
![]()
74. Дайте определение однородной функции первой степени.
Однородная функция
функция одного или нескольких переменных, удовлетворяющая следующему условию: при одновременном умножении всех аргументов функции на один и тот же (произвольный) множитель значение функции умножается на некоторую степень этого множителя, т. е. для О. ф. f (x, y,..., u) при всех значениях х, у,..., u и любом λ должно иметь место равенство:
f (λx, λу,..., λu) = λnf (х, y,..., u), однородная функция степени n
75.
![]() От
каких переменных зависят эти величины,
если жидкость находится в равновесии
с насыщенным паром.
От
каких переменных зависят эти величины,
если жидкость находится в равновесии
с насыщенным паром.
Это функции одной лишь температуры.
76. Вывести формулу Клайперона для равнофесия жидкость газ с помощью потенциала Гибса.
