
- •ПРЕДИСЛОВИЕ
- •ВВЕДЕНИЕ
- •Часть I. ПРОБОЙ ГАЗОВ
- •Глава 1. Электронные и ионные процессы в газовом разряде
- •1.1. Законы сохранения энергии при столкновении атомных частиц
- •1.2. Интегральные характеристики столкновения
- •1.3. Энергия взаимодействия атомных частиц
- •1.4. Подвижность заряженных частиц
- •1.5. Диффузия заряженных частиц
- •1.6. Возбуждение и ионизация атомов и молекул
- •1.7. Термическая ионизация
- •1.8. О возможности ионизации газа ионами
- •1.9. Рекомбинация заряженных частиц
- •1.10. Термоэлектронная, автоэлектронная, взрывная эмиссия. Фотоэффект на катоде
- •1.11. Элементы кинетического уравнения для электронов
- •Глава 2. Теория пробоя Таунсенда
- •2.1. Первый коэффициент Таунсенда
- •2.2. Прилипание электронов к атомам и молекулам. Отрыв электронов от отрицательных ионов
- •2.3. Второй коэффициент Таунсенда
- •2.4. Электронная лавина
- •2.5. Условие самостоятельности разряда. Закон Пашена
- •2.6. Отступления от закона Пашена
- •2.7. Время разряда
- •Глава 3. Пробой газа в различных частотных диапазонах
- •3.1. СВЧ-пробой
- •3.2. ВЧ-пробой
- •3.3. Оптический пробой
- •Глава 4. Искровой разряд в газах
- •4.1. Наблюдения за развитием разряда в ионизационной камере
- •4.2. Схемы развития лавинно-стримерных процессов
- •4.3. Граница таунсендовского и стримерного разрядов
- •4.4. Пробой газов в наносекундном диапазоне времени
- •4.5. Длинная искра, разряд в виде молнии
- •4.6. Главный разряд
- •Глава 5. Самостоятельные разряды в газах
- •5.1. Тихий разряд
- •5.2. Тлеющий разряд
- •5.3. Дуговой разряд
- •5.4. Коронный разряд
- •5.5. Разряд по поверхности твердого диэлектрика
- •5.6. Зависимость пробивного напряжения газа от межэлектродного расстояния
- •Список литературы к разделу «Пробой газов»
- •Часть II. ПРОБОЙ ТВЕРДЫХ ДИЭЛЕКТРИКОВ
- •Глава 1. Тепловой пробой твердых диэлектриков
- •1.1. Теория теплового пробоя Вагнера
- •1.2. Другие теории теплового пробоя
- •Глава. 2. Классические теории электрического пробоя
- •2.1. Теория Роговского. Разрыв ионной кристаллической решетки
- •2.2. Разрыв твердого диэлектрика по микротрещине. Теория Горовица
- •2.3. Теория А. Ф. Иоффе
- •2.4. Теория А.А. Смурова. Теория электростатической ионизации
- •Глава 3. Квантово-механические теории электрического пробоя неударным механизмом
- •3.1. Теория Зинера. Теория безэлектродного пробоя
- •3.2. Теория Фаулера. Пробой электродного происхождения
- •3.3. Теория Я.И. Френкеля. Теория термической ионизации
- •Глава 4. Теории пробоя твердых диэлектриков вследствие ударной ионизации электронами
- •4.1. Теории Хиппеля и Фрелиха
- •4.2. Теории пробоя, основанные на решении кинетического уравнения. Теория Чуенкова
- •4.3. Некоторые замечания по теориям пробоя, основанных на рассмотрении механизма ударной ионизации электронами
- •Глава 5. Экспериментальные данные, укладывающиеся в представления о пробое твердых диэлектриков ударной ионизацией электронами
- •5.1. Стадии пробоя твердых диэлектриков
- •5.2. Развитие разряда в однородном и неоднородном полях в твердых диэлектриках
- •5.3. Эффект полярности при пробое в неоднородном электрическом поле
- •5.4. Влияние материала электродов на пробой твердых диэлектриков
- •5.5. Зависимость времени разряда от толщины диэлектрика. Формирование многолавинно-стримерного механизма разряда
- •Глава 6. Процессы, наблюдаемые в диэлектриках в области сверхсильных электрических полей
- •6.1. Электрическое упрочнение
- •6.2. Электронные токи в микронных слоях ЩГК в сильных электрических полях
- •6.3. Свечение в микронных слоях ЩГК
- •6.4. Дислокации и трещины в ЩГК перед пробоем
- •Глава 7. Другие теории пробоя твердых диэлектриков
- •7.2. Энергетический анализ электрической прочности твердых диэлектриков по теории Ю.Н. Вершинина
- •7.4. Термофлуктуационная теория разрушения твердых диэлектриков электрическим полем В.С. Дмитревского
- •7.5. Особенности пробоя полимерных диэлектриков. Теория электрического пробоя Артбауэра
- •7.6. Теория электромеханического пробоя Старка и Гартона
- •Глава 8. Некоторые особенности и закономерности электрического пробоя твердых диэлектриков
- •8.1. Статистический характер пробоя твердых диэлектриков
- •8.2. Минимальное пробивное напряжение
- •8.3. Неполный пробой и последовательный пробой
- •8.4. Кристаллографические эффекты при пробое кристаллов
- •8.5. Зависимость электрической прочности от температуры
- •8.6. Зависимость электрической прочности от времени воздействия напряжения
- •8.7. Пробой диэлектрических пленок
- •8.8. Формованные системы металл–диэлектрик–металл (МДМ)
- •8.9. Заключение по механизму электрического пробоя твердых диэлектриков
- •Глава 9. Электрохимический пробой
- •9.1. Электрическое старение органической изоляции
- •9.2. Кратковременное пробивное напряжение
- •9.3. Старение бумажной изоляции
- •9.4. Старение неорганических диэлектриков
- •Список литературы к разделу «Пробой твердых диэлектриков»
- •Часть III. ПРОБОЙ ЖИДКИХ ДИЭЛЕКТРИКОВ
- •Глава 1. Пробой жидкостей высокой степени очистки
- •1.1. Проводимость жидких диэлектриков
- •1.2. Пробой жидкостей вследствие ударной ионизации электронами
- •1.3. Пробой жидкостей неударным механизмом
- •Глава 2. Пробой жидких диэлектриков технической очистки
- •2.1. Влияние влаги
- •2.2. Влияние механических загрязнений
- •2.3. Влияние газовых пузырьков
- •2.4. Теории теплового пробоя жидких диэлектриков
- •2.5. Вольтолизационная теория пробоя жидких диэлектриков
- •2.6. Влияние формы и размеров электродов, их материала, состояния поверхности и расстояния между ними на пробой жидкостей
- •2.7. Развитие разряда и импульсный пробой в жидкостях
- •2.8. Влияние ультразвука на электрическую прочность
- •2.9. Внедрение разряда в твердый диэлектрик, погруженный в изолирующую жидкость
- •Список литературы к разделу «Пробой жидких диэлектриков»
- •ОГЛАВЛЕНИЕ
Часть I. Глава 2.Теория пробоя Таунсенда
Глава 2. Теория пробоя Таунсенда
Многие исследователи, в том числе и русские, занимались экспериментами по пробою газов, но первую теорию газового разряда создал в начале ХХ столетия Таунсенд [1,7]. Вначале он предположил, что электроны, вышедшие из катода, ускоряются электрическим полем и, достигнув необходимой энергии, производят ионизацию атомов и молекул газа. Таунсенд ввел коэффициент α , показывающий, сколько ионизаций производит электрон на пути в 1 см. Впоследствии α был назван первым коэффициентом Таунсенда. Далее, по первому мнению Таунсенда, образовавшиеся в результате ударной ионизации положительные ионы движутся к катоду и тоже производят ударную ионизацию. Такая ионизация может быть оценена коэффициентом ионизации
β .
Однако вскоре экспериментально было показано, что положительные ионы не способны производить ударную ионизацию в слабоионизованной плазме из-за их малой подвижности. Поэтому Таунсенд был вынужден отказаться от указанного механизма. Взамен этого он предположил, что положительные ионы, двигаясь к катоду, бомбардируют его и выбивают электроны, которые, в свою очередь, ускоряясь в электрическом поле, также производят ударную ионизацию. Для учета этого механизма Таунсенд ввел коэффициент γ , который показывает,
сколько электронов выбивает из катода один ион. Этот коэффициент впоследствии был назван вторым коэффициентом Таунсенда [1,4].
2.1. Первый коэффициент Таунсенда
Допустим, из какой-то точки газового разряда вылетает no электронов. Проходя путь х, только n электронов не претерпевают столк-
новений. Тогда dn = −dx / λ . Проинтегрировав это выражение, |
получа- |
ем n / no = e−x / λ . Оказывается, что при x = λи n / no = 0.37 |
, а при |
x =10λ n / no =1 / 2200. |
|
Дальнейшие вычисления для определения α требуют решения кинетического уравнения (о чем говорилось ранее), что сопряжено с определенными трудностями. Таунсенд в свое время сделал упрощенный вывод уравнения для определения коэффициента α . Для этого он сделал три небезупречных предположения:
1.Электрон ионизует только тогда, когда его энергия равна или больше We ≥ Wи .
2.После ионизации электрон полностью теряет свою кинетиче-
скую энергию.
29
Часть I. Глава 2.Теория пробоя Таунсенда
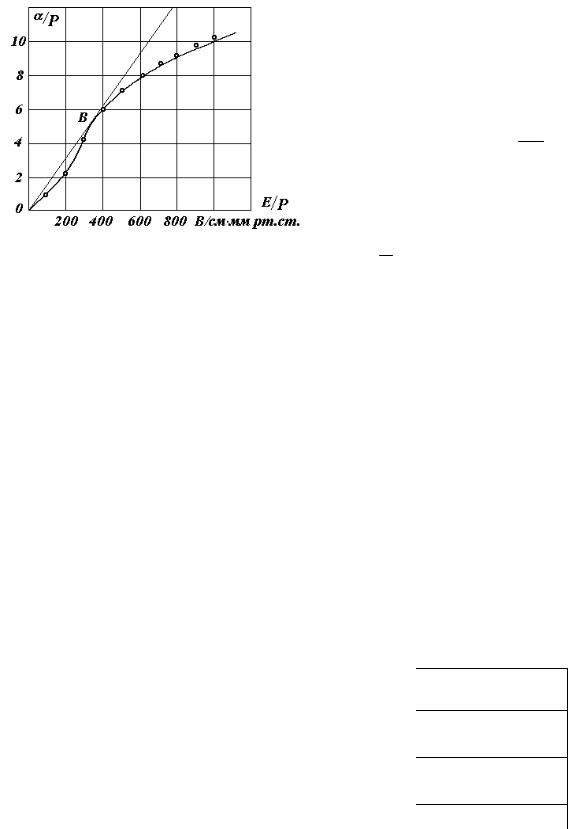
Рис. 2.1. Зависимость α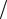 Р = f (Р) для
Р = f (Р) для
воздуха при атмосферном давлении
3. Электрон набирает энергию для ионизации Wи
на пути хи.
Отсюда энергия электрона We = q E xu .
Тогда xu = Wu = Uu , qE E
где Uu называется по-
тенциалом ионизации. Вероятность такого пробега
−xu
ϕ= e λ .
|
|
|
|
|
|
|
|
|
|
|
|
Среднее число столкно- |
||
вений электрона с молекулами газа на пути в 1 см равно |
Z =1 / λ . |
|||||||||||||
Тогда α = Z ϕ = |
1 |
|
e− |
xu |
|
|
|
|
|
|
|
|||
|
λ |
. |
|
|
|
|
|
|
(2.1) |
|||||
λ |
|
|
1 |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||
В п. 1.2 было показано, что |
|
= AP при постоянной температуре. |
||||||||||||
λ |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
Тогда α = APe− |
APUu |
|
|
|
α |
|
= Ae− |
B |
|
|||||
E |
или |
|
E / P |
, |
(2.2) |
|||||||||
|
|
|
|
|
|
|
P |
|
|
|
|
|
||
где А и В – постоянные газа.
Полученная зависимость α / Р = f (E / P) представлена на рис. 2.1.
Экспериментальные данные для α отличаются от результатов расчета по уравнению (2.2). Однако, все же следует, что проведенные опыты подтверждают наличие зависимости α / Р = f (E / P). Значения
констант А и В приведены в табл. 2.1 [4,9].
|
|
|
Таблица 2.1 |
Газ |
А, |
В, |
Е/Р, |
|
В/см см мм рт.ст. |
В/см мм рт.ст. |
В/см мм рт.ст. |
Воздух |
14.6 |
366 |
150÷160 |
Аргон |
13.6 |
235 |
100÷600 |
Углекислота |
20 |
466 |
500÷1000 |
Водород |
5.0 |
130 |
150÷400 |
Гелий |
2.8 |
34 |
20÷150 |
Аналогичные результаты, подтверждающие наличие такой зависимости были получены А.Г. Столетовым еще задолго до появления теории Таунсенда. Согласно его данным, число ионизаций при напря-
30
Часть I. Глава 2.Теория пробоя Таунсенда
жении 1В равно: η =α / qЕ. Обратная величина 1/ η = qЕ / α показыва-
ет, сколько требуется энергии на одну ионизацию. |
Эту величину |
(1 / ηмин ) Таунсенд назвал постоянной Столетова, ей |
соответствует |
точка В на рис. 2.1. |
|
2.2.Прилипание электронов к атомам и молекулам. Отрыв электронов от отрицательных ионов
На развитие ударной ионизации в газах влияют процесс прилипания электронов к атомам и молекулам и обратный процесс – отрыв электрона от отрицательных ионов [6,9]. Вероятность прилипания электронов к атомам зависит от величины электронного сродства Wcp ,
показывающего энергию, выделяющуюся при присоединении к атому электрона. Величина Wcp положительна для электроотрицательных
атомов и отрицательна для атомов нейтральных газов. Данные для Wcp
приведены в табл. 2.2 [17,18].
Таблица 2.2
Атом |
Н |
0 |
F |
Сl |
N |
He |
Ne |
Ar |
|
|
|
|
|
|
|
|
|
Wcp , эВ |
0.75 |
1.46 |
3.45 |
3.61 |
–0.21 |
–0.22 |
–0.22 |
–0.37 |
Чем больше Wcp , тем сильнее связь электрона с атомом. Для ато-
мов нейтральных газов отрицательные ионы отсутствуют. Отрицательные ионы наблюдаются в молекулах O2 , NO2 , NO3 , OH, H2O и др. Наряду с образованием отрицательных ионов происходит отрыв электронов от них. Последний процесс изучен слабее из-за трудности получения большой концентрации отрицательных ионов. В большинстве случаев вероятность образования отрицательных ионов превышает вероятность отрыва электрона от отрицательного иона. Поэтому для коэффициента ударной ионизации можно записать:
αизм =αд −η ,
где αизм – значение по данным измерения, αд – действительное значение,
η – коэффициент, учитывающий прилипание электронов. Для инертных газов αизм =αд.
2.3. Второй коэффициент Таунсенда
Как уже отмечалось, вырывание электронов с катода может происходить также при бомбардировке его положительными ионами. Следует отметить, что положительные ионы, подходящие к металлическо-
31
Часть I. Глава 2.Теория пробоя Таунсенда
му электроду (катоду), могут вызвать эмиссию электронов как за счет упругого взаимодействия ионов с поверхностью катода, так и за счет образования сильного электрического поля вблизи катода [3,6].
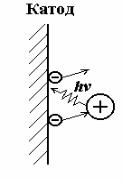
Различают потенциальное вырывание электронов медленными ионами и кинетическое вырывание, когда кинетическая энергия ионов достигает порядка сотен эВ и более. На рис. 2.2 показан механизм потенциального вырывания электронов положительными ионами. Подошедший к катоду ион создает сильное электрическое поле. За счет этого с поверхности катода вырывается электрон, который движется к положительному иону и рекомбинирует с ним. Часть энергии Wи −Wв выделяется в виде
кванта света, под действием которого может произойти вырывание еще одного электрона с поверхности металла. Этот электрон является свободным и определяет эмиссию с катода.
Условие вырывания второго электрона можно записать так: (2.3)
Отсюда Wu ≥ 2Wв . |
(2.4) |
Если просмотреть данные табл. 1.3 и 1.4, то видно, что данное условие соблюдается. Быстрые ионы появляются в газовом разряде в разряженном газе при давлении порядка 1 мм рт.ст. и менее. При этом число вырванных с катода электронов при бомбардировке положительными ионами возрастает.
Кроме этого, имеется еще два механизма вырывания электронов с катода. Первый – это вырывание электронов с катода за счет фотонов, излучаемых электронной лавиной. Второй – вырывание электронов с катода также фотонами за счет диффузии резонансного излучения.
Все три указанных механизма вырывания электронов с поверхности катода пропорциональны количеству ионов в электронной лавине. Поэтому общий вид для коэффициента γ :
γ = γи +γv +γ g , |
(2.5) |
где γu – вырывание электронов положительными ионами электронной лавины, γv – вырывание электронов фотонами, излучаемыми лавиной,
γg – вырывание электронов за счет диффузии резонансного излучения.
Встационарном режиме все составляющие добавляют друг друга. Но при импульсном воздействии напряжения большую роль в развитии
разряда оказывает в основном составляющая γv [3,7].
32
