
- •Задания и методические указания к выполнению практических работ по дисциплине «транспортная энергетика»
- •С о д е р ж а н и е
- •1. Занятие № 1: Анализ основных термодинамических процессов и термодинамических циклов двс
- •1.1. Краткие теоретические сведения
- •1.1.1. Основные понятия и определения
- •Теплоемкости идеального газа
- •1.1.2. Термодинамические процессы с участием идеальных газов Изотермический процесс
- •Изохорный процесс
- •Изобарный процесс
- •Адиабатный процесс
- •Цикл Карно
- •Цикл двигателя внутреннего сгорания с подводом теплоты
- •Цикл двигателя внутреннего сгорания с сообщением теплоты постоянном давлении (цикл Дизеля)
- •Цикл двигателя с сообщением теплоты при постоянных объеме и давлении (смешанный цикл Тринклера)
- •1.2. Примеры и задачи
- •1.2.1. Анализ термодинамических процессов
- •Пример 1: Изотермический процесс
- •Пример 2: Изохорный процесс
- •Пример 3: Изобарный процесс
- •Пример 4: Адиабатный процесс
- •Условие задания
- •Пример 1: Цикл Карно
- •Пример 2: Цикл Отто
- •Пример 3: Цикл Дизеля
- •Пример 4: Цикл Тринклера
- •1.3. Контрольные вопросы
- •2. Занятие №2: Расчет процессов теплопередачи
- •2.1. Краткие теоретические сведения
- •2.2. Примеры и задачи
- •2.3. Контрольные вопросы
- •3. Занятие №3: Расчет процессов горения топлив в двс
- •3.2. Примеры и задачи
- •3.3. Контрольные вопросы:
2.3. Контрольные вопросы
1. Назовите три основные виды теплообмена.
2. Дайте определение теплового потока.
3. Объясните механизм обмена энергии в процессе теплопроводности.
4. Дайте определение конвективного теплообмена.
5. Объясните процесс теплового излучения.
6. Как определить тепловой поток через стенку?
7. Назовите виды процесса конвенции. Объясните их механизм действия.
8. Назовите основные критерии подобия. В чем их физический смысл?
9. Какая схема лежит в основе процесса лучистого теплообмена?
10. Объясните понятие «степень черноты тела».
11. Что такое теплопередача? Приведите пример сложного теплообмена.
12. Как определить сопротивление теплопередачи через многослойную стенку?
3. Занятие №3: Расчет процессов горения топлив в двс
Цель и задачи занятия - формирование у студентов знаний и умений применения теоретических основ теории горения для практического проведения расчетов сжигания топлив в двигателях внутреннего сгорания
Количество часов, отводимых на занятие – 2 часа.
Краткие теоретические сведения
Свойства жидких топлив
|
Топливо |
Элементный (средний) состав 1 кг топлива |
Молекулярная масса μТ, кг/кмоль |
QH, кДж/кмоль | ||
|
С |
О |
N | |||
|
Автомобильный бензин |
0,855 |
0,145 |
- |
110 – 120 |
44000 |
|
Дизельное |
0,870 |
0,126 |
0,004 |
180 – 200 |
42500 |
|
Дизельное моторное |
0,870 |
0,125 |
0,005 |
220 – 280 |
41800 |
Сгорание топлива представляет собой химическое соединение составных элементов топлива с кислородом:
С+О2=СО2, 2Н2+О2=2Н2О, (3.1)
при неполном сгорании углерода:
2С+О2= 2СО. (3.2)
Для полного сгорания 1 кг топлива (состав С+Н+О= 1) требуется количество кислорода:
в киломолях
![]() (3.3)
(3.3)
в килограммах
![]() (3.4)
(3.4)
В окружающем воздухе кислорода по массе содержится примерно 23 %, а по объему 21 %. Поэтому количество воздуха, которое теоретически необходимо для сгорания топлива массой 1 кг и состава С + Н + О= 1, выражают стехиометрическим соотношением, кмоль,
![]()
![]() (3.5)
(3.5)
или, кг
![]()
![]() (3.6)
(3.6)
Кажущаяся молекулярная масса воздуха μВ= 29 кг/кмоль, следовательно,
m0= μВМ0= 29М0. (3.7)
Отношение количества воздуха m, действительно поступающего в цилиндр двигателя, к теоретически необходимому количествуm0называется коэффициентом избытка воздуха α:
![]() ,
или
,
или![]() .
(3.8)
.
(3.8)
Если α < 1 (недостаток кислорода), смесь называют богатой, при α > 1 (избыток кислорода) смесь называют бедной.
При полном сгорании 1 кг топлива в двигателях с искровым зажиганием общее количество горючей смеси, кмоль, состоящей из паров топлива и воздуха,
![]() ,
(3.9)
,
(3.9)
где μТ- молекулярная масса топлива (см. табл.1).
В дизелях из-за малого объема, занимаемого жидким топливом, величиной 1/μТ можно пренебречь, поэтому
МТ= αМ0. (3.10)
При полном сгорании жидкого топлива (α > 1) продукты сгорания состоят из образовавшихся в результате реакции СО2,Н2О, избыточного кислорода и азота. Количество отдельных составляющих продуктов сгорания, кмоль, определяется по следующим формулам:
![]() ;
(3.11)
;
(3.11)
![]() ;
(3.12)
;
(3.12)
![]() ,
(3.13)
,
(3.13)
где 0,21α М0- количество поступившего кислорода, кмоль; 0,21М0– количество кислорода, принявшего участие в реакции, кмоль.
MN2= 0,79 αМ0.
Общее количество продуктов сгорания МПС, кмоль, отнесенное к 1 кг топлива:
![]() .
.
Подставляя в это выражение значения,
![]() ,
получим:
,
получим:
![]()
Для стехиометрического состава смеси (α = 1):
![]() .
(3.14)
.
(3.14)
Для значения α > 1 количество, кмоль, продуктов сгорания с учетом избыточного азота ΔΜN2 = 0,79(α – 1)M0 и избыточного кислорода ΔΜО2 = 0,21(α – 1)M0 в продуктах сгорания определится:
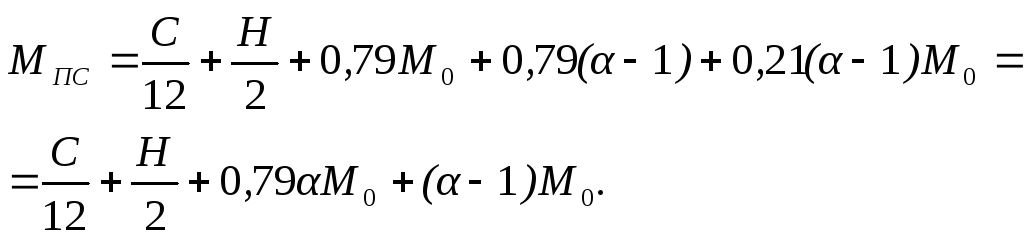 (3.15)
(3.15)
Масса продуктов сгорания GПС, кг, при сгорании 1 кг жидкого топлива
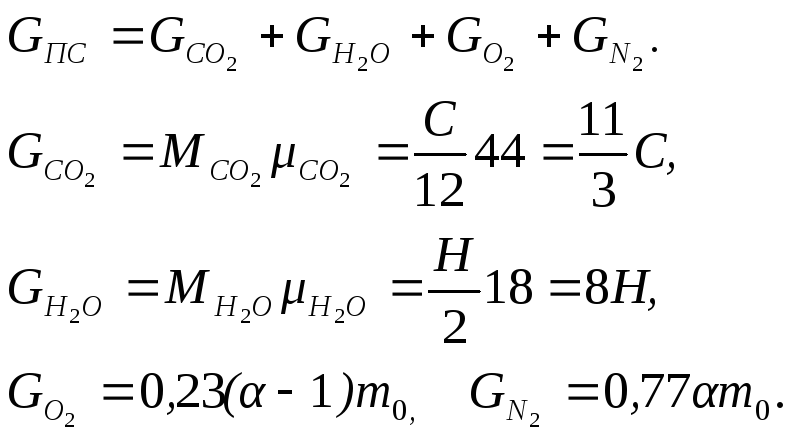
Тогда
![]() (3.16)
(3.16)
При неполном сгорании жидкого топлива (α < 1) из-за недостатка кислорода часть углерода топлива сгорает в окись углерода, а часть водорода не реагирует с кислородом.
Эксперименты показывают, что отношение числа молей водорода к окиси углерода примерно постоянно для данного топлива и не зависит от величины α. Обозначим это отношение через К.
![]() (3.17)
(3.17)
Согласно опытным данным для бензинов, у которых Н/С= 0,17 – 0,19,К= 0,45 – 0,50, а приН/С= 0,13,К= 0,30.
Вследствие неполноты сгорания топлива выделившееся количество теплоты уменьшается на доли не выделившейся теплоты находящихся в продуктах сгорания окиси углерода водорода (ΔQН)CO и (ΔQН)Н2. Суммарную долю не выделившейся теплоты (ΔQН)хим= (ΔQН)CO+ (ΔQН)Н2можно подсчитать по уравнению, Дж/кг
(ΔQН)хим= А(1 –α)М0, (3.18)
где А =114· 106приК= 0,5 – 0,45 и А = 116·106приК= 0,3.
Опуская промежуточные выкладки, запишем выражение для компонентов, входящих в состав продуктов сгорания в случае α < 1. Количество каждого компонента, кмоль, определяется по следующим формулам:
![]() (3.19)
(3.19)
![]() (3.20)
(3.20)
![]() (3.21)
(3.21)
![]() (3.22)
(3.22)
![]() (3.23)
(3.23)
В то время как массы, кг, продуктов сгорания и горючей смеси до сгорания одинаковы (GПС=GT), количество молей продуктов сгорания и количество молей горючей смеси до сгорания неравны. Изменение количества молей смеси (ΔМ) при сгорании происходит вследствие изменения числа молекул газообразных продуктов сгорания по сравнению с числом молекул горючей смеси до сгорания, т.е. ΔМ=МПС–МТ.
Изменение количества молей принято выражать относительной величиной - теоретическим коэффициентом молекулярного изменения
![]() (3.24)
(3.24)
Для бензиновых двигателей с искровым зажиганием
 (3.25)
(3.25)
 (3.26)
(3.26)
Для дизелей (α > 1)
![]() . (3.27)
. (3.27)
