
МЕТОДИЧЕСКОЕ ПОСОБИЕ- Орг. химия-Часть 2
.pdf
|
|
|
O |
|
|
|
|
|
O |
CH |
3 |
|
C |
+ C H OH |
|
HCl + CH3 |
|
C |
|
|
|
|
|||||||
|
|
||||||||
|
|
Cl |
2 |
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
OC2H5 |
|
уксусноэтиловый сложный эфир, этилацетат, этилэтаноат
в) аммонолиз хлорангидрида или ацетилирование аммиака
|
|
O |
|
|
|
|
O |
CH3 |
|
C + 2NH3 |
|
CH3 |
|
C |
+ NH4Cl |
|
|
||||||
|
|
|
|||||
|
|
Cl |
|
|
|
|
NH2 |
ацетамид, этанамид, амид уксусной кислоты
г)
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
|
|
O |
CH3 |
C |
уксусный |
||
CH3 |
|
C |
+ CH3 |
|
C |
|
AgCl + |
|
O |
|
|
|
|
|
ангидрид |
||||||
|
|
Cl |
|
|
OAg |
CH3 |
|
C |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
O |
|
– В результате отщепления воды от двух молекул кислоты также образуются ангидриды кислот
CH3 |
|
O |
|
|
|
|
|
O |
|
C |
|
CH3 |
|
|
C |
||
|
|
|
|
|||||
|
|
|||||||
|
|
OH |
|
|
|
|
|
O + H2O |
|
|
OH |
|
|
|
|
|
|
|
|
|
CH3 |
|
|
C |
||
CH3 |
|
C |
|
|
|
|||
|
|
|
|
|
|
O |
||
|
|
O |
|
ангидрид |
||||
|
|
|
уксусной кислоты |
|||||
или ангидрид этановой кислоты
Таким путём ангидриды получаются лишь в очень жёстких условиях: или в присутствии сильных водоотнимающих средств (Р2О5), или в присутствии катализаторов (Al2O3) при высоких температурах. Обычно их синтезируют действием галогенангидридов на соли кислот
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
O |
|
CH3 |
|
C |
|||
|
|
|
|
||||||||
CH3 |
|
C |
+ CH3 |
|
C |
|
|
|
|
|
O + NaCl |
|
|
|
|
|
|
|
|||||
|
|
|
ONa |
Cl |
|
CH3 |
|
|
C |
||
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
O |
11

Ангидрид могут образовывать и две различные кислоты.
Ангидриды кислот – вещества весьма активные:
с водой они дают соответствующие кислоты
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
CH3 |
|
C |
|
|
|
|
|
|
O |
||||
|
|
|
|
|
|
|
|
O + H2O |
|
|
|
2 CH3 |
|
C |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
CH3 |
|
C |
|
|
|
|
|
|
OH |
||||
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
, |
|||||
со спиртами и аммиаком образуют смеси кислот со сложными |
|||||||||||||||||||
эфирами и амидами соответственно. |
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
C |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|||||
|
|
|
|
|
|
O + C H OH |
|
|
|
|
CH3 |
|
C |
|
+ CH COOH |
||||
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
2 |
5 |
|
|
|
|
|
|
|
|
|
3 |
|
CH3 |
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
OC2H5 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
C |
+ NH3 |
|
|
|
|
|
|
|
O |
|
+ CH3COOH |
||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
O |
|
|
CH3 |
|
|
C |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
CH |
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
NH2 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O
Ангидриды кислот являются хорошими ацилирующими средствами. Однако половина молекулы ангидрида не ацилирует, а выделяется в виде кислоты.
– Амиды кислот. Их обычно получают через галогенангидриды и ангидриды кислот (см. выше). В промышленности амиды синтезируют действием аммиака на кислоты
|
|
O |
|
|
O |
CH3 |
|
C + NH |
3 |
|
CH3 C |
|
|
||||
|
|
OH |
|
ONH4 |
|
|
|
|
|
аммонийная соль уксусной кислоты
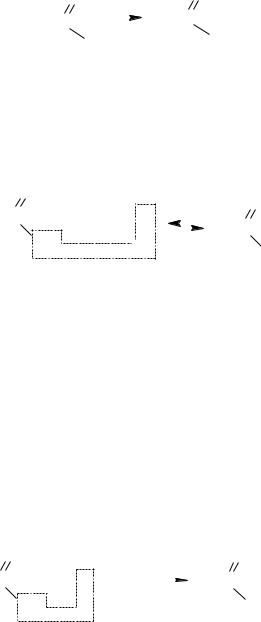
При сухой перегонке аммонийная соль выделяет воду с образованием амида
|
|
O |
|
|
O |
|
CH3 |
|
C |
|
H O + CH3 |
|
C |
|
|
|
||||
|
||||||
|
|
|||||
|
|
ONH4 |
2 |
|
NH2 |
|
|
|
|
|
|||
|
|
|
|
ацетамид |
||
12
Ацетамид по номенклатуре ИЮПАК будет называться этанамидом. При ацилировании аминов получаются алкил- и диалкиламиды,
имеющие промышленное значение.
|
|
|
O |
|
|
|
O |
+ СH3NH2 |
. HCl |
2 СH3NH2 |
+ R |
|
C |
|
R |
|
C |
||
|
|
|
|||||||
|
|||||||||
|
|
|
Cl |
|
|
|
NHCH3 |
|
|
|
|
|
|
|
метиламид |
|
|
||
|
|
|
|
|
|
кислоты |
|
|
|
– Сложные эфиры можно получать прямым взаимодействием кислоты со спиртом, т.е. реакцией этерификации кислот спиртами в присутствии кислого катализатора
|
|
|
O |
R'OH |
|
|
|
|
|
O |
|
R |
|
C |
+ |
|
|
|
|
|
|||
|
|
|
R |
|
C |
+ H2O |
|||||
|
|
|
|
||||||||
|
|
|
OH |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
OR' |
|
|
|
|
|
|
|
|
|
|
|
|
|
Эта реакция давно интересовала химиков. В 1862 году Бертло установил, что реакция обратима и равновесие наступает, когда прореагирует примерно по 2/3 моля исходных веществ. В конце ХIХ века Н. А. и Н. Б. Меншуткины обнаружили, что скорость реакции этерификации зависит от строения кислоты и спирта. Было установлено, что скорость этерификации падает при увеличении числа и объёма радикалов при α-углеродном атоме по отношению к карбоксилу. Этот факт, очевидно, объясняется экранированием углеродного атома карбоксила замещающими радикалами.
С помощью меченых атомов (изотоп кислорода О18) было показано, что вода при этерификации образуется за счёт гидроксила кислоты и водорода спирта
|
|
|
O |
|
|
|
|
O |
||
R |
|
C |
+ HO18 |
|
R` |
|
R |
|
C |
+ H2O |
|
|
|
|
|||||||
|
|
|
OH |
|
|
|
|
O18 − R' |
||
Названия сложных эфиров по тривиальной номенклатуре строятся по следующей схеме: название радикала спирта плюс название кислотного радикала, в котором окончание -ил заменено на -ат. По номенклатуре ИЮПАК: название радикала спирта плюс название кислоты, в котором окончание -овая заменено на -оат.
13
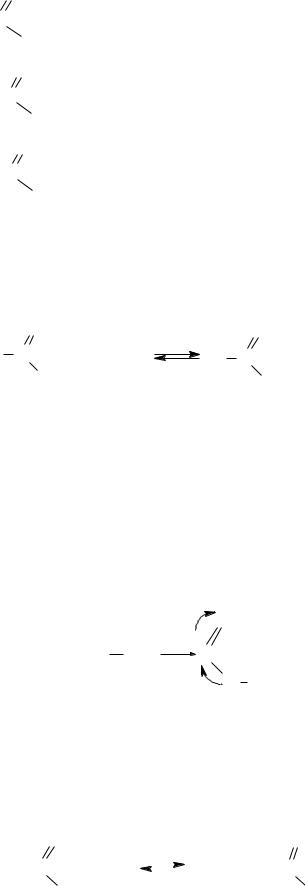
|
|
|
|
|
|
O |
метилформиат, метилметаноат |
H |
|
|
|
C |
|||
|
|
|
|||||
|
|
|
|
|
|
OCH3 |
|
|
|
|
|
|
|
O |
этилацетат, этилэтаноат |
CH3 |
|
|
|
|
C |
||
|
|
|
|||||
|
|
|
|
|
|
OC2H5 |
|
|
|
|
|
|
|
O |
бутилпропионат, бутилпропаноат |
C2H5 |
|
|
|
C |
|||
|
|
|
|||||
|
|
|
|
|
|
OC4H9 |
|
Как показано выше, сложные эфиры можно также получать взаимодействием спиртов с ангидридами и галогенангидридами кислот.
В реакции со спиртами сложные эфиры способны обмениваться с ними радикалами. Эта реакция называется переэтерификацией.
|
O |
|
O |
R C |
+ R"OH |
R C |
+ R'OH |
|
OR' |
|
OR" |
– Галогензамещенные кислоты
Хотя в карбоксильной группе наблюдается значительное смещение электронной плотности к кислороду, углеродный атом карбоксила обладает не столь большим положительным зарядом, как углерод карбонила в кетонах и альдегидах. Это обусловлено частичной нейтрализацией электронной ненасыщенности углерода смещением электронов от гидроксила
|
δ − |
|
R αСН2 |
O |
|
δ +C .. |
H |
|
|
O |
|
|
.. |
|
И всё же карбоксил оказывает влияние на соединённый с ним углеводородный радикал, оттягивая на себя электронную плотность и повышая активность водородных атомов, прежде всего у α-углерода.
Прямое хлорирование и бромирование карбоновых кислот происходит на свету с вступлением галогенов в α-положение.
|
|
|
|
|
O |
|
|
|
|
|
O |
|
R |
|
CH2 |
|
C |
+ Cl2 |
|
R |
|
CHCl |
|
C |
+ HCl |
|
|
|
|
|
||||||||
|
|
|
|
|
||||||||
|
|
|
|
|
OH |
|
|
|
|
|
|
OH |
14
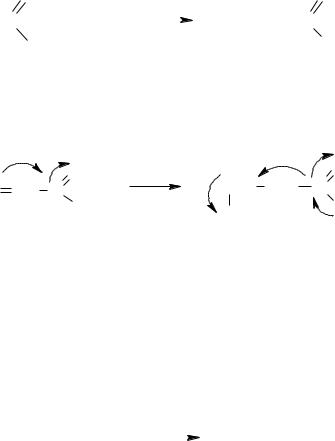
Обычным же способом синтеза α-галогензамещённых кислот является метод Гелль-Фольганд-Зелинского, заключающийся в действии на карбоновую кислоту молекулярного хлора или брома в присутствии фосфора
|
|
|
|
|
O |
|
|
|
|
|
|
O |
3R |
|
CH2 |
|
C |
+ P + 11Br |
|
3R |
|
CHBr |
|
C |
+ HPO3 + 5HBr |
|
|
|
|
|
||||||||
|
|
|
|
|
OH |
|
|
|
|
|
|
Br |
Другой метод синтеза, приводящий к β-галогензамещенным кислотам, заключается в гидрохлорировании α,β-ненасыщенных
карбоновых кислот
|
|
δ + |
δ − |
δ + δ − |
|
O |
δ + |
δ − |
O |
HCl |
CH2 |
||
H C |
CH |
C |
|
|
CH2 C |
|
2 |
|
|
ОН |
|
Cl |
ОН |
акриловая |
|
|||||
|
β |
- хлорпропионовая |
||||
кислота |
|
|||||
|
|
|
кислота |
|||
|
|
|
|
|
|
|
Присоединение НCl протекает вопреки правилу Марковникова изза смещения электронной плотности по системе сопряжения молекулы к кислороду и в соответствии с зарядами атомов.
Действие галогеноводородных кислот на гидроксикислоты
также приводит к желаемому результату
HO |
|
CH2 |
|
CH2 |
|
COOH |
HCl |
CH2Cl |
|
CH2 |
|
COOH |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|||||||
|
|
гидракриловая |
|
β - хлорпропионовая |
||||||||
Замещение α-водорода галогеном значительно повышает силу кислоты. Галоген сильно оттягивает электронную пару от α-углерода, обнажая его положительный заряд. Он, в свою очередь, через углерод карбоксила притягивает к себе электроны гидроксильной группы. Таким образом, посредством индукционного эффекта, протон гидроксила активируется. Подобная картина, правда, менее выражено, наблюдается и при удалении галогена от карбоксила.
При замене водорода в радикале кислоты на I, Br, Cl, F, а также увеличении числа атомов галогена, последовательно увеличивается сила и константы диссоциации кислот (К).
15

|
|
|
|
Например: |
К·105 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
К·105 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH3 |
|
|
|
COOH |
1,75 |
CH2F |
|
|
|
COOH |
|
|
|
5700 |
|||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
CH2F |
|
|
|
|
COOH |
200 |
CF3 |
|
|
|
COOH |
|
|
|
|
|
|
50000 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
CH2Cl |
|
|
|
|
COOH |
150 |
CH3 |
|
|
|
CH2 |
CHCl |
|
|
COOH |
140 |
|||||||||
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||
CH2Br |
|
|
|
COOH |
150 |
CH3 |
|
CHCl |
|
|
CH2 |
|
|
|
COOH |
9 |
|||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||
CH2I |
|
|
COOH |
75 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Галогенкислоты благодаря большой активности нашли широкое применение.
Отдельные представители
Муравьиная кислота – жидкость с tкип = 100,8 °C и резким запахом. При попадании на кожу вызывает ожоги.
В промышленности её получают из оксида углерода и едкого натра
CO + NaOH |
125 - 1500C |
H |
|
|
C |
|
ONa |
||||||||||||
|
|
|
|||||||||||||||||
5 - 10 ат |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
2 H |
|
C |
|
ONa + H2SO4 |
|
|
|
|
2 H |
|
C |
|
OH + Na2SO4 |
||||||
|
|
|
|
|
|
|
|
||||||||||||
O
Муравьиная кислота занимает особое место в ряду кислот. Наряду с карбоксилом в ней может быть выделена и альдегидная группа.
H C  OH
OH
O 
Поэтому, обладая всеми свойствами кислот, она вступает в реакции окисления: серебряного зеркала, с фелинговой жидкостью, – т.е. в типично альдегидные реакции.
Муравьиная кислота используется для дезинфекции в медицине и промышленности, при крашении тканей, в ряде синтезов.
Уксусная кислота
Безводная уксусная кислота при температуре +16,6 °С застывает и называется поэтому ледяной. tкип.= 118,5 °С.
Получают её гидратацией ацетилена, окислением этилового спирта и предельных углеводородов, уксуснокислым брожением сахаристых веществ и другими методами.
В химическом отношении – это обычная карбоновая кислота.
16

Применяется как прекрасный растворитель, в кожевенном производстве, лакокрасочной, пищевой, химической и других отраслях промышленности. Причём расходуется в больших количествах.
Высшие жирные кислоты
Наиболее известны пальмитиновая С15Н31СООН и стеариновая С17Н35СООН кислоты. Эти кислоты имеют молекулы с нормальной цепочкой углеродных атомов. Их получают при омылении жиров и каталитическим окислением парафинов.
Соли этих кислот – мыла. Натриевые и калиевые соли этих кислот хорошо растворимы в воде и хорошо «мылятся». Соли магния, кальция, бария и др. (соли жёсткости) плохо растворяются в воде. Поэтому в жёсткой воде обычные мыла переходят в нерастворимое состояние и не «мылятся».
Для изготовления свечей используют твердую смесь высших жирных кислот – стеарин.
5.1.2 Одноосновные ненасыщенные кислоты
К ряду ненасыщенных карбоновых кислот можно отнести
следующие: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
H2C |
|
|
|
|
CH |
|
|
|
COOH |
|
|
|
|
|
акриловая, пропеновая |
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
H2C |
|
|
|
|
CH |
|
|
|
CH2 |
|
|
COOH |
|
|
|
|
|
винилуксусная, бутен-3-овая |
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
CH3 |
|
|
CH |
|
|
|
CH |
|
|
|
COOH |
|
|
|
|
|
кротоновая, бутен-2-овая |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
H2C |
|
|
|
|
C |
|
|
COOH |
|
|
|
|
|
метакриловая, 2-метилпропеновая |
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(CH2)7 |
|
|
|
COOH |
||||||||||||||||||||||||||||||
CH3 |
|
|
|
|
(CH2)7 |
|
|
|
|
CH |
|
|
|
CH |
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
олеиновая, октадецен-9-овая |
||||||||||||||||||
CH3 |
|
|
(CH2)4 |
|
|
CH |
|
CH |
|
CH2 |
|
CH |
|
CH |
|
(CH2)7 |
|
COOH |
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
линолевая, октадекадиен-9,12-овая |
||||||||||||||||||
CH3 |
|
|
CH2 |
|
CH |
|
CH |
|
CH2 |
|
CH |
|
CH |
|
CH2 |
|
CH |
|
CH |
|
(CH2)7 |
|
COOH |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
линолевая, |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
октадекатриен-9,12,15- овая |
||||||||||||||||||
CH3 (CH2)4 CH CH CH2 CH
CH CH2 CH CH CH2 CH
CH CH2 CH CH CH2 CH
CH CH2 CH CH (CH2)3 COOH
CH (CH2)3 COOH
|
|
|
арахидоновая, |
HC |
|
C COOH |
эйкозатетраен-5,8,10,13-овая |
|
Про пропиоловая, пропиновая |
||
|
|||
|
|||
|
Необходимо отметить, что кислоты типа
O
C C C
C C
OH
17

с сопряжёнными двойными связями (карбонильной и этиленовой) обычно называют α,β-ненасыщенными кислотами. Они резко отличаются по способам получения и свойствам от кислот с изолированными двойными связями.
Кпоследним относятся олеиновая, линолевая, линоленовая, арахидоновая кислоты, остатки которых входят в состав молекул жиров.
Кα,β–ненасыщенным кислотам, относятся акриловая и метакриловая кислоты.
Акриловая кислота – жидкость с резким запахом, tкип.= 140 °С. В промышленности получают из этилена или ацетилена
H2C |
|
|
CH2 |
|
|
|
O2 |
CH2 |
|
|
|
CH2 |
HCN |
|
HO |
|
CH2 |
|
CH2 |
|
CN |
|
+H2O |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
Ag+1 |
|
О |
|
|
|
|
|
t |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
нитрил |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
β − гидроксипропионовой |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислоты |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
H2C |
|
CH |
|
C |
|
|
|
+ NH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
HC |
|
|
CH |
|
|
|
HCN |
|
H2C |
|
|
CH |
|
|
CN |
2 H2O |
|
NH3 + H2C |
|
|
CH |
|
COOH |
||||||||||||||
|
|
|
Cu2(CN)2 |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
акрилонитрил |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
В промышленности в основном используются производные акриловой кислоты, прежде всего, сложные эфиры кислоты. Например, метиловый эфир – метилакрилат – легко полимеризуется и используется, поэтому в производстве органического стекла и других полимеров.
Акриловая кислота и соответствующий ей альдегид, акролеин, образующиеся в небольших количествах при длительном нагревании растительных масел (приготовление олифы, чипсов), оказывает негативное воздействие на живой организм.
Кротоновая кислота
Эта кислота существует в форме двух геометрических изомеров: цис-изомер называют изокротоновой, транс-изомер – кротоновой кислотой.
H |
|
|
H |
H |
|
|
COOH |
H3C C |
|
C |
COOH |
H3C C |
|
C |
H |
|
|
||||||
|
|
||||||
|
|||||||
изокротоновая |
кротоновая |
||||||
18

Кротоновая кислота является энергетически более устойчивой формой по сравнению с изокротоновой.
Из высших ненасыщенных кислот наибольшее значение имеет олеиновая кислота. Она также представлена цис- и транс-изомерами. Причём транс-форма, называемая эландиновой кислотой, на 32,2 кДж∙моль-1 устойчивее цис-олеиновой кислоты.
H |
|
(CH2)7− COOH |
H |
|
H |
C |
|
C |
C |
|
C |
|
|
||||
|
|
||||
CH3− (CH2)7 |
|
H |
CH3− (CH2)7 |
|
(CH2)7− COOH |
транс− |
|
цис− |
|||
Щелочные соли олеиновой кислоты являются мылами и используются в технике, остатки цис-олеиновой кислоты входят в состав молекул жиров.
5.1.3 Двухосновные насыщенные кислоты
Примерами предельных двухосновных кислот могут служить:
O |
C |
|
|
|
|
C |
O |
|
щавелевая, |
|||||||||||||||
HO |
|
|
|
|
OH |
|
этандиовая (дикарбоновая) |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
HOOC |
|
|
|
|
CH2 |
|
|
|
COOH |
|
малоновая, пропандиовая |
|||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
HOOC |
|
|
|
|
CH2 |
|
|
|
|
CH2 |
|
|
COOH |
|
янтарная, бутандиовая |
|||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
HOOC |
|
|
|
|
CH |
|
|
|
COOH |
|
метилмалоновая, |
|||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
метилпропандиовая |
|
|
|
|
|
|
CH3 |
|
|
|
|
|
COOH |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
HOOC |
|
|
|
(CH2)3 |
|
|
глутаровая, пентандиовая |
|||||||||||||||||
|
|
|
|
|||||||||||||||||||||
HOOC |
|
|
|
|
CH2 |
|
|
|
|
CH2 |
|
CH2 |
|
CH2 |
|
COOH адипиновая, гександиовая |
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
и т.д. |
Кислоты этого ряда являются кристаллическими веществами, хорошо растворимыми в воде. Также как и в ряду одноосновных кислот, температуры плавления двухосновных кислот с чётным числом углеродных атомов выше температур плавления. соседних гомологов с нечётным числом углеродов.
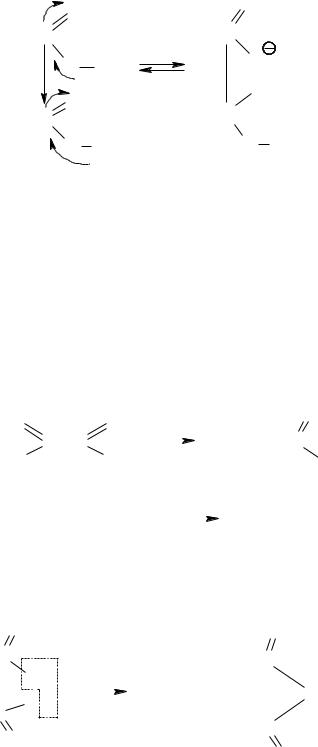
Константа диссоциации первого карбоксила из-за мощного взаимного влияния карбоксильных групп выше, чем у одноосновных кислот.
19
δ −
δ + |
O |
HC |
|
|
O H |
|
δ − |
δ + HC O |
|
|
O H |
O
C
H
OH |
+ H |
Е |
O |
|
|
|
|
C
H
O H
В то же время константа диссоциации второго карбоксила ниже, чем у монокарбоновых кислот, вследствие большого (+2) отрицательного заряда иона, удерживающего протон.
Двухосновные кислоты имеют те же химические свойства, что и монокарбоновые, только в реакции могут вступать два карбоксила. Вместе с тем присутствие в молекуле сразу двух карбоксилов обуславливает и некоторые особенности в их химическом поведении.
Например, щавелевая и малоновая кислоты при нагревании выше температуры плавления разлагаются с отщеплением в виде диоксида углерода одного карбоксила
O |
|
|
|
|
|
O |
|
|
|
|
O |
||||
C |
|
C |
CO2 |
+ H |
|
C |
|||||||||
HO |
|
|
|
|
|
||||||||||
|
OH |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
OH |
|||||
HOOC |
|
CH2 |
|
COOH |
|
|
CO2 + CH3 |
|
COOH |
||||||
|
|
|
|
|
|||||||||||
Янтарная и глутаровая кислоты способны к внутримолекулярному отщеплению воды при нагревании. В результате получаются внутренние ангидриды
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
CH2 |
|
|
C |
OH |
3000C |
CH2 |
|
|
C |
ангидрид |
|
|
|
|
||||||||||
|
|
|
|
|
||||||||
|
|
|||||||||||
|
|
|
|
|
H2O + |
|
|
|
|
|||
|
|
|
C |
OH |
|
|
|
|
|
O янтарной |
||
|
|
|
|
|
|
|
||||||
CH2 |
|
|
|
|
|
|
|
кислоты |
||||
|
O |
|
CH2 |
|
|
C |
||||||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
При пиролизе кальциевых солей адипиновой кислоты и некоторых её гомологов происходит образование циклических кетонов.
20
