
МЕТОДИЧЕСКОЕ ПОСОБИЕ- Орг. химия-Часть 2
.pdf
кислот и оснований. Поэтому его можно сульфировать и нитровать непосредственно кислотами. При гидрировании пиразола образуется пиразолин, а затем и пиразолидин:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
N |
|
|
|
NH |
|||||
|
|
|
|
|
|
|
|
||||||||
|
N |
|
|
N |
|
|
N |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
H |
|
|
H |
||||||||
Пиразолин легко окисляется. Его оксопроизводное, пиразолон, лежит в основе получения многих лекарственных препаратов.
H2C |
|
|
CH |
4 |
|
|
3 |
|
|
H3C |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
HC |
|
|
|
C |
CH |
N |
|
|
|
C |
|
|
C |
|
|
CH3 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
H3C |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
C |
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
O |
|
C |
|
|
2 N |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
1 |
|
|
O |
|
|
C |
|
|
N |
|
CH3 |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
N |
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
C6H5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C6H5 |
|
|
|||||||||
|
пиразолон |
1-фенил-2,3-диметил- |
|
|
|
пирамидон |
|
|
|||||||||||||||||||||||||
|
пиразолон-5 |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
антипирин
(жаропонижающее)
Тиазол
HC |
|
N |
|||||||
|
|||||||||
HC |
|
|
|
|
|
|
|
|
|
|
|
|
CH |
||||||
|
|
|
|
|
S |
||||
Ядро тиазола входит в состав многих природных соединений. При гидрировании тиазол даёт тиазолидин.
H2C |
|
NH |
||
|
||||
|
|
|
|
|
H2C |
|
CH2 |
||
|
|
S |
||
Первым открытым и практически используемым антибиотиком, который используется для лечения бактериальных инфекционных заболеваний, является пенициллин. Пенициллин является производным тиазолидина
HOOC |
|
CH |
|
N |
|
|
|
C |
|
|
O |
||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
H3C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
C |
|
CH |
|
CH |
|
|
NH |
|
C |
|
R |
||||||||
|
|
|
|
|
|
|
|
||||||||||||||
H3C |
S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||||||
Известны пять пенициллинов, различающихся радикалами R.
111
13.2 Шестичленные гетероциклические соединения
Пиридин
Пиридин – простейшее шестичленное азотсодержащее гетероциклическое соединение, обладающее ярко выраженным ароматическим характером.
|
|
γ |
|
|
|
|
|
|
CH |
|
|
|
|
β ` HC |
5 |
4 |
3 |
|
|
CHβ |
|
|
|
|
|||
|
6 |
1 |
2 |
|
|
|
α ` HC |
|
CHα |
||||
|
|
N |
|
|
|
|
Основным источником пиридина является каменноугольная смола (≤ 0,1 %). Пиридин извлекают из неё водными растворами кислот и выделяют затем обработкой щёлочью. Большие потребности в пиридине и его гомологах обусловили развитие синтетических методов их получения. Наиболее развитым из них является синтез пиколина (β-метилпиридина) из акролеина и аммиака.
|
|
|
|
|
|
|
|
|
|
CH |
|
|
||
|
|
|
|
O |
|
|
|
HC |
|
C |
|
CH3 |
||
|
|
|
|
|
|
|
|
|
||||||
2CH2 |
|
CH |
|
C |
+ NH3 |
|
|
|
|
|
|
|
|
+ 2H2O |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
H |
|
|
|
HC |
CH |
|||||
|
|
|
|
|
|
|
|
|
|
N |
пиколин |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Пиридин |
имеет |
сильный |
неприятный |
запах. |
tкип.= 115 °С, |
|||||||||
tпл.= –38 °С. Смешивается с водой в любых соотношениях.
Химические свойства
Измерения электронной дифракции показало, что молекула пиридина плоская и представляет собой почти правильный шестиугольник. Это явная аналогия с бензолом – пиридин является ароматическим соединением. Ниже указаны длины связей (в нм) и распределение электронной плотности по различным положениям цикла пиридина: на углеродах цикла эти плотности меньше единицы.
|
0 |
|
|
|
|
|
, |
|
|
|
|
|
1 |
|
|
|
|
|
|
3 |
|||
|
|
|
9 |
||
1200C |
|
|
|
931 |
|
|
|
||||
|
|
|
|
|
,0 |
|
|
|
|
|
|
|
|
|
7 |
||
N |
0 |
3 |
|||
|
1 |
|
|||
|
, |
|
|
|
|
|
0,822 |
|
5 |
4 |
3 |
|
||
|
|
|
6 |
1 |
2 |
|
|
|
|
N |
|
|
1,586 |
|
0,947
0,849
112
У бензола соответствующие плотности больше и равны единице. Поэтому пиридин менее реакционноспособен в реакциях электрофильного замещения (атакующая частица положительна), чем бензол, и легче бензола вступает в реакции нуклеофильного замещения. Из-за неравномерности распределения электронов положения 2,4,6
более удобны для атаки нуклеофильных, а положения 3 и 5 – электрофильных реагентов. Сильно повышенная эленктронная плотность на азоте свидетельствует об основных свойствах пиридина (способности его присоединять и удерживать протон).
Реакции электрофильного замещения
–При низких температурах галогены присоединяются к пиридину
собразованием N-галогенидов, которые при нагревании превращаются
в β-галогенпиридины.
|
|
|
+ |
|
|
|
CH |
|
CH |
|
CH |
CH |
CH |
CH |
CH |
CH |
C Cl |
|
+ Cl2 |
|
Cl− |
|
+ HCl |
CH |
CH |
CH |
CH |
CH |
CH |
|
N |
|
N |
|
N |
Cl
– Сульфирование и нитрование кислотами требует жёстких условий. Так, пиридин-3-сульфокислота образуется при нагревании пиридина с дымящей H2SO4 до температуры 220 °С в течении суток и в присутствии, кроме того, катализатора – сульфата ртути.
|
SO3H |
+ HOSO3H |
+ H2O |
N |
N |
– Нитрование идёт при температуре 300 °С раствором нитрата калия в смеси концентрированных азотной и серной кислот и в присутствии железного катализатора
|
3000C |
|
|
NO |
|
|
|
||
+ HNO3 |
|
2 |
||
|
|
|
+ H2O |
|
Fe |
|
|
||
|
|
|
||
N  N
N 3-нитропиридин
3-нитропиридин
113
Реакции нуклеофильного замещения
– При нагревании пиридина с амидом натрия образуется α-аминопиридин
+ NaNH2 |
+ H2 |
+H2O |
+ NaOH |
|
|||
N |
NH2Na |
|
NH2 |
N |
|
N |
– При контакте паров пиридина с сухим КОН получается α-гидроксипиридин
+ KOH |
+ H2 |
+H2O |
+ KOH |
|
|||
N |
OK |
|
OH |
N |
|
N |
Реакции пиридина как третичного амина
Пиридин и его гомологи – слабые основания: константа
основности пиридина kосновн.=1,7·10-9 (у анилина kосновн. =4,0·10-10) Поэтому они легко дают соли с сильными кислотами.
|
+ |
|
|
+ HCl |
− |
5 5 Ч |
|
или C H N HCl |
|||
|
Cl |
||
N |
N |
|
H
С галоидными алкилами пиридин даёт галогеналкилаты, при нагревании которых происходит изомеризация с перемещением радикала в положения 2 или 4.
|
+ |
+ |
+ RX |
X− нагревание |
X− |
N |
N |
R |
N |
||
|
R |
H |
Отдельные представители
Пиридин используется в качестве растворителя и катализатора, как мягкое органическое основание.
114
α-Винилпиридин
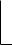 CH
CH CH2 N
CH2 N
используется как сополимер с дивинилом при производстве специальных видов каучуков.
Пиперидин может быть получен при каталитическом гидрировании пиридина.
|
|
|
|
|
CH2 |
||
|
|
H |
H2C |
|
|
CH2 |
|
|
|||||||
|
2 |
|
|
|
|
|
|
|
|
Ni |
|
|
|
|
|
|
|
H2C |
|
|
CH2 |
||
|
|||||||
N |
|
|
N |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
||
По аналогии с циклогексаном кольцо пиперидина имеет креслообразную форму. В химическом отношении ведёт себя как вторичный амин. Кольцо пиперидина входит в состав многих алкалоидов.
Никотиновая кислота (β-пиридинкарбоновая кислота)
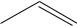
 C
C O OH
O OH
N
По химическим свойствам подобна кислотам бензольного ряда. Никотиновая кислота содержится в печени, молоке, экстракте дрожжей.
Никотиновая кислота и ее амид под названием витамина РР
используется для витаминизации хлеба и других пищевых продуктов. Витамин РР предохраняют животных и человека от заболевания пеллагрой (сухость кожи, изъязвление языка, поражение центральной нервной системы). Потребность в ней человека – 20…30 мг в сутки.
Кониин, никотин, анабазин
Эти три соединения являются алкалоидами. Алкалоиды – это особая группа азотистых органических соединений основного характера и сложного состава. Алкалоиды содержатся в растениях и часто обладают сильным физиологическим и фармакологическим действием. Большинство алкалоидов обладает оптической активностью.
Кониин, или 2-пропилпиперидин, содержится в болиголове.
115
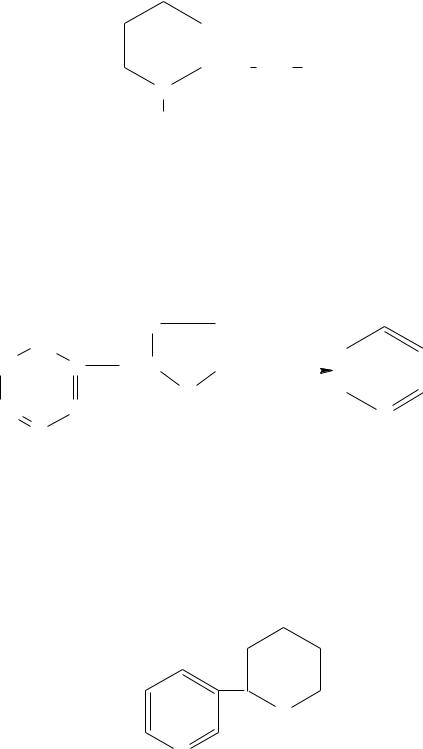
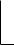 CH2 CH2 CH3 N
CH2 CH2 CH3 N
H
Маслообразная жидкость вращает плоскость поляризации влево. Чрезвычайно ядовит, вызывает паралич двигательных нервных
окончаний.
Никотин, или 3-[2-(N-метилпирролидин)] пиридин, находится в листьях и корнях табака. Окислением никотина получают никотиновую кислоту.
5 6
CH
CH
CH
4
1 N
3
2
C
CH
3 H2C
H2C
2
|
|
4 |
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
COOH |
|
|
|
5 |
[O] |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
1 |
CH2 |
|
|
|
|
|
|||
|
|
|
|
|
|
||||
|
|
|
|
|
|
||||
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
||||
|
|
|
|
|
|
|
|||
CH3 |
|
|
|
||||||
Небольшие количества никотина возбуждают нервную систему, большие – вызывают паралич дыхательных центров. Смертельная разовая доза для человека ~ 40 мг.
Никотин в больших количествах используется как инсектицид для борьбы с вредителями сельского хозяйства.
Анабазин, или 2-(3-пиридил)-пиперидин является изомером никотина. Очень ядовит и обладает высоким инсектицидным действием.
N
N
Хинолин
Хинолин, или бензопиридин, является аналогом нафталина, в котором одна группа –СН– в замещена атомом азота.
116
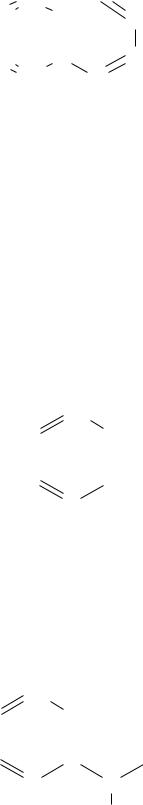
6 7
CH |
CH |
C |
|||
5 |
|||||
|
|
|
|
||
|
|
|
|||
|
|
|
|
||
CH CH C |
|||||
|
|
8 |
|
|
|
γ
CH  4
4
1 N
3CH β
2CH α
Хинолин впервые выделен из продуктов перегонки каменноугольной смолы.
Электрофильные заместители атакуют бензольную часть молекулы, нуклеофильные – пиридиновую. Это факт становится понятным в связи с тем, что электронная плотность на углеродах в бензоле выше, чем в пиридине. Хинолин, как и пиридин, слабое основание. Он вступает в соответствующие основаниям реакции.
Хинолин и его замещённые используются в производстве лекарственных препаратов и красителей.
Пиримидин
|
|
4 |
|
|
|
N |
CH 5 |
||||
|
CH |
||||
3 |
|
|
|
|
|
|
|
|
|
|
|
HC |
|
|
|
|
CH |
2 |
N |
6 |
|||
|
|
|
|||
|
|
1 |
|
|
|
В химическом отношении сходен с пиридином. Имеет ароматический характер. Благодаря электронной плотности двух атомов азота является более сильным основанием по сравнению с пиридином.
Пурин
|
|
CH |
|
|
|
|
||
N |
C |
|
N |
|||||
|
||||||||
|
|
|
|
|
|
|
|
|
HC |
|
|
C |
|
|
CH |
||
|
|
N |
N |
|||||
H
Пурин представляет собой конденсированную систему пиримидина имидазола. Обладает ароматическими свойствами, амфотерен.
117
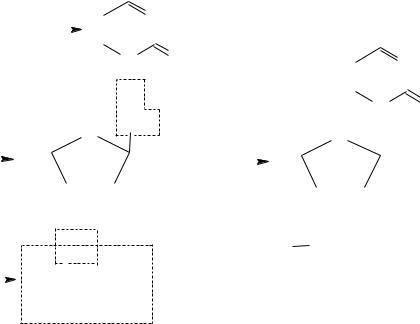
Нуклеиновые гетероциклические основания (агликоны)
Известно, что главную роль в процессах синтеза белка и передачи наследственной информации играют нуклеиновые кислоты. Нуклеиновые кислоты – это биополимеры, макромолекулы которых состоят из
многократно повторяющихся звеньев – нуклеотидов.
В состав нуклеотида – структурного звена нуклеиновых кислот –
входят три составные части:
1)Азотистое основание – пиримидиновое или пуриновое. В нуклеиновых кислотах содержатся основания 4-х разных видов: два из них относятся к классу пуринов и два – к классу пиримидинов. Азот, содержащийся в циклах, придает молекулам основные свойства.
2)Моносахарид – рибоза или 2-дезоксирибоза. В зависимости от вида моносахарида, присутствующего в нуклеотиде, различают два вида нуклеиновых кислот – рибонуклеиновые кислоты (РНК), которые содержат остатки рибозы, и дезоксирибонуклеиновые кислоты (ДНК), содержащие остатки дизоксирибозы.
3)Остаток фосфорной кислоты. Нуклеиновые кислоты являются
кислотами потому, что в их молекулах содержится остаток фосфорной кислоты.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Азотистое |
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
NH2 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
основание |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
N |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N O |
|||||
Моносахарид: |
|
|
ОН |
|
|
|
CH2 |
|
|
|
|
|
|
ОН |
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
O |
ОН |
|
CH |
O |
|
|
||||||||||||||||||||||||
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
рибоза (R=ОН) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ферменты |
|
2 |
|
|||||||||||||||
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- 2H2O |
|
|
|
|
|
|
|
|
|
|
|||
дезоксирибоза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(R=Н) |
|
|
|
|
|
|
|
|
О |
|
|
|
|
R |
|
|
|
|
|
|
|
О |
|
|
R |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О |
|
H |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
P |
|
|
||||||||||||
Фосфорная |
|
|
|
|
|
|
|
|
ОН |
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
О |
|
|
H |
|
|
|
|
|
|
|
О |
|
|
|
|
|
|
||||
|
|
|
|
HO |
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
Нуклетид |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
О |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Молекула ДНК человека – носитель генетической информации, которая записана в виде последовательности нуклеотидов с помощью генетического кода. В результате репликации ДНК происходит передача генов ДНК от поколения к поколению.
118
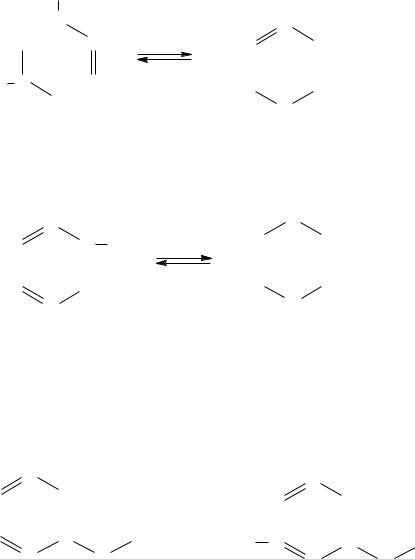
Пиримидиновые основания:
NH2
C
N CH
CH
HO C CH
 N
N
|
|
|
|
OH |
|||
|
|
|
|
|
|
||
|
|
|
|
C |
|||
|
|
N |
|
C CH3 |
|||
HO |
|
|
|
|
|
|
|
|
C |
|
CH |
||||
|
|
||||||
|
|
|
|
N |
|||
Пуриновые основания:
|
|
|
NH2 |
аденин |
||||||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
||
|
|
C |
|
|
|
|
|
|||
N |
|
C |
|
|
N |
|||||
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
HC |
|
|
|
C |
|
|
|
CH |
||
|
|
N |
N |
|||||||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
H |
||||
|
|
|
|
|
NH2 |
||
|
|
|
|
|
|
||
|
|
|
|
C |
|||
|
|
N |
|
CH |
|||
O |
|
|
|
|
|
|
цитозин |
|
C |
|
|
|
CH |
||
|
|
|
|
||||
|
|
|
|
||||
|
|
|
|
N |
|||
|
|
|
|
|
|
||
|
|
|
|
H |
|||
|
|
|
|
O |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
C |
CH3 |
|
|||||
|
HN |
|
|
C |
|
|
тимин |
||||
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
CH |
|
|
||||||
|
|
|
|
||||||||
|
|
|
|
||||||||
|
|
|
|
N |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
H |
|
|
|||||
|
OH |
|
|
|
гуанин |
||||
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
N |
C |
|
|
N |
|||||
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
H2N C |
C |
|
|
|
CH |
||||
|
N |
|
|
N |
|||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
H |
||||
14 ТЕРПЕНЫ
Терпе́нами называют углеводороды – продукты биосинтеза общей формулы (C5H8)n, с углеродным скелетом, формально являющимся производным изопрена СН2=С(СН3)-СН=СН2. В больших количествах терпены содержатся в хвойных растениях, во многих эфирных маслах. Терпены – основной компонент смол и бальзамов, Например, скипидар получают из живицы деревьев хвойных пород. Эфирные масла обнаруживаются в различных частях растений: корне, стволе, листьях, цветах, плодах. Они имеют сильный приятный запах, что и обуславливает их применение.
119

Кислородные производные терпенов обычно называют терпеноидами.
По своим физическим свойствам терпены – это бесцветные жидкости, нерастворимые в воде и легче её. Кипят при температурах от 140 до 190 °С.
Терпены классифицируют по числу изопреновых звеньев, образующих углеродный скелет молекулы:
∙Монотерпены (терпены) C10H16,
∙Сесквитерпены (полуторатерпены) C15H24,
∙Дитерпены C20H32, (C10H16)2 ,
∙Тритерпены, C30H48, (C10H16)3 ,
∙Тетратерпены C40H64, (C10H16)4 ,
∙Политерпены (C5H8)n, где n > 8.
Они могут быть алифатическими и моно-, би- и трициклическими
Алифатические терпены и терпеноиды
К ним можно отнести мирцен и гераниол.
Мирцен (2-метил-6-метиленоктадиен-2,7) содержится в масле хмеля
CH3 C CH CH2 CH2 C CH
CH CH2 CH2 C CH CH2OH
CH2OH
CH3 CH2
Гераниол (транс-3,7-диметилоктадиен-2,7-ол-1) содержится как главная составная часть в эфирном масле листьев герани и обуславливает их запах. Содержится он также в розовом масле.
CH3 |
|
C |
|
CH |
|
CH2 |
|
CH2 |
|
C |
|
CH |
|
CH2OH |
||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
CH3 |
||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|||||
Алифатические терпены, как и вообще терпены, построены по так называемому «изопреновому правилу»: молекулу каждого соединения можно разделить (мысленно) на 2 скелетных остатка изопрена. Натуральный каучук в этом смысле является политерпеном.
Моноциклические терпены и терпеноиды
Ментол, терпенеол, лимонен
Этот ряд соединений называют ментановыми терпенами, так как их можно рассматривать как производные ментана (1-изопропил-4- метилциклогексан). Сам ментан в природе не встречается, но его спирт – ментол, составляет главную часть мятного масла. При восстановлении ментол даёт ментан, при окислении – ментон (входит в мятное масло).
120
