
Основы ССХ, пороки (Бокерия Л.А
.).pdfВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА
теза простагландинов, приводящая к закрытию протока в 88-90% случаев при внутривен ном введении препарата в течение 2-3-х дней.
В 1968 г. W. Porstmann предложил катетеризационный метод закрытия ОАП. Данный метод эндоваскулярнои эмболизации ОАП нашел широкое распространение при закрытии протоков малых размеров [58]. В настоящее время накапливается материал и по эндоско пическому клиппированию ОАП. Операция выполняется с помощью торакоскопической техники через 3 или 4 отверстия диаметром не более 5-6 мм, произведенных в третьемчетвертом межреберьях по передней, средней и задней подмышечным линиям [33, 65].
Первая успешная операция перевязки ОАП выполнена R. Gross в 1938 г., пересечение протока - в 1944 г. В пашей стране успешная операция впервые была проведена А. Н. Ба кулевым в 1948 г.
ОАП закрывают путём перевязки его двойной лигатурой либо его пересечением с после дующим ушиванием обоих концов. Промежуточное положение занимает метод прошива ния протока танталовыми скрепками аппаратом УАП-20. В настоящее время большинство хирургов применяют перевязку протока двойной лигатурой. Эта методика проста, сравни тельно безопасна и даёт надежные результаты.
В НЦССХ им. А. Н. Бакулева РАМН применяют заднебоковой доступ по третьему межреберью. Над аортой продольно рассекают париетальную плевру до устья подключичной артерии и вниз i m 2 см ниже протока. На медиальный край плевры накладывают держалки и отводят их вправо. С плеврой отводят в сторону возвратный нерв. Освобождается область протока. Затем тупым и острым путями выделяют верхнюю и нижнюю ямки. С помощью зажима Федорова под проток проводят две шелковые лигатуры (шелк №8) и на фоне сниженного АД до 80 мм рт. ст. перевязывают сначала аортальный, а затем легочный концы протока, стараясь оставить меж ду ними промежуток. Дрожание на ЛА исчезает Ушивают над аортой париетальную плевру. Ра ну грудной клетки послойно ушивают с оставлением дренажа в плевральной полости.
Закрытие ОАП при наличии высокой Л Г требует широкого, но щадящего хирургического доступа, в значительной степени обеспечивающего успех операции. Необ ходимым условием является мобилизация аорты выше и ниже протока и взятие её на дер жалки. Осторожно выделяют заднюю и боковые поверхности аорты, чтобы не повредить грудной лимфатический проток. Под контролем зрения под проток проводят лигатуры. Пе ред завязыванием снижают АД до 75-80 мм рт. ст. или на короткое время пережимают аор ту. Однако при наличии широкого и короткого протока у больных с ЛГ перевязка протока бывает недостаточна. В таких случаях показано пересечение протока. Для этого помимо аорты выделяют ещё и ЛЛА. Оба сосуда пристеночно отжимают, проток пересекают, затем непрерывным швом ушивают дефекты в стенках сосудов. При выраженном кальцинозе протока A. Morrow, W. Clark (1966 г.) рекомендуют оперировать в условиях ИК из левосто роннего доступа, закрывая проток заплатой со стороны просвета аорты [55].
Отдаленные резилыпаты хирургического лечения ОАП показывают, что свое временная операция позволяет добиться полного выздоровления [54]. У больных с высокой ЛГ полной нормализации гемодинамики, как правило, не наступает (кроме младенцев), повидимому, за счет наличия склеротических изменений в отдельных легочных сосудах. Одна ко значительное улучшение показателей внутрисердечной гемодинамики и функционально го состояния сосудов МКК свидетельствует об эффективности хирургического лечения.
Следует отметить и такой факт, что у ряда больных наблюдается повышение давления в МКК в отдаленные сроки после операции при адекватной коррекции порока. По-видимо му, прогрессирует склероз легочных сосудов.
Процесс клинической реабилитации в основном проходит в течение первого года, но у больных с высокой Л Г он более длительный.
У всех больных с ЛГ склеротической формы в отдаленные сроки после операции сохра няется высокая ЛГ, обусловленная дегенеративными изменениями легочных сосудов, ка чество жизни не улучшается.
- а -
ДЕФЕКТ АОРТОЛЕГОЧНОИ ПЕРЕГОРОДКИ
Л. Р. ПЛОТНИКОВА
ш
Дефект аор то лег очной перегородки - внутриперикардиальное сообщение между восходящей аортой и легочной артерией (ЛА). Порок редкий - 0,2-0,3% случаев всех врожденных пороков сердца (ВПС). Впервые данная аномалия описана Elliotson в 1830 г.
Эмбр иология. В возникновении дефекта аортолегочной перегородки ведущая роль принадлежит остановке роста и отсутствию развития аортолегочной перегородки [61]. Разделение примитивного, или эмбрионального, артериального ствола на восходящую аорту и легочный ствол осуществляется за счет образования первичной артериальной пе регородки, которая возникает дистально, и проксимально - за счет роста трункальной пе регородки (между 6-7 неделями внутриутробной жизни). В случае нарушения этого про цесса возникает дефект аортолегочной перегородки.
Пато лого -анатомически ми критериями этого порока являются наличие сооб щения мелсду смелшыми отделами восходящей аорты и легочного ствола; присутствие двух обособленных фиброзных колец аортального и легочного клапанов со сформирован ными выводными отделами соответствующих л^елудочков. Форма, расположение и разме ры дефектов могут быть различны.
ВНЦССХ им. А. Н. Бакулева РАМН принята следующая классификация порока [9]*:
1.Дефект находится в средней части аортолегочной перегородки на достаточном рас стоянии от синусов Вальсальвы и имеет выраженные края. ПЛА и ЛЛА отходят нор мально и дистальнее верхнего края дефекта.
2.Собственно аортолегочное окно, распололсепное непосредственно над синусами Вальсальвы.
3.Дефект располол^сн в дистальной части аортолегочной перегородки, вдали от сину сов Вальсальвы. Проксимальная часть перегородки частично сформирована. Ветви ЛА отходят в области вершины дефекта.
4.Дефект расположен дистально и захватывает область отхождения ПЛА так, что вос ходящая аорта сообщается как с ЛА, так и с ПЛА.
5.Полностью отсутствует аортолегочная перегородка, ветви ЛА отходят от задней стенки общего сосуда, но клапаны аорты и ЛА развиты нормально. Наличие послед него фактора и отсутствие ДМЖП позволяет дифференцировать данный порок от общего артериального ствола.
Обычно встречается один, реже два дефекта, молшт встречаться комбинация с другими ВПС: открытым артериальным протоком (ОАП), транспозицией магистральных сосудов (ТМС), подклапанным стенозом аорты и др.
* Литература на с. 228.
206
ВРОЖДЕННЫЕ |
ПОРОКИ |
СЕРДЦА |
Гемодинамика. Нарушения гемодинамики сходны |
с таковыми при ОАП. |
Большой |
сброс крови из аорты в ЛА ведет к МКК и перегрузке левых отделов сердца, а при ЛГ - и ПЖ. Величина а/в сброса крови определяется размерами дефекта и соотношением сосудистых сопротивлений обоих кругов кровообращения. При большом диаметре дефекта Л Г наблюда ется с рождения ребенка, и связано это с передачей высокого давления с аорты, а при низком расположении дефекта - с передачей силы изгнания левого желудочка на сосуды легких.
При данном пороке наблюдается три типа реакций сосудов МКК на массивный а/в сброс крови:
/ тип- нормальная или несколько замедленная физиологическая инволюция легочных сосудов после рождения ребенка с постепенным снижением ОЛС и увеличением а/в сбро са крови. При этом обнаруживается гиперволемическая форма ЛГ.
II тип - с развитием рефлекторного спазма легочных сосудов выявляется смешан ная форма ЛГ.
III тип - отсутствие физиологической инволюции легочных сосудов после рождения - врожденная склеротическая форма ЛГ.
Каждый тип реакции легочных сосудов зависит от индивидуальных особенностей ор ганизма. При I типе можно ожидать сравнительно позднее развитие распространенных склеротических изменений (в юношеском и более позднем возрасте). При II типе измене ния в легочных сосудах развиваются раньше, поэтому даже у детей моложе двух лет мож но наблюдать остаточную Л Г после коррекции порока, обусловленную наличием склеро тических изменений в части легочных сосудов.
Диагностика порока трудна и требует применения специальных методов исследо вания, так как при небольших размерах аортолегочного сообщения клиника его сходна с клиникой ОАП, а при больших - ДМЖП, осложненного высокой ЛГ.
Клиника. Дети отстают в физическом развитии, бледны, часто болеют ОРЗ и пневмо ниями, быстро утомляются. Иногда при плаче у младенца выявляется цианоз носогубного треугольника за счет обратного сброса крови. Выражены явления НК.
В связи с наличием ЛГ рано развивается гипертрофия сердца, приводящая к образова нию «сердечного горба». При небольшом а/в сбросе крови во втором-третьем межреберьях слева от грудины может пальпироваться систолическое дрожание.
А у с кулътати в на я картина зависит от величины сброса крови. При неболь ших размерах сообщения выслушивается систолодиастолический шум в третьем-четвер- том межреберьях, который обнаруживается лишь в 9-15% случаев [6].
Чаще выслушивается негромкий систолический шум во втором-третьем, реже в четвертом межреберье слева от грудины. На ФКГ он занимает 1/3-2/3 систолы. I тон нормальный или несколько усилен на верхушке. II тон большой, нерасщепленный. Может быть систолический тон изгнания. Иногда на ЛА фиксируется низкоамп литудный убывающий протодиастолический шум Грехема Стилла относительной не достаточности клапана ЛА.
У больных с высокой ЛГ склеротической формы, чаще в 3-й декаде жизни, в различной степени выражен цианоз, появляющийся при малейшей физической нагрузке, что объяс няется ростом ОЛС и развитием перекрестного или обратного сброса крови; «сердечный горб». Выслушивается звуковая триада ЛГ: 1) большой иерасщепленный II тон; 2) систоли ческий тон изгнания; 3) шум Грехема Стилла.
ЭКГ. Электрическая ось нормальная или отклонена вправо. У младенцев с большим сбросом крови в ЛА преобладают признаки гипертрофии ЛЖ, а признаки гипертрофии ПЖ минимальны или отсутствуют. Это может служить косвенным признаком, позволяю щим дифференцировать данную патологию с ДМЖП. У старших детей выражена диастолическая перегрузка ЛЖ и систолическая - ПЖ.
207
РАЗДЕЛ II
При уменьшении а/в сброса крови отмечается гипертрофия обоих желудочков, в боль шей степени правого. Однако сохранение глубоких зубцов Qv6 является показателем хоро
шего легочного кровотока. |
|
|
Рентгенологическая |
картина |
неспецифична: усилен легочный рисунок за |
счет артериального, реже венозного русла, сердце увеличено за счет обоих желудочков и Л П. Сосудистый пучок всегда расширен, выбухает дуга ЛА, нередко ствол и ветви ЛА рез ко расширены. Восходящая аорта может быть нормальной, но у 50% больных расширена, пульсация её усилена. Усилена пульсация ствола ЛА, нередко пульсируют и корни легких.
У старших детей и взрослых с увеличением ОЛС отмечается обеднение легочного рисун ка на периферии наряду с расширенными корнями легких. Сердце небольшое. При разви тии НК сердце значительно увеличено в размерах, больше за счет правых отделов.
На Эхо КГ в проекции длинной оси виден дефект аортолегочпой перегородки. Данный метод позволяет установить локализацию дефекта, его размеры, исключить сопутствую щие пороки сердца.
Катетеризация сердца позволяет установить величину и направление сброса кро ви, степень ЛГ
Для диагностики ценную информацию даст проведение катетера из ЛА в восходящую аорту и далее в правую сонную артерию. При выведении катетера из аорты в ЛА не регис трируется давление ПЖ. Этим исключается прохождение катетера через ДМЖП.
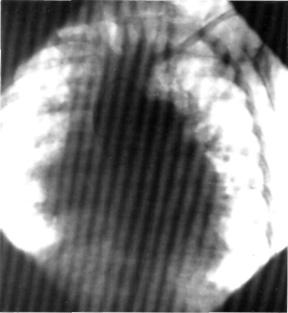
Наиболее точным диагностическим методом является аортография. На апгиограммах контрастное вещество из восходящей аорты непосредственно попадает в ствол ЛА над по лулунными клапанами аорты (рис. 2).
Прогноз зависит от размеров сообщения. При диаметре сообщения более 10 мм про гноз серьезный. Приблизительно 25-30% больных умирают в течение первых 6-ти меся цев жизни, около 15% - в школьном возрасте.
В литературе имеются лишь единичные со общения о пациентах, доживших до 40 лет (Yeatner R. et al., 1962). Средняя продолжи тельность жизни - 14 лет.
Единственное средство спасения больного - хирургическое лечение, так как случаев спонтанного закрытия дефекта аортолегочной перегородки не описано.
Показания к операции строятся
только с учетом степени нарушения гемодина мики. Операцию следует выполнять при боль шом дефекте в ранние сроки - до одного года, в более старшем возрасте операция противо показана лишь при склеротической форме ЛГ.
Хирургическое |
лечение. |
Закрытые |
|
|
|
методы коррекции порока (перевязка и рассе |
|
|
|
||
чение соустья с последующим ушиванием сте |
|
|
|
||
нок) в настоящее время оставлены, как и уши |
|
|
|
||
вание дефекта в условиях гипотермии [63]. |
|
|
|
||
В 1957 г. II. Shumachcr предложил вы |
|
|
|
||
полнять операцию в условиях искусствен |
|
|
|
||
ного кровообращения (ИК). В СССР первую |
Рис. 2. |
Аортограмма больной с |
диагно- |
||
успеишую операцию выполнил В. И. Бура- |
зом: |
дефект аортолегочпой |
пере |
||
копский в 1965 г. |
|
|
городки. |
|
|
208
ВРОЖДЕННЫЕ |
ПОРОКИ |
СЕРДЦА |
Закрытие дефекта в условиях ИК осуществляется путём ушивания или пластики дефек та доступами через просвет ЛЛ [35, 36] или аорты [20, 60], либо с обеих сторон [6, 53]. В на стоящее время операция производится в условиях ИК, гипотермии - 20-24°С и фармакохолодовой кардиоплсгии (ФХКП) с использованием трансаортального доступа, который позволяет четко видеть края дефекта, устья коронарных артерий и створки аортального клапана. После срединной стернотомии и подключения аппарата ИК с введением артери альной канюли выше соустья выделяют правую и левую ЛА и берут их в турникеты. После начала охлаждения пережимают их турникетами во избежание переполнения легких кро вью. Кардиоплегию проводят в корень аорты либо раздельно в коронарные артерии. Не большие дефекты ушивают непрерывным двухрядным швом, а большие закрывают ксеноперикардиалыюй или синтетической заплатой, фиксируемой непрерывным швом.
После опер ацио н пая летальность остаётся высокой - 15-20%.
Отдаленные результаты зависят от степени ЛГ. По данным НЦССХ им. А. Н. Ба кулева РАМН, операция приводит к улучшению состояния и практическому выздоровлению 65,2% пациентов. Снижение давления в ЛАу больных с высокой Л Г наступает лишь у боль ных с ОЛС до операции не выше 10 ед. [52, 54].
ДЕФЕКТ МЕЖЖЕЛУДОЧКОВОЙ ПЕРЕГОРОДКИ
Л. Р. ПЛОТНИКОВА
111
Дефект межжелудочковой перегородки (ДМЖП) - порок, при котором име ется сообщение между желудочками. Он встречается в среднем в 20% всех врожденных по роков сердца (ВПС) и наблюдается одинаково часто среди лиц обоего пола как изолирован ная аномалия, а также в сочетании с другими пороками.
Впервые порок описан в 1872 г. П. Ф. Толочиловым и в 1879 г. Roger. В последние годы
наибольшее распространение получила классификация, предложенная R. |
Anderson, |
Л. Becker (1983 г.) [27]*. Межжелудочковая перегородка делится на 3 отдела: |
1) входную, |
или приточную, часть; 2) трабекулярную, или мышечную, часть; 3) выходную, или отточпую, часть. В зависимости от локализации выделяют три группы дефектов:
1. Перимембрапозные дефекты: а) приточной части; б) трабскулярной части; в) отточной части.
2. Подартериальные отточные дефекты.
3. Мышечные дефекты: а) приточной части; б) трабекулярной части; в) отточной части.
Наиболее часто встречаются перимембранозиые дефекты. Какова же связь дефекта с проводящей системой сердца? Наиболее опасной зоной при перимсмбранозном дефекте трабекулярной части является место соединения нижнего (мышечного) края дефекта с задним (фиброзным). Образуемый угол, расположенный под перегородочной створкой и прикрытый ею, часто закрыт хордами и труднодоступен для хирурга. При приточном де фекте «опасная зона» захватывает не только задненижний угол, но и значительную часть нижнего края дефекта. Но опасность повреждения проводящей системы сердца снижает ся при наличии ДМЖП выходной части перегородки, так как она расположена дальше от задненижиего края. Проводящая система лежит в стороне и от подартериальных отточных дефектов [21].
Если мышечные дефекты трабекулярной и выходной частей перегородки находятся до статочно далеко от проводящей системы, то последняя располагается слева от хирурга в тканях верхней границы приточного мышечного дефекта.
В основе нарушения гемодинамики лелшт сброс крови из ЛЖ в ПЖ через дефект, веду щий к переполнению малого круга кровообращения и перегрузке обоих желудочков. Вели чина сброса крови определяется размерами и локализацией дефекта, соотношением ОЛС и ОПС. Если дефект мал, он оказывает большее сопротивление кровотоку и а/в сброс крови
* Литература на с. 228.
210

ПОРОКИ |
СЕРДЦА |
РАЗДЕЛ II
патологический III тон, возникающий вследствие усиленного диастолического напол нения ЛЖ. II тон обычно расщеплен. С развитием Л Г II тон становится большим и нерасщепленным [17].
У больных с высокой Л Г и малым а/в сбросом крови шум может отсутствовать. Нередко во втором межреберье слева от грудины выслушивается протодиастолический шум Грехема Стилла относительной недостаточности клапана ЛЛ.
ЭКГ при малых размерах дефекта не отличается от нормальной. В других случаях чаще наблюдается нормальное положение электрической оси сердца, признаки гипер трофии ЛЖ или обоих желудочков (рис. ЗБ). С уменьшением а/в сброса крови уменьша ются признаки гипертрофии ЛЖ. С ростом ОЛС электрическая ось отклоняется вправо, преобладает гипертрофия ПЖ.
При рентгенологическом исследовании больных с малыми размерами
ДМЖП изменения отсутствуют или незначительны. У всех больных с высокой ЛГ и боль шим а/в сбросом крови отмечается усиление легочного рисунка за счёт переполнения ар териального и нередко венозного русла легких вследствие относительного митрального стеноза и повышения «легочно-капиллярного» давления, выбухание ствола ЛА. Сердце уве личено за счет обоих желудочков и Л П. У больных с высокой Л Г и незначительным а/в сбросом крови легочный рисунок обеднен по периферии, резко расширен ствол ЛА, сердце умеренно увеличено в размерах за счет ПЖ.
У всех больных выявляется усиленная пульсация обоих желудочков и ствола ЛА, иногда самостоятельная пульсация корней легких.
ЭхоКГ даёт исчерпывающую информацию о наличии ДМЖП. На основании всех вы шеперечисленных признаков врач уже в поликлинике устанавливает диагноз ДМЖП.
В настоящее время лишь при наличии высокой Л Г производится внутрисердечное исследование по программе, включающей катетеризацию сердца, аортографию и ле вую вентрикулографию. При катетеризации полостей сердца выявляется повышение на сыщения крови кислородом на уровне желудочков; регистрируется давление в полостях сердца. При высокой ЛГ необходима одновременная запись давления в ЛА и системной ар терии. При аортографии исключается наличие ОАП. Левая вентрикулография позволяет установить локализацию и количество дефектов.
Прогно.з. При малых размерах ДМЖП прогноз, как правило, благоприятный. Подан ным НЦССХ им. А. Н. Бакулева РАМН, в 43,5% случаев отмечено спонтанное закрытие де фекта, при этом в 86% в возрасте до 4 лет. ЛГ не развивается. Опасность развития бакте риального эндокардита невелика - до 1%.
При умеренных размерах ДМЖП у детей раннего возраста часто развиваются явления НК. При правильном и длительном терапевтическом лечении большинство детей пережи вают этот ранний «критический» период. Спустя 1-2 года у них наблюдается значительное клиническое улучшение состояния. В более старшем возрасте на первое место среди ослож нений заболевания выступает ЛГ. НК наблюдается значительно реже, чем у младенцев.
Спонтанное закрытие дефекта отмечалось лишь у 13,8% этой категории больных.
При больших размерах ДМЖП прогноз серьёзный. Наиболее опасен для жизни период раннего возраста, когда наиболее выражены явления НК и пневмонии, являющиеся основ ными причинами гибели детей. В течение первого года жизни погибают 3/4 детей, боль шинство из них в первые 6 месяцев. Если дети выживают в этот период, то наступает фа за относительного благополучия. В ряде случаев этому способствуют: 1) развитие инфундибулярного стеноза; 2) уменьшение размеров дефекта с ростом самого сердца; 3) повышение ОЛС за счет спазма легочных сосудов, а также начинающегося развития склероза. Уже в первую декаду жизни может развиться склеротическая форма ЛГ, приво дящая к преждевременной инвалидности [34, 39].
212
ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА
Вторым осложнением, нередко встречающимся у больных с возросшим легочным кровотоком, является ПК, которую нельзя рассматривать как противопоказание к опе рации. Квалифицированное терапевтическое лечение до операции не должно превы шать более 1-1,5 месяцев.
Продолжительность жизни больных с ДМЖП - 23-27 лет [31].
Показанием к операции у детей раннего возраста служат: 1) стойкая или реци дивирующая НК, не поддающаяся длительному медикаментозному лечению; 2) выражен ная и прогрессирующая ЛГ; 3) частые респираторные заболевания и гипотрофия [23].
Оперативное лечение у младенцев может быть двояким: 1) паллиативная операция су жения ЛА; 2) радикальная коррекция порока.
Паллиативная операция показана у очень маленьких детей с высокой Л Г на фоне большо го а/в сброса крови. Операция сужения ствола ЛА впервые описана в 1952 г. W. Н. Muller и J. F. Dammann [56] и состоит в иссечении участка стенки ЛА с последующим ушиванием её раны. В 1958 г. Ы. М. Albert [26] упростил эту операцию, заменив пристеночный шов сужени ем ствола ЛА с помощью тесьмы. По методике Б. А. Константинова (1968 г.) [ 15] применяется левосторонний переднебоковои доступ во втором межреберье. Тесьму следует накладывать строго по середине ствола ЛА. При наложении тесьмы близко к клапанам ЛА возможно раз витие структурных изменений створок: они утолщаются, иногда прирастают к стенке ЛА.
Контролем адекватности сужения ЛА являются: повышение АД на 15-20 мм рт. ст., ста бильная гемодинамика в течение 15-20 мин, давление дистальнсе тесьмы не должно пре вышать 60 мм рт. ст.
В отдаленные сроки после операции явления НК исчезают. Это позволяет перелшть «критический» период жизни и отсрочить радикальную коррекцию порока до более благо приятного возраста.
У детей старшего возраста операция показана всем больным, кроме пациентов с высо кой ЛГ и незначительным а/в сбросом крови, т.к. ЛГ сохраняется после операции.
Радикальная коррекция ДМЖП выполняется в условиях ИК с раздельной капюляцией полых вен, гипотермии, пережатия аорты на фоне ФХКП. У больных первого года лшзни в ЫЦССХ им. А. Н. Бакулева РАМН используют метод глубокой гипотермии с капюляцией правого предсердия (ПП) одной канюлей, быстрым охлаждением тела до 18° С и снижени ем объёмных скоростей перфузии [8, 32].
Выбор доступа к дефекту определяется локализацией дефекта и зависит от опыта бригады хирургов: через ПП, ПЖ, ЛЖ, ЛА. С целью наиболее щадящего миокард досту па к межжелудочковой перегородке в 1957 г. D. A. Cooley [36] впервые ушил ДМЖП че рез ПП при разведении створок трикуспидального клапана. Кау Е. В. с соавт. (1960 г.) [48] предлолшли рассекать поперёк створку трикуспидального клапана, благодаря че му снизилась летальность с 50 до 13%, a A. S. Hudspeth с соавт. (1962 г.) [47] для лучше го доступа отсекали временно перегородочную створку в 2-3 мм от фиброзного кольца. В СССР последний метод был внедрен Г. М. Соловьёвым (1962 г.) [22]. В настоящее вре мя большинство хирургов для закрытия ДМЖП предпочитают чреспредсердный до ступ без отсечения перегородочной створки трикуспидального клапана, позволяющий закрыть около 70-80% всех встречающихся дефектов [32]. При необходимости правую вентрикулотомию выполняют поперечно или косопоперечно между ветвями коронар ных сосудов на границе приточного и выводного отделов. Множественные ДМЖП ино гда закрывают через левую вентрикулотомию. Редко используется доступ через ЛА при подартериальиых отточпых дефектах.
Существуют два способа закрытия дефектов: ушивание и пластика его заплатой. Уши вают дефекты до 1 см в диаметре отдельными П-образными швами на прокладках, однако если дефект округлой формы, лучше закрыть его заплатой.
213
РАЗДЕЛ II
Для пластики ДМЖП применяются синтетические ткани (тефлон, дакрон) или ксенопсрикард, которые фиксируются отдельными П-образными швами на прошгадках к краям дефекта.
Радикальная коррекция ДМЖП после операции Мюллера выполняется спустя не более 2-3-х лет, в противном случае может развиться стеноз выводного отдела ГОК, картина «тетрализации» порока [40]. На операции после выполнения продольной вептрикулотомии ДМЖП закрывается заплатой, затем под контролем пальца, введенного в ствол ЛЛ, рассе кается и удаляется тесьма. Если стенка ЛА не расправляется, то её продольно рассекают. При локальном сужении ствола иногда достаточно ушить стенку ЛА поперечно. В против ном случае вшивается ксенонерикардиальная заплата.
После ушивания стенки I"1П или 11Ж подшиваются электроды ЭКС для профилактики развития AV-блокады. Гемостаз. Дренажи в полость перикарда и в переднее средостение. Перед закрытием грудной клетки обязательно измеряется давление в ПЖ и системное АД.
По еле one рацио иная, летальность равна нулю при малых и |
средних размерах |
ДМЖП и 5% - при высокой ЛГ с большим а/в сбросом крови. |
|
Существует прямая зависимость отдаленных результатов от |
исходного состо |
яния легочно-сосудистого русла. У больных с ОЛС до 40-45% от ОПС гемодинамика полно стью нормализуется. После операции, проведенной у больных в возрасте старше 3 лет с бо лее высокими цифрами ОЛС, полной нормализации гемодинамики не наступает, по-видимому, за счет наличия склеротических изменений в отдельных легочных сосудах. Однако показатели внутрисердечной гемодинамики и функционального состояния сосу дов МКК значительно улучшаются, что свидетельствует об эффективности хирургическо го лечения и в этой группе больных [8, 45, 49].
— И —
