
- •Глава 1. Галоидпроизводные углеводородов
- •Номенклатура алкилгалогенидов, алкенилгалогенидов, алкинилгалогенидов и арилгалогенидов
- •1. Получение алкилгалогенидов
- •1.1. Галогенирование алканов
- •1.2. Присоединение галогеноводородов к алкенам
- •1.3. Замещение гидроксильной группы на галоген.
- •1.4. Свойства Галоидпроизводных углеводородов
- •1.4.1. Реакции нуклеофильного замещения
- •1.4.2. Механизм sn1
- •Дифенилметилгалогенид Трифенилметилгалогенид
- •1.4.3. Механизм sn2
- •1.4.4. Реакции отщепления
- •1.4.5. Реакции алкилгалогенидов с металлами
- •Глава 2. Спирты
- •Номенклатура одноатомных спиртов
- •2.4. Синтез спиртов из карбонильных соединений с помощью магнийорганических соединений
- •2.5. Гидролиз алкилгалогенидов
- •2.6. Свойства одноатомных спиртов
- •Температуры кипения некоторых спиртов и изомерных им простых эфиров
- •Кислотно-основные свойства спиртов
- •Кислотность спиртов
- •Из этих данных следует, что равновесие в системе спирт – щелочь всегда смещено в сторону спирта, а не алкоголята:
- •Замещение гидроксильной группы на галоген. Получение алкилгалогенидов
- •Получение алкилгалогенидов из спирта и галогеноводородных кислот
- •Получение алкилгалогенидов из спиртов и галогенидов фосфора
- •Дегидратация спиртов
- •2.10. Образование простых эфиров из спиртов
- •2.11. Получение простых эфиров по Вильямсону
- •2.12. Окисление спиртов
- •Восстановление спиртов
- •Взаимодействие с щелочными и щелчноземельными металлами.
- •2.15. Двухатомные спирты
- •2.16. Получение диолов
- •2.17. Свойства диолов
- •2.21. Расщепление простых эфиров кислотами
- •Глава 3. Тиолы и сульфиды
- •3.1 Получение тиолов
- •3.2 Свойства тиолов
- •Решения некоторых тестовых задач по теме спирты и тиолы
- •Только в реакциях 3) и 4) используются третичные спирты. Поскольку стабильность третичного карбениевого иона бензильного типа выше, чем стабильность третичного карбениевого иона алкильного типа:
- •5. Какого алкена образуется меньше при дегидратации 3-метилгексанола-3?
- •Глава 4. Альдегиды и кетоны
- •Альдегиды классификация
- •Строение карбонильной группы
- •4.1. Реакционные центры в молекулах альдегидов и кетонов
- •4.2. Химические свойства альдегидов и кетонов
- •4.3. Реакции альдегидов и кетонов по механизму нуклеофильного присоединения (an)
- •4.4. Реакции нуклеофильного присоединения по карбонильной группе с последующим отщеплением воды.
- •4.5. Окисление альдегидов и кетонов.
- •4.6. Реакция Канниццаро -Тищенко
- •4.7. Реакции полимеризации.
- •Получение альдегидов и кетонов
- •4.9. Медико-биологическое значение соединений с карбонильной группой
- •Отдельные представители альдегидов и кетонов
- •Эталонное решение задач
Номенклатура одноатомных спиртов
В номенклатуре IUPAC в названии спиртов к названию углеводорода добавляется суффикс «ол». В качестве родоначальной структуры выбирают самую длинную цепь, содержащую гидроксильную группу. Нумерация цепи осуществляется таким образом, чтобы гидроксильная группа получила наименьший номер. Заместители обозначаются в префиксе.
-
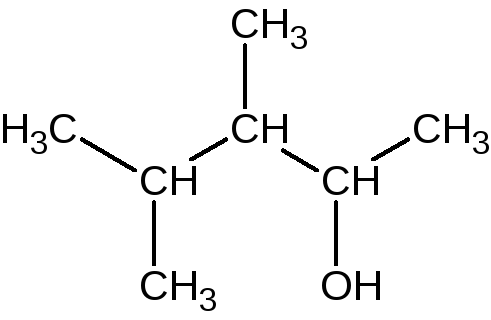
3,4-диметилпентанол-2
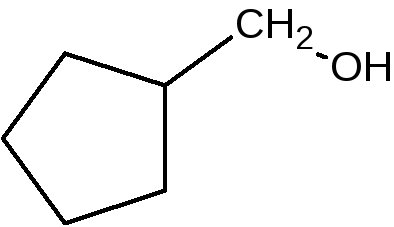
циклопентилметанол
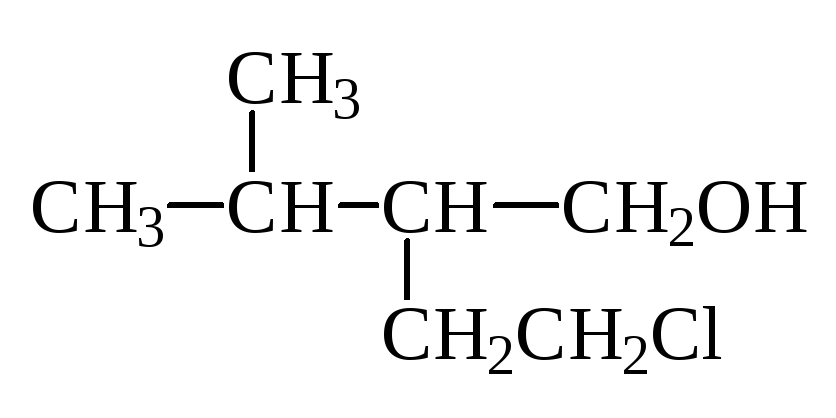
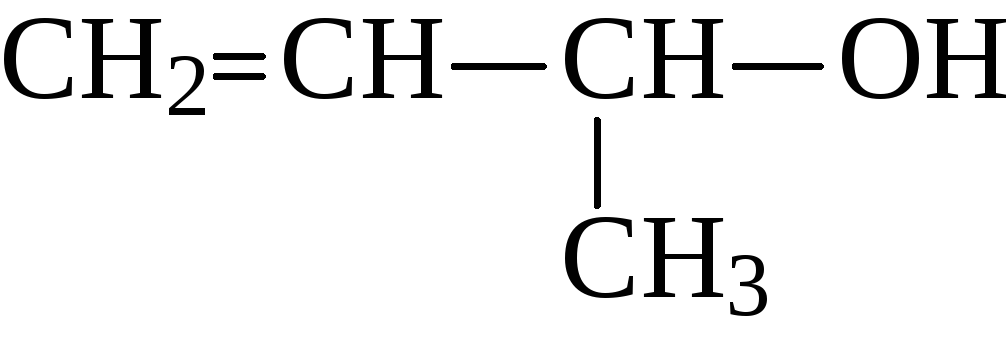
2-изопропил-4-хлор-бутанол
бутен-3-ол-2
ПОЛУЧЕНИЕ ОДНОАТОМНЫХ СПИРТОВ
2.1. ГИДРАТАЦИЯ АЛКЕНОВ
Гидратация алкенов протекает в водных растворах кислот с промежуточным образованием карбениевого иона, который далее быстро реагирует с водой с образованием спирта и регенерацией иона водорода. Процесс может осложняться перегруппировками. Направление присоедине-ния соответствует правилу Марковникова.
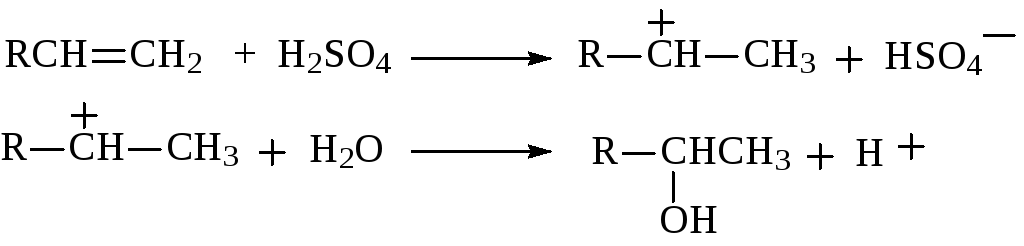
2.2. ВОССТАНОВЛЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ КОМПЛЕКСНЫМИ ГИДРИДАМИ
Как LiAlH4 так и NaBH4 восстанавливают альдегиды до первичных, а кетоны до вторичных спиртов. Предпочтительнее использовать боргидрид натрия вследствие большей безопасности в обращении. Он может быть использован даже в водном и спиртовом растворах, тогда как алюмогидрид лития бурно реагирует как с водой так и со спиртом.
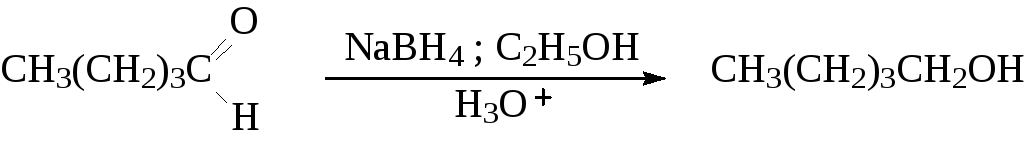
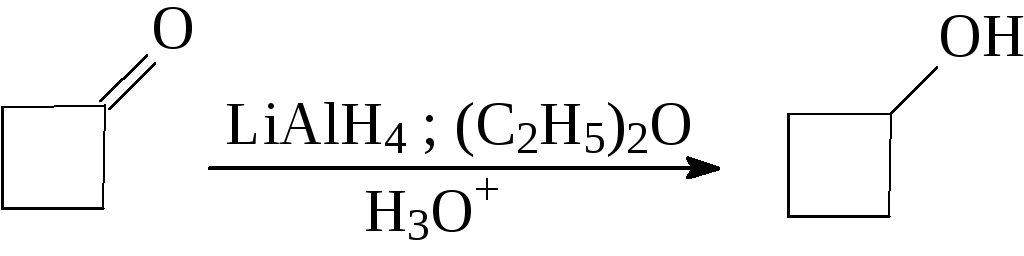
2.3. ВОССТАНОВЛЕНИЕ СЛОЖНЫХ ЭФИРОВ И КАРБОНОВЫХ КИСЛОТ ДО ПЕРВИЧНЫХ СПИРТОВ
Первичные спирты образуются при восстановлении сложных эфиров и карбоновых кислот алюмогидридом лития в эфире и тетрагидрофуране (ТГФ). Особенно удобен в препаративном отношении метод восстановления сложных эфиров алюмогидридом лития (согласно номенклатуре неорганических соединений его следует называть тетрагидридоалюминатом лития, но приведённое выше “неправильное” название повсеместно используется в русской химической периодике).
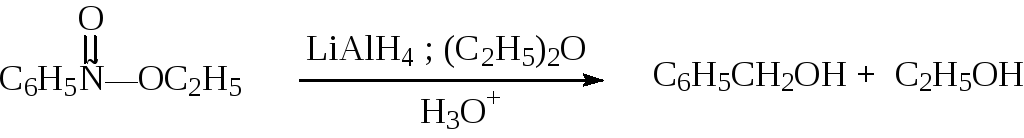
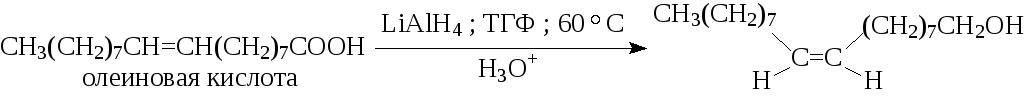
Восстановление карбонильных соединений комплексными гидридами относится к реакциям нуклеофильного присоединения к карбонильным соединениям.
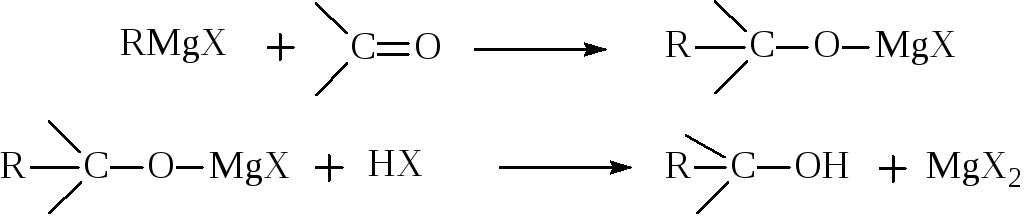
2.4. Синтез спиртов из карбонильных соединений с помощью магнийорганических соединений
Формальдегид и RMgX дают первичные спирты (здесь и далее X=Cl, Br, J, если не указано особо) :
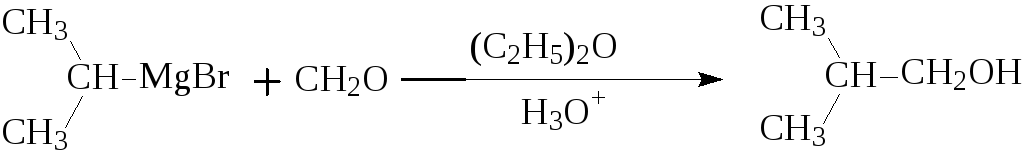
Альдегиды и RMgX дают вторичные спирты:
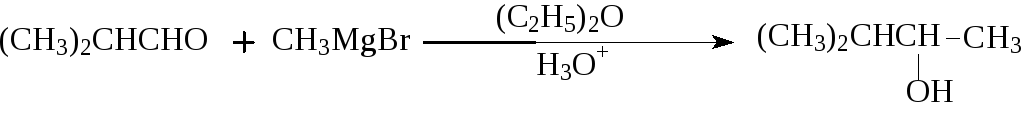
Кетоны и RMgX дают третичные спирты:
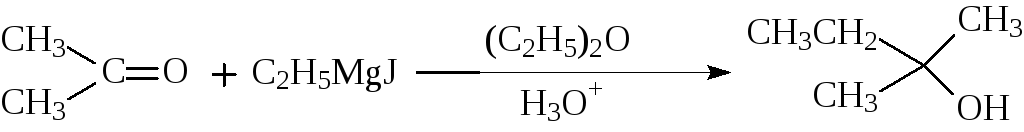
Во всех, приведённых выше реакциях, присоединение происходит однотип-но, углеводородный радикал из RMgX присоединяется к атому углерода карбонильной группы, а MgX к кислороду, с образованием в качестве промежуточного продукта смешанного алкоголята, гидролиз которого в кислой среде даёт соответствующий спирт.
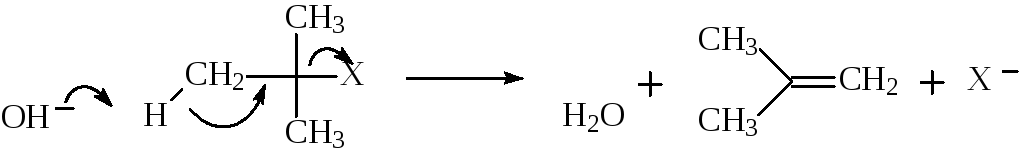
2.5. Гидролиз алкилгалогенидов
Скорость гидролиза алкилгалогенидов (RX) возрастает при переходе от хлоридов к иодидам, а гидролиз может протекать как в нейтральной, так и в щелочной среде. В случае третичных галогенидов возможно образование алкенов в качестве побочных продуктов (эти реакции подробно рассмотрены в главе 1)
![]()
2.6. Свойства одноатомных спиртов
Многие свойства спиртов обусловлены наличием гидроксильной группы. Одним из важнейших свойств спиртов, связанных с наличием гидроксильной группы, является их способность образовывать прочные меж-молекулярные водородные связи. Наличие межмолекулярных водородных связей обусловливает более высокие температуры кипения низших спиртов по сравнению с простыми эфирами с такой же молярной массой (см. Табл.1). Низшие спирты ( до бутилового) смешиваются с водой во всех отношениях, что также является следствием образования межмолекулярных водородных связей между молекулами спирта и воды.
Таблица 1
