- •Перечень условных обозначений
- •Введение
- •1. Методы синтеза пиразолоизохинолинов
- •2. Гликозилирование ароматических соединений
- •3. Материалы и методика исследования
- •Синтез 8-[4-(2-aцетамидо-3,4,6-три-о-ацетил-2-дезокси-β-d-глюкопиранозилокси)фенил]-3-метил-5,6-диметокси-1-фенилпиразо[4,5‑c]изохинолина (75)
- •Синтез 8-[4-(2-aцетамидо-3,4,6-три-о-ацетил-2-дезокси-β-d-глюкопиранозилокси-3-метокси)фенил]-5,6-диметокси-1-фенил-3-этилпиразо[4,5-c]изохинолина (77)
- •Синтез 8-[4-(2-aцетамидо-3,4,6-три-о-ацетил-2-дезокси-β-d-глюкопиранозилокси)фенил]-5,6-диметокси-1-фенил-3-этилпиразо[4,5‑c]изохинолина (79)
- •Синтез 8-[4-(2-aцетамидо-3,4,6-три-о-ацетил-2-дезокси-β-d-глюкопиранозилокси)фенил]-3-метил-5,6-диметокси-пиразо[4,5‑c]изохинолина (81)
- •Синтез 1-(2-aцетамидо-3,4,6-три-о-ацетил-2-дезокси--d-глюкопиранозил)-3,8-диметил-5,6-диметокси-пиразо[4,5‑c]изохинолина (83)
- •4. Охрана труда и безопасность в черезвычайных ситуациях
- •4.1. Карбонат калия
- •4.2. Ацетонитрил
- •4.3. Хлороформ
- •4.4. Изопропиловый спирт
- •4.5. Ацетон
- •4.6. Бромид ртути (II)
- •4.7.Краун-эфиры
- •4.8. Электробезопасность
- •4.9. Техника безопасности при работе с персональным компьютером
- •5. Обсуждение результатов
- •Список литературы
Список литературы
1. Использование производных изохинолина в качестве лекарственных средствhttp://www.pharmasvit.com/v3/Spravochniki/2134.html
2. Алексеев В. В. Оптическая изомерия и фармакологическая активность лекарственных препаратов / В. В. Алексеев // Военно-медицинская академия. Журн. – 1998.– № 1. – С. 49-55.
3. Phase-transfer catalyzed synthesis of acetylated aryl β-D-glucopyranosides and aryl β-D-galactopyranosides / D. Dess, H. Kleine, D. Weinderg [et al.] // Synthesis. – 1981. – № 11. – P. 883-885.
4. Roy R. Stereospecific synthesis of aril β-D-N-acetylglucopyranosides by phase-transfer catalysis / R. Roy, F. Tropper // Synth. Commun. – 1990. – Vol. 20, № 14. – P. 2097-2102.
5. Lewis P. T. Regiospecific 4-O-β-glucosidation of isoflavones / P. T. Lewis, K. Wähälä // Tetrahedron Lett. – 1998. – Vol. 39. – P. 9559-9562.
6. Грагеров И. П. Краун-соединения в органическом синтезе./ И. П. Грагеров. – Киев: Наукова думка, 1994. – 345 с.
7. Jensen K. J. O-Glycosylations under neutral or basic conditions / K. J. Jensen // Chem. Soc., Perkin Trans. – 2002. – № 1. – P. 2219-2233
8. Royer J. Chiral heterocycles by iminium ion cyclization / J. M. Royer, L. Bonin // – Chem. Rev. – 2004. – Vol. 104, № 5. – P. 2311-2352.
9. Cox E. D. The Pictet-Spengler condensation: a new direction for an old reaction / E. D. Cox, J. Cook // – Chem. Rev. – 1995. – Vol. 95, № 9. – P. 1797-1842.
10. Tsuji R. An efficient synthetic approach to optically active β-carboline derivatives via Pictet–Spengler reaction promoted by trimethylchlorosilane / R. Tsuji, M. Nakagawa, A. Nishida // Tetrahedron Asymmetry. – 2003. – Vol. 14, № 2. – P. 177-180.
11. Jiang W. Synthesis of optically pure pyrroloquinolones via Pictet–Spengler and Winterfeldt reactions / W. Jiang, Z. Sui, X. Chen // Tetrahedron Lett. – 2002. – Vol. 43, № 16. – P. 8941-8945.
12. Waldmann H. Asymmetric steering of the Pictet–Spengler reaction by means of amino acid esters as chiral auxiliary groups / H. Waldmann, G. Schmidt, M. Jansen [et al.] // Tetrahedron. – 1994. – Vol. 50, №47. – P. 11865-11884.
13. Kaljuste K. Solid phase synthesis of 1,2,3,4-tetrahydro-β-carbolines; implications for combinatorial chemistry / K. Kaljuste, A. Unden // Tetrahedron Lett. – 1995. – Vol. 36, № 50. – P. 9211-9214.
14. Connors R. V. The regio- and stereoselective addition of carbon nucleophiles to trifluoromethylphenylsulfanyl acetylene: a novel and expeditious approach to 3-trifluoromethylfurans / R. V. Connors, A. J. Zhang, S. J. Shuttleworth // Tetrahedron Lett. – 2002. – Vol. 43, № 4. – P. 665-667.
15. Solid phase sequential 1,3-dipolar cycloaddition Pictet–Spengler reactions / H. A. Dondas, R. Grigg, W. S. MacLachlan [et al.] // Tetrahedron Lett. – 2000. – Vol. 41, № 6. – P. 967-970.
16. Klein C. Solid-phase synthesis of new fused tetra, penta and hexa-cyclic:-carboline derivatives / C. Klein, J.M. Ostrech, A. Nefzi // Tetrahedron Lett. – 2003. – Vol. 44, № 10. – P. 2211-2215.
17. Hutchins S. M. Solid phase synthesis of tetrahydroisoquinolines&tetrahydroimidazopyridines / S. M.Hutchins, K. T.Chapman // Tetrahedron Lett. –1996. – Vol. 37, № 28. – P. 4865-4868.
18. Циклизации N-гетарил-5-аминопиразолов в реакциях азосочетания и пикте-шпенглера / С. Ю. Зинченко, С. В. Гресько, С. Ю. Суйков [и др.] // Науковіпраці ДонНТУ. – 2008. – № 137(11). – С. 82-92.
19. Богза С. Л. Взаимодействие орто-арилзамещенных аминоазолов с бензальдегидами. / С. Л. Богза // Cтруктура органических соединений и механизмы реакций – 1999. – Т. 2. – С. 25-30.
20. A versatile synthesis of pyrazolo[3,4 - c]isoquinoline derivatives by reaction of 4 ‑ aryl 5- amino-pyrazoles with aryl/heteroaryl aldehydes: the effect of heterocycle on the reaction pathways / S. L. Bogza, K. I. Kobrakov, A. A. Malienko [et.al] // J. Org. Biomol. Chem., 2005. – № 3. – P. 932-940.
21. Богза С. Кислотні циклізації аміноазолів. Синтез поліядерних гетероциклів з фрагментами ізохіноліну та цинноліну / С. Богза, С. Зинченко, С. Суйко // Вісник наукового товариства ім. Шевченка. Донецьке відділення. Хімія, – 2006. – Т. 10. – С. 94-100.
22. Синтез 1,2-транс-арилгликозидов по Гельфериху при катализе ортофосфорной кислотой / Е. Р Новик., В. М. Соколов, Е. П. Студенцов [ и др.] // Журн. Общей химии. – 1986. – Т. 56, вып 1. – С. 181-187.
23. Бочков А. Ф. Образование и расщепление гликозидных связей / А. Ф. Бочков, В. А. Афанасьев. – М.: Наука, – C. 1978. – 180.
24. Konishi F. Synthesis and taste of some flavones and dihydrochalcone glycosides in which carbohydrate moieties are located at differing positions of the aglycones / F. Konishi, S. Esaki, Sh. Kamiya // Agric. Biol. Chem. – 1983. – Vol. 47, № 7. – P. 1419-1429.
25. Tanaka M. The rates of hydrolysis of some substituted phenyl 2-acetamido-2-deoxy-α- and –β-D-glucopyranozides / M. Tanaka, S. Kyosaka, Y. Ito // Chem. Pharm. Buii. – 1973. – Vol. 21, № 9. – P. 1971-1977
26. Rothermel J. Phase-transfer-catalyzedsynthesisof aryl(α-ketosides of N-acetylneuraminicacid / J. Rothermel, H. Faillard //Biochemie. – 1990.– № 190. – P. 29-40.
27. Лазарева Н. В. Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей / Н. В. Лазарева, Э. Н. Левина. – Л.: Химия, 1976. – Т. 1. –. C. 592.
28. Лазарева Н. В. Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей / Н. В. Лазарева, Э. Н. Левина. – Л.: Химия, 1976. – Т. 2. –. C. 624.
29. Лазарева Н. В. Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей / Н. В. Лазарева, Э. Н. Левина. – Л.: Химия, 1976. – Т. 3. – C. 608.
30.Лазарева Н. В. Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей / Н. В. Лазарева, Э. Н. Левина. – Л.: Химия, 1976. – Т. 3. – C. 384.
31. Хираока М. Краун-соединения / М. Хираока. – М.: Мир, –. C. 1986. – 363.
32. Симонович С. В. Компьютер в вашей школе / С. В. Симонович. – М.: Информком-Пресс, –. C. 2001. – 336.
33. Особенности межфазного каталитического гликозилирования салициловой кислоты / Т. А Чупахина., Ю. H. Гончаренко, В. О. Курьянов [и др.] // Ученые записки ТНУ. – 2011. – Т. 24(63), № 2. – С. 396-401.
34. Синтез арил-О-β-D-глюкозаминидов и оценка их биологической активности в тесте ингибирования биолюминисценции морских светящихся бактерий / В. О. Курьянов, А. М. Кацев, Т. А. Чупахина [и др.] // Журнал орг. та фармхімії. – 2009. – Т. 7, вип. 4(28). – С. 30-40.
35. Чупахина Т. А. Синтез и исследование антимикробной активности глюкозаминидов 8-гидроксихинолинов / Т. А. Чупахина, А. М. Кацев, В. О Курьянов // Биоорган. химия. – 2012. – Т. 38, № 4. – С. 482-488.
36. Синтез гетероароматических S- и N-β-гликозидов N-ацетилглюкозамина в межфазных условиях / В. О. Курьянов, Т. А. Чупахина, А. Е. Земляков [и др.] // Биоорган. химия. – 2012. – Т. 38, № 4. – С. 482-488.
37. Bräuniger H. Benzazolglycoside. IV. Darsterllung von 1-β-D glucosaminopyranosyl-benzazolen / H. Bräuniger, A. Koine // Arch. Pharmaz. und Ber. Dеtsch. pharmaz. Ges. – 1965. – B. 298, № 9. – S. 768-777.
38. Zinner H. Benzazole. XIX. Glycoside des benzthiazolthions / H. Zinner, K. Peseke // Chem. Ber. – 1965. – B. 98, № 11. – S. 3508-3514.
|
ПРИЛОЖЕНИЕ |
|
|
|
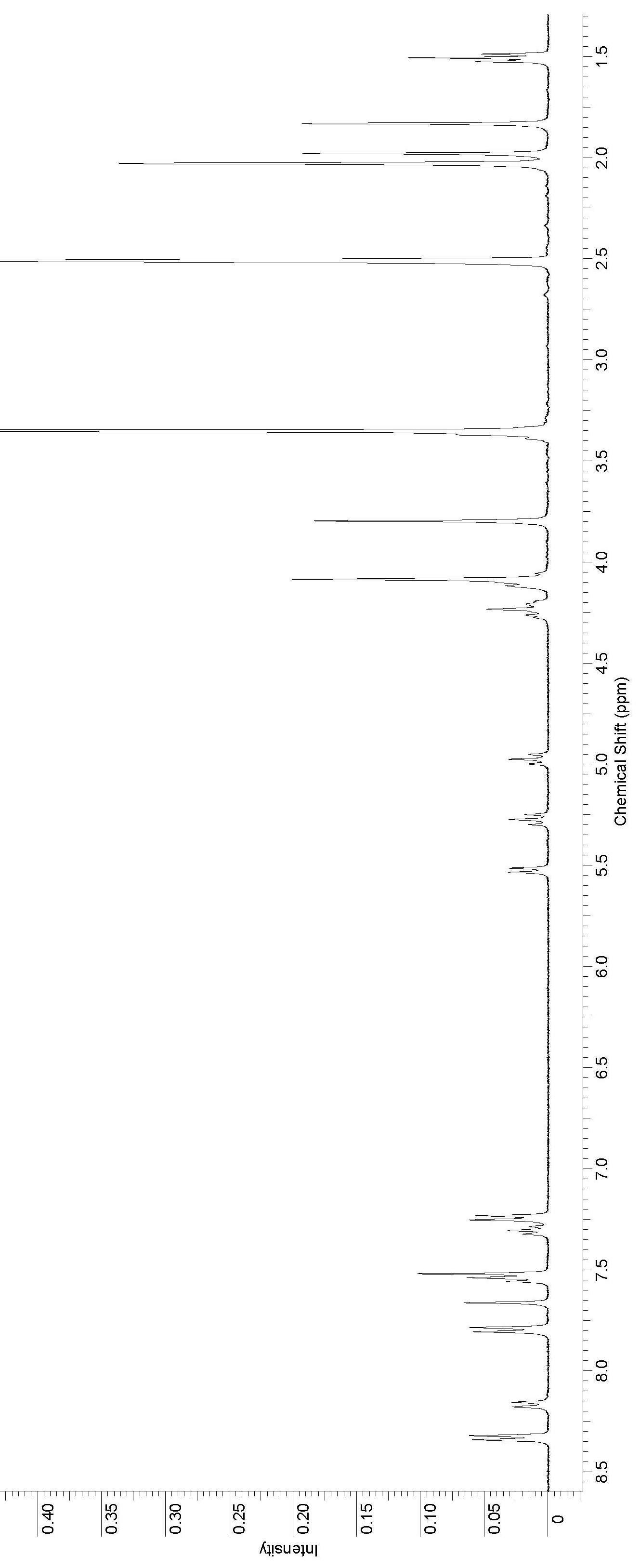
Рисунок 1. 1Н ЯМР спектр соединения 75. |
|
|
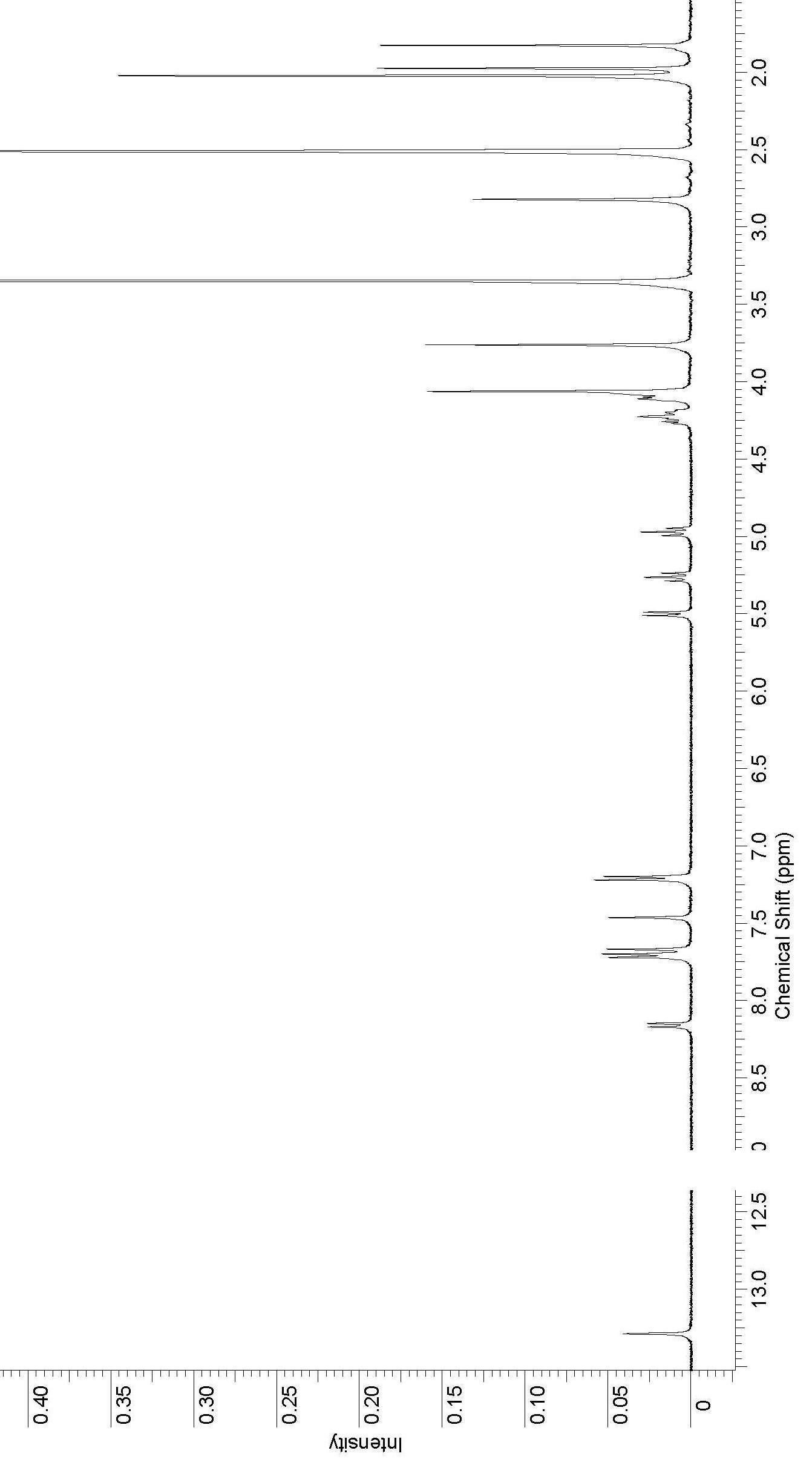
Рисунок 2. 1Н ЯМР спектр соединения 77. |
|
|
Рисунок 3. 1Н ЯМР спектр соединения 79. |
|
|
Рисунок 4. 1Н ЯМР спектр соединения 81. |
|
|
Рисунок 5. 1Н ЯМР спектр соединения 83. |