
- •Введение
- •Человеческой культуры
- •1. 1. Иерархия уровней культуры
- •1. 2. Иерархия естественных наук
- •1. 3. Уровни и формы научного познания
- •1. 4. Универсальный принцип естествознания — принцип дополнительности Бора
- •2. Основные этапы развития естествознания
- •2.1 Античная натурфилософия
- •2.2 Средние века и эпоха возрождения
- •2.3. Новое время
- •3. Особенности механики Ньютона
- •3.1 Ньютон и естествознание в его время
- •3.2 Механика Ньютона
- •3.3 Силы в природе
- •3.4 Законы сохранения
- •3.5 Механическая картина мира
- •4. Классическая физика
- •4.1 Учение о теплоте и электричестве
- •5. Неклассическая физика.
- •5.1 Атомизм, периодический закон.
- •5.2 Биологическая эволюция
- •6. Термодинамика
- •6.1 Микроскопические и макроскопические переменные
- •6.2 Калорические параметры состояния и функции процесса
- •6.3 Уравнение состояния
- •6.4 Основы молекулярно – кинетической теории
- •6.5 Теплоемкость
- •6.6 Второе начало термодинамики
- •6.7 Третье начало термодинамики
- •7. Физика полей
- •7.1. Определение понятия поля
- •7.2 Законы Фарадея — Максвелла для электромагнетизма
- •7.3 Электромагнитное поле
- •7.4 Гравитационное поле
- •7.5 Электромагнитная картина мира
- •8 Теория относительности Эйнштейна
- •8.1 Постулаты Эйнштейна в сто
- •8.2 Принцип относительности Галилея
- •8.3 Преобразования Лоренца
- •8.4 Постулаты ото
- •8.5 Основные итоги основ теории относительности
- •9. Колебания и волны
- •9.1 Корпускулярная и континуальная концепции описания природы
- •9.2 Колебания
- •9.3 Волновые процессы
- •9.4 Корпускулярно волновой дуализм излучения частиц
- •9.5 Принцип неопределенности Гейзенберга
- •9.6 Виртуальные частицы и состояния
6. Термодинамика
6.1 Микроскопические и макроскопические переменные
Термодинамика занимается изучением свойств тел и изменением состояния вещества, не рассматривая их атомно-молекулярной структуры. Этот подход используется в классической или, как ее еще называют, феноменологической термодинамике. На основании обобщения огромного фактического материала в классической термодинамике постулируется ряд основополагающих гипотез – начала термодинамики, которые затем перешли в ряд фундаментальных законов. Выводы термодинамики как науки актуальны для естествознания в целом, ибо имеют весьма общий характер.
Молекулярно – кинетическая теория объясняет, описывает макроскопические параметры термодинамических систем (давление, температура и др.) как суммарный результат воздействия частиц, из которых эта система состоит. Для этого используются статистические методы и аппарат теории вероятностей, позволяющие рассматривая поведение каждой частицы получить зависимости, описывающие поведение всего ансамбля в целом. Микроскопическими характеристиками атомов молекул являются их массы, скорости, кинетические энергии, потенциальная энергия взаимодействия, энтропия, энтальпия, внутренняя энергия и другие потенциалы.
Наблюдая за термодинамической системой необходимо вводить понятия микро - и макросостояний. Некоторое конкретно взятое макросостояние термодинамической системы может обеспечиваться достаточно большим числом различных микросостояний. Это требует введения оценочных параметров таких свойств системы как макрообъекта, которых нет у отдельно взятой частицы: давление, температура и т. д.
Под давлением в естествознании понимается сила, действующая на единицу поверхности
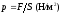 .
.
Единица
измерения давления один Паскаль, равный
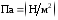 .
.
Для расчета давления в идеальном газе Максвеллом в рамках молекулярно-кинетической теории (МКТ) была получена зависимость, известная как основное уравнение МКТ
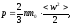
где
n
– концепция молекул; m0
– масса молекулы;
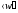 – среднеквадратичная скорость молекулы.
– среднеквадратичная скорость молекулы.
Температура является энергетической макроскопической характеристикой состояния системы и отражает меру отклонения ее внутренней энергии от внутренней энергии системы принятой за ноль отсчета. Единицей измерения является 1º С в эмпирической шкале и 1 К в термодинамической шкале, причем 1º С=1 К. Это не означает, что температура тела в этих шкалах отражается одинаковым численными значениями. Между ними имеется определенная взаимосвязь
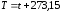 ,
,
где Т – температура системы в абсолютной термодинамической шкале; t – температура системы в эмпирической шкале.
Для системы, состоящей из идеального газа, может быть получена зависимость расчета температуры через кинетическую энергию молекулы
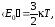
где
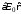 – среднеквадратичная кинетическая
энергия одной молекулы, Дж;
– среднеквадратичная кинетическая
энергия одной молекулы, Дж;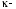 постоянная Больцмана, Дж/К;Т
–
термодинамическая температура, К.
постоянная Больцмана, Дж/К;Т
–
термодинамическая температура, К.
Под идеальным газом понимается модель газа, состоящая из частиц (атомов) не имеющих размеров (материальных точек), не взаимодействующих друг с другом, движение которых по всем направлениям равновероятны, а энергия распределена по всем степеням свободы равномерно, соударения молекул между собой и со стенками сосуда абсолютно упруги.
Важной характеристикой в термодинамике, определяющей тепловое состояние покоящейся системы, является внутренняя энергия U (Дж), или удельная внутренняя энергия u (Дж/кг).
Для идеального газа, исключающего взаимодействие молекул, внутренняя энергия состоит лишь из кинетической составляющей. При этом необходимо сделать оговорку, если не учитывать химическую, внутриатомную и внутриядерную ее компоненты. Кинетическая энергия системы при ее движении как целого, а также ее потенциальная энергия, определяемая отстоянием ее центра масс от нулевого уровня, во внутреннюю энергию не входят.
Термодинамические системы могут обмениваться энергией между собой в двух формах в виде передачи теплоты или работы.
Передача работы происходит на макроуровне, при котором возможно наблюдение конечного перемещения систем или их деформация – изменение геометрии, положения в пространстве.
Передача теплоты происходит на микроуровне при наличии, как правило, теплового контакта. Исключение составляет теплообмен излучением. Таким образом, теплота и работа представляют собой количественные меры, оценивающие передачу энергии от одного объекта (системы) к другому. Они не являются параметрами состояния, а относятся к функциям происходящих процессов.
