
- •Различают 4 вида субстратной специфичности ферментов:
- •Применение ферментов в качестве лекарственных препаратов
- •Окислительное декарбоксилирование пировиноградной кислоты: суммарное уравнение, строение и регуляция пируватдегидрогеназного комплексeа, связь с цпэ, биологическое значение.
- •Цикл трикарбоновых кислот (цитратный цикл): последовательность реакций, связь с цпэ, регуляция, биологическая роль.
- •Энергетическая
- •Теория Митчелла. Условия синтеза атф. Коэффициент фосфорилирования р/о.
- •Анаэробный гликолиз: схема процесса, энергетический эффект, и биологическое значение.
- •Лактатный цикл. Биологическое значение.
- •Глюконеогенез из аминокислот и глицерина. (схема процесса). Глюкозо- аланиновый цикл. Биологическое значение.
- •Синтез пуриновых нуклеотидов: схема, ферменты, регуляция, запасные пути синтеза.
- •Нарушения обмена пуриновых нуклеотидов: гиперурикемия, синтдром Леша-Нихана. Биохимические основы лечения подагры.
- •Биосинтез пиримидиновых нуклеодитов: схема, ферменты, регуляция, нарушения.
- •Нарушение обмена пиримидиновых нуклеотидов
- •Наследственная форма
- •Приобретенная форма
- •Распад пиримидиновых нуклеотидов: схема, ферменты.
- •Аденилатциклазная система передачи сигналов в клетки, роль g-белков в механизме трансдукции сигнала, вторичные посредники.
- •Либерины, статины, тропные гормоны гипофиза.
- •Адреналин: строение, синтез, регуляция секреции, ткани-мишени, механизм передачи сигнала, влияние на метаболизм в тканях-мишенях.
- •Мишени и эффекты
- •Ну или проще
- •80. Обмен железа: всасывание, транспорт, депонирование, регуляция, Роль железа в организме. Нарушения обмена железа в организме человека.
- •Существуют три способа перемещения железа из просвета кишечника в энтероциты:
- •Регуляция
- •Роль железа в организме:
- •Избыток железа
- •Железодефицит
- •Противосвертывающие системы крови: антитромбиновая и фибринолитическая.
- •Функции протеина s (ps):
- •Механизмы обезвреживания токсических веществ в печени: микросомальное окисление, реакции конъюгации
- •Nadph-зависимая монооксигеназная система
- •Nadh-зависимая монооксигеназная система
- •Распад гема, образование и обезвреживание билирубина. «Прямой» и
- •Биохимические изменения при нарушении обмена билирубина
- •Референтные величины концентрации общего билирубина в
- •Гемолитическая (надпеченочная) желтуха
- •Паренхиматозная (печёночная) желтуха.
- •Лабораторная диагностика
- •Механическая или обтурационная (подпеченочная) желтух.
- •Диагностическое значение определения билирубина и других желчных пигментов в крови и моче.
- •Эластин.
- •Свойства:
- •Возвращается в первоначальное состояние после снятия нагрузки.
- •Структурные и регуляторные белки мышц и их роль в мышечном сокращении
- •Функции субъединиц тропонина
- •Толстые нити образованы белком миозином
- •– Й этап.
- •На этой стадии атф не расщепляется, т.Е. Служит не источником энергии, а аллостерически изменяет конформацию миозиновой головки и тем самым ослабляет связь миозина с актином
- •Мышечное расслабление
- •Сокращение гладких мышц
- •Стадия – стадия начальных изменений
- •Стадия – стадия поздних изменений
- •Усилением:
- •Ослаблением:
Стадия – стадия начальных изменений
Поврежденный эндотелий и активированные тромбоциты вырабатывают медиаторы воспаления, факторы роста, эндогенные окислители. В результате через поврежденный эндотелий в интиму сосудов еще более активно проникают моноциты и способствуют развитию воспаления. При этом ЛПНП, попавшие под интиму, начинают изменяться (модифицироваться), т.е. подвергаются окислению, гликозилированию, ацетилированию.
Стадия – стадия поздних изменений
увеличение количества коллагена, эластина и гликозаминогликанов, т.е. накопление межклеточного вещества,
пролиферация и гибель пенистых клеток (апоптоз),
накопление в межклеточном пространстве свободного ХС и этерифицированного ХС,
инкапсулирование холестерола и формирование фиброзной бляшки. 4 стадия – стадия осложнений
На этой стадии происходят:
кальцификация бляшки и ее изъязвление, приводящее к эмболии сосудов,
тромбоз из-за адгезии и активации тромбоцитов,
разрыв сосуда.
 103.
Репликация
–
синтез
ДНК:
матрица,
затравка,
субстраты,
ферменты
и
белки
репликации
103.
Репликация
–
синтез
ДНК:
матрица,
затравка,
субстраты,
ферменты
и
белки
репликации
Матрица – одноцепочная ДНК
Затравка – 3` конец двуцепочечной ДНК спаренный с матрицей
Субстраты для синтеза – dАТФ, dГТФ, dЦТФ, ТТФ
Ферменты:
Топоизомераза – разрезание молекулы ДНК
Хеликазы – раскручивание ДНК
ДНК- связывающий белок – стабилизирует расплетённые нити ДНК
ДНК- полимераза α – синтез РНК – затравки на основе ДНК
ДНК- полимераза β – репарация повреждений
ДНК- лигаза – сшивка фрагментов Оказаки
Этапы репликации:

Принципы репликации:
Комплементарность.
Антипараллельность.
Униполярность. (5` 3`)
Полуконсервативность (дочерняя ДНК состоит из одной матричной цепи и одной вновь синтезированной)
Потребность в затравке.
Прерывистость.
104. Основные повреждения в ДНК и их репарация
Повреждения в составе генома: (влияние окружающая среда)
изменение нуклеотида
сшивки азотистых оснований друг с другом
разрывы цепей, отрыв пуриновых нуклеотидов
Такие изменения быстро определяются специальными ферментами, пораженный участок удаляется экзонуклеазами, заполняется ДНК- полимеразой β и сшивается ДНК-лигазой
Виды повреждения:
Апуринизация – потеря пуриновых оснований. Разрывается N- гликозидная связь между пуриновым основанием и дезоксирибозой.
Причины: изменение рH , повышение T
Дезаминирование
Аденин превращается в гипоксантин
Гуанин превращается в ксантин
Цитозин образуется в Урацил
Тимин не может быть дезаминирован
Тимидовые димеры
Под действием УФ- света сшиваются пиримидины и образуются димеры. Фотолиаза – узнает и разрывает тимидовые димеры.
Транскрипция: матрица, субстраты, ферменты и белки трапликации
матрица – одна из цепей ДНК
субстрат для синтеза – рибонуклеотиды (УТФ, ГТФ, ЦТФ, АТФ) ферменты – РНК-полимеразы.
Принципы транскрипции:
Комплементарность.
Антипараллельность.
Униполярность.
Беззатравочность.
Асимметричность

Этапы транскрипции:
Инициация – узнавание и связывание РНК- полимеразы с ДНК. Синтез затравочного фрагмента РНК.
Элонгация – РНК- полимераза движется вдоль ДНК (5` 3`) и наращивает РНК.
Терминация- РНК- полимераза достигает Терминатора и останавливается. Ферменты теряют сродство к ДНК и отделяются вместе с РНК (с помощью ро-фактора).
 Процессинг
РНК:
посттранскрипционные
превращения
различных
типов
РНК
Процессинг
РНК:
посттранскрипционные
превращения
различных
типов
РНК
- транскрипция пре-рРНК;
- связывание 45S- рРНК с белками и 5S-рРНК;
- метилирование пре-рРНК и расщепление на отдельные фрагменты;
- дальнейшее укорочение рРНК и формирование 40S- и 60S-субъединиц рибосом

- удаляются участки полинуклеотидной цепи на 5'- и 3'- концах молекулы пре-тРНК и интрон в центральной области молекулы;
- модифицируются азотистые основания, к 3-концу присоединяется триплет ССА; 3 - в цитоплазму
Процессинг предшественника мРНК
Кэпирование (англ. cap - шапка) – надевание "шапочки". "Сар" представляет собой
метилированный ГТФ, присоединенный в необычной позиции 5'-5' и две метилированные рибозы в первых двух нуклеотидах mРНК.

При особом процессе – сплайсинге (англ. splice – склеивать встык) происходит удаление интронов и сохранение экзонов.

Полиаденилирование – при помощи полиаденилат-полимеразы с использованием молекул АТФ происходит присоединение к 3’-концу 100-200 адениловых нуклеотидов, формирующих поли (А)-хвост.

Биосинтез белка (трансляция): основные этапы (инициация, элонгация, терминация). Посттрансляционные изменения полипептидных цепей и образование функционально-активных белков
Трансляция- биосинтез белка на матрице мРНК
Этапы

Инициация
В начале этой стадии формируются два тройных комплекса. После их объединения и присоединения большой субъединицы начинается стадия элонгации
Элонгация
Для этой стадии необходимы все
20 аминокислот,
тРНК,
белковые факторы элонгации
ГТФ
Осуществляется пошаговым присоединением АК
Терминация
Рибосома достигает стоп-кодонов УАА, УАГ, УГА, происходит отщепление полипептидной цепи и разборка рибосомы.
Посттрансляционная модификация белков:
Модификация N– конца и С – конца (удаление с N-конца метионина)
Удаление сигнальных последовательностей
Частичный протеолиз – удаление части пептидной цепи
Образование дисульфидных мостиков между остатками цистеина
Присоединение химической группы к аминокислотным остаткам
Добавление простетических групп
Фолдинг – это процесс сворачивания полипептидной цепи в правильную структуру
Объединение протомеров в единый олигомерный белок
Транспорт полипептидных цепей.
Перекисное окисление липидов (ПОЛ): субстраты, продукты ПОЛ, стадии, механизмы повреждающего действия (перекисная гипотеза гибели клеток)
Перекисное окисление липидов:
снижает гидрофобность и нарушает устойчивость мембран
изменяет работу мембрано-связанных ферментов
повышает проницаемость мембран для ионов Субстраты: ЛПВП, ЛПНП, ЛПОНП
Стадии:
Инициация.
Образование свободного радикала ЖК (L-)
Развитие.
Развитие цепи происходит при присоединении О2 и образуется липопероксирадикал (LOO-) или пероксид липида (LOOH)
Разветвление.
Разрушается структура липидов
Обрыв цепи.
Взаимодействие радикалов между собой

Продукты ПОЛ
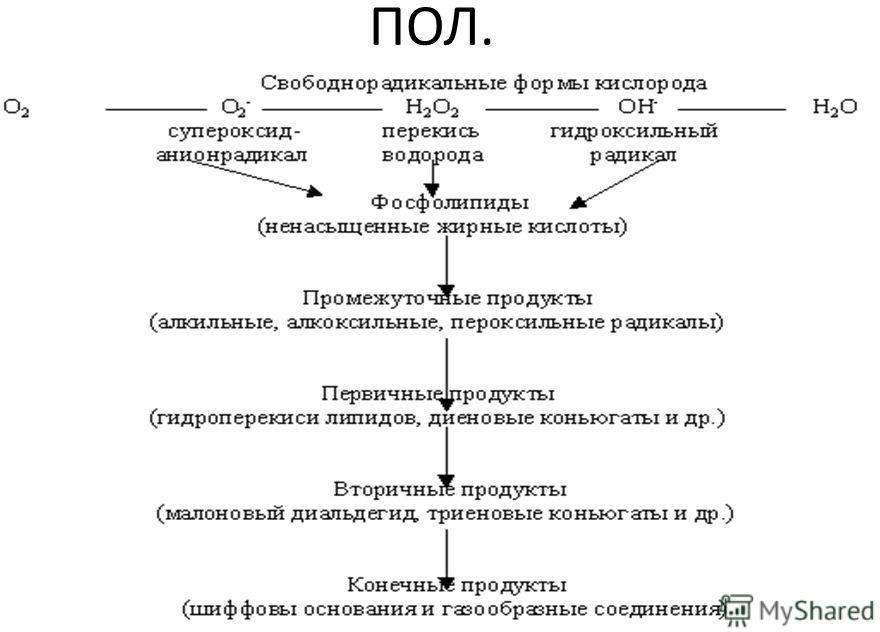
Перекисная гипотеза гибели клеток
Повреждающий фактор образование свободных радикалов активация ПОЛ разрушение фосфолипидов нарушение функции мембран повышается проницаемость, нарушение рецепции ГИБЕЛЬ КЛЕТКИ
Ферментативная и неферментативная антиоксидантная система (АОС) организма.
АОС – система для защита от свободных радикалов. Локализация: плазма крови, мембранные, внутриклеточные
По природе и действию

2(Н2О2)2(Н2О) + RO2
Обеззараживание Н2О2
 Молекулярные
механизмы клеточной гибели: внешний,
внутренний и
перфорингранзимный
пути
реализации
клеточной
гибели.
Молекулярные
механизмы клеточной гибели: внешний,
внутренний и
перфорингранзимный
пути
реализации
клеточной
гибели.Особые свойства опухолевых клеток и молекулярный механизм их приобретения.
Канцерогенез возможен из двух источников: из нормальной клетки ткани, ставшей прежде стволовой клеткой или из стволовой клетки ткани.
В составе клеток опухоли клетки неодинаковые:
основную массу клеток составляют нераковые клетки: они быстро делятся и после
выполнения функций ткани сами погибают через апоптоз; именно эти клетки - мишени для лекарств стандартной химиотерапии;
значительно меньшую часть составляют раковые стволовые клетки, которые
асимметричным делением копируют себя и генерируют нераковые клетки в составе клеток рака.
Раковые стволовые клетки делятся редко и медленно - это причина того, что лекарства стандартной химиотерапии оказываются неэффективными против раковых стволовых клеток
Раковая стволовая клетка возникает из нормальной или стволовой клетки ткани из-за дерепрессии в ней генов фетальных белков и одновременно репрессии генов- супрессоров метилированием CpG-динуклеотидов промотора этих генов или мутаций в генах.
Раковая клетка становится более живучей, чем нормальная клетка этого же типа, она несёт в себе ряд уловок, делающих её неуязвимой и способной к самостоятельному
существованию в организме пациента.
Эта дефектная клетка не просто клетка, а целый одноклеточный организм – паразит
Потеря чувствительности к сигналам, сдерживающим процесс пролиферации,
обусловленная инактивацией супрессорных (антимитотических) белков.
Замедление процессов программируемой клеточной гибели, опосредованное дисбалансом биохимической регуляции процессов апоптоза.
Неограниченный репликативный потенциал клеток, сопряжѐнный с реактивацией экспрессии фермента теломеразы, и, как следствие, отсутствием физиологического укорачивания теломер.
Стимуляция процессов ангиогенеза в опухоли, вызванная экспрессией трансформированными клетками ангиогенных факторов и направленная на удовлетворение повышенных потребностей в оксигенации быстроделящихся неопластических компонентов.
Способность к инвазии и метастазированию, ассоциированная с продукцией опухолью гистолитических ферментов (протеаз), а также факторов, угнетающих локальный
иммунитет. 7. Геномная нестабильность, опосредованная инактивацией систем репарации ДНК и нарушениями в молекулярном контроле клеточного цикла.
Перестройка стромальных компонентов, создающая более благоприятные условия для развития злокачественного клона.
Биохимические изменения метаболизма в опухолевых клетках.
Обмен углеводов в опухолевой клетке характеризуется:
