- •Различают 4 вида субстратной специфичности ферментов:
- •Применение ферментов в качестве лекарственных препаратов
- •Окислительное декарбоксилирование пировиноградной кислоты: суммарное уравнение, строение и регуляция пируватдегидрогеназного комплексeа, связь с цпэ, биологическое значение.
- •Цикл трикарбоновых кислот (цитратный цикл): последовательность реакций, связь с цпэ, регуляция, биологическая роль.
- •Энергетическая
- •Теория Митчелла. Условия синтеза атф. Коэффициент фосфорилирования р/о.
- •Анаэробный гликолиз: схема процесса, энергетический эффект, и биологическое значение.
- •Лактатный цикл. Биологическое значение.
- •Глюконеогенез из аминокислот и глицерина. (схема процесса). Глюкозо- аланиновый цикл. Биологическое значение.
- •Синтез пуриновых нуклеотидов: схема, ферменты, регуляция, запасные пути синтеза.
- •Нарушения обмена пуриновых нуклеотидов: гиперурикемия, синтдром Леша-Нихана. Биохимические основы лечения подагры.
- •Биосинтез пиримидиновых нуклеодитов: схема, ферменты, регуляция, нарушения.
- •Нарушение обмена пиримидиновых нуклеотидов
- •Наследственная форма
- •Приобретенная форма
- •Распад пиримидиновых нуклеотидов: схема, ферменты.
- •Аденилатциклазная система передачи сигналов в клетки, роль g-белков в механизме трансдукции сигнала, вторичные посредники.
- •Либерины, статины, тропные гормоны гипофиза.
- •Адреналин: строение, синтез, регуляция секреции, ткани-мишени, механизм передачи сигнала, влияние на метаболизм в тканях-мишенях.
- •Мишени и эффекты
- •Ну или проще
- •80. Обмен железа: всасывание, транспорт, депонирование, регуляция, Роль железа в организме. Нарушения обмена железа в организме человека.
- •Существуют три способа перемещения железа из просвета кишечника в энтероциты:
- •Регуляция
- •Роль железа в организме:
- •Избыток железа
- •Железодефицит
- •Противосвертывающие системы крови: антитромбиновая и фибринолитическая.
- •Функции протеина s (ps):
- •Механизмы обезвреживания токсических веществ в печени: микросомальное окисление, реакции конъюгации
- •Nadph-зависимая монооксигеназная система
- •Nadh-зависимая монооксигеназная система
- •Распад гема, образование и обезвреживание билирубина. «Прямой» и
- •Биохимические изменения при нарушении обмена билирубина
- •Референтные величины концентрации общего билирубина в
- •Гемолитическая (надпеченочная) желтуха
- •Паренхиматозная (печёночная) желтуха.
- •Лабораторная диагностика
- •Механическая или обтурационная (подпеченочная) желтух.
- •Диагностическое значение определения билирубина и других желчных пигментов в крови и моче.
- •Эластин.
- •Свойства:
- •Возвращается в первоначальное состояние после снятия нагрузки.
- •Структурные и регуляторные белки мышц и их роль в мышечном сокращении
- •Функции субъединиц тропонина
- •Толстые нити образованы белком миозином
- •– Й этап.
- •На этой стадии атф не расщепляется, т.Е. Служит не источником энергии, а аллостерически изменяет конформацию миозиновой головки и тем самым ослабляет связь миозина с актином
- •Мышечное расслабление
- •Сокращение гладких мышц
- •Стадия – стадия начальных изменений
- •Стадия – стадия поздних изменений
- •Усилением:
- •Ослаблением:
Роль железа в организме:
Обратимое связывание, транспорт и сохранение кислорода (гемоглобин и миоглобин)
Перенос электронов (железосерные белки, цитохромы а,b, с, цитохром с оксидаза)
Функционирование активных центров окислительно- восстановительных ферментов
окисление биомолекул (цитР450, пероксидазы)
разрушение (каталаса, супероксиддисмутаза) и генерирование активных форм кислорода (НАДФН-оксидаза)
Избыток железа
Существует аутосомно-рецессивное заболевание гемохроматоз, связанное с нарушением гепсидиновой регуляции и избыточным всасыванием железа в кишечнике. В результате железо накапливается в органах и тканях.
Общее содержание железа в организме достигает 20-60 г при
норме 2-4 г. Постепенно развиваются цирроз печени, кардиомиопатии, сахарный диабет 1 типа, артрит.
Железодефицит
Причинами железодефицита являются недостаток его в пище,
заболевания ЖКТ со снижением всасывания (гастриты), потери железа с кровью при менструальных, кишечных или иных кровотечениях
При недостаточности железа в организме мобилизация резервов происходит в следующем порядке:
железо из депо (ферритин),
затем в клетках (кроме эритроидных) снижается количество гемопротеинов до жизнеспособного минимума,
далее истощаются запасы сывороточного железа (холотрансферрин),
в последнюю очередь страдает синтез гемоглобина.
Таким образом, железодефицитная анемия является проявлением
крайнего дефицита железа, и нормальная концентрация гемоглобина крови не должна быть критерием обеспеченности организма железом.
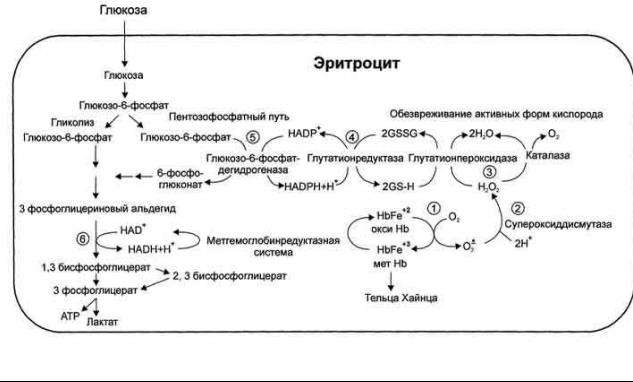
Особенности метаболизма в эритроцитах. Механизмы свободно- радикального окисления (СРО) и антиоксидантная защита в эритроцитах (АОЗ).
Зрелые эритроциты лишены ядра, поэтому в клетке не синтезируются белки.
Эритроциты не имеют митохондрий, поэтому в клетке не протекают реакции ЦТК, ЦПЭ, β- окисления жирных кислот.
Основным энергетическим субстратом эритроцита является глюкоза – лактат в кровь.
Энергия, поставляемая гликолизом, обеспечивает поддержание целостности плазматической мембраны и работу Na+, K+-АТФазы.
Присутствие в них фермента дифосфоглицератмутазы. Дифосфоглицератмутаза катализирует образование 2,3- дифосфоглицерата из 1,3-дифосфоглицерата.
.Образующийся только в эритроцитах 2,3-дифосфоглицерат служит аллостерическим регулятором связывания О2 гемоглобином.
В реакции дегидрирования глицеральдегид-3-фосфата в гликолизе образуется НАДН. Этот кофермент является кофактором фермента метгемоглобинредуктазы, участвующей в восстановлении метгемоглобина в гемоглобин по следующей схеме:
![]()
10 % глюкозы распадается в эритроците в пентозофосфатном пути. Образующийся при этом НАДФН обеспечивает восстановление глутатиона и поддерживает его оптимальную концентрацию. Восстановленный глутатион необходим для поддержания в
восстановленной форме SH-групп белков; препятствует окислению гемоглобина; предотвращает перекисное окисление липидов мембран.
Защита от СРО:
Эритроциты содержат ферментативную систему, предотвращающую токсическое действие активных форм кислорода и разрушение мембран эритроцитов.
Супероксидный анион супероксиддисмутазой превращается в пероксид водорода: O2- + O2- + Н+
→ H2О2 + O2.
Пероксид водорода под действием каталазы (2Н2О → 2Н2О + О2) или глутатионпероксидазы
(2GSH + 2Н2О2 → GSSG + 2Н2О) превращается в Н2О и О2. Донором водорода для глутатионпероксидазы является восстановленный глутатион (GSH).
Окисленный глутатион (GSSG) восстанавливается ферментом глутатионредуктазой, кофермент которого NADPН образуется в пентозофосфатном пути катаболизма глюкозы.
 Внешний
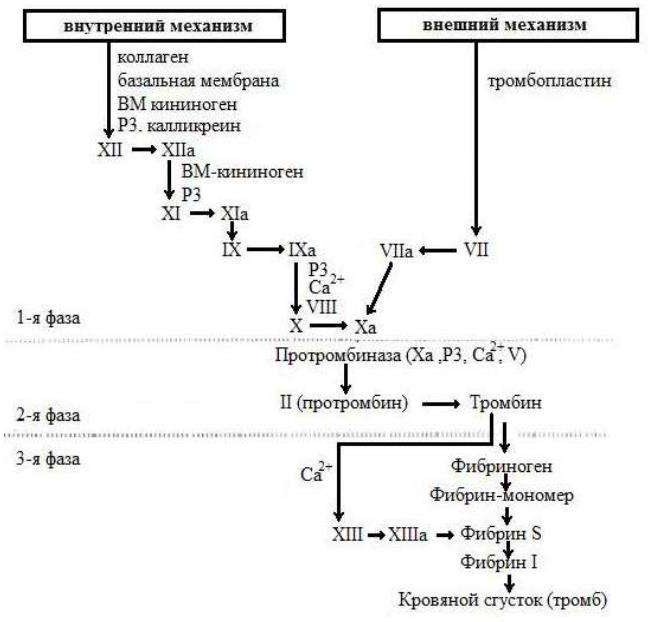
и внутренний пути свертывания крови.
Каскад реакций
прокоагулянтного
этапа свертывания крови. Механизмы
активации
ферментов
свертывающей
системы
крови.
Витамин
К
и
его
антагонисты
(дикумарол).
Внешний
и внутренний пути свертывания крови.
Каскад реакций
прокоагулянтного
этапа свертывания крови. Механизмы
активации
ферментов
свертывающей
системы
крови.
Витамин
К
и
его
антагонисты
(дикумарол).
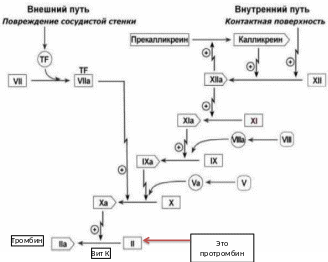
TF – тканевый фактор.
Ферменты активируются каскадно за счет постепенного присоединения к неактивной форме кофактора (TF,калликреин, Va, Xа и тд).
В печени при участии витамина К происходит синтез его неактивного предшественника –
протромбина, который в дальнейшем циркулирует в плазме. В плазме крови превращение
протромбина в тромбин происходит непосредственно под действием фактора Xa (совместно с Va). Дикумарол блокирует переход витамина К в активную форму.
На всякий случай