
- •Различают 4 вида субстратной специфичности ферментов:
- •Применение ферментов в качестве лекарственных препаратов
- •Окислительное декарбоксилирование пировиноградной кислоты: суммарное уравнение, строение и регуляция пируватдегидрогеназного комплексeа, связь с цпэ, биологическое значение.
- •Цикл трикарбоновых кислот (цитратный цикл): последовательность реакций, связь с цпэ, регуляция, биологическая роль.
- •Энергетическая
- •Теория Митчелла. Условия синтеза атф. Коэффициент фосфорилирования р/о.
- •Анаэробный гликолиз: схема процесса, энергетический эффект, и биологическое значение.
- •Лактатный цикл. Биологическое значение.
- •Глюконеогенез из аминокислот и глицерина. (схема процесса). Глюкозо- аланиновый цикл. Биологическое значение.
- •Синтез пуриновых нуклеотидов: схема, ферменты, регуляция, запасные пути синтеза.
- •Нарушения обмена пуриновых нуклеотидов: гиперурикемия, синтдром Леша-Нихана. Биохимические основы лечения подагры.
- •Биосинтез пиримидиновых нуклеодитов: схема, ферменты, регуляция, нарушения.
- •Нарушение обмена пиримидиновых нуклеотидов
- •Наследственная форма
- •Приобретенная форма
- •Распад пиримидиновых нуклеотидов: схема, ферменты.
- •Аденилатциклазная система передачи сигналов в клетки, роль g-белков в механизме трансдукции сигнала, вторичные посредники.
- •Либерины, статины, тропные гормоны гипофиза.
- •Адреналин: строение, синтез, регуляция секреции, ткани-мишени, механизм передачи сигнала, влияние на метаболизм в тканях-мишенях.
- •Мишени и эффекты
- •Ну или проще
- •80. Обмен железа: всасывание, транспорт, депонирование, регуляция, Роль железа в организме. Нарушения обмена железа в организме человека.
- •Существуют три способа перемещения железа из просвета кишечника в энтероциты:
- •Регуляция
- •Роль железа в организме:
- •Избыток железа
- •Железодефицит
- •Противосвертывающие системы крови: антитромбиновая и фибринолитическая.
- •Функции протеина s (ps):
- •Механизмы обезвреживания токсических веществ в печени: микросомальное окисление, реакции конъюгации
- •Nadph-зависимая монооксигеназная система
- •Nadh-зависимая монооксигеназная система
- •Распад гема, образование и обезвреживание билирубина. «Прямой» и
- •Биохимические изменения при нарушении обмена билирубина
- •Референтные величины концентрации общего билирубина в
- •Гемолитическая (надпеченочная) желтуха
- •Паренхиматозная (печёночная) желтуха.
- •Лабораторная диагностика
- •Механическая или обтурационная (подпеченочная) желтух.
- •Диагностическое значение определения билирубина и других желчных пигментов в крови и моче.
- •Эластин.
- •Свойства:
- •Возвращается в первоначальное состояние после снятия нагрузки.
- •Структурные и регуляторные белки мышц и их роль в мышечном сокращении
- •Функции субъединиц тропонина
- •Толстые нити образованы белком миозином
- •– Й этап.
- •На этой стадии атф не расщепляется, т.Е. Служит не источником энергии, а аллостерически изменяет конформацию миозиновой головки и тем самым ослабляет связь миозина с актином
- •Мышечное расслабление
- •Сокращение гладких мышц
- •Стадия – стадия начальных изменений
- •Стадия – стадия поздних изменений
- •Усилением:
- •Ослаблением:
Сокращение гладких мышц
Пусковой механизм в сокращении гладких мышц – повышение [Ca2+] в клетке.
Ca2+ связывается с кальмодулином, активирует киназу легких цепей миозина.
Фосфорилирование легких цепей миозина
Взаимодействие его с актином скольжение нитей, вызывает сокращение аналогично со скелетными мышцами
Процесс сокращения в гладких мышцах происходит значительно медленнее.

Особенности энергетического обмена быстро- и медленно сокращающихся миофибрилл.
Особенности метаболизма в миокарде.
Особенности метаболизма в миокарде
Чувствительность к недостатку О2
В норме аэробный характер гликолиза
Большой расход АТФ
Минимальный запас макроэргических соединений
Различия в потребляемых субстратах для АТФ
Активный ПФП
Субстраты для получения АТФ в миокарде:
ВЖК
Глюкоза
Лактат
ПВК
•Кетоновые тела (при сахарном диабете и голодании)
Используются в зависимости от:
энергетических потребностей
характера питания
доступности тех или иных субстратов
состояния миокарда
Использование субстратов для получения АТФ в зависимости от состояния миокарда
При приеме пищи в абсорбтивный период:
I – е место глюкоза (аэробный гликолиз)
II – е место ВЖК (β-окисление)
В постабсорбтивный период. При выполнении умеренной работы:
I – е место ВЖК (β-окисление)
II – е место глюкоза (аэробный гликолиз)
При выполнении тяжелой физической нагрузки (независимо от приема пищи):
Лактат – 50%
ВЖК - 22%
Глюкоза -17 %
При ишемии глюкоза в процессе анаэробного гликолиза
Содержание АТФ и креатинфосфата в сердечной мышце ниже, чем в скелетной мускулатуре, а расход АТФ велик. В связи с этим ресинтез АТФ в миокарде должен происходить намного интенсивнее, чем в скелетной мускулатуре.

Биохимические основы реперфузионного повреждения миокарда: кальциевый и кислородный парадокс.
Восстановление коронарного кровотока даже после непродолжительной ишемии может вызвать реперфузионное повреждение сердца, для которого характерны следующие проявления:
сократительная дисфункция сердца
нарушения сердечного ритма
феномен невосстановленного кровотока
Основными механизмами реперфузионного повреждения миокарда являются так называемые кальциевый парадокс и кислородный парадокс.
Кислородный парадокс — это токсическое действие кислорода, которое испытывает миокард в момент реоксигенации после ишемии.
Дефицит кислорода приводит к восстановлению переносчиков электронов (НАДНдегидрогеназ, убихинон, цитохромы) в дыхательной цепи митохондрий.
В момент реоксигенации эти переносчики становятся донорами электронов для молекул кислорода. Последние при этом превращаются в свободные радикалы (активные формы кислорода).
Генерация основного избытка продукция активных форм кислорода, повреждающих ткани, наступает при реперфузии, когда под действием ксантиноксидазы кислород преобразует гипоксантин в ксантин и мочевую кислоту
Активные формы кислорода повреждают молекулы ферментов, осуществляющих энергозависимый транспорт ионов в кардиомиоцитах. В результате происходит нарушение внутриклеточного ионного гомеостаза, развивается перегрузка кардиомиоцитов Са2+ и, как следствие, страдает сократительная функция сердца.

Кальциевый парадокс - это перегрузка кардиомиоцитов ионами кальция.
Ионы кальция в избытке проникают через сарколемму кардиомиоцитов, накапливаясь в саркоплазматическом ретикулуме и митохондриях.
Механизм усиленного проникновения Са2+ через клеточную мембрану тесно связан с нарушением Na+/ Са2+ обмена. Если в норме основное поступление Са2+ в клетку происходит через медленные Са2+-каналы, то в условиях реперфузии резко активируется Na+/Са2+-транспорт (обмен внутриклеточного Na+ на внеклеточный Са2+), который осуществляется белком- переносчиком, расположенным на сарколемме.

Биохимические изменения в миокарде при ишемии
Ишемическая болезнь сердца - патологическое состояние, характеризующееся абсолютным или относительным нарушением кровоснабжения миокарда.
Возникает несоответствие между потребностями миокарда в кислороде и уровнем оксигенации кардиомиоцитов.
В результате возникшего дефицита О2 в клетках сердечной мышцы нарушаются энергообразование, а также другие метаболические процессы, что приводит: к изменению сократительной функции миокарда в зоне ишемии и появлению болевого синдрома (стенокардии).
Биохимические нарушения метаболизма в миокарде при ишемии
Гипоксия
Снижение: активности ферментов аэробного дыхания, синтеза клеточных структур, транспорта субстратов, обмена веществ и катионов
Перестройка изоферментного спектра
Изменение ионного равновесия
Накопление лактата, неокисленных жирных кислот
Ацидоз
Снижение количества гликогена и глюкозы
Активация СРО и накопление токсичных продуктов ПОЛ
Повреждение клеточных структур, некроз
Содержание АТФ и креатинфосфата в клетке резко снижается в результате нарушения окислительного фосфорилирования в митохондриях.

При продолжительной ишемии эти изменения ведут к еще большему нарушению мембранной проницаемости и целостности мембран, что способствует выходу из клетки ионов, в том числе ионов К+ и ферментов.
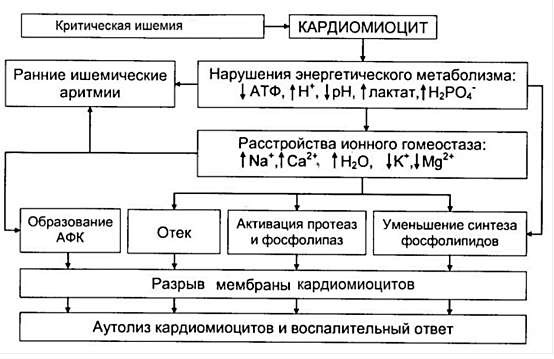
Дефицит энергетических ресурсов и нарушение ионного состава обусловливают торможение функциональной активности мышечных клеток и их постепенную гибель.
Мембраны: структурная организация, основные компоненты, избирательная проницаемость. Механизмы переноса веществ через мембраны (примеры). Схема гипотетического механизма действия Na+/K+–АТФ-азы


Легче всего проходят простой диффузией через липидную мембрану малые неполярные молекулы, такие как О2, стероиды, а также жирные кислоты.
Облегчённая диффузия (унипорт) глюкозы в эритроциты с помощью ГЛЮТ-1.
Примером активного антипорта яляется натрий–калиевая АТФаза. Она переносит в клетку ионы калия, а из клетки - ионы натрия.

Особенности химического состава и обмена веществ в нервной ткани.

Особенности энергетического обмена в нервной ткани.
Головной мозг составляет около 2% массы тела, при спокойном состоянии организма он утилизирует около 20% поглощенного кислорода. Мозг потребляет кислород больше, чем постоянно функционирующий миокард. За 10 секунд мозг поглощает весь кислород, находящийся в ткани.
Высокая активность митохондриальных ферментов цикла лимонной кислоты предотвращает накопление лактата в тканях мозга; большая часть пирувата окисляется до Ацетил-КоА.
Основное количество Ацетил-КоА подвергается окислению в цикле лимонной кислоты и дает энергию. Небольшая часть
Ацетил-КоА используется для образования нейромедиатора ацетилхолина.
Метаболиты цикла Кребса используется для синтеза аспартата и глутамата. Эти аминокислоты обеспечивают обезвреживание аммиака в тканях мозга.
Запасы гликогена в клетках головного мозга незначительны.
В отличие от других тканей организма человека ВЖК не проникают через ГЭБ и не могут быть использованы в качестве энергетического материала.
Аминокислоты не могут служить источником энергии для синтеза АТФ (АТР), поскольку в нейронах отсутствует глюконеогенез.
Основным энергетическим субстратом является глюкоза
Только при продолжительном голодании и сахарном диабете нервная ткань переключается на кетоновые тела. В крайних случаях такие аминокислоты как глутамат и аспартат
превращаются в соответствующие кетокислоты, которые способны к окислению с образованием энергии.

Особенности обмена углеводов в нервной ткани
Наиболее распространенным углеводом нервной ткани является глюкоза. Мозг активно потребляет глюкозу из крови. Известно, что ткань головного мозга потребляет до 70% эндогенной глюкозы, которая образуется в организме в процессе глюконеогенеза.
Глюкоза –важнейший предшественник биосинтеза аминокислот (особенно глутамата, аспартата, аланина, глицина) и других метаболитов.
Проникновение глюкозы в ткань мозга не зависит от действия инсулина. Инсулин не проходит через гематоэнцефалический барьер.
Высокая скорость потребления глюкозы нервными клетками обеспечивается работой высокоактивной гексокиназы мозга (активность гексокиназыв мозге выше по сравнению с другими тканями).
Отсутствует фермент глюкозо-6-фосфатаза, катализирующий дефосфорилирование глю-6-фосфата и выход глюкозы из клетки
В нейронах ПФП выражен незначительно.
В нейроглии ПФП является одним из основных метаболических путей глюкозы.
Образующийся в процессе ПФП НАДФН2 используется для синтеза в клетках головного мозга:
жирных кислот
- холестерина.
Метаболит глюкозы – ацетил-КоА – является предшественником для синтеза:
жирных кислот
холестерина
Содержание гликогена в нем невелико, всего около 0,1% от
общей массы углеводов. Однако интенсивность его обмена в мозге очень высока. В мозге новорожденных уровень этого полисахарида втрое выше такового у взрослых.
Глюкоза, галактоза, N-ацетилгалактозамин, сиаловые кислоты нужны для синтеза углеводных компонентов ганглиозидов, выполняющих рецепторные функции.
Галактоза и реже глюкоза являются углеводными компонентами цереброзидов, которые предохраняют нервный импульс от иррадиации в окружающую среду.
При гипоксии снижается скорость аэробного окисления глюкозы и накапливаются лактат и пируват.
Образование (пуриновый цикл) и обезвреживание аммиака в нервной ткани.
Еще одним источником образования аммиака в нервной ткани является гидролитическое дезаминирование АМФ.
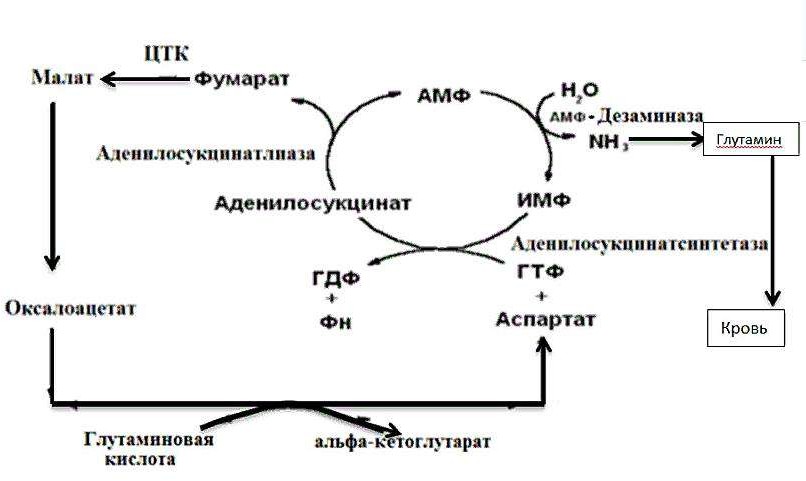
Роль пуринового цикла заключается в образовании и выведении аммиака из нервной ткани в составе глутамина, который проникает через ГЭБ и доставляет аммиак в печень для синтеза мочевины.

Гемато-энцефалический барьер. Нейромедиаторы: синтез и функции катехоламинов, ГАМК, ацетилхолина, серотонина, глутамата, глицина, гистамина. Нарушения обмена биогенных аминов при заболеваниях нервной системы и психических заболеваниях. Ингибиторы моноаминооксидазы в лечении депрессивных состояний.
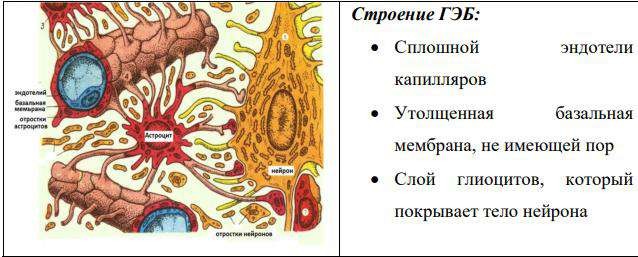
Функции ГЭБ
Регуляторная – создание избирательной проницаемости веществ в нервные клетки( проходят глюкоза, глутамин, кетоновые тела. Не проходят ВЖК, глутаминовая к-та, катехоламины)
Защитная
-
Название медиатора
Название медиатора
Ацетилхолин

сложный эфир холина и уксусной кислоты
является медиатором для всех двигательных нейронов, многих интернейронов ЦНС, а также
нейронов парасимпатической нервной системы.
Норадреналин

биохимический предшественник норадреналина и адреналина.
действует на адренэргические рецепторы: α1, α2, β1 и β2
Серотонин
производное аминокислоты триптофана.

название его связано с
первоначальным выделением из сыворотки крови и сократителъным действием на гладкие мышцы
возбуждающий медиатор ЦНС
облегчает двигательную активность, благодаря усилению секреции субстанции Р в окончаниях сенсорных нейронов
Гистамин

производное аминокислоты гистидина
оказывают влияние на состояние бодрствования, мышечную
активность, прием пищи, сексуальные отношения и обменные процессы в мозге.
Дофамин
биогенный амин
биохимический предшественник норадреналина и адреналина
действует через вторичные мессенджеры
повышение цАМФ приводит к фосфорилированию белков
постсинаптической мембраны
гамма-аминомасляная кислота

открывает хлорные каналы
вызывает гиперполяризацию
тормозит возбудимость
постсинаптической мембраны
Глицин

простейшая алифатическая аминокислота.
открывает хлорные каналы
вызывает гиперполяризацию
тормозит возбудимость
постсинаптической мембраны
Глутаминовая кислота
Трансаминирование на альфа-кетоглутарат
возбуждающий медиатор ЦНС
открывает неспецифический ионный канал для катионов
принимают участие в процессах обучения
Витамин А: химическая природа, медицинское название, суточная потребность, источники, биологическая роль. Гипо- и авитаминозы.
Химическая природа: β-иононовое кольцо с метильными заместителями и изопреновой цепью. В организме спиртовая группа ретинола окисляется в свои активные формы: альдегидную (ретиналь) или карбоксильную (ретиноевая кислота) группы.
Медицинское название: РЕТИНОЛ, АНТИКСЕРОФТАЛЬМИЧЕСКИЙ
Суточная потребность: 1,0-2.5 мг
Источники: С пищевыми продуктами в организм поступает как витамин А, так и каротины – вещества, схожие с ним по строению.
витамин А содержат рыбий жир, печень морских рыб, печень крупного рогатого скота и свиньи, жирномолочные продукты (сливочное масло, сливки, сметана), желток яиц,
каротиноиды имеются в моркови, красном перце, томатах (красные овощи), в пальмовом масле, облепиховом масле.
Биологическая роль.
Регуляция экспрессии генов.
Ретиноевая кислота служит лигандом для суперсемейства ядерных рецепторов, к числу которых относятся рецепторы к стероидным гормонам, к витамину D, трийодтиронину, простагландинам. Эта кислота необходима для экспрессии генов, участвующих в реакции клетки на гормон и ростовые стимулы.
В результате ретиноевая кислота:
регулирует нормальный рост и дифференцировку клеток эмбриона и молодого организма,
стимулирует деление и дифференцировку быстро делящихся тканей – хряща, костной ткани, сперматогенного эпителия, плаценты, эпителия кожи, слизистых оболочек, клеток иммунной системы

Участие в фотохимическом акте зрения.
Ретиналь в комплексе с белком опсином формирует зрительный пигмент родопсин, который находится в клетках сетчатки глаза, отвечающих за черно-белое сумеречное зрение ("палочки")
3. Антиоксидантная функция.
Осуществляет нейтрализацию свободных кислородных радикалов, особенно эта функция проявляется у каротиноидов.
Гипо- и авитаминозы.
Причины:
Пищевая недостаточность
Нехватка витаминов Е и С, защищающих ретинол от окисления,
Снижение функции щитовидной железы (гипотиреоз), т.к. в кишечнике и печени превращение каротиноидов в витамин А катализируют железо-содержащие ферменты, активируемые тиреоидными гормонами.
Клиническая картина.
Стерильность
При сильном гиповитаминозе и авитаминозе происходит нарушение темновой адаптации – куриная слепота
Задержка роста, похудание, истощение
Специфические поражения глаз, слизистых оболочек, кожи:
ороговение кожи, сухость и шелушение – "жабья кожа"
ороговение эпителия слезного канала, сухость роговой оболочки глаза, воспаление роговой оболочки.
поражение эпителия желудочнокишечного тракта, дыхательных путей и мочеполовой системы (также нарушение сперматогенеза). Поражение эпителия дыхательных путей приводит к снижению местного иммунитета, вплоть до ларинготрахеобронхита и пневмонии.
Витамин Е: химическая природа, медицинское название, суточная потребность, источники, биологическая роль. Гипо- и авитаминозы.
Химическая природа: Молекула токоферола состоит из кольца производного бензохинона и изопреноидной боковой цепи.
Медицинское название: ТОКОФЕРОЛ, АНТИСТЕРИЛЬНЫЙ
Суточная потребность: 20-50 мг
Источники: Растительные масла (кроме оливкового), пророщенное зерно пшеницы, бобовые, яйца.
Биологическая роль
Лимитирует свободнорадикальные реакции в быстроделящихся клетках – слизистые оболочки, эпителий, клетки эмбриона. Этот эффект лежит в основе положительного действия витамина в репродуктивной функции.
Защищает витамин А от окисления.
Защищает жирнокислотные остатки мембранных фосфолипидов, и, следовательно, любые клеточные мембраны от перекисного окисления липидов.
Гипо- и авитаминозы.
Причины:
Пищевая недостаточность
Нарушения всасывания жиров
Недостаток аскорбиновой кислоты, имеющей также антиоксидантную функцию.
Клиническая картина.
Пониженная устойчивость и гемолиз эритроцитов
Анемия
Увеличение проницаемости мембран
Мышечная дистрофия
Слабость
Арефлексия
Снижение проприоцептивной и вибрационной чувствительности
Витамин С: химическая природа, медицинское название, суточная потребность, источники, биологическая роль. Гипо- и авитаминозы.
Медицинское название: АСКОРБИНОВАЯ КИСЛОТА
Суточная потребность 100 мг
Химическая природа витамина C является ВОДОРАСТВОРИМЫМ витамином
Источники: содержится в цитрусовых продуктах, сладком перце, ягодах, моркови.
Роль: участвует в ОВР, превращении проколлагена в коллаген, укрепляет стенки сосуда.
Гиповитаминоз: вялость, кровоточивость десен, выпадение зубов, плохое заживление ран, потеря волос.
Авитаминоз: развивается ЦИНГА - нарушение синтеза коллагена, что приводит к поражению соединительной ткани.
Биохимические основы развития атеросклероза
Базовой метаболической «предпосылкой» развития атеросклероза является гиперхолестеролемия. (повышенное содержание холестерола в крови).
Гиперхолестеролемия развивается:
вследствие избыточного поступления ХС, углеводов и жиров;
генетической предрасположенности, заключающейся в наследственных дефектах структуры рецепторов ЛПНП или апоВ-100, а также в повышенном синтезе или секреции апоВ-100 (в случае семейной комбинированной гиперлипидемии, при которой в крови повышены концентрации и ХС и ТАГ).

стадия – повреждение эндотелия
